Tamponnade cardiaque
| Maladie | |||
 Schéma d'une tamponnade cardiaque | |||
| Caractéristiques | |||
|---|---|---|---|
| Signes | Tachycardie , Tachypnée , Triade de Beck, Distension des veines jugulaires, Pulsus paradoxus, Bruits cardiaques atténués, Absence de frottement péricardique, Signe de Kussmaul , Hypotension artérielle , Température corporelle élevée | ||
| Symptômes |
Dyspnée , Vertige , Lipothymie , Altération de l'état de conscience , Syncope , Palpitations , Température corporelle élevée | ||
| Diagnostic différentiel |
Embolie pulmonaire, Insuffisance cardiaque, Oesophagite, Gastrite, Ulcère gastro-duodénal, Infarctus du myocarde, Cirrhose hépatique, Péricardite constrictive, Dissection aortique, Pneumothorax sous tension | ||
| Informations | |||
| Terme anglais | Cardiac tamponade | ||
| Wikidata ID | Q929313 | ||
| Spécialités | Cardiologie, Soins intensifs, Médecine d'urgence, Médecine interne | ||
| |||
La tamponnade cardiaque est causée par l'accumulation excessive de fluide dans l'enveloppe péricardique, ce qui entrave le remplissage des cavités cardiaques et ainsi le statut hémodynamique des patients. Si elle n'est pas reconnue rapidement et traitée adéquatement, elle peut évoluer vers le choc cardiogénique et la mort. Elle est une conséquence grave d'un épanchement péricardique.
Épidémiologie
L'épidémiologie de la tamponnade cardiaque est mal décrite dans la littérature. Il est estimé que son incidence est de 2 par 10 000 par année, la majorité des études décrivant plutôt la prévalence des épanchements péricardiques. [1]
Étiologies
Toute cause de péricardite ou d'épanchement cardiaque peut évoluer vers la tamponnade cardiaque. Selon la cause, l'épanchement péricardique peut être de nature transsudative ou exsudative, être formé de sang, ou plus rarement être un empyème. [2] Le tableau suivant traite des principales étiologies.
| Catégories | Exemples | |
|---|---|---|
| Non-infectieuses | Néoplasique (33 %) |
|
| Traumatique (12 %) |
| |
| Métabolique |
| |
| Auto-immune et auto-inflammatoire |
| |
| Cardiaque |
| |
| Médicamenteuse |
| |
| Infectieuses | Bactérienne (4 %) |
|
| Virale |
| |
| Fongique |
| |
| Parasitique |
| |
| idiopathique |
| |
Physiopathologie
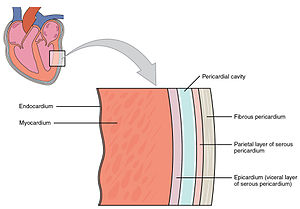
Péricarde
Le péricarde est une membrane enveloppant le cœur. Il comprend le péricarde fibreux externe (non élastique) et le péricarde séreux interne (élastique) à deux couches : la couche viscérale et la couches pariétale. Celles-ci sont séparées par la cavité péricardique contenant 15 à 35 mL de transsudat chez les personnes en bonne santé. Le péricarde protège mécaniquement le cœur et réduit la friction induite par les battements continuels du coeur. [9][10] Les deux péricardes jouent aussi un rôle dans la fonction diastolique du coeur ; en favorisant le recul élastique pour le péricarde viscéral, tandis que le péricarde pariétal permet pour sa part le maintient d'un angle cardiaque optimal pour le remplissage des cavités cardiaques via son attachement aux structures médiastinales et thoraciques adjacentes. Finalement, le péricarde pariétal agit aussi comme barrière contre la dissémination d'infections pulmonaires par contiguïté. [4]
De façon physiologique, le péricarde pariétal, malgré son inélasticité, possède un certain volume de réserve péricardique. Cette réserve est donnée par les sinus transverse et oblique qui sont des endroits auxquels l'accolement des feuillets péricardiques est incomplet. Ce volume de réserve permet ainsi d'accommoder les variations de volume sanguin intracardiaque donnés par les diverses phases respiratoires et par les changements de position, sans augmenter les pressions intracardiaques. Lorsque ce volume de réserve est dépassé dans certains contextes pathologiques (ex : en status asthmaticus où l'effort inspiratoire entraîne un retour veineux important), alors il est possible de retrouver un pouls paradoxal. Ce signe clinique est occasionné par la compétition entre le remplissage des chambres cardiaques gauches et droite qui varient selon les cycles inspiratoire et expiratoire, donnant une chute de la pression systolique de plus de 10 mmHg à l'inspiration. [4][11]
Pression intra-péricardique
En condition physiologique, la pression intrapéricardique (PIP) est inférieure aux pressions intracardiaques ; elle reflète notamment la pression intrathoracique, et est donc négative lors de l'inspiration. Le péricarde permet d'ailleurs la transmission de la pression intrathoracique négative aux cavités cardiaques, augmentant ainsi le retour veineux en phase inspiratoire.
En condition pathologique, la PIP est déterminée par la relation entre la compliance du péricarde externe et le volume de fluide péricardique. C'est donc la relation pression-volume qui importe plutôt que la quantité absolue de fluide. La rapidité de l'installation influence aussi grandement la PIP puisque le péricarde fibreux n'a pas le temps de s'acclimater et d'augmenter le nombre de cellules le composant. [4]
Continuum des atteintes péricardiques
Les maladies péricardiques incluent notamment la péricardite aiguë ou chronique, l'épanchement péricardique, la tamponnade cardiaque et la péricardite constrictive. Ces entités, à l'exception de la péricardite constrictive, évoluent sur un spectre, bien que l'évolution ne soit pas toujours prévisible.
Péricardite
La péricardite est définie comme la simple inflammation du péricarde, quelle soit accompagnée ou non d'un épanchement.
Il est à noter que la péricardite constrictive ne s'inscrit pas dans le continuum menant à la tamponnade cardiaque. Elle est plutôt le résultat d'un péricarde non compliant qui limite le remplissage et la dynamique cardiaque. [12]
Épanchement péricardique
Il consiste en l'accumulation supra-physiologique d'un liquide au sein du sac péricardique, le plus souvent lié à une péricardite aiguë ou chronique. Tout épanchement péricardique n'est pas dû à une péricardite. Les symptômes qu'il entraîne sont proportionnels à sa taille et inversement proportionnels à sa rapidité d'installation en raison du remodelage du péricarde pariétal. [13][4]
Selon la cause, il peut être de diverses natures :
- séreux en contexte de péricardite idiopathique
- séro-sanguin en contexte de péricardite induite par des maladies inflammatoires ou de certaines néoplasies
- purulent en contexte d'infection
- sanguin lorsqu'à la suite d'une intervention coronarienne percutanée avec perforation cardiaque. [4]
Tamponnade cardiaque
La tamponnade cardiaque est une affection grave qui survient après une accumulation soudaine et / ou excessive de liquide dans l'espace péricardique, augmentant considérablement la PIP. Le péricarde fibreux devient inextensible et est considéré comme un volume fixe. Les chambres cardiaques et leur contenu en sang font donc compétition au sein de ce volume fixe, ce qui restreint le remplissage approprié des cavités cardiaques. Il en résulte une perturbation de l'hémodynamie normale. L'oreillette droite - en raison de ses basses pressions, de ses parois minces et de sa morphologie avec une grande surface péricardique - est particulièrement vulnérable à l'augmentation de la PIP.
Plusieurs mécanismes compensatoires existent et reposent sur l'adrénergisme, notamment via la stimulation alpha adrénergique. Parmi les mécanismes compensatoires, on compte la tachycardie, l'augmentation de la contractilité ventriculaire et la vasoconstriction artérielle. Finalement, l'augmentation de la tension veineuse centrale et ainsi le retour veineux sont médiés par la vénoconstriction et par la rétention hydrosodée.
Il en résulte défaut de remplissage des cavités cardiaques et donc le volume d'éjection fixe. Conséquemment, le débit cardiaque dépend grandement de la fréquence cardiaque (DC = VES x Fc).
Un concept important de la tamponnade cardiaque est le last drop. Il s'agit de l'état terminal lors duquel le collapsus diastolique de l'oreillette droite entraîne une baisse du débit cardiaque si importante que la perfusion coronarienne devient insuffisante. Cette baisse de la perfusion, associée à la tachycardie, à la dysfonction diastolique et à la PIP comprimant les vaisseaux coronaires, rend le myocarde particulièrement vulnérable à l'ischémie. Il en résulte une réponse vagale importante, une bradycardie et un choc cardiogénique répondant mal aux cathécolamines et à la réanimation cardio-respiratoire, malgré un drainage rapide de l'épanchement péricardique. Le décès est alors difficilement évitable. [4]
L'effet de la tamponnade sur les diverses chambres cardiaques sera discutée plus longuement à la section sur les trouvailles échographiques.
Présentation clinique
Questionnaire
Les symptômes de l'épanchement péricardique sont non spécifiques. Conséquemment, il faut garder un haut indice de suspicion pour le suspecter et le diagnostiquer. L'établissement de la chronologie et la recherche d'un élément déclencheur ou d'une étiologies sont aussi importants. On recherche [2]:
- la dyspnée
- des étourdissements
- des épisodes de syncope ou de lipothymie
- une altération de l'état de conscience
- de la fièvre
- des palpitations
- la douleur thoracique pleurétique ou de pression thoracique, pouvant être aigüe, sub-aigüe ou chronique selon la cause de la tamponnade.
Examen clinique
L'examen physique ciblé à la recherche d'une tamponnade cardiaque n'est ni sensible ni spécifique. Classiquement, il est possible de retrouver une triade de Beck[Se: 0.41 %[14]], soit l'hypotension artérielle, la distension des veines jugulaires et une diminution des bruits cardiaques. Étant donné la faible sensibilité de cette triade, son utilité est limitée.
À l'examen physique, on recherchera les éléments suivants :
- aux signes vitaux (Éliminer une tamponnade cardiaque) [2][3][15]:
- l'hypotension artérielle
- le pulsus paradoxus [note 5]
- la tachycardie
- la tachypnée[note 6]
- la fièvre (selon l'étiologie suspectée)
- à l'examen du cou (Éliminer une tamponnade cardiaque) à la recherche de :
- à l'examen cardiaque (Éliminer une tamponnade cardiaque)
- à l'examen pulmonaire (Éliminer une tamponnade cardiaque)
- des signes de surcharge pulmonaire, par exemple des crépitants.
Examens paracliniques
Bilan sanguin
Lors de la présentation initiale, le bilan sanguin comprendra :
- la FSC à la recherche d'une leucocytose
- les électrolytes, incluant la calcémie et la magnésémie
- la créatinine et l'urée
- pouvant être toutes deux augmentées dans le contexte d'une péricardite urémique
- la protéine C réactive et l'élévation des marqueurs inflammatoires orientant vers une étiologie inflammatoire
- les troponines :
- une élévation oriente vers des dommages myocardiques et est un marqueur de gravité de la condition
- un gaz sanguin, des lactates, une glycémie sérique, un INR/TCA, un bilan hépatique, notamment en présence d'un choc à l'examen clinique.
À la recherche de l'étiologie, les laboratoires suivants peuvent être demandés :
- les sérologies pour le VIH
- les anticorps anti-nucléaires (ANA) et le facteur rhumatoïde (FR)
- les hémocultures, notamment lorsqu'on pense à un abcès périvalvulaire secondaire à une endocardite infectieuse
- les peptides natriurétiques (BNP / NT-proBNP).

ECG
L'électrocardiogramme montrant :
- une tachycardie sinusale
- des QRS de basse amplitude
- un pattern d'alternance électrique à l'ECG, signe de balancement du coeur au sein de l'épanchement péricardique au rythme des battements
- un abaissement du PR dans toutes les dérivations.

Il est également pertinent de rechercher les signes électrocardiographiques de la péricardite (élévation concave diffuse du segment ST et abaissement diffus du PR lors de la phase aiguë).
Radiographie thoracique
La radiographie thoracique à laquelle on peut retrouver un élargissement de la silhouette cardiaque avec un index cardio-thoracique augmentée (> 0.6) à la vue postéro-antérieure (PA). Cette trouvaille est plus fréquente en contexte d'épanchement progressif permettant une certaine accommodation de l'enveloppe péricardique et nécessite > 200 mL de fluide pour produite une image de cardiomégalie. Les plages pulmonaires sont le plus souvent claires. [16]
En contexte d'urgence, les vues antéro-postérieures (AP) obtenues sont peu fiables pour identifier l'élargissement médiastinal.

Échocardiogramme
L'échocardiogramme permet de mettre en évidence un épanchement péricardique et ses répercussions sur la physiologie cardiaque. L'échochardiographie par voie trans-thoracique (ETT) est la modalité d'imagerie la plus couramment employée. Elle permet notamment de montrer l'épanchement péricardique, d'en apprécier l'étendue et de donner une idée sur la nature du fluide. [2]
- Une petite quantité de liquide sera contenue au niveau du sillon auriculo-ventriculaire postérieur, tandis qu'un épanchement massif enveloppera le coeur.
- La quantité de liquide peut être estimée selon la distance séparant les feuillets péricardiques en diastole :
- petit (< 10mm) = 300 mL
- modéré (10-20mm) = 500 mL
- grand ( > 20mm) > 700 mL.
Elle permet notamment l'étude de l'impact hémodynamique de l'épanchement péricardique.
- En présence d'un pattern classique de swinging heart, la présence concomitante d'un compromis hémodynamique oriente vers la tamponnade cardiaque. [17]
- Lorsque l'épanchement est moins volumineux, les images bi-dimensionnelles permettent de retrouver certains signes cliniques :
- un collapsus en fin de diastole de l'oreillette droite[Se: 0.50-1.00 %[18]][Sp: 0.33-1.00 %[19]] (vue apicale quatre chambres ou sous-costale)[note 9]
- Cependant, un collapsus de l'oreillette droite > 1/3 du cycle cardiaque est hautement suggestive d'une tamponnade cardiaque, avec une sensibilité de 94% et une spécificité de 100%. [4]
- un collapsus ventriculaire droit en début ou au milieu de la diastole[Se: 0.48-1.00 %[20]][Sp: 0.72-1.00 %[21]] (vue sous-costale ou parasternale court axe)
- un collapsus de l'oreillette gauche[Se: 0.13 %[22]][Sp: 0.98 %[23]] retrouvé chez 13-25% des patients qui est hautement spécifique d'une tamponnade
- un déplacement du septum interventriculaire vers le ventricule gauche lors de l'inspiration et vers le ventricule droit lors de l'expiration (vue apicale quatre chambres)
- une veine cave inférieure fixe et dilatée[Se: 0.97 %[24]][Sp: 0.40 %[25]] (vue sous-costale).
- un collapsus en fin de diastole de l'oreillette droite[Se: 0.50-1.00 %[18]][Sp: 0.33-1.00 %[19]] (vue apicale quatre chambres ou sous-costale)[note 9]
Si l'épanchement est loculé et en regard du coeur gauche, ou encore s'il y a présence d'une hypertension pulmonaire concomitante, alors un collapsus de l'oreillette gauche ou rarement du ventricule gauche peut être objectivé. Un oedème pulmonaire cardiogénique est alors probable. [17][26]

L'utilisation du mode doppler permet l'identification de signes indiquant une faible réserve hémodynamique :
- alors que la variabilité de la vélocité du flot au niveau des valves cardiaques selon les phases inspiratoires est normalement < 20%, en contexte de tamponnade, on peut retrouver :
- une augmentation du flot cardiaque au travers des valves tricuspides et pulmonaires de plus de 40-50%
- une diminution du flot cardiaque au sein des valves cardiaques gauches de plus de 25-40%.
- un ratio E/A inversé au niveau tricuspidien ou mitral
- Oriente vers une perte de la compliance ventriculaire
- un pattern adiastolique au niveau des veines sus-hépatiques caractérisé par une composante systolique prédominante et la nette diminution des ondes diastoliques. [17][26]
L'ETT a finalement un rôle dans l'évaluation et l'exécution d'un drainage percutané. [17]
Analyse du liquide péricardique
À la suite de la péricardiocentèse ou d'un drainage chirurgical, le liquide prélevé sera envoyé à des fins d'analyse. Les examens pouvant être effectués :
- l'examen macroscopique
- le décompte cellulaire (rarement déterminant pour guider le diagnostic)[note 10]
- la culture bactérienne et la coloration de Gram
- la cytologie
- l'amplification en chaîne par polymérase (PCR)
- certaines analyses pour certaines mycobactéries, tuberculose, etc.
- la biopsie du péricarde (approche chirurgicale seulement). [27]
Autres investigations
Dans certains cas, notamment lorsqu'on suspecte une atteinte myocardique, une tomodensitométrie (TDM) ou une IRM cardiaque peuvent être obtenus. La TDM peut aussi servir à étudier un épanchement loculé en vue de prévoir son drainage. [2][16]
Lorsqu'un monitoring cardiaque invasif est en place (tel une voie veineuse centrale, une canule artérielle ou un cathéter de Swan-Ganz), on peut utiliser les valeurs obtenues pour identifier :
- un pulsus paradoxus
- l'absence d'onde Y de la pression veineuse jugulaire (PVJ) et l'élévation de la PVJ
- la pression des diverses chambres cardiaques, et parfois même utiliser des techniques de thermodilution pour estimer le débit cardiaque. [4]
Diagnostic
Le diagnostic de la tamponnade cardiaque repose sur l'histoire et les trouvailles typiques à l'examen physique - qui sont peu spécifiques, mais qui permettent d'évoquer le diagnostic. Les examens paracliniques, étant généralement facilement accessibles en temps opportuns, permettent de poser le diagnostic rapidement et d'orienter la prise en charge.
Une littérature grandissante a démontré que les médecins de première ligne ayant reçu une formation adéquate en échographie ciblée parviennent à identifier cette condition avec une sensibilité de 96% et une spécificité de 98%, comparativement aux cardiologues. Il s'agit définitivement d'un facteur favorisant l'identification rapide de cette condition dont la prise en charge urgente diminue la morbidité et la mortalité. [26]
Une hypotension réfractaire en contexte post-opératoire de chirurgie cardiothoracique nécessite inévitablement une échographie cardiaque afin d'éliminer une tamponnade cardiaque iatrogénique. [4]
Diagnostic différentiel
Le diagnostic différentiel inclut notamment les entités cliniques pouvant entraîner des choc cardiogéniques ou obstructifs. Le causes de douleurs thoraciques, de dyspnée, d'augmentation de la TVC et d'anasarque doivent également être considérés dans le diagnostic différentiel [2][16]:
- l'embolie pulmonaire
- le pneumothorax sous tension
- la péricardite constrictive
- la dissection aortique
- l'infarctus myocardique
- l'insuffisance cardiaque congestive
- la cirrhose hépatique avec décompensation oedémato-ascitique, ou encore compliquée d'un syndrome cardio-hépatique ou hépato-rénal
- l'ulcère gastro-duodénal
- la gastrite
- l'oesophagite.
Traitement
La prise en charge de la tamponnade cardiaque repose sur le drainage urgent de l'épanchement causant la tamponnade. Le choix de traitement reposera sur l'estimation de la pression intrapéricardique, ainsi que le volume, la chronicité et la présence ou l'absence de loculation de l'épanchement. On tiendra compte également des comorbidités du patient et de l'étiologie probable. [4]
Il y a urgence d'intervenir, indépendamment de la taille de l'épanchement, si on retrouve une tachycardie, une tachypnée, un pulsus paradoxus, et des critères de tamponnade à l'échographie en mode doppler. [4]
Traitement de support ou de réanimation
Dans certains cas, et dans l'attente de pouvoir procéder au drainage de l'épanchement péricardique, on peut recourir à des traitements de support. Les principes à employer visent à obtenir un statut cardiovasculaire « fast, full and tight ». Il en découle les principes suivants :
- la pré-charge : s'assurer d'un bon retour veineux avec une pré-charge optimale
- la contractilité myocardiaque : maintenir et éviter la dépression myocardique
- la fréquence cardiaque : maintenir, voire l'augmenter
- le rythme : conserver à tout prix un rythme sinusal
- les résistances vasculaires systémiques : maintenir ou augmenter, pour favoriser le retour veineux et éviter le collapsus du coeur droit. [28][29]
Pour ce faire, les interventions suivantes doivent être envisagées.
- Une réplétion volémique est nécessaire lorsqu'en présence d'une hypovolémie.
- L'objectif est de renverser le collapsus du coeur droit en favorisant le retour veineux malgré une pression auriculaire droite élevée. Ses effets sont toutefois mitigés.
- Elle permet une amélioration de l'index cardiaque > 10% (jugée significative) chez seulement 48% des patients. En contrepartie, une diminution non cliniquement significative de l'index cardiaque chez 31% des patients.
- Facteur prédictif d'une réponse appropriée = TAsystolique < 100 mmHg.
- Si une réplétion volémique est tentée, de petits volumes sont recommandés tout en surveillant étroitement la réponse hémodynamique. [17]
- Il est possible de suivre la compressibilité de la veine cave inférieure (VCI) et de donner des bolus jusqu'à ce qu'elle ne soit plus compressible. [4]
- Il est strictement contrindiqué d'administrer des diurétiques IV en raison du risque important de diminution de la pré-charge et ainsi du risque de décès. [30]
- L'objectif est de renverser le collapsus du coeur droit en favorisant le retour veineux malgré une pression auriculaire droite élevée. Ses effets sont toutefois mitigés.
- L'administration de vasopresseurs est à considérer. [17] La norépinéphrine est le premier choix.[note 11]
- Il faut éviter la ventilation à pression positive (VPP) en raison de la diminution associée du retour veineux. [28] Une intubation pourrait précipiter un arrêt cardiaque.
Traitement de la condition
Deux avenues existent, soient la péricardiocentèse et la péricardiotomie chirurgicale.
| Procédure | Description |
|---|---|
| péricardiocentèse |
|
| péricardiotomie chirurgicale |
|
Complications
Lorsque laissé non traité, la tamponnade cardiaque évoluera probablement de façon défavorable. L'évolution est souvent frustre lorsque les mécanismes compensatoires sont dépassés : un réflexe vaso-vagal réfractaire (bradycardie, vasodilatation) peut s'installer et ainsi entraîner un échec de la réanimation cardio-respiratoire malgré un drainage de l'épanchement (concept du « last drop »). Un signe clinique précurseur est l'absence de flot à l'oreillette droite lors de l'expiration visualisée à l'échocardiogramme en mode doppler des veines sus-hépatiques.
Il en résulte alors :
- un choc obstructif ou un choc cardiogénique
- un arrêt cardiaque, se soldant le plus souvent par le décès. [4][31]
Évolution
L'évolution de la tamponnade cardiaque, une fois résolue, varie beaucoup selon l'étiologie. Le prise en charge devrait ainsi être orientée vers le traitement de l'étiologie, et la prévention des récidives. Dans le contexte d'épanchement réfractaire aux traitements médicaux, alors une péricardiotomie chirurgicale avec création d'une fenêtre pleuro-péricardique devrait être envisagée de façon élective. [2]
Prévention
La prévention des récidives reposera notamment sur le contrôle de l'étiologie de la tamponnade. Elle peut inclure :
- pour les péricardites idiopathiques ou d'étiologie inflammatoire : les anti-inflammatoires non stéroïdiens (AINS), la colchicine, les corticostéroïdes ou d'autres agents immunosuppresseurs
- pour la péricardite urémique : la prévention de l'urémie et l'hémodialyse
- pour les épanchements péricardiques récidivants : la mise en place d'une fenêtre péricardique
- etc. [2][17][32]
Pour plus d'informations selon les étiologies spécifiques, se référer à la page sur les épanchements péricardiques.
Notes
- ↑ Via un phénomène de myxoedème.
- ↑ Pouvant être considéré comme une cause auto-immune, en raison du développement d'anticorps contre les antigènes myocardiques exposés lors de l'infarctus.
- ↑ Devant être de classification de De Bakey de type 1 ou 2 (atteignant l'aorte ascendante)
- ↑ Via l'induction d'une cardiomyopathie
- ↑ Diminution de plus de 10 mmHg de pression systolique lors de l'inspiration (normalement < 5%). Cette baisse de la TA est causée par l'augmentation du retour veineux au coeur droit avec un déplacement conséquent du septum interventriculaire vers la gauche, ce qui entraîne une diminution du volumeproto-systolique du VG (en début de systole) et donc une diminution du volume d'éjection du ventricule gauche lors de la phase inspiratoire de la respiration.
- ↑ En raison de la production accrue de CO2 et de lactates
- ↑ Une augmentation de la pression veineuse jugulaire lors de l'inspiration.
- ↑ On perd les frottements péricariques en présence d'une tamponnade puisque l'accumulation liquidienne empêche désormais le frottement des feuillets péricardiques.
- ↑ Le collapsus des cavités cardiaques droites peut aussi être retrouvé en contexte d'hypovolémie importante ou d'épanchement pleural volumineux.
- ↑ Les critères de Light ne devraient pas être utilisés pour identifier la cause de l'épanchement péricardique
- ↑ La norépinéphrine permet de maintenir la fréquence cardiaque, comparativement à l'épinéphrine qui peut l'augmenter beaucoup, ce qui n'est pas l'idéal dans cette situation.
Références
- Cette page a été modifiée ou créée le 2020/11/07 à partir de Acute Cardiac Tamponade (StatPearls / Acute Cardiac Tamponade (2020/08/15)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/30521227 (livre).
- ↑ Scott Kahan et Bimal H. Ashar, In a page. Medicine, Wolters Kluwer Health/Lippincott Williams & Wilkins, (ISBN 978-0-7817-7035-4 et 0-7817-7035-1, OCLC 222134574, lire en ligne)
- ↑ 2,0 2,1 2,2 2,3 2,4 2,5 2,6 2,7 2,8 et 2,9 Nitish K. Sharma et James R. Waymack, StatPearls, StatPearls Publishing, (PMID 30521227, lire en ligne)
- ↑ 3,0 et 3,1 Eric Stashko et Jehangir M. Meer, StatPearls, StatPearls Publishing, (PMID 28613742, lire en ligne)
- ↑ 4,00 4,01 4,02 4,03 4,04 4,05 4,06 4,07 4,08 4,09 4,10 4,11 4,12 4,13 et 4,14 Christopher Appleton, Linda Gillam et Konstantinos Koulogiannis, « Cardiac Tamponade », Cardiology Clinics, vol. 35, no 4, , p. 525–537 (ISSN 1558-2264, PMID 29025544, DOI 10.1016/j.ccl.2017.07.006, lire en ligne)
- ↑ (en) Massimo Imazio et Fiorenzo Gaita, « Acute and Recurrent Pericarditis », Cardiology Clinics, vol. 35, no 4, , p. 505–513 (DOI 10.1016/j.ccl.2017.07.004, lire en ligne)
- ↑ « UpToDate », sur www.uptodate.com (consulté le 10 janvier 2021)
- ↑ 7,0 et 7,1 (en) Laurent Bodson, Koceïla Bouferrache et Antoine Vieillard-Baron, « Cardiac tamponade: », Current Opinion in Critical Care, vol. 17, no 5, , p. 416–424 (ISSN 1070-5295, DOI 10.1097/MCC.0b013e3283491f27, lire en ligne)
- ↑ 8,0 et 8,1 (en) Shomron Ben-Horin, Ilan Bank, Victor Guetta et Avi Livneh, « Large Symptomatic Pericardial Effusion as the Presentation of Unrecognized Cancer: A Study in 173 Consecutive Patients Undergoing Pericardiocentesis », Medicine, vol. 85, no 1, , p. 49–53 (ISSN 0025-7974, DOI 10.1097/01.md.0000199556.69588.8e, lire en ligne)
- ↑ Matthew J. Snyder, Jennifer Bepko et Merima White, « Acute pericarditis: diagnosis and management », American Family Physician, vol. 89, no 7, , p. 553–560 (ISSN 1532-0650, PMID 24695601, lire en ligne)
- ↑ Massimo Imazio, Fiorenzo Gaita et Martin LeWinter, « Evaluation and Treatment of Pericarditis: A Systematic Review », JAMA, vol. 314, no 14, , p. 1498–1506 (ISSN 1538-3598, PMID 26461998, DOI 10.1001/jama.2015.12763, lire en ligne)
- ↑ Matthew N. Van Dam et Brian M. Fitzgerald, StatPearls, StatPearls Publishing, (PMID 29493917, lire en ligne)
- ↑ (en) Terrence D. Welch et Jae K. Oh, « Constrictive Pericarditis », Cardiology Clinics, vol. 35, no 4, , p. 539–549 (DOI 10.1016/j.ccl.2017.07.007, lire en ligne)
- ↑ Massimo Imazio et Yehuda Adler, « Management of pericardial effusion », European Heart Journal, vol. 34, no 16, , p. 1186–1197 (ISSN 1522-9645, PMID 23125278, DOI 10.1093/eurheartj/ehs372, lire en ligne)
- ↑ 10.1016/0736-4679(88)90017-0
- ↑ Mena Yacoub, Bryan S. Quintanilla Rodriguez et Kunal Mahajan, StatPearls, StatPearls Publishing, (PMID 30137863, lire en ligne)
- ↑ 16,0 16,1 et 16,2 « UpToDate », sur www.uptodate.com (consulté le 19 février 2021)
- ↑ 17,0 17,1 17,2 17,3 17,4 17,5 17,6 17,7 et 17,8 Laurent Bodson, Koceïla Bouferrache et Antoine Vieillard-Baron, « Cardiac tamponade », Current Opinion in Critical Care, vol. 17, no 5, , p. 416–424 (ISSN 1531-7072, PMID 21716107, DOI 10.1097/MCC.0b013e3283491f27, lire en ligne)
- ↑ 26746413
- ↑ 26746413
- ↑ 26746413
- ↑ 26746413
- ↑ 26746413
- ↑ 26746413
- ↑ 26746413
- ↑ 26746413
- ↑ 26,0 26,1 et 26,2 Elisa Ceriani et Chiara Cogliati, « Update on bedside ultrasound diagnosis of pericardial effusion », Internal and Emergency Medicine, vol. 11, no 3, , p. 477–480 (ISSN 1970-9366, PMID 26746413, DOI 10.1007/s11739-015-1372-8, lire en ligne)
- ↑ « UpToDate », sur www.uptodate.com (consulté le 10 mai 2021)
- ↑ 28,0 et 28,1 Arthur Atchabahian, The anesthesia guide, McGraw-Hill Medical, (ISBN 978-0-07-177207-5 et 0-07-177207-3, OCLC 841486320, lire en ligne)
- ↑ (en) « Anesthetic Considerations of Cardiac Tamponade », sur considerations (consulté le 12 mars 2021)
- ↑ « Cardiac tamponade - Clinical overview », sur Clinical Key, (consulté le 12 mars 2021)
- ↑ (en) Mark J. Kearns et Keith R. Walley, « Tamponade: Hemodynamic and Echocardiographic Diagnosis », CHEST, vol. 153, no 5, , p. 1266–1275 (ISSN 0012-3692, PMID 29137910, DOI 10.1016/j.chest.2017.11.003, lire en ligne)
- ↑ Massimo Imazio et Fiorenzo Gaita, « Diagnosis and treatment of pericarditis », Heart (British Cardiac Society), vol. 101, no 14, , p. 1159–1168 (ISSN 1468-201X, PMID 25855795, DOI 10.1136/heartjnl-2014-306362, lire en ligne)
