Hémothorax
| Maladie | |||
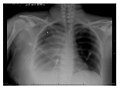
 Radiographie pulmonaire d'un hémothorax droit massif | |||
| Caractéristiques | |||
|---|---|---|---|
| Signes | Pneumothorax, Hématome, Insuffisance respiratoire, Pression veineuse jugulaire, Extrémités froides, Tachycardie , Tachypnée , Tamponnade cardiaque, Emphysème sous-cutané, Fracture costale, ... [+] | ||
| Symptômes |
Dyspnée , Douleur thoracique | ||
| Diagnostic différentiel |
Pneumothorax, Empyème, Mésothéliome, Chylothorax, Tamponnade cardiaque, Épanchement pleural | ||
| Informations | |||
| Terme anglais | Hemothorax | ||
| Wikidata ID | Q369073 | ||
| SNOMED CT ID | 31892009 | ||
| Spécialités | Médecine d'urgence, Chirurgie thoracique, Soins intensifs, Traumatologie, Chirurgie générale, Pneumologie | ||
| |||
L'hémothorax est une accumulation de sang (hématocrite > 50%) dans l'espace pleural, un espace potentiel entre les plèvres viscérale et pariétale.
Épidémiologie
Les atteintes thoraciques surviennent dans environ 60 % des cas de polytraumatismes et sont responsables de 20 à 25 % des décès par traumatisme.[1] 30 à 50 % des patients souffrant d'une sévère agression thoracique présentent une contusion pulmonaire, un pneumothorax et un hémothorax concomitants.[2]
Étiologies
Il existe trois catégories étiologiques d'hémothorax :
- les traumatismes thoraciques contondants sont les plus fréquents, suivi par les traumatismes traumatismes thoraciques pénétrants ; ces deux mécanismes traumatiques regroupe la majeure partie des hémothorax
- les hémothorax spontanés (séquestration pulmonaire, vasculaire, néoplasie, coagulopathies, cataménial et processus infectieux)
- l'iatrogénie.
Physiopathologie
Les saignements dans l'hémithorax peuvent provenir de blessures diaphragmatiques, médiastinales, pulmonaires, pleurales, de la paroi thoracique et de l'abdomen. Les saignements peuvent provenir de vaisseaux de la paroi thoracique, des artères mammaires internes, des artères intercostales, des gros vaisseaux, du médiastin, du myocarde, du parenchyme pulmonaire, du diaphragme ou de l'abdomen.
Chaque hémithorax peut contenir 40 % du volume sanguin circulant d'un patient. La réponse physiologique précoce d'un hémothorax comporte des composantes hémodynamiques et respiratoires.
La gravité de la réponse physiologique dépend de la localisation de la lésion, de la réserve fonctionnelle du patient, du volume de sang et de la vitesse d'accumulation dans l'hémithorax.[3][4][5] Dans la réponse précoce, l'hypovolémie aiguë entraîne une diminution de la précharge, une dysfonction du ventricule gauche et une diminution du débit cardiaque. Le sang dans l'espace pleural affecte la capacité vitale fonctionnelle du poumon en créant une hypoventilation alvéolaire, un décalage V/Q et un shunt anatomique. Un hémothorax important peut entraîner une augmentation de la pression hydrostatique qui exerce une pression dans la veine cave et le parenchyme pulmonaire, entraînant une diminution de la précharge et une augmentation de la résistance vasculaire pulmonaire. Ces mécanismes entraînent une physiologie de l'hémothorax sous tension et provoquent une instabilité hémodynamique, un collapsus cardiovasculaire et la mort.
En cas d'hémothorax non traité ou résiduel, il existe une réponse tardive qui comprend des risques d'infections augmentées, une cicatrisation anormale qui peut mener au fibrothorax. En effet, l'hémothorax résiduel est une complication qui se produit lorsque le sang reste trop longtemps dans la cavité plurale, diminuant ainsi la capacité vitale fonctionnelle. Le sang peut coaguler et être difficile à retirer par un cathéter ou par un drain thoracique. Le sang qui reste trop longtemps peut se surinfecter par translocation ou contamination par les drains et devenir un empyème. Les membranes pleurales et le tissu pulmonaire sont également plus enclins à se cicatriser en cas d'hémothorax non traité. Avec le temps, cela peut conduire à une fibrose de ces tissus entraînant un fibrothorax.
Présentation clinique
Facteurs de risque
Les facteurs de risque de développer un hémothorax sont :
- un mécanisme traumatique à haute énergie[3] :
- la prise d'anticoagulants et d'antiaggrégants plaquettaires.
Questionnaire
Outre les autres plaintes en lien avec le traumatisme, le patient avec un hémothorax se plaindra généralement d'une douleur thoracique et de la dyspnée.
Lorsque le patient n'est pas en mesure de répondre aux questions, le mécanisme traumatique peut être questionné auprès des services préhospitaliers ou des témoins.
Étant donné que la majorité des hémothorax sont d'origine thoraciques, le questionnaire sera généralement calqué sur l'ATLS.
Examen clinique
À l'examen physique, les signes à rechercher lors d'un hémothorax sont[1] :
- aux signes vitaux et à l'apparence générale du patient, rechercher des signes de choc hémorragique, de tamponnade cardiaque ou d'insuffisance respiratoire (tachycardie, hypotension artérielle, hypoxie, tachypnée, extrémités froides, remplissage capillaire augmenté, RHJ augmenté, TVC augmentée, etc.)
- à l'examen pulmonaire :
- rechercher des hématomes thoraciques et des plaies pénétrantes thoraciques
- à l'auscultation, l'hémothorax se manifestera surtout par une diminution du murmure vésiculaire du côté atteint
- rechercher des atteintes concomitantes (pneumothorax, emphysème sous-cutané, fracture costale, volet thoracique)
- faire l'ensemble de l'examen standard du patient traumatisé (ATLS)
Examens paracliniques
Examens de laboratoire
Le bilan recommandé pour un hémothorax comprend:[3]
- une FSC qui pourrait révéler une anémie (en aiguë, l'anémie peut être absente même si le saignement est volumineux)
- les électrolytes
- la calcémie (particulièrement si un protocole de transfusion massive est envisagé)
- l'INR/TCA
- une créatininémie
- une troponine avec un électrocardiogramme s'il y a un contexte de traumatisme thoracique (contusion myocardique)
- un gaz et des lactates sériques pour dépister un choc hémorragique secondaire à l'hémothorax.
Imageries
| Modalité d'imagerie | Commentaires |
|---|---|
| Angiotomodensitométrie thoracique |
|
| Tomodensitométrie thoracique C+ |
|
| Échographie thoracique[Se: 67 %][Sp: 99 %][10] |
|
| Radiographie pulmonaire[Se: 54 %][Sp: 99 %][10] |
|
-
Radiographie d'un hémothorax droit
-
TDM thoracique montrant un hémothorax du côté droit, un épanchement pleural gauche et un épanchement péricardique.
-
Le sang "soulève" les poumons en emplissant l'espace pleural, suite à une intoxication aux anti-coagulants.
-
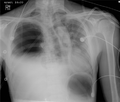
Radiographie pulmonaire montrant un hémopneumothorax sous tension du côté droit.
-
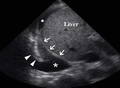
Image échographique d'une grande collection de liquide (*) vue ici au-dessus du diaphragme (flèches) autour du lobe inférieur droit effondré (pointes de flèches). Notez également le liquide intra-abdominal libre (étoile blanche).
-
L'image échographique d'un épanchement pleural est caractérisée par un espace anéchoique (noire) entre les plèvres viscérale et pariétale.
Diagnostic
Dans un contexte traumatique, l'hémothorax est suspecté cliniquement (mécanisme, traumatisme thoracique, dyspnée), puis confirmé radiologiquement (échographie, TDM, RXP).
Dans un contexte non traumatique, l'hémothorax est suspecté radiologiquement, puis confirmé lors de l'analyse du liquide pleural.
Diagnostic différentiel
Certaines conditions cliniques qui peuvent se présenter similairement à un hémothorax sont [1]:
- un pneumothorax
- un épanchement pleural
- un empyème
- un mésothéliome
- un chylothorax
- une tamponnade cardiaque.
Traitement
Prise en charge médicale
| Modalité thérapeutique | Explications |
|---|---|
| Désanticoagulation |
|
| Analgésie |
|
| Antifibrinolytique |
|
| Transfusion sanguine |
|
| ATLS |
|
| Maladie sous-jacente |
|
Prise en charge chirurgicale
Une collection minime de sang (définie comme inférieure à 300 mL) dans la cavité pleurale ne nécessite généralement aucun traitement chirurgical ; le sang se résorbe en quelques semaines. Si le patient est stable et ne présente pas de détresse respiratoire majeure, une intervention chirurgicale n'est généralement pas nécessaire. Si l'hémothorax n'est pas drainé, on peut répéter une imagerie après 4 à 6 heures et 24 heures.[12]
| Modalité thérapeutique | Explications |
|---|---|
| Drain thoracique |
|
| Thoracotomie d'urgence | Les indications d'une intervention chirurgicale par thoracotomie d'urgence comprennent :
|
| Chirurgie thoracoscopique vidéo-assistée
(VATS) |
|
| Embolisation artérielle transcathéter |
|
| Thrombolytique intrapleural |
|
-
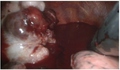
Détection peropératoire d'une tumeur pleurale hémorragique entourée d'un hémothorax massif
-
La thoracoscopie montre des hémorragies sous-pleurales au niveau des côtes T3 et T4 gauches ainsi qu'une pénétration de la plèvre entre les côtes T4 et T5 gauches.
-
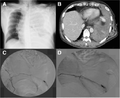
(A) Hémothorax sous tension gauche à la radiographie pulmonaire (B) Saignement dans l'espace thoracique à partir d'une branche de l'artère phrénique inférieure gauche à la TDM. (C) Fuite de produit de contraste dans l'espace thoracique à l'angiographie de l'artère phrénique gauche. (D) Saignement réduit post-embolisation.
-
Radiographie du thorax montrant en a) un hémothorax gauche et une silhouette cardiaque élargie et en b) un hémothorax résiduel et une silhouette cardiaque élargie persistante après le drainage par tube pleural
Suivi
Après le drainage de l'hémothorax, le suivi intrahospitalier inclut :
- la quantité de sang drainé via le drain thoracique (quantifié en cc/h)
- une radiographie thoracique après la pose du drain thoracique puis périodiquement ensuite
- le suivi de l'hémoglobine.
Complications
Les complications de l'hémothorax sont :
- le choc hémorragique
- l'anémie ferriprive
- l'insuffisance respiratoire
- la tamponnade cardiaque (compression du médiastin par l'hémothorax)
- l'empyème[note 2]
- le fibrothorax[note 3].
Le caillot résiduel (défini comme une collection non drainée de 500 mL ou plus) est une séquelle bien connue après une thoracostomie initiale par tube pour hémothorax et doit être évacué tôt dans le parcours hospitalier du patient, si l'état clinique le permet. Il pourra être estimée par tomodensitométrie [TDM] ou une opacification d'un tiers ou plus du thorax sur la radiographie thoracique. Une intervention précoce dans le cas d'un caillot retenu peut être réalisée par thoracoscopie, à condition que l'opération soit planifiée dans la semaine suivant l'épisode hémorragique, sinon les risques opératoires sont augmentés.
Évolution
La morbidité et la mortalité de l'hémothorax traumatique sont corrélées à la gravité de la blessure et aux personnes à risque de complications tardives, à savoir l'empyème et le fibrothorax/poumon piégé ; de même qu'aux autres blessures du patient polytraumatisé. Les patients présentant un hémothorax retenu risquent de développer un empyème, ce qui entraîne un séjour prolongé en soins intensifs ou à l'hôpital. Il est donc important de suivre l'état du patient.[13]
De plus, le pronostic du patient dépend également de l'origine de l'hémothorax et peut parfois signer une détérioration de la condition clinique comme dans le cas des néoplasies.
Les hémothorax résultant d'un mécanisme contondant auraient une mortalité globale de 9,4%[14].
Prévention
L'origine de l'hémothorax peut être très diversifiée et la prévention de l'hémothorax passe par la prévention de chacune de ces conditions. Cependant, l'étiologie la plus fréquente de l'hémothorax étant les traumatismes, des études montrent que l'absence de dispositifs de retenue et l'affaiblissement des facultés du conducteur sont les principaux facteurs contribuant aux blessures graves dans les accidents de la route.[15][16] Les prestataires de soins de santé devraient encourager l'adoption de mesures de sécurité telles que le port de la ceinture de sécurité, l'évitement de la conduite en état d'ébriété et les stratégies de transport alternatives.[17][18][19]
Note
- ↑ Insérer le drain plus bas augmente les risques de traumatismes d'organes abdominaux. En effet, l'espace thoracique est souvent contracté par la douleur et l'hypoventilation.
- ↑ Un placement inadéquat du drain thoracique peut entraîner un drainage insuffisant de l'hémothorax, ce qui favorise la formation d'un empyème. Il y aurait une incidence de 26,8 % d'empyème chez les patients présentant un hémothorax retenu post-traumatique.
- ↑ Le fibrothorax résulte d'un dépôt de fibrine dans l'espace pleural. Un drainage inadéquat de l'hémothorax provoque un revêtement inflammatoire dans l'espace pleural entraînant une compression pulmonaire avec altération de la fonction pulmonaire, notamment une diminution de la capacité vitale fonctionnelle.
Références
- Cette page a été modifiée ou créée le 2021/05/26 à partir de Hemothorax (StatPearls / Hemothorax (2020/08/10)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/30855807 (livre).
- Cet article a été créé en partie ou en totalité le 2021/07/11 à partir de Chirurgie (application), créée par Dre Hélène Milot, Dr Olivier Mailloux et collaborateurs et partagé sous la licence CC-BY-SA 4.0 international
- ↑ 1,0 1,1 1,2 1,3 et 1,4 Laura Pumarejo Gomez et Vu H. Tran, StatPearls, StatPearls Publishing, (PMID 30855807, lire en ligne)
- ↑ Mehmet Sirmali, Hasan Türüt, Salih Topçu et Erkmen Gülhan, « A comprehensive analysis of traumatic rib fractures: morbidity, mortality and management », European Journal of Cardio-Thoracic Surgery: Official Journal of the European Association for Cardio-Thoracic Surgery, vol. 24, no 1, , p. 133–138 (ISSN 1010-7940, PMID 12853057, DOI 10.1016/s1010-7940(03)00256-2, lire en ligne)
- ↑ 3,0 3,1 et 3,2 Eric J. Morley, Scott Johnson, Evan Leibner et Jawad Shahid, « Emergency department evaluation and management of blunt chest and lung trauma (Trauma CME) », Emergency Medicine Practice, vol. 18, no 6, , p. 1–20 (ISSN 1559-3908, PMID 27177417, lire en ligne)
- ↑ Yi-Pin Chou, Hsing-Lin Lin et Tzu-Chin Wu, « Video-assisted thoracoscopic surgery for retained hemothorax in blunt chest trauma », Current Opinion in Pulmonary Medicine, vol. 21, no 4, , p. 393–398 (ISSN 1531-6971, PMID 25978625, Central PMCID 5633323, DOI 10.1097/MCP.0000000000000173, lire en ligne)
- ↑ M. F. Scott, R. A. Khodaverdian, J. L. Shaheen et A. L. Ney, « Predictors of retained hemothorax after trauma and impact on patient outcomes », European Journal of Trauma and Emergency Surgery: Official Publication of the European Trauma Society, vol. 43, no 2, , p. 179–184 (ISSN 1863-9941, PMID 26619854, DOI 10.1007/s00068-015-0604-y, lire en ligne)
- ↑ A. Brooks, B. Davies, M. Smethhurst et J. Connolly, « Emergency ultrasound in the acute assessment of haemothorax », Emergency medicine journal: EMJ, vol. 21, no 1, , p. 44–46 (ISSN 1472-0213, PMID 14734374, Central PMCID 1756377, DOI 10.1136/emj.2003.005438, lire en ligne)
- ↑ Paul-André C. Abboud et John Kendall, « Emergency department ultrasound for hemothorax after blunt traumatic injury », The Journal of Emergency Medicine, vol. 25, no 2, , p. 181–184 (ISSN 0736-4679, PMID 12902006, DOI 10.1016/s0736-4679(03)00168-9, lire en ligne)
- ↑ Kirsty McEwan et Peter Thompson, « Ultrasound to detect haemothorax after chest injury », Emergency medicine journal: EMJ, vol. 24, no 8, , p. 581–582 (ISSN 1472-0213, PMID 17652688, Central PMCID 2660093, DOI 10.1136/emj.2007.051334, lire en ligne)
- ↑ Leonardo Jönck Staub, Roberta Rodolfo Mazzali Biscaro, Erikson Kaszubowski et Rosemeri Maurici, « Chest ultrasonography for the emergency diagnosis of traumatic pneumothorax and haemothorax: A systematic review and meta-analysis », Injury, vol. 49, no 3, , p. 457–466 (ISSN 1879-0267, PMID 29433802, DOI 10.1016/j.injury.2018.01.033, lire en ligne)
- ↑ 10,0 et 10,1 Vafa Rahimi-Movaghar, Mahmoud Yousefifard, Parisa Ghelichkhani et Masoud Baikpour, « Application of Ultrasonography and Radiography in Detection of Hemothorax; a Systematic Review and Meta-Analysis », Emergency (Tehran, Iran), vol. 4, no 3, , p. 116–126 (ISSN 2345-4563, PMID 27299139, Central PMCID 4902204, lire en ligne)
- ↑ « UpToDate », sur www.uptodate.com (consulté le 6 septembre 2023)
- ↑ 12,0 et 12,1 (en) Nathan T. Mowery, Oliver L. Gunter, Bryan R. Collier et Jose' J. Diaz, « Practice Management Guidelines for Management of Hemothorax and Occult Pneumothorax », Journal of Trauma: Injury, Infection & Critical Care, vol. 70, no 2, , p. 510–518 (ISSN 0022-5282, DOI 10.1097/TA.0b013e31820b5c31, lire en ligne)
- ↑ Timothy Gleeson et David Blehar, « Point-of-Care Ultrasound in Trauma », Seminars in ultrasound, CT, and MR, vol. 39, no 4, , p. 374–383 (ISSN 1558-5034, PMID 30070230, DOI 10.1053/j.sult.2018.03.007, lire en ligne)
- ↑ Stephen R. Broderick, « Hemothorax: Etiology, diagnosis, and management », Thoracic Surgery Clinics, vol. 23, no 1, , p. 89–96, vi–vii (ISSN 1558-5069, PMID 23206720, DOI 10.1016/j.thorsurg.2012.10.003, lire en ligne)
- ↑ T. Bunn, M. Singleton et I.-Chen Chen, « Use of multiple data sources to identify specific drugs and other factors associated with drug and alcohol screening of fatally injured motor vehicle drivers », Accident; Analysis and Prevention, vol. 122, , p. 287–294 (ISSN 1879-2057, PMID 30396030, DOI 10.1016/j.aap.2018.10.012, lire en ligne)
- ↑ Mengtao Zhu, Yunjie Li et Yinhai Wang, « Design and experiment verification of a novel analysis framework for recognition of driver injury patterns: From a multi-class classification perspective », Accident; Analysis and Prevention, vol. 120, , p. 152–164 (ISSN 1879-2057, PMID 30138770, DOI 10.1016/j.aap.2018.08.011, lire en ligne)
- ↑ Emily Morgan, « Driving Dilemmas: A Guide to Driving Assessment in Primary Care », Clinics in Geriatric Medicine, vol. 34, no 1, , p. 107–115 (ISSN 1879-8853, PMID 29129210, DOI 10.1016/j.cger.2017.09.006, lire en ligne)
- ↑ Liisa Ecola, Steven W. Popper, Richard Silberglitt et Laura Fraade-Blanar, « The Road to Zero: A Vision for Achieving Zero Roadway Deaths by 2050 », Rand Health Quarterly, vol. 8, no 2, , p. 11 (ISSN 2162-8254, PMID 30323994, Central PMCID 6183773, lire en ligne)
- ↑ Guang-Ming Han, Ashley Newmyer et Ming Qu, « Seatbelt use to save money: Impact on hospital costs of occupants who are involved in motor vehicle crashes », International Emergency Nursing, vol. 31, , p. 2–8 (ISSN 1878-013X, PMID 27177737, DOI 10.1016/j.ienj.2016.04.004, lire en ligne)