Pneumothorax
| Classe de maladie | |||
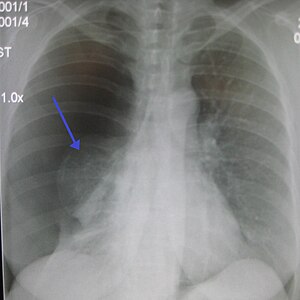 Un important pneumothorax primaire droit, la flèche montre le poumon collabé | |||
| Caractéristiques | |||
|---|---|---|---|
| Signes | Tachycardie , Tirage , Tachypnée , Emphysème sous-cutané, Diminution du murmure vésiculaire unilatérale, Diminution des vibrations vocales unilatérale, Tympanisme thoracique, Diminution de l’amplitude thoracique ipsilatérale, Augmentation du volume thoracique ipsilatéral, Déviation de la trachée du côté ipsilatéral, ... [+] | ||
| Symptômes |
Dyspnée , Douleur à l'épaule, Douleur thoracique , Toux , Douleur pleurétique , Asymptomatique | ||
| Étiologies |
Maladie pulmonaire obstructive chronique, Cause idiopathique, Néoplasie pulmonaire, Endométriose, Fibrose kystique, Fistule bronchopulmonaire, Ventilation à pression positive, Biopsie pulmonaire à l'aiguille, Cathétérisme veineux central, Perforation oesophagienne, ... [+] | ||
| Informations | |||
| Wikidata ID | Q203601 | ||
| Spécialités | Pneumologie, chirurgie générale, chirurgie thoracique | ||
| |||
Un pneumothorax est défini comme une accumulation d'air à l'extérieur du poumon mais à l'intérieur de la cavité pleurale.[1]
Épidémiologie
Le pneumothorax spontané primaire survient principalement entre 20 et 30 ans. Son incidence aux États-Unis est de 7 pour 100 000 hommes et de 1 pour 100 000 femmes par an [2]. La majorité des récidives surviennent au cours de la première année et l'incidence de celles-ci varie largement de 25% à 50%. Le taux de récidive est le plus élevé au cours des 30 premiers jours. [1]
Le pneumothorax spontané secondaire est plus observé chez les patients âgés de 60 à 65 ans. Son incidence est de 6,3 pour 1000 000 hommes et 2 pour 100 000 femmes. Le ratio homme/femme est de 3:1.[1]
L'incidence du pneumothorax iatrogène est de 5 pour 10 000 admissions à l'hôpital.[1] Il survient plus fréquemment que le pneumothorax spontané[1], et son incidence est directement proportionnelle au nombre de procédures invasives effectuées[3].
L'incidence du pneumothorax sous tension est difficile à déterminer car un tiers des cas dans les centres de traumatologie présentaient des thoracostomies à l'aiguille de décompression avant d'arriver à l'hôpital, et tous n'étaient pas atteints de pneumothorax sous tension.[1]
Étiologies
Il est possible de classifier les pneumothorax selon leur étiologie. [1]
- Le pneumothorax spontané primaire (PSP) survient lorsque le patient n'a pas d'antécédents de maladie pulmonaire sous-jacente (idiopathique).
- Il se produit chez les jeunes grands et minces en raison de forces de cisaillement accrues ou d'une pression plus négative à l'apex du poumon.
- Le pneumothorax spontané secondaire (PSS) est associé à des antécédents de maladie pulmonaire sous-jacente (MPOC, fibrose kystique, pneumonie, néoplasie pulmonaire, fistule bronchopulmonaire).[4][5]
- Un pneumothorax traumatique peut être le résultat d'un traumatisme thoracique contondant ou pénétrant.[1]
- Il est possible de subdiviser cette classe en pneumothorax traumatique fermé et ouvert. Le pneumothorax est ouvert s'il y a communication entre l'espace pleural et l'extérieur du poumon.
- Le pneumothorax iatrogène survient en raison d'une complication d'une procédure médicale ou chirurgicale.
- Toute intervention à proximité de l'abdomen et en particulier du thorax, peut provoquer un pneumothorax iatrogène (biopsie pulmonaire à l'aiguille, cathétérisme veineux central, ventilation à pression positive)[5][1][6].
- Le pneumothorax sous tension survient lorsque la pression à l'intérieur de la cavité thoracique augmente et cause un état de choc obstructif. Ce type de pneumothorax fera l'objet d'une page à part.
- Il y a également des causes plutôt rares et qui ne sont pas inclut dans la classification ci-haut :
- le pneumothorax par perforation oesophagienne
- le pneumothorax cataménial[7] (secondaire à l'endométriose thoracique).
La notion de pneumothorax occulte [8] existe également. Cette classification ne correspond pas à une étiologie particulière : il est défini comme un pneumothorax visible au TDM, mais non visible à la radiographie pulmonaire[8]. Un pneumothorax occulte peut aussi se présenter comme un pneumothorax résiduel suite à un drainage pleural par tube de thoracostomie qui est visible au TDM, mais non-visible à la radiographie pulmonaire[8]
Les pneumothorax peuvent être aussi classés comme simples, sous tension ou ouverts. Cette classification n'est pas en fonction de l'étiologie, mais elle est tout de même importante à mentionner.
- Un pneumothorax simple ne déplace pas les structures médiastinales comme le fait un pneumothorax sous tension.
- Le pneumothorax sous tension survient le plus souvent dans les services de soins intensifs, chez les patients ventilés à pression positive, il survient lorsque la pression dans l'espace pleural est positive tout au long du cycle respiratoire[5].
- Le pneumothorax ouvert est une plaie ouverte dans la paroi thoracique à travers laquelle l'air entre et sort.[1]
Physiopathologie
Le gradient de pression à l'intérieur du thorax change avec un pneumothorax. Normalement, la pression de l'espace pleural est négative par rapport à la pression atmosphérique. Lorsque la paroi thoracique se dilate vers l'extérieur, le poumon se dilate également vers l'extérieur en raison de la tension superficielle entre les plèvre pariétale et viscérale. Les poumons ont tendance à s'affaisser en raison du recul élastique.[1]
Lorsqu'il y a communication entre les alvéoles et l'espace pleural, l'air s'accumule entre les plèvres pariétale et viscérale à l'intérieur de la poitrine, ce qui change le gradient de pression à l'intérieur du thorax.[1] L'accumulation d'air exerce une pression sur le poumon et celui-ci s'affaisse. Le degré d'affaissement du poumon détermine la présentation clinique du pneumothorax.
L'air peut pénétrer dans l'espace pleural par deux mécanismes [1]:
- par un traumatisme provoquant une communication à travers la paroi thoracique
- par le poumon par rupture de la plèvre viscérale.
Le pneumothorax spontané est un processus multifactoriel et a été associé à des augmentations de la pression transpulmonaire et à des anomalies de la plèvre viscérale. L'inflammation pulmonaire et le stress oxydatif sont essentiels à la pathogenèse du pneumothorax spontané primaire. Les fumeurs actifs ont une augmentation des cellules inflammatoires dans les petites voies respiratoires et courent donc un risque accru de pneumothorax.D es augmentations aiguës de la pression alvéolaire qui dépassent la pression interstitielle pulmonaire peuvent entraîner une rupture alvéolaire et une fuite d'air pleural. En outre, des points de faiblesse dans la plèvre viscérale dus à des bulles sous-pleurales, des bulles, une nécrose pulmonaire et d'autres anomalies du tissu conjonctif peuvent prédisposer les alvéoles à se rompre dans les deux types de pneumothorax spontané, bien que le mécanisme exact de la façon dont cela ne soit pas entièrement compris. Des bulles intactes sans défaut explicite de la plèvre viscérale se sont avérées associées à un pneumothorax spontané; cependant, les analyses histopathologiques et les études au microscope électronique à balayage des tissus obtenus à partir de thoracotomies suggèrent que la desquamation des cellules pleurales mésothéliales peut jouer un rôle significatif dans le développement du pneumothorax spontané.[9][10][7][1]
Le pneumothorax spontané primaire se produit chez les jeunes grands et minces en raison de forces de cisaillement accrues ou d'une pression plus négative à l'apex du poumon.
Le pneumothorax spontané secondaire survient le plus fréquemment en raison de la rupture de bulles d'emphysème asymptomatiques.
Les pneumothorax traumatiques peuvent résulter d'un traumatisme contondant ou pénétrant, ceux-ci créent souvent une valve unidirectionnelle dans l'espace pleural (laissant l'air entrer mais pas sortir) et donc un compromis hémodynamique.[1]
Présentation clinique
Facteurs de risque
| Type | Facteurs de risque |
|---|---|
| Pneumothorax spontané primaire | |
| Pneumothorax spontané secondaire |
|
| Pneumothorax iatrogène |
|
| Pneumothorax traumatique | |
| Pneumothorax occulte |
|
Questionnaire
Le pneumothorax peut être totalement asymptomatique, surtout chez les patients en bonne santé qui subisse un pneumothorax spontané primaire. Par contre, voici les éléments à rechercher au questionnaire [7][1]:
- une douleur thoracique unilatérale à caractère pleurétique (légère à sévère)
- la douleur est parfois rétrosternale
- une douleur thoracique qui irradie à l'épaule ipsilatérale
- une toux sèche[18]
- une dyspnée d'apparition subit, de légère à sévère[note 4].
Examen clinique
Chez les patients présentant un pneumothorax plus petit, l'examen peut être normal.
À l'examen physique d'un pneumothorax plus important (plus de 15% de l'hémithorax), les constatations suivantes peuvent être notées [1][19]:
- aux signes vitaux : de la tachypnée, de la tachycardie, de la désaturation, une tension artérielle normale (si le pneumothorax n'est pas sous tension)
- à l'examen cardiaque : normal, TVC normale
- à l'examen pulmonaire :
- une diminution du murmure vésiculaire unilatérale
- une diminution de l’amplitude thoracique ipsilatérale, mais augmentation du volume thoracique ipsilatéral[note 5]
- une déviation de la trachée du côté ipsilatéral (contro-latéral dans le cas d'un pneumothorax sous-tension)
- une diminution des vibrations vocales unilatérale
- du tympanisme thoracique à la percussion
- de l'emphysème sous-cutané (quasi-pathognomonique)
- l'utilisation des muscles respiratoires accessoires (tirage intercostal, sus-sternal, sous-costal) dans les pneumothorax les plus importants.
Examens paracliniques
Laboratoires
Les examens de laboratoire suivants sont pertinents pour le pneumothorax lorsqu'une procédure est indiquée :
D'autres examens de laboratoire peuvent s'ajouter en fonction du diagnostic différentiel. Un gaz capillaire peut être indiqué si le patient est dyspnéique.
Imageries
| Modalité | Signes paracliniques et commentaires |
|---|---|
| Radiographie pulmonaire[Se: 83 %] [20](inspiration/expiration) |
|
| Échographie thoracique[Se: 90.9 %[21]][Sp: 98.2 %[22]][LR+: 50.5[23]][LR-: 0.09[24]] |
|
| Tomodensitométrie thoracique |
|
Approche clinique
Lorsqu'un patient se présente avec une douleur thoracique pleurétique unilatérale ainsi que de la dyspnée, il convient de suspecter un pneumothorax. Il est alors important de s'informer auprès du patient d'antécédents personnels ou familiaux de pneumothorax ainsi que de la présence ou non de maladie pulmonaire sous-jacente. Il est aussi important de suspecter un pneumothorax chez un patient aux soins intensifs ayant eu un cathétérisme veineux central, une biopsie pulmonaire ou une ventilation à pression positive. À l'examen physique, tachycardie, diminution du murmure vésiculaire unilatérale et emphysème sous-cutané orientent fortement vers un pneumothorax. De plus, il faut rester à l'affût de signes tels que trachée déviée, hypotension, hypoxémie et distension veineuse jugulaire qui sont indicateurs de pneumothorax sous tension, ce qui nécessite une prise en charge urgente.
Afin de confirmer la suspicion clinique, l'imagerie de choix est une radiographie pulmonaire. Un décollement de la ligne pleurale à l'apex est observée avec une hyperclarté indiquant un espace dépourvu de marques pulmonaires. Un TDM thoracique peut aussi être effectué, particulièrement chez les patients traumatisés, afin de vérifier la présence d'un pneumothorax occulte. Un gaz artériel est aussi fait afin d'évaluer les possibles conséquences d'un pneumothorax.
Diagnostic
Le diagnostic de pneumothorax spontané repose d'abord sur une suspicion clinique à l'histoire et l'examen physique, mais est confirmé par imagerie.[4][5] La radiographie thoracique, l'échographie ou la tomodensitométrie peuvent être utilisées pour le diagnostic, bien que le diagnostic à partir d'une radiographie pulmonaire soit plus courant.[1] Le diagnostic est posé lorsqu'on objective un décollement pleural par une modalité d'imagerie.
Diagnostic différentiel
Le diagnostic différentiel de pneumothorax comprend [1][28]:
- l'aspiration
- la pneumonie
- la dissection aortique
- le syndrome coronarien aigu (STEMI, NSTEMI, angine instable)
- l'embolie pulmonaire
- la péricardite aiguë
- le spasme œsophagien
- la rupture œsophagienne
- la fracture des côtes
- l'hémothorax
- l'épanchement pleural
- la pleurésie.
Traitement
Immédiat
La prise en charge dépend du scénario clinique.[1]
- Il faut d'abord déterminer si le patient est stable ou instable.[29]
- Le traitement a priorité sur l'imagerie.
- L'étiologie probable du pneumothorax doit être déterminé.
- En général, pour les patients avec un pneumothorax minime et sans compromis hémodynamique, une simple observation est acceptable: le patient doit rester au repos et une radiographie de contrôle est faite.
- Si le patient est instable hémodynamiquement, la thoracostomie à l'aiguille ou au doigt est habituellement nécessaire.
- De l'oxygène par ventimask 100 % est utile chez la majorité des patients pour une période de 4-6h. Ceci augmente la vitesse de résorption du pneumothorax.[30][31][32][33][note 6]
| Sous-type de pneumothorax | Traitement |
|---|---|
| Pneumothorax spontané primaire | Premier épisode
Épisodes subséquents[33]
|
| Pneumothorax spontané secondaire[35][30][31][32][33] | Guide de pratique de la British Thoracic Society 2010
|
| Pneumothorax traumatique |
|
| Pneumothorax iatrogène | Le traitement du pneumothorax iatrogène consiste en [12]:
Chez tous les patients ventilés mécaniquement, la thoracostomie est nécessaire. |
| Pneumothorax occulte |
|
| Femme enceinte[12] |
|
| Fibrose kystique[12] |
|
| Pneumothorax sous tension |
Intervention chirurgicale
Il existe deux types d'approche chirurgicale pour le pneumothorax lorsqu'indiqué : la chirurgie thoracique vidéo-assistée (VATS) ou la thoracotomie. Ces deux approches se sont avérés être une mesure efficace dans le traitement et la prévention de la récidive spontanée de pneumothorax.[33]
Les indications de l'intervention chirurgicale comprennent [1]:
- une fuite d'air continue pendant plus de 5-7 jours[12]
- des pneumothorax bilatéraux
- le premier épisode chez un patient ayant un profession à haut risque (plongeurs, pilotes)
- la récidive de pneumothorax ipsilatéral
- le pneumothorax en controlatéral[12]
- les patients atteints du SIDA[1]
- l'hémothorax spontané[12]
- la grossesse[12].
La chirurgie consiste en une bullectomie, une pleurectomie et une pleurodèse.[33] Il existe deux types de pleurodèse [1].
| Procédure | Détails | Récidive |
|---|---|---|
| Pleurectomie', bullectomie et pleurodèse mécanique'[12] |
|
|
| Pleurodèse chimique |
|
|
Suivi
Pour un petit pneumothorax spontané primaire asymptomatique (profondeur généralement inférieure à 2 cm) pour lequel aucun traitement invasif n'est nécessaire, un suivi en ambulatoire est fait après 2 à 4 semaines.[1]
Complications
La complication la plus notable de tout pneumothorax est le pneumothorax sous tension[36]. Cette complication met la vie en danger du patient et nécessite une intervention immédiate.
Les complications possibles d'un pneumothorax sont [1]:
- l'insuffisance respiratoire ou l'arrêt respiratoire
- l'arrêt cardiaque
- l'empyème
- le pneumopéricarde
- le pneumopéritoine
- l'hémothorax
- le pneumothorax persistant.
Évolution
Le pneumothorax spontané primaire (PSP) est généralement bénin et se résout principalement de lui-même sans aucune intervention majeure. La récidive peut survenir jusqu'à trois ans, mais le risque est le plus élevé au cours du premier mois[37][28]. Le taux de récidive dans les cinq années suivantes est de 30% pour les PSP et de 43% pour les PSS. Le risque de récidive augmente avec chaque pneumothorax subséquent; il est de 30% avec le premier, 40% après un deuxième et plus de 50% après la troisième récurrence. Le pneumothorax spontané primaire n'est pas considéré comme une menace majeure pour la santé, mais des décès ont été signalés.[1]
Les pneumothorax spontanés secondaires (PSS) sont plus mortels, tout dépendant de la maladie pulmonaire sous-jacente et de la taille du pneumothorax. Les patients atteints de MPOC et du VIH ont une mortalité élevée après un pneumothorax. Le taux de mortalité du pneumothorax spontané secondaire est de 10%.[1]
La mortalité due au pneumothorax sous tension est élevée si les mesures appropriées ne sont pas prises. [1]
Un pneumothorax à Pneumocystis jiroveci ou carinii (chez un patient portant du VIH) a un haut taux de récidive et de fuite persistante ainsi qu'une mortalité élevée.[12]
Prévention
Les patients atteints de pneumothorax doivent être informés qu'ils ne doivent pas voyager par avion ou dans des régions éloignées avant la résolution complète du pneumothorax, soit pour un minimum de deux semaines après la résolution de leur pneumothorax. Si le transport aérien est nécessaire, une sonde de thoracostomie doit être placée avant le transport.[1] Chez les patients qui ont subi une thoracostomie, il est sécuritaire pour eux de voler dès 72 heures après le retrait de la sonde sans risque accru de récidive.[37][28]
Les patients ayant des professions à haut risque comme les plongeurs sous-marins et les pilotes doivent être informés qu'ils ne doivent pas plonger ou voler tant que la prise en charge chirurgicale définitive de leur pneumothorax n'est pas terminée. Les patients ayant des antécédents connus de pneumothorax spontané ne doivent pas être médicalement autorisés à exercer des activités de vol ou de plongée sous-marine[1]. Le pneumothorax est donc une contre-indication formelle à la plongée sous-marine sauf si le patient a subi une pleurectomie bilatérale et qu'il y a eu confirmation de la résolution complète de leur pneumothorax par un TDM thoracique.[12]
Il est conseillé à tous les patients d'arrêter de fumer. Ils devraient être évalués pour leur volonté d'arrêter de fumer; ils doivent être éduqués et recevoir une pharmacothérapie s'ils décident d'arrêter.[1]
L'aggravation de l'emphysème sous-cutané peut être associée à une mauvaise position d'un drain thoracique, c'est pourquoi un repositionnement avec un nouveau drain thoracique est recommandé. La thoracostomie ne doit jamais être réinsérée car cela peut augmenter le risque d'empyème pour le patient.[1]
Notes
- ↑ Pneumothorax spontané = 1 non fumeur pour 102 fumeurs.
- ↑ Le pneumothorax chez un patient portant du VIH est souvent associé à pneumocystis jiroveci ou carinii.
- ↑ Six erreurs techniques courantes au cours de cette procédure peuvent entraîner un pneumothorax : 1) une identification inadéquate du repère 2) une mauvaise position d'insertion 3) l'insertion de l'aiguille à travers le périoste 4) une trajectoire trop peu profonde avec l'aiguille 5) une trajectoire de l'aiguille à angle céphalique excessif 6) le fait de ne pas maintenir l'aiguille en place pour le passage du fil.
- ↑ En général, la dyspnée est plus légère chez le patient avec un pneumothorax spontané primaire (sans maladie pulmonaire sous-jacente) tandis que la dyspnée est plus fréquemment sévère chez le patient atteint d'un pneumothorax spontané secondaire (avec maladie pulmonaire sous-jacente) en raison d'une diminution de la réserve pulmonaire.
- ↑ Il y a augmentation du volume thoracique ipsilatéralement, mais le volume thoracique varie beaucoup moins.
- ↑ L'air peut être réabsorbé de l'espace pleural à un taux de 1,5% / jour; l'utilisation d'oxygène supplémentaire peut augmenter ce taux de réabsorption.
Références
- Cet article a été créé en partie ou en totalité le 2021/01/30 à partir de Chirurgie (application), créée par Dre Hélène Milot, Dr Olivier Mailloux et collaborateurs et partagé sous la licence CC-BY-SA 4.0 international
- Cette page a été modifiée ou créée le 2020/11/09 à partir de Iatrogenic Pneumothorax (StatPearls / Iatrogenic Pneumothorax (2020/08/10)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/30252313 (livre).
- Cette page a été modifiée ou créée le 2020/11/09 à partir de Pneumothorax (StatPearls / Pneumothorax (2020/08/11)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/28722915 (livre).
- Cette page a été modifiée ou créée le 2020/11/09 à partir de Spontaneous Pneumothorax (StatPearls / Spontaneous Pneumothorax (2020/07/26)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/29083723 (livre).
- ↑ 1,00 1,01 1,02 1,03 1,04 1,05 1,06 1,07 1,08 1,09 1,10 1,11 1,12 1,13 1,14 1,15 1,16 1,17 1,18 1,19 1,20 1,21 1,22 1,23 1,24 1,25 1,26 1,27 1,28 1,29 1,30 1,31 1,32 1,33 1,34 1,35 et 1,36 Catherine L. McKnight et Bracken Burns, StatPearls, StatPearls Publishing, (PMID 28722915, lire en ligne)
- ↑ L. J. Melton, N. G. Hepper et K. P. Offord, « Incidence of spontaneous pneumothorax in Olmsted County, Minnesota: 1950 to 1974 », The American Review of Respiratory Disease, vol. 120, no 6, , p. 1379–1382 (ISSN 0003-0805, PMID 517861, DOI 10.1164/arrd.1979.120.6.1379, lire en ligne)
- ↑ B. Celik, E. Sahin, A. Nadir et M. Kaptanoglu, « Iatrogenic pneumothorax: etiology, incidence and risk factors », The Thoracic and Cardiovascular Surgeon, vol. 57, no 5, , p. 286–290 (ISSN 1439-1902, PMID 19629891, DOI 10.1055/s-0029-1185365, lire en ligne)
- ↑ 4,0 et 4,1 Muhammad A. Baig, Muhammad B. Majeed, Bashar M. Attar et Zubair Khan, « Efficacy and Safety of Indwelling Pleural Catheters in Management of Hepatic Hydrothorax: A Systematic Review of Literature », Cureus, vol. 10, no 8, , e3110 (ISSN 2168-8184, PMID 30338185, Central PMCID 6175258, DOI 10.7759/cureus.3110, lire en ligne)
- ↑ 5,0 5,1 5,2 5,3 5,4 et 5,5 Jafet A. Ojeda Rodriguez et John E. Hipskind, StatPearls, StatPearls Publishing, (PMID 30252313, lire en ligne)
- ↑ Andrea Loiselle, James M. Parish, James A. Wilkens et Dawn E. Jaroszewski, « Managing iatrogenic pneumothorax and chest tubes », Journal of Hospital Medicine, vol. 8, no 7, , p. 402–408 (ISSN 1553-5606, PMID 23765922, DOI 10.1002/jhm.2053, lire en ligne)
- ↑ 7,00 7,01 7,02 7,03 7,04 7,05 7,06 7,07 7,08 7,09 et 7,10 John Costumbrado et Sassan Ghassemzadeh, StatPearls, StatPearls Publishing, (PMID 29083723, lire en ligne)
- ↑ 8,0 8,1 8,2 8,3 8,4 8,5 et 8,6 Chad G. Ball, Andrew W. Kirkpatrick et David V. Feliciano, « The occult pneumothorax: what have we learned? », Canadian Journal of Surgery. Journal Canadien De Chirurgie, vol. 52, no 5, , E173–179 (ISSN 1488-2310, PMID 19865549, Central PMCID 2769131, lire en ligne)
- ↑ Steven P. Walker, Anna C. Bibby, Paul Halford et Louise Stadon, « Recurrence rates in primary spontaneous pneumothorax: a systematic review and meta-analysis », The European Respiratory Journal, vol. 52, no 3, (ISSN 1399-3003, PMID 30002105, DOI 10.1183/13993003.00864-2018, lire en ligne)
- ↑ Luca Bertolaccini, Maria Teresa Congedo, Alessandro Bertani et Piergiorgio Solli, « A project to assess the quality of the published guidelines for managing primary spontaneous pneumothorax from the Italian Society of Thoracic Surgeons », European Journal of Cardio-Thoracic Surgery: Official Journal of the European Association for Cardio-Thoracic Surgery, vol. 54, no 5, 11 01, 2018, p. 920–925 (ISSN 1873-734X, PMID 29788194, DOI 10.1093/ejcts/ezy199, lire en ligne)
- ↑ D. Gupta, A. Hansell, T. Nichols et T. Duong, « Epidemiology of pneumothorax in England », Thorax, vol. 55, no 8, , p. 666–671 (ISSN 0040-6376, PMID 10899243, Central PMCID 1745823, DOI 10.1136/thorax.55.8.666, lire en ligne)
- ↑ 12,00 12,01 12,02 12,03 12,04 12,05 12,06 12,07 12,08 12,09 12,10 12,11 12,12 12,13 12,14 12,15 12,16 12,17 12,18 12,19 12,20 12,21 12,22 et 12,23 M Henry, T Arnold et J Harvey, « BTS guidelines for the management of spontaneous pneumothorax », Thorax, vol. 58, no Suppl 2, , ii39–ii52 (ISSN 0040-6376, PMID 12728149, Central PMCID 1766020, DOI 10.1136/thorax.58.suppl_2.ii39, lire en ligne)
- ↑ 13,0 et 13,1 Lisa Shieh, Minjoung Go, Daniel Gessner et Jonathan H. Chen, « Improving and sustaining a reduction in iatrogenic pneumothorax through a multifaceted quality-improvement approach », Journal of Hospital Medicine, vol. 10, no 9, , p. 599–607 (ISSN 1553-5606, PMID 26041246, Central PMCID 5548000, DOI 10.1002/jhm.2388, lire en ligne)
- ↑ 14,0 et 14,1 Michael J. Kilbourne, Grant V. Bochicchio, Thomas Scalea et Yan Xiao, « Avoiding common technical errors in subclavian central venous catheter placement », Journal of the American College of Surgeons, vol. 208, no 1, , p. 104–109 (ISSN 1879-1190, PMID 19228511, DOI 10.1016/j.jamcollsurg.2008.09.025, lire en ligne)
- ↑ Sunil Kumar Garg, Pragya Garg, Nidhi Anchan et Ashish Jaiswal, « Iatrogenic Bilateral Simultaneous Pneumothorax: Call for Vigilance », Indian Journal of Critical Care Medicine: Peer-Reviewed, Official Publication of Indian Society of Critical Care Medicine, vol. 21, no 9, , p. 607–609 (ISSN 0972-5229, PMID 28970663, Central PMCID 5613615, DOI 10.4103/ijccm.IJCCM_108_17, lire en ligne)
- ↑ Alberto A. Arteaga, Kristen D. Pitts et Andrea F. Lewis, « Iatrogenic pneumothorax during hypoglossal nerve stimulator implantation », American Journal of Otolaryngology, vol. 39, no 5, , p. 636–638 (ISSN 1532-818X, PMID 29941192, DOI 10.1016/j.amjoto.2018.06.014, lire en ligne)
- ↑ Rumi Tagami, Takashi Moriya, Kosaku Kinoshita et Katsuhisa Tanjoh, « Bilateral tension pneumothorax related to acupuncture », Acupuncture in Medicine: Journal of the British Medical Acupuncture Society, vol. 31, no 2, , p. 242–244 (ISSN 1759-9873, PMID 23449179, DOI 10.1136/acupmed-2012-010284, lire en ligne)
- ↑ Bates, Barbara, (1928- ...).,, Szilagyi, Peter G. (médecin),, Babinet, Paul, et Retbi, Jean-Marc,, Guide de l'examen clinique, Arnette, impr. 2010 (ISBN 978-2-7184-1222-1 et 2-7184-1222-4, OCLC 690853376, lire en ligne)
- ↑ « UpToDate », sur www.uptodate.com (consulté le 5 janvier 2021)
- ↑ 20,0 et 20,1 M. Swierzy, M. Helmig, M. Ismail et J. Rückert, « [Pneumothorax] », Zentralblatt Fur Chirurgie, vol. 139 Suppl 1, , S69–86; quiz S87 (ISSN 1438-9592, PMID 25264729, DOI 10.1055/s-0034-1383029, lire en ligne)
- ↑ https://pubmed.ncbi.nlm.nih.gov/21868468/
- ↑ https://pubmed.ncbi.nlm.nih.gov/21868468/
- ↑ https://pubmed.ncbi.nlm.nih.gov/21868468/
- ↑ https://pubmed.ncbi.nlm.nih.gov/21868468/
- ↑ https://radiopaedia.org/articles/pneumothorax-ultrasound-1?lang=us
- ↑ https://radiopaedia.org/articles/pneumothorax-ultrasound-1?lang=us
- ↑ Hugh Scott, « Le pneumothorax, à qui de s'en occuper? », Le Médecin du Québec, (lire en ligne)
- ↑ 28,0 28,1 et 28,2 Jafet A. Ojeda Rodriguez et John E. Hipskind, StatPearls, StatPearls Publishing, (PMID 30252313, lire en ligne)
- ↑ Keegan Tupchong, « Update: Is Needle Aspiration Better Than Chest Tube Placement for the Management of Primary Spontaneous Pneumothorax? », Annals of Emergency Medicine, vol. 72, no 1, , e1–e2 (ISSN 1097-6760, PMID 29615265, DOI 10.1016/j.annemergmed.2018.02.025, lire en ligne)
- ↑ 30,0 30,1 30,2 et 30,3 Jost Schnell, Meinrad Beer, Stephan Eggeling et Wolfgang Gesierich, « Management of Spontaneous Pneumothorax and Post-Interventional Pneumothorax: German S3 Guideline », Respiration; International Review of Thoracic Diseases, vol. 97, no 4, , p. 370–402 (ISSN 1423-0356, PMID 30041191, DOI 10.1159/000490179, lire en ligne)
- ↑ 31,0 31,1 31,2 et 31,3 Amy Wong, Elena Galiabovitch et Krishna Bhagwat, « Management of primary spontaneous pneumothorax: a review », ANZ journal of surgery, vol. 89, no 4, , p. 303–308 (ISSN 1445-2197, PMID 29974615, DOI 10.1111/ans.14713, lire en ligne)
- ↑ 32,0 32,1 32,2 et 32,3 Conceição Santos, Saurabh Gupta, Melissa Baraket et Peter J. Collett, « Outcomes of an initiative to improve inpatient safety of small bore thoracostomy tube insertion », Internal Medicine Journal, vol. 49, no 5, , p. 644–649 (ISSN 1445-5994, PMID 30230151, Central PMCID 6851751, DOI 10.1111/imj.14110, lire en ligne)
- ↑ 33,0 33,1 33,2 33,3 33,4 33,5 33,6 33,7 et 33,8 John Costumbrado et Sassan Ghassemzadeh, StatPearls, StatPearls Publishing, (PMID 29083723, lire en ligne)
- ↑ (en) « Spontaneous pneumothorax - WikEM », sur wikem.org (consulté le 5 janvier 2021)
- ↑ (en) Andrew MacDuff, Anthony Arnold et John Harvey, « Management of spontaneous pneumothorax: British Thoracic Society pleural disease guideline 2010 », Thorax, vol. 65, no Suppl 2, , ii18–ii31 (ISSN 0040-6376 et 1468-3296, PMID 20696690, DOI 10.1136/thx.2010.136986, lire en ligne)
- ↑ Derek J. Roberts, Simon Leigh-Smith, Peter D. Faris et Christopher Blackmore, « Clinical Presentation of Patients With Tension Pneumothorax: A Systematic Review », Annals of Surgery, vol. 261, no 6, , p. 1068–1078 (ISSN 1528-1140, PMID 25563887, DOI 10.1097/SLA.0000000000001073, lire en ligne)
- ↑ 37,0 et 37,1 David Zonies, Joel Elterman, Christopher Burns et Vincent Paul, « Trauma patients are safe to fly 72 hours after tube thoracostomy removal », The Journal of Trauma and Acute Care Surgery, vol. 85, no 3, , p. 491–494 (ISSN 2163-0763, PMID 29782482, DOI 10.1097/TA.0000000000001976, lire en ligne)
