Épanchement pleural
| Classe de maladie | |
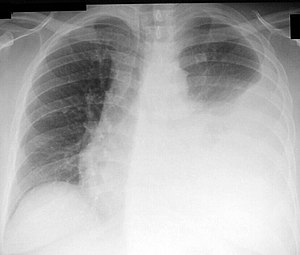 Épanchement pleural au poumon gauche | |
| Caractéristiques | |
|---|---|
| Signes | |
| Symptômes |
|
| Étiologies |
Embolie pulmonaire, Insuffisance cardiaque, Hypothyroïdie, Syndrome néphrotique, Dialyse péritonéale, Cirrhose hépatique |
| Informations | |
| Terme anglais | Pleural effusion |
| Autres noms | Effusion pleurale |
| Spécialités | Chirurgie thoracique, Pneumologie |
|
| |
Épanchement pleural (76)
L'épanchement pleural est l'accumulation de liquide dans la cavité pleurale, c'est-à-dire entre les plèvres viscérale et pariétale. Il peut survenir seul ou être le résultat d'une maladie localisée ou systémique comme une infection, une malignité ou des conditions inflammatoires[1].
Épidémiologie
L'épanchement pleural est la maladie la plus courante parmi toutes les pathologies pleurales, elle affecte 1,5 million de patients par an aux États-Unis.[2] Une grande variété d'affections peuvent se présenter avec des épanchements pleuraux comme des maladies impliquant principalement le poumon ou la plèvre, des désordres systémiques et même des maladies qui affectent principalement d'autres organes. [3][1]
Physiopathologie
Tous les humains en bonne santé ont une petite quantité de liquide pleural qui lubrifie l'espace et facilite les mouvements pulmonaires normaux pendant la respiration. La quantité de liquide pleural normale est d'environ 0,1 ml / kg à 0,3 ml/kg et est constamment échangée. Cet équilibre délicat de fluide est maintenu par la pression oncotique, la pression hydrostatique et le drainage lymphatique.
Le liquide pleural provient des vaisseaux des membranes pleurales et est absorbé par les lymphatiques dans les surfaces diaphragmatiques et médiastinales dépendantes de la plèvre pariétale. On pense que la pression hydrostatique des vaisseaux systémiques qui alimentent la plèvre pariétale entraîne le liquide interstitiel dans l'espace pleural, il y possède donc une teneur en protéines inférieure à celle du sérum. L'accumulation d'un excès de liquide peut se produire s'il y a une production excessive, une diminution de l'absorption ou si les deux phénomènes submergent le mécanisme homéostatique normal. [4][5][1]
Classification
Les épanchements pleuraux peuvent être classifiés selon leur contenu.
- Hydrothorax (liquide séreux)
- Hémothorax (sang)
- Chylothorax (chyle)
- Empyème (pus)
- Urinothorax (urine)
Ils peuvent également être classés selon s'ils sont d'une étiologie exsudative ou transsudative.
Étiologies
Le liquide pleural est classé comme transsudat ou exsudat sur la base des critères de Light modifiés. L'épanchement est considéré exsudatif si au moins un des critères est rempli.
Étiologies transsudatives
Le liquide pleural est qualifié de transsudat lorsqu'il traverse des parois vasculaires intactes pour rejoindre l'espace pleural. Ce processus est généralement causé par une augmentation de la pression hydrostatique ou une diminution de la pression oncotique.[6] L'épanchement pleural trassudatif entraîne généralement une atteinte bilatérale.
Par augmentation de la pression hydrostatique :
- insuffisance cardiaque congestive;
- Péricardite constrictive.
Par diminution de la pression oncotique :
Autres (peuvent aussi être des exsudats) :
- embolie pulmonaire;
- hypothyroïdisme (myxoedème);
- Atélectasie;
- Urinothorax.[7]
Étiologies exsudatives
Le liquide pleural est qualifié d'exsudat s'il s'échappe des vaisseaux sanguins et lymphatiques par des lésions dans ceux-ci. L'inflammation résulte en une fuite protéique. Un mouvement de liquide de l'espace péritonéal peut également entraîner un exsudat.[6]
- Étiologies infectieuses
- Pneumonie (épanchement parapneumonique);
- Empyème;
- Tuberculose;
- Infection virale, fongique ou parasitique;
- Abcès : infradiaphragmatique, hépatique, splénique;
- Hépatite;
- Cholécystite;
- Rupture spontanée de l'œsophage.
- Étiologies néoplasiques
- Carcinome pulmonaire;
- Lymphome et leucémies;
- Métastases : lésion primaire principalement du sein, ovaire, rein;
- Mésothéliome;
- Myélome.
- Étiologies inflammatoires
- Maladies auto-immunes :
- Polyarthrite rhumatoïde;
- Lupus érythémateux;
- Vasculites;
- Sarcoïdose.
- Embolie pulmonaire;
- Pancréatite;
- Pleurésie amiantosique.
- Maladies auto-immunes :
- Étiologies intra-thoraciques
- Atélectasie;
- Poumon trappé;
- Perforation oesophagienne.
- Étiologies intra-abdominales
- Pancréatite;
- Abcès sous-diaphragmatique;
- Syndrome de Meigs (ascite et hydrothorax associé avec le fibrome ovarien ou autre tumeur pelvienne).
- Étiologies traumatiques
- Hémothorax;
- Pneumothorax;
- Chylothorax;
- Iatrogénique.
- Autres étiologies
- Hypothyroïdie;
- Médicamenteux;
- Idiopathique.[8]
Présentation clinique
Questionnaire
L'épanchement pleural est souvent asymptomatique, surtout avec de petits volumes.[6] Toutefois, selon sa sévérité et son étiologie, on peut rechercher au questionnaire:
- dyspnée, orthopnée
- douleur pleurétique
- toux sèche sans expectoration
- Symptômes de la cause sous-jacente, par exemple :
- Fièvre lors d'origine infectieuse
- Symptômes B lors de néoplasie
- Autres symptômes de surcharge si insuffisance cardiaque.
Examen physique
À l'examen pulmonaire, les signes suivants pourront être recherchés:
- diminution du murmure vésiculaire du côté de l'épanchement;
- matité à la percussion
- asymétrie de l'amplitude respiratoire (diminution du côté de l'épanchement);
- diminution des vibrations vocales
- crépitants
- déviation de la trachée (du côté controlatéral)
- frottement pleural.
Un examen physique complet sera également nécessaire. Selon l'étiologie, d'autres trouvailles permettront d'orienter le diagnostic. En voici quelques exemples :
- stigmates de cirrhose;
- cachexie (cause néoplasique);
- signes de surcharge (distension veineuse jugulaire, œdème des membres inférieurs).
Examens paracliniques
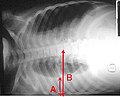
Radiographie pulmonaire
Cet examen est utilisé pour confirmer la présence de liquide pleural. L'épanchement pleural sera visible à l'angle costo-diaphragmatique (signe du ménisque) s'il est supérieur à 200 ml en antéro-postérieur ou 50 ml en latéral.[6] Lors de grands épanchements, on peut aussi noter :
- Opacification complète du poumon;
- Déviation controlatérale de la trachée et du médiastin.
-
En décubitus latéral, la lettre A indique le niveau de liquide tandis que la lettre B indique la largeur normale de la cavité thoracique
-
Épanchement parapneumonique
-
Épanchement bilatéral
TDM thoracique
Cette modalité diagnostique est plus sensible pour détecter un épanchement (jusqu'à 3-5 ml de liquide), mais moins utilisée que la radiographie en raison de la radiation et du contraste. Elle permet également d'évaluer le parenchyme pulmonaire et la plèvre pour déterminer la source de l'épanchement, mettre en évidence des loculations.[9]
-
Épanchement bilatéral
-
TDM démontrant un épanchement loculé
-
Hémothorax
-
Chylothorax
Thoracocenthèse diagnostique
La thoracenthèse est utilisée afin d'analyser le liquide pleural. Attention au risque d'œdème de réexpansion si plus de 1.5L est retiré!
Indications :
- L'épanchement est une nouvelle trouvaille;
- Épanchement unilatéral de >1 cm sur une radiographie;
- Historique de tumeur maligne avec un épanchement de >1 cm sur la radiographie;
- Pneumonie avec épanchement parapneumonique >5 cm sur la radiographie;
- Insuffisance cardiaque avec trouvailles atypiques (ex: douleur thoracique pleurétique, fièvre, épanchement unilatéral);
- Suspicion de transsudat avec trouvailles atypiques (ex : fièvre, douleur thoracique, asymétrie des épanchements). [6]
Les tests couramment effectués sur le liquide pleural pour déterminer l'étiologie sont une mesure du pH, des protéines, de l'albumine, de la LDH, du glucose, des triglycérides, du différentiel de numération des cellules, de la coloration et de la culture de Gram et de la cytologie des fluides.
Il n'y a pas de contre-indications absolues à la thoracocenthèse, mais il y a une contre-indication relative s'il y a une infection au site de ponction ou si le patient a une coagulopathie.
Critères de Light modifiés
Ces critères d'analyse du liquide pleural sont utilisés pour la classification d'un épanchement pleural en transsudat / exsudat. Lorsque l'un des critères suivant est rempli, la cause de l'épanchement pleural est probablement exsudative:[10]
- Le ratio protéines du liquide pleural / protéines du sérum > 0,5;
- Le ratio des LDH du liquide pleural / LDH du sérum > 0,6;
- Les LDH du liquide pleural sont de 0.6 fois la limite supérieur pour le sérum
Les critères de Light doivent être interprétés dans le contexte clinique car ils diagnostiquent à tort 20% des transsudats comme exsudatifs. Un exemple serait qu'un patient qui a subi une diurèse chronique pour une insuffisance cardiaque peut augmenter le niveau de protéines du liquide pleural et peut être classé comme un exsudat.[1]
Autres modalités diagnostiques
- Échographie thoracique: pour guider une thoracocentèse ou mettre en évidence un épanchement de petite taille;
- Biopsie pleurale: si l'on suspecte la tuberculose, un mésothéliome ou une néoplasie (et que la cytologie est négative).
Traitement
Un épanchement pleural asymptomatique ne nécessite généralement pas de traitement lui-même, car il se résorbe généralement spontanément lorsque l'on traite la cause sous-jacente. [7]
Thoracocenthèse thérapeutique
Le but de ce traitement est de retirer le liquide de la cavité pleurale. Habituellement, retirer 400-500 ml est suffisant pour soulager les symptômes, mais il est possible de retirer plus de liquide (ne faut pas oublier qu'il y a un risque d'œdème de réexpansion si plus de 1,5 L de liquide pleural est retiré).
Les indications pour une thoracocenthèse thérapeutique sont :
- Épanchements avec dyspnée ou décompensation cardiaque;
- Épanchement parapneumonique compliqué.
Si plusieurs drainages récidivants sont nécessaires, un cathéter pleural à demeure peut être installé pour éviter de ponctionner à répétition.[6]
Procédures chirurgicales
Pour les procédures suivantes, une consultation en chirurgie thoracique est requise. Une radiographie pulmonaire de contrôle devrait être demandée après chacune d'entre elles pour vérifier la présence d'une pneumothorax iatrogénique.
Drain thoracique
Le drain thoracique devrait être envisagé dans les situations suivantes :
- Drainage urgent d'un épanchement infecté ou loculé;
- Épanchement récidivant;
- Drainage de liquide à haute viscosité à risque d'occlure le drain (ex : hémothorax, empyème).[6]
Thoracoscopie
Il peut être utile d'opter pour une chirurgie minimalement invasive si :
- L'on veut récolter des biopsie ou échantillons pour préciser le diagnostic;
- Un épanchement parapneumonique n'est pas contrôlé suffisamment par un drain thoracique;
- Le drainage d'un empyème nécessite un débridement.[6]
Pleurodèse
La pleurodèse consiste à injecter un produit chimique (ex : talc) dans la cavité pleurale dans le but de créer des adhérences entre la plèvre viscérale et la plèvre pariétale.
Il est pertinent d'envisager la pleurodèse en présence d'épanchements malins récurrents ou qui ne répondent pas aux traitements de la cause sous-jacente. [6]
Évolution
Le pronostic dépend de la cause de l'épanchement pleural. Les épanchements bénins peuvent être guéris mais si la cause est une tumeur maligne, le pronostic est très mauvais. Une autre caractéristique des épanchements pleuraux est la récidive qui peut également survenir avec des troubles bénins tels que le lupus, l'urémie et la polyarthrite rhumatoïde. Si l'épanchement pleural n'est pas drainé, il peut conduire à une dyspnée et même à un empyème.[1]
Complications
Si un épanchement pleural important est drainé rapidement et que des volumes supérieurs à 1,5 L sont retirés, la ré-expansion rapide du poumon effondré peut occasionnellement conduire à un œdème pulmonaire de ré-expansion.
Consultations
- Pneumologue
- Chirurgien thoracique [1]
Notes
Références
- Cette page a été modifiée ou créée le 2021/01/04 à partir de Pleural Effusion (StatPearls / Pleural Effusion (2020/10/28)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/28846252 (livre).
- ↑ 1,0 1,1 1,2 1,3 1,4 et 1,5 Rachana Krishna et Mohan Rudrappa, StatPearls, StatPearls Publishing, (PMID 28846252, lire en ligne)
- ↑ (en) Richard W. Light, « Pleural Effusions », Medical Clinics of North America, vol. 95, no 6, , p. 1055–1070 (DOI 10.1016/j.mcna.2011.08.005, lire en ligne)
- ↑ Ria Dancel, Daniel Schnobrich, Nitin Puri et Ricardo Franco-Sadud, « Recommendations on the Use of Ultrasound Guidance for Adult Thoracentesis: A Position Statement of the Society of Hospital Medicine », Journal of Hospital Medicine, vol. 13, no 2, , p. 126–135 (ISSN 1553-5606, PMID 29377972, DOI 10.12788/jhm.2940, lire en ligne)
- ↑ Julien Guinde, Samer Georges, Valerian Bourinet et Sophie Laroumagne, « Recent developments in pleurodesis for malignant pleural disease », The Clinical Respiratory Journal, vol. 12, no 10, , p. 2463–2468 (ISSN 1752-699X, PMID 30252207, DOI 10.1111/crj.12958, lire en ligne)
- ↑ David T. Arnold, Duneesha De Fonseka, Siobhan Perry et Anna Morley, « Investigating unilateral pleural effusions: the role of cytology », The European Respiratory Journal, vol. 52, no 5, (ISSN 1399-3003, PMID 30262573, DOI 10.1183/13993003.01254-2018, lire en ligne)
- ↑ 6,0 6,1 6,2 6,3 6,4 6,5 6,6 6,7 et 6,8 « AMBOSS login », sur www.amboss.com (consulté le 16 janvier 2021)
- ↑ 7,0 et 7,1 « Épanchement pleural - Troubles pulmonaires », sur Édition professionnelle du Manuel MSD (consulté le 16 janvier 2021)
- ↑ Mark Shafarenko, Tara Tofighi, Toronto Notes, Toronto,
- ↑ (en) Tina Binesh Marvasti et Sydney McQueen, Toronto Notes 2018, 34e éd., R22
- ↑ (en) RICHARD W. LIGHT, « Pleural Effusions: The Diagnostic Separation of Transudates and Exudates », Annals of Internal Medicine, vol. 77, no 4, , p. 507 (ISSN 0003-4819, DOI 10.7326/0003-4819-77-4-507, lire en ligne)