« Fibrillation ventriculaire » : différence entre les versions
(30 minutes - 1ere lecture + références) |
(2020-10-31 - 1h - Références + Structuration du texte) |
||
| Ligne 16 : | Ligne 16 : | ||
|ajouter_liens=1 | |ajouter_liens=1 | ||
|ajouter_propriétés_sémantiques=1 | |ajouter_propriétés_sémantiques=1 | ||
}}{{Section ontologique|classe=Maladie|nom=Introduction}}Les arythmies | }}{{Section ontologique|classe=Maladie|nom=Introduction}} | ||
[[Fichier:Ventricular fibrillation.png|vignette|ECG : Fibrillation ventriculaire]] | |||
Les arythmies qui proviennent du myocarde ventriculaire ou du système His-Purkinje sont regroupées dans la classe des arythmies ventriculaires (AV). Cela comprend un sous-ensemble d'arythmies telles que la tachycardie ventriculaire (TV), la fibrillation ventriculaire (FV), les contractions ventriculaires prématurées (PVC) et le flutter ventriculaire. La tachycardie complexe large (WCT) est utilisée pour définir toutes les tachyarythmies dont la durée du complexe QRS est supérieure à 0,12 seconde. La FV est une WCT causée par une activité électrique irrégulière et caractérisée par une fréquence ventriculaire généralement supérieure à 300 avec des complexes QRS discrets sur l'électrocardiogramme (ECG). La morphologie du QRS dans la FV varie en forme, en amplitude et en durée avec un rythme irrégulier proéminent.<ref name=":1">{{Citation d'un article|nom1=American College of Cardiology/American Heart Association Task Force on Clinical Data Standards (ACC/AHA/HRS Writing Committee to Develop Data Standards on Electrophysiology)|prénom2=Alfred E.|nom2=Buxton|prénom3=Hugh|nom3=Calkins|prénom4=David J.|nom4=Callans|titre=ACC/AHA/HRS 2006 key data elements and definitions for electrophysiological studies and procedures: a report of the American College of Cardiology/American Heart Association Task Force on Clinical Data Standards (ACC/AHA/HRS Writing Committee to Develop Data Standards on Electrophysiology)|périodique=Circulation|volume=114|numéro=23|date=2006-12-05|issn=1524-4539|pmid=17130345|doi=10.1161/CIRCULATIONAHA.106.180199|lire en ligne=https://pubmed.ncbi.nlm.nih.gov/17130345/|consulté le=2020-09-10|pages=2534–2570}}</ref> La FV est un rythme extrêmement dangereux compromettant considérablement le débit cardiaque et conduisant finalement à la mort subite cardiaque (SCD) .<ref name=":0">{{Citation d'un ouvrage|prénom1=Dipesh|nom1=Ludhwani|prénom2=Amandeep|nom2=Goyal|prénom3=Mandar|nom3=Jagtap|titre=StatPearls|éditeur=StatPearls Publishing|date=2020|pmid=30725805|lire en ligne=http://www.ncbi.nlm.nih.gov/books/NBK537120/|consulté le=2020-09-10}}</ref> | |||
La FV a été identifiée chez près de 70% des patients en arrêt cardiaque. Sans traitement, la condition est mortelle en quelques minutes. Les taux de survie des patients atteints de FV en dehors des hôpitaux ont légèrement augmenté, mais beaucoup continuent de présenter des lésions cérébrales anoxiques résiduelles et des déficits neurologiques. | La FV a été identifiée chez près de 70% des patients en arrêt cardiaque. Sans traitement, la condition est mortelle en quelques minutes. Les taux de survie des patients atteints de FV en dehors des hôpitaux ont légèrement augmenté, mais beaucoup continuent de présenter des lésions cérébrales anoxiques résiduelles et des déficits neurologiques. | ||
== Épidémiologie == | == Épidémiologie == | ||
{{Section ontologique|classe=Maladie|nom=Épidémiologie}}En 2017, la mise à jour de l'American Heart Association (AHA) a estimé le fardeau annuel total de l'arrêt cardiaque hors hôpital (OHCA) à 356500. Au moins 23% des OHCA traités par le service médical d'urgence (EMS) ont la FV / TV comme rythme initial. Avec plus de 60% des décès cardiovasculaires résultant d'un arrêt cardiaque, il reste la principale cause de décès dans le monde.<ref name=":6">{{Citation d'un article|prénom1=A. Selcuk|nom1=Adabag|prénom2=Russell V.|nom2=Luepker|prénom3=Véronique L.|nom3=Roger|prénom4=Bernard J.|nom4=Gersh|titre=Sudden cardiac death: epidemiology and risk factors|périodique=Nature Reviews. Cardiology|volume=7|numéro=4|date=2010-04|issn=1759-5010|pmid=20142817|pmcid=5014372|doi=10.1038/nrcardio.2010.3|lire en ligne=https://pubmed.ncbi.nlm.nih.gov/20142817/|consulté le=2020-09-10|pages=216–225}}</ref> Les progrès modernes dans les dispositifs d'assistance tels que le défibrillateur cardiaque implantable (ICD) ont eu un impact significatif sur ces chiffres. De nombreuses études ont identifié la FV comme l'arythmie sous-jacente la plus courante chez les patients atteints de SCD. Parmi les patients hospitalisés pour un infarctus du myocarde aigu, 5% à 10% souffriront de FV ou de TV, et 5% auront une FV ou une TV dans les 48 heures suivant l'admission | {{Section ontologique|classe=Maladie|nom=Épidémiologie}}En 2017, la mise à jour de l'American Heart Association (AHA) a estimé le fardeau annuel total de l'arrêt cardiaque hors hôpital (OHCA) à 356500. Au moins 23% des OHCA traités par le service médical d'urgence (EMS) ont la FV / TV comme rythme initial. Avec plus de 60% des décès cardiovasculaires résultant d'un arrêt cardiaque, il reste la principale cause de décès dans le monde.<ref name=":6">{{Citation d'un article|prénom1=A. Selcuk|nom1=Adabag|prénom2=Russell V.|nom2=Luepker|prénom3=Véronique L.|nom3=Roger|prénom4=Bernard J.|nom4=Gersh|titre=Sudden cardiac death: epidemiology and risk factors|périodique=Nature Reviews. Cardiology|volume=7|numéro=4|date=2010-04|issn=1759-5010|pmid=20142817|pmcid=5014372|doi=10.1038/nrcardio.2010.3|lire en ligne=https://pubmed.ncbi.nlm.nih.gov/20142817/|consulté le=2020-09-10|pages=216–225}}</ref> Les progrès modernes dans les dispositifs d'assistance tels que le défibrillateur cardiaque implantable (ICD) ont eu un impact significatif sur ces chiffres. De nombreuses études ont identifié la FV comme l'arythmie sous-jacente la plus courante chez les patients atteints de SCD. Parmi les patients hospitalisés pour un infarctus du myocarde aigu, 5% à 10% souffriront de FV ou de TV, et 5% auront une FV ou une TV dans les 48 heures suivant l'admission. Sur la base des données du Resuscitation Outcomes Consortium (ROC), la survie à la sortie de l'hôpital pour les patients FV était de 31,4% .<ref name=":0" /> | ||
== Étiologies == | == Étiologies == | ||
{{Section ontologique|classe=Maladie|nom=Étiologies}}La FV est souvent liée à une maladie cardiaque structurelle sous-jacente. 3 à 12% des cas d'infarctus du myocarde (IM) développent une FV pendant la phase aiguë.<ref name=":2">{{Citation d'un article|prénom1=Charlotte|nom1=Glinge|prénom2=Stefan|nom2=Sattler|prénom3=Reza|nom3=Jabbari|prénom4=Jacob|nom4=Tfelt-Hansen|titre=Epidemiology and genetics of ventricular fibrillation during acute myocardial infarction|périodique=Journal of geriatric cardiology: JGC|volume=13|numéro=9|date=2016-09|issn=1671-5411|pmid=27899944|pmcid=5122505|doi=10.11909/j.issn.1671-5411.2016.09.006|lire en ligne=https://pubmed.ncbi.nlm.nih.gov/27899944/|consulté le=2020-09-10|pages=789–797}}</ref> MI avec une occlusion coronaire complète sur une angiographie, un infarctus de la paroi antérieure, une fibrillation auriculaire et une angor pré-infarctus sont plus susceptibles de développer une FV. <ref name=":3">{{Citation d'un article|prénom1=Reza|nom1=Jabbari|prénom2=Thomas|nom2=Engstrøm|prénom3=Charlotte|nom3=Glinge|prénom4=Bjarke|nom4=Risgaard|titre=Incidence and risk factors of ventricular fibrillation before primary angioplasty in patients with first ST-elevation myocardial infarction: a nationwide study in Denmark|périodique=Journal of the American Heart Association|volume=4|numéro=1|date=2015-01-05|issn=2047-9980|pmid=25559012|pmcid=4330064|doi=10.1161/JAHA.114.001399|lire en ligne=https://pubmed.ncbi.nlm.nih.gov/25559012/|consulté le=2020-09-10|pages=e001399}}</ref> De nombreuses affections courantes associées à la FV comprennent les anomalies électrolytiques (hypokaliémie / hyperkaliémie, hypomagnésémie) | {{Section ontologique|classe=Maladie|nom=Étiologies}}La FV est souvent liée à une maladie cardiaque structurelle sous-jacente. 3 à 12% des cas d'[[Infarctus du myocarde avec élévation du segment ST|infarctus du myocarde]] (IM) développent une FV pendant la phase aiguë.<ref name=":2">{{Citation d'un article|prénom1=Charlotte|nom1=Glinge|prénom2=Stefan|nom2=Sattler|prénom3=Reza|nom3=Jabbari|prénom4=Jacob|nom4=Tfelt-Hansen|titre=Epidemiology and genetics of ventricular fibrillation during acute myocardial infarction|périodique=Journal of geriatric cardiology: JGC|volume=13|numéro=9|date=2016-09|issn=1671-5411|pmid=27899944|pmcid=5122505|doi=10.11909/j.issn.1671-5411.2016.09.006|lire en ligne=https://pubmed.ncbi.nlm.nih.gov/27899944/|consulté le=2020-09-10|pages=789–797}}</ref> MI avec une occlusion coronaire complète sur une [[angiographie]], un infarctus de la paroi antérieure, une fibrillation auriculaire et une angor pré-infarctus sont plus susceptibles de développer une FV. <ref name=":3">{{Citation d'un article|prénom1=Reza|nom1=Jabbari|prénom2=Thomas|nom2=Engstrøm|prénom3=Charlotte|nom3=Glinge|prénom4=Bjarke|nom4=Risgaard|titre=Incidence and risk factors of ventricular fibrillation before primary angioplasty in patients with first ST-elevation myocardial infarction: a nationwide study in Denmark|périodique=Journal of the American Heart Association|volume=4|numéro=1|date=2015-01-05|issn=2047-9980|pmid=25559012|pmcid=4330064|doi=10.1161/JAHA.114.001399|lire en ligne=https://pubmed.ncbi.nlm.nih.gov/25559012/|consulté le=2020-09-10|pages=e001399}}</ref> | ||
De nombreuses affections courantes associées à la FV comprennent : | |||
* les anomalies électrolytiques ([[hypokaliémie]] / [[hyperkaliémie]], [[hypomagnésémie]]) | |||
* l'acidose | |||
* l'hypothermie | |||
* l'hypoxie | |||
* les [[cardiomyopathies]] | |||
* les antécédents familiaux de mort cardiaque subite | |||
* les anomalies congénitales de l'intervalle QT | |||
* le [[Syndrome de Brugada|syndrome de Brugada]] | |||
* la consommation d'alcool | |||
* Les patients ayant des antécédents d'AV, en particulier une TV monomorphe ou polymorphe soutenue, peuvent passer à la FV chez les patients sensibles.<ref name=":4">{{Citation d'un article|prénom1=F. H.|nom1=Samie|prénom2=J.|nom2=Jalife|titre=Mechanisms underlying ventricular tachycardia and its transition to ventricular fibrillation in the structurally normal heart|périodique=Cardiovascular Research|volume=50|numéro=2|date=2001-05|issn=0008-6363|pmid=11334828|doi=10.1016/s0008-6363(00)00289-3|lire en ligne=https://pubmed.ncbi.nlm.nih.gov/11334828/|consulté le=2020-09-10|pages=242–250}}</ref> | |||
* La prédisposition génétique à la FV est maintenant de plus en plus reconnue. La première association à l'échelle du génome a été rapportée dans l'étude AGNES identifiant le locus de susceptibilité pour la FV à 21q21.<ref name=":5">{{Citation d'un article|prénom1=Connie R.|nom1=Bezzina|prénom2=Raha|nom2=Pazoki|prénom3=Abdennasser|nom3=Bardai|prénom4=Roos F.|nom4=Marsman|titre=Genome-wide association study identifies a susceptibility locus at 21q21 for ventricular fibrillation in acute myocardial infarction|périodique=Nature Genetics|volume=42|numéro=8|date=2010-08|issn=1546-1718|pmid=20622880|pmcid=3966292|doi=10.1038/ng.623|lire en ligne=https://pubmed.ncbi.nlm.nih.gov/20622880/|consulté le=2020-09-10|pages=688–691}}</ref><ref name=":0" /> | |||
== Physiopathologie == | == Physiopathologie == | ||
| Ligne 34 : | Ligne 49 : | ||
* Activité déclenchée: tôt et tard après la dépolarisation, peut dépasser le seuil réfractaire et générer un potentiel déclenché provoquant des extrasystoles.<ref name=":0" /> | * Activité déclenchée: tôt et tard après la dépolarisation, peut dépasser le seuil réfractaire et générer un potentiel déclenché provoquant des extrasystoles.<ref name=":0" /> | ||
* Les circuits de rentrée fonctionnels et anatomiques aident à maintenir l'arythmie ventriculaire. <ref name=":0" /> | |||
* | * | ||
== Présentation clinique == | == Présentation clinique == | ||
{{Section ontologique|classe=Maladie|nom=Présentation clinique}}La présentation la plus courante de la FV est l'arrêt cardiaque soudain conduisant à une SCD. Cela résulte d'une contraction ventriculaire inappropriée entraînant un faible débit cardiaque. Les patients peuvent présenter des signes d'infarctus du myocarde aigu tels que douleurs thoraciques, essoufflement, nausées et vomissements avant l'événement. Les patients ayant des antécédents connus de maladie coronarienne ou d'insuffisance cardiaque congestive peuvent présenter une aggravation des symptômes chroniques tels que l'angor, la dyspnée, l'orthopnée, la dyspnée nocturne paroxystique et l'œdème des membres inférieurs. Lors de l'arythmie, les patients sont inconscients, ne répondent pas et n'ont pas de pouls palpable. Sans action rapide, cela conduit à la mort dans les prochaines minutes. Les patients atteints de DCI pour la prévention primaire ou secondaire peuvent subir un choc dû au déclenchement du DCI au moment de la FV. <ref name=":0" /> | {{Section ontologique|classe=Maladie|nom=Présentation clinique}}La présentation la plus courante de la FV est l'arrêt cardiaque soudain conduisant à une SCD. Cela résulte d'une contraction ventriculaire inappropriée entraînant un faible débit cardiaque. Les patients peuvent présenter des signes d'infarctus du myocarde aigu tels que douleurs thoraciques, essoufflement, nausées et vomissements avant l'événement. Les patients ayant des antécédents connus de maladie coronarienne ou d'[[Insuffisance cardiaque|insuffisance cardiaque]] congestive peuvent présenter une aggravation des symptômes chroniques tels que l'angor, la dyspnée, l'orthopnée, la dyspnée nocturne paroxystique et l'œdème des membres inférieurs. Lors de l'arythmie, les patients sont inconscients, ne répondent pas et n'ont pas de pouls palpable. Sans action rapide, cela conduit à la mort dans les prochaines minutes. Les patients atteints de DCI pour la prévention primaire ou secondaire peuvent subir un choc dû au déclenchement du DCI au moment de la FV. <ref name=":0" /> | ||
===Facteurs de risque=== | ===Facteurs de risque=== | ||
{{Section ontologique|classe=Maladie|nom=Facteurs de risque}} | {{Section ontologique|classe=Maladie|nom=Facteurs de risque}} | ||
===Questionnaire=== | ===Questionnaire=== | ||
{{Section ontologique|classe=Maladie|nom=Questionnaire}} | {{Section ontologique|classe=Maladie|nom=Questionnaire}} | ||
===Examen clinique=== | ===Examen clinique=== | ||
| Ligne 77 : | Ligne 91 : | ||
* Intervalle QT long ou court | * Intervalle QT long ou court | ||
* WPW | * WPW | ||
* Toxicité de la digitaline | * Toxicité de la [[digitaline]] | ||
* Signe d'Epsilon (cardiomyopathie ventriculaire droite arythmogène) <ref name=":0" /> | * Signe d'Epsilon (cardiomyopathie ventriculaire droite arythmogène) <ref name=":0" /> | ||
Version du 31 octobre 2020 à 14:21
| Maladie | |
| Caractéristiques | |
|---|---|
| Signes | Apnée, Absence de bruits cardiaques, Asystolie, Inconscient, Absence de tension artérielle, Respiration agonique |
| Symptômes |
Altération de l'état de conscience |
| Diagnostic différentiel |
Embolie pulmonaire, Rythme idioventriculaire accéléré, Torsade de pointes, Asystolie, Tachycardie ventriculaire polymorphe, Flutter ventriculaire, Tachycardie supraventriculaire avec aberration, Dissection aortique, Activité électrique sans pouls |
| Informations | |
| Wikidata ID | Q848662 |
|
| |
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: | |
| Exemple: | |
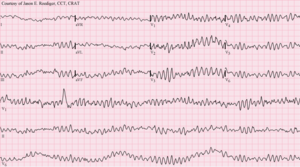
Les arythmies qui proviennent du myocarde ventriculaire ou du système His-Purkinje sont regroupées dans la classe des arythmies ventriculaires (AV). Cela comprend un sous-ensemble d'arythmies telles que la tachycardie ventriculaire (TV), la fibrillation ventriculaire (FV), les contractions ventriculaires prématurées (PVC) et le flutter ventriculaire. La tachycardie complexe large (WCT) est utilisée pour définir toutes les tachyarythmies dont la durée du complexe QRS est supérieure à 0,12 seconde. La FV est une WCT causée par une activité électrique irrégulière et caractérisée par une fréquence ventriculaire généralement supérieure à 300 avec des complexes QRS discrets sur l'électrocardiogramme (ECG). La morphologie du QRS dans la FV varie en forme, en amplitude et en durée avec un rythme irrégulier proéminent.[1] La FV est un rythme extrêmement dangereux compromettant considérablement le débit cardiaque et conduisant finalement à la mort subite cardiaque (SCD) .[2]
La FV a été identifiée chez près de 70% des patients en arrêt cardiaque. Sans traitement, la condition est mortelle en quelques minutes. Les taux de survie des patients atteints de FV en dehors des hôpitaux ont légèrement augmenté, mais beaucoup continuent de présenter des lésions cérébrales anoxiques résiduelles et des déficits neurologiques.
Épidémiologie
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section contient les données épidémiologiques sur la maladie (ex. incidence, prévalence, coûts en hospitalisation, proportion d'hommes-femmes, régions où la prévalence est plus élevée, etc.). Chaque donnée épidémiologique doit être appuyée par une référence. Idéalement, des statistiques canadiennes et québécoises sont mentionnées lorsque disponibles. |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: | Les facteurs de risque ne sont pas présentés ici, mais bien dans la sous-section Facteurs de risque (Présentation clinique). Le pronostic et l'évolution naturelle de la maladie sont décrits dans la section Évolution. |
| Exemple: | La FRP est une maladie relativement rare qui affecte le plus souvent les patients âgés de 40 à 60 ans. Une prédominance masculine est observée avec un ratio H : F estimé à environ 2:1 ou 3:1. L'incidence de la FRP est inconnue, mais est estimée à 1 pour 200 000 à 500 000 par an. |
En 2017, la mise à jour de l'American Heart Association (AHA) a estimé le fardeau annuel total de l'arrêt cardiaque hors hôpital (OHCA) à 356500. Au moins 23% des OHCA traités par le service médical d'urgence (EMS) ont la FV / TV comme rythme initial. Avec plus de 60% des décès cardiovasculaires résultant d'un arrêt cardiaque, il reste la principale cause de décès dans le monde.[3] Les progrès modernes dans les dispositifs d'assistance tels que le défibrillateur cardiaque implantable (ICD) ont eu un impact significatif sur ces chiffres. De nombreuses études ont identifié la FV comme l'arythmie sous-jacente la plus courante chez les patients atteints de SCD. Parmi les patients hospitalisés pour un infarctus du myocarde aigu, 5% à 10% souffriront de FV ou de TV, et 5% auront une FV ou une TV dans les 48 heures suivant l'admission. Sur la base des données du Resuscitation Outcomes Consortium (ROC), la survie à la sortie de l'hôpital pour les patients FV était de 31,4% .[2]
Étiologies
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section décrit les étiologies de la maladie, c'est-à-dire ce qui cause la maladie (ex. le diabète de type 2 cause la néphropathie diabétique). Les étiologies doivent être identifiées avec le modèle Étiologies. |
| Formats: | Texte, Liste à puces, Tableau |
| Balises sémantiques: | Étiologie |
| Commentaires: |
|
| Exemple: | Parmi les étiologies les plus courantes d'occlusion de l'intestin grêle, on retrouve :
|
La FV est souvent liée à une maladie cardiaque structurelle sous-jacente. 3 à 12% des cas d'infarctus du myocarde (IM) développent une FV pendant la phase aiguë.[4] MI avec une occlusion coronaire complète sur une angiographie, un infarctus de la paroi antérieure, une fibrillation auriculaire et une angor pré-infarctus sont plus susceptibles de développer une FV. [5]
De nombreuses affections courantes associées à la FV comprennent :
- les anomalies électrolytiques (hypokaliémie / hyperkaliémie, hypomagnésémie)
- l'acidose
- l'hypothermie
- l'hypoxie
- les cardiomyopathies
- les antécédents familiaux de mort cardiaque subite
- les anomalies congénitales de l'intervalle QT
- le syndrome de Brugada
- la consommation d'alcool
- Les patients ayant des antécédents d'AV, en particulier une TV monomorphe ou polymorphe soutenue, peuvent passer à la FV chez les patients sensibles.[6]
- La prédisposition génétique à la FV est maintenant de plus en plus reconnue. La première association à l'échelle du génome a été rapportée dans l'étude AGNES identifiant le locus de susceptibilité pour la FV à 21q21.[7][2]
Physiopathologie
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | La physiopathologie traite des mécanismes biologiques qui conduisent à l'apparition d'une maladie. |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: | L'histopathologie doit figurer dans la section Examen paraclinique, et non dans la section physiopathologie. |
| Exemple: | Le VIP est une neurohormone composée de 28 acides aminés et appartenant à la famille des sécrétines-glucagon. Il est produit dans le système nerveux central ainsi que dans les neurones des voies gastro-intestinales, respiratoires et urogénitales. Il agit, via l'expression d'adénylate cyclase cellulaire (AMPc), à titre de vasodilatateur et de régulateur de l'activité des muscles lisses, de stimulateur de la sécrétion d'eau et d'électrolytes par le tractus intestinal, d'inhibiteur de la sécrétion d'acide gastrique et de promoteur du flux sanguin principalement dans le tractus gastro-intestinal. L'ensemble de ces éléments peuvent entraîner une hypokaliémie, une hyperglycémie, une hypomagnésémie et une hypercalcémie qui sont habituellement responsables de la présentation clinique. |
La FV se produit lorsque des parties du myocarde ventriculaire se dépolarisent de manière erratique et non coordonnée. La FV résulte de ce qui suit: [2]
- Formation d'impulsion anormale [2]
- Augmentation de l'automaticité: les cellules de Purkinje autour des zones ischémiques pendant l'IM peuvent déclencher une tachycardie ventriculaire.
- Activité déclenchée: tôt et tard après la dépolarisation, peut dépasser le seuil réfractaire et générer un potentiel déclenché provoquant des extrasystoles.[2]
- Les circuits de rentrée fonctionnels et anatomiques aident à maintenir l'arythmie ventriculaire. [2]
Présentation clinique
Toute contribution serait appréciée.
| Description: | Cette section contient la sous-section optionnelle Facteurs de risque et les sous-sections obligatoires Questionnaire et Examen clinique. |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: |
|
| Exemple: |
(Aucun texte)
(Texte)
(Texte)
(Texte) |
La présentation la plus courante de la FV est l'arrêt cardiaque soudain conduisant à une SCD. Cela résulte d'une contraction ventriculaire inappropriée entraînant un faible débit cardiaque. Les patients peuvent présenter des signes d'infarctus du myocarde aigu tels que douleurs thoraciques, essoufflement, nausées et vomissements avant l'événement. Les patients ayant des antécédents connus de maladie coronarienne ou d'insuffisance cardiaque congestive peuvent présenter une aggravation des symptômes chroniques tels que l'angor, la dyspnée, l'orthopnée, la dyspnée nocturne paroxystique et l'œdème des membres inférieurs. Lors de l'arythmie, les patients sont inconscients, ne répondent pas et n'ont pas de pouls palpable. Sans action rapide, cela conduit à la mort dans les prochaines minutes. Les patients atteints de DCI pour la prévention primaire ou secondaire peuvent subir un choc dû au déclenchement du DCI au moment de la FV. [2]
Facteurs de risque
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section contient les facteurs de risque de la maladie. Ces facteurs de risque peuvent être des maladies, des anomalies génétiques, des caractéristiques individuelles (l'âge, le sexe, l'origine ethnique, un certain type d'alimentation), etc. |
| Formats: | Liste à puces, Tableau |
| Balises sémantiques: | Facteur de risque |
| Commentaires: |
|
| Exemple: | Les facteurs de risque de l'infarctus du myocarde sont :
|
Questionnaire
Toute contribution serait appréciée.
| Description: | Cette section traite des symptômes à rechercher à l'anamnèse (questionnaire). Les symptômes sont ressentis et exprimés par les patients. |
| Formats: | Liste à puces |
| Balises sémantiques: | Symptôme, Élément d'histoire |
| Commentaires: |
|
| Exemple: | Les symptômes de l'infarctus du myocarde sont :
D'autres éléments à rechercher au questionnaire de l'infarctus sont :
Il est parfois pertinent de mentionner des symptômes qui sont absents, comme dans la pharyngite à streptocoque. Les symptômes de la pharyngite à streptocoque sont :
|
Examen clinique
Toute contribution serait appréciée.
| Description: | Cette section traite des signes à rechercher lors de l'examen clinique. |
| Formats: | Liste à puces |
| Balises sémantiques: | Examen clinique, Signe clinique |
| Commentaires: |
|
| Exemple: | L'examen physique de l'appendicite démontrera les éléments suivants :
|
Examens paracliniques
Toute contribution serait appréciée.
| Description: | Cette section concerne les tests à demander lorsque la maladie est suspectée et les résultats attendus en présence de la maladie. |
| Formats: | Liste à puces, Tableau |
| Balises sémantiques: | Examen paraclinique, Signe paraclinique |
| Commentaires: |
|
| Exemple: | Les examens suivants sont utiles dans la démarche d'investigation du VIPome :
|
La présentation aiguë des symptômes et les résultats de l'ECG conduisent au diagnostic.[2]
Résultats ECG [2]
- Ondes de fibrillation d'amplitude et de forme variables.
- Pas d'ondes P, de complexes QRS ou d'ondes T identifiables
- Fréquence cardiaque comprise entre 150 et 500 par minute [2]
Tempête FV: identifiée par 3 épisodes ou plus de FV ou des chocs appropriés de la CIM dans les 24 heures [2]
Les patients qui survivent à la FV doivent avoir une anamnèse et un examen physique approfondis. Il faut noter les antécédents familiaux de décès cardiaque inexpliqués. Les médecins devraient examiner de près les antécédents cardiaques du patient et la liste des médicaments qui pourraient être arythmogènes. Ils doivent également rechercher et corriger les causes réversibles de la FV telles que les anomalies électrolytiques, l'acidose et l'hypoxie. Le professionnel de la santé doit également évaluer les patients pour une cardiopathie ischémique sous-jacente avec une échocardiographie et une angiographie d'urgence. Parmi tous les OHCA, plus de 50% ont une coronaropathie importante à l'angiographie. [8][2]
Les études de laboratoire appropriées comprennent: [2]
- Electrolytes sériques
- Gaz artériel
- FSC
- Enzymes cardiaques
- Niveaux de médicaments
- Écran de toxicologie
- Niveaux BNP[2]
L'ECG peut révéler: [2]
- MI
- Syndrome de Brugada
- Intervalle QT long ou court
- WPW
- Toxicité de la digitaline
- Signe d'Epsilon (cardiomyopathie ventriculaire droite arythmogène) [2]
L'ECHOCARDIOGRAPHIE est généralement effectuée pour évaluer le mouvement de la paroi cardiaque, la fraction d'éjection et tout problème valvulaire. De plus, l'Echo identifiera tout liquide péricardique qui aurait pu résulter de la RCR.[2]
L'EPS est effectué une fois que le patient est stable pour différencier les patients atteints de FV inductible de ceux atteints de FV non inductible. Les patients souffrant d'arythmies ventriculaires monomorphes induites peuvent être des candidats à un DCI.[2]
Approche clinique
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Alors que les sections Questionnaire, Examen clinique et Examens paracliniques servent à énumérer, cette section sert à intégrer tous ces éléments pour discuter du raisonnement du clinicien. C'est en quelque sorte la manière dont les cliniciens réfléchissent lorsque confrontés à cette maladie : c'est la section par excellence pour l'enseignement. |
| Formats: | Texte, Liste à puces, Tableau |
| Balises sémantiques: | |
| Commentaires: |
|
| Exemple: | |
Types de VF sur ECG[2]
- Coarse VF: la majorité des formes d'onde mesurent 3 mm ou plus
- Fine VF: la majorité des formes d'onde mesurent moins de 3 mm [2]
Diagnostic
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section traite de la manière dont on peut diagnostiquer une maladie en tenant compte de l'histoire, de l'examen clinique et des investigations. C'est dans cette section que se retrouveront les critères permettant d'infirmer ou de confirmer la présence de la maladie (lorsqu'ils existent). |
| Formats: | Texte, Liste à puces, Tableau |
| Balises sémantiques: | |
| Commentaires: |
|
| Exemple: | L'asystolie est un diagnostic électrocardiographique. L'absence d'activité électrique chez un patient inconscient sans pouls permet de confirmer le diagnostic, tout en s'assurant qu'il n'y a pas de cable débranché et que la calibration du moniteur est adéquate.
Selon le Fourth Universal Definition of Myocardial Infarction, l'infarctus aigu du myocarde est diagnostiqué lorsqu'il y a :
|
Diagnostic différentiel
Toute contribution serait appréciée.
| Description: | Cette section traite du diagnostic différentiel de la maladie, c'est-à-dire aux autres diagnostics à évoquer lorsque confronté à ce diagnostic. |
| Formats: | Liste à puces |
| Balises sémantiques: | Diagnostic différentiel |
| Commentaires: |
|
| Exemple: | Le diagnostic différentiel de l'appendicite comprend :
|
Il est important de différencier la VF de l'activité électrique sans impulsions (PEA) / asystole car ces deux conditions sont gérées différemment selon le protocole ACLS. D'autres causes d'effondrement soudain telles que la dissection aortique et l'embolie pulmonaire doivent être envisagées. Les conditions suivantes peuvent être facilement confondues avec la FV sur un ECG et doivent être exclues.[2]
- Tachycardie ventriculaire polymorphe
- Torsade de pointes
- Flutter ventriculaire
- Activité électrique sans impulsions
- Rythme idioventriculaire accéléré
- SVT avec aberrance [2]
Traitement
Toute contribution serait appréciée.
| Description: | Cette section décrit le traitement de la maladie. |
| Formats: | Liste à puces, Tableau, Texte |
| Balises sémantiques: | Traitement, Traitement pharmacologique |
| Commentaires: |
|
| Exemple: | |
Gestion aiguë[2]
En raison du taux de mortalité élevé et de l'extrême acuité de la maladie, les patients FV méritent une attention immédiate. Les professionnels de la santé doivent immédiatement initier une prise en charge conforme aux lignes directrices du protocole d'Advanced Cardiac Life Support (ACLS). La probabilité de survie est moindre si le professionnel de la santé s'écarte des recommandations de l'AATC. [9] Tous les patients souffrant d'un arrêt cardiaque doivent subir une évaluation initiale tout en recevant une RCP de qualité. La TV et la FV sans impulsions sont toutes deux des rythmes choquables, et une fois que le personnel identifie le rythme comme FV, les patients doivent être immédiatement choqués avec 120 à 200 joules sur un défibrillateur biphasique ou 360 joules à l'aide d'un monophasique. Les patients recevant une défibrillation rapide ont montré une survie améliorée (39,3%) par rapport aux patients chez qui la défibrillation a été retardée de 2 minutes ou plus (22,2%). [10] Administrer de l'épinéphrine et de l'amiodarone selon le protocole ACLS chez les patients avec de la FV soutenue indépendamment de recevoir 3 chocs. L'amiodarone améliore considérablement la survie à l'admission à l'hôpital sans affecter la survie à la sortie de l'hôpital.[11] Identifier et traiter la cause de l'événement incitant est tout aussi important. Les professionnels doivent prendre des mesures spécifiques à la cause telles que la sécurisation des voies respiratoires, la correction des électrolytes, l'administration de liquides, la décompression du pneumothorax, le drainage de la tamponnade lors de la réanimation du patient. Une fois que le patient a atteint le retour de la circulation spontanée (ROSC), les médecins devraient commencer une évaluation définitive de la maladie coronarienne.[2]
Gestion préventive [2]
La prévention primaire a été un facteur important dans la réduction des SCD liés à la FV. La plupart des transitions de la VF entre la TV et d'autres AV et par conséquent l'identification de ces arythmies à un stade précoce peuvent aider à prévenir la FV. Chez les patients présentant des symptômes suspectés d'être liés à l'AV, une détection par électrocardiographie ambulatoire et des moniteurs cardiaques implantés est recommandée. [12]. Les professionnels de la santé devraient proposer aux membres de la famille des patients atteints de syndromes d'arythmie héréditaire des tests génétiques et des conseils pour la stratification des risques.
Thérapie médicamenteuse [2]
L'amiodarone est l'antiarythmique le plus couramment étudié pour la prévention de la SCD. L'effet global de l'amiodarone sur la survie est controversé. La plupart des études n'ont pas montré de bénéfice supplémentaire par rapport au placebo ou à la CIM.[13] Le sotalol, en revanche, est associé à un risque accru de mortalité en diminuant le seuil de défibrillation. Une méta-analyse publiée en 2007 a montré une réduction significative du risque de SCD avec un traitement par statine.[14] Une incidence plus faible de SCD a été rapportée chez des patients sous traitement chronique par bêtabloquants pour insuffisance cardiaque avec une fraction d'éjection réduite.
Défibrillateurs[2]
Des essais contrôlés randomisés tels que MADIT-I (essai d'implantation de défibrillateur automatisé multicentrique), MADIT-II, SCD-HeFT (essai sur la mort cardiaque soudaine dans l'insuffisance cardiaque) ont clairement démontré des avantages de mortalité avec la DCI par rapport au traitement médical standard. Des essais comparant la DCI à un traitement antiarythmique tel que AVID (Antiarythmic Versus Implantable Defibrillator) ont montré des résultats similaires.[2]
Le placement d'un DCI est recommandé pour la prévention primaire de la drépanocytose chez les patients présentant un risque accru de FV / TV potentiellement mortelles. La pose d'un DCI est également indiquée pour la prévention secondaire de la drépanocytose chez les patients ayant des épisodes antérieurs de FV et une TV soutenue.[2]
Suivi
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section traite du suivi de la maladie. |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: |
|
| Exemple: | |
Complications
Toute contribution serait appréciée.
| Description: | Cette section traite des complications possibles de la maladie. |
| Formats: | Liste à puces, Texte |
| Balises sémantiques: | Complication |
| Commentaires: |
|
| Exemple: | Les complications de l'infarctus du myocarde sont :
|
- Lésion cérébrale anoxique
- Arythmies post-défibrillation
- Blessures causées par la RCP et la réanimation
- Brûlures cutanées
- Handicap de longue durée
- Blessure myocardique
- Décès[2]
Évolution
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section contient le pronostic et évolution naturelle de la maladie. Le pronostic est lié à la survie du patient atteint de la maladie. L'évolution naturelle est la manière dont évoluera la maladie du patient dans le temps. |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: | |
| Exemple: | La dissection aortique est associée une mortalité très élevée. Au moins 30% des patients décèdent après leur arrivée à l'urgence, et ce, même après une intervention chirurgicale. Pour ceux qui survivent à la chirurgie, la morbidité est également très élevée et la qualité de vie est mauvaise. La mortalité la plus élevée d'une dissection aortique aiguë est dans les 10 premiers jours. Les patients qui ont une dissection chronique ont tendance à avoir un meilleur pronostic, mais leur espérance de vie est raccourcie par rapport à la population générale.[1] Sans traitement, la mortalité est de 1 à 3% par heure au cours des 24 premières heures, 30% à une semaine, 80% à deux semaines et 90% à un an. |
Le pronostic de la FV dépend du délai entre le début de l'intervention précoce et la défibrillation. Des retards plus courts sont associés à des taux de survie aussi élevés que 50% .[15] Chez les patients présentant un IM d'élévation du ST, la FV précoce (moins de 24 heures) est associée à une mortalité accrue par rapport à la FV tardive (plus de 24 heures) .[16][2]
La FV en dehors de l'hôpital peut être inversée car aujourd'hui, des défibrillateurs sont disponibles dans de nombreux endroits. Mais le succès de l'inversion diminue à un taux de 5 à 10% pour chaque minute retardée. Même dans des circonstances idéales, 30 à 40% des patients survivent, mais beaucoup développent également des déficits neurologiques résiduels en raison de l'anoxie. La récupération complète est rare. [2]
Prévention
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section traite des mesures préventives et du dépistage précoce de la maladie (lorsque pertinent). |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: | |
| Exemple: | La prévention primaire consiste à la prise en charge des facteurs de risque :
|
Références
- Cette page a été modifiée ou créée le 2020/08/28 à partir de Ventricular Fibrillation (StatPearls / Ventricular Fibrillation (2020/08/10)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/30725805 (livre).
- ↑ American College of Cardiology/American Heart Association Task Force on Clinical Data Standards (ACC/AHA/HRS Writing Committee to Develop Data Standards on Electrophysiology), Alfred E. Buxton, Hugh Calkins et David J. Callans, « ACC/AHA/HRS 2006 key data elements and definitions for electrophysiological studies and procedures: a report of the American College of Cardiology/American Heart Association Task Force on Clinical Data Standards (ACC/AHA/HRS Writing Committee to Develop Data Standards on Electrophysiology) », Circulation, vol. 114, no 23, , p. 2534–2570 (ISSN 1524-4539, PMID 17130345, DOI 10.1161/CIRCULATIONAHA.106.180199, lire en ligne)
- ↑ 2,00 2,01 2,02 2,03 2,04 2,05 2,06 2,07 2,08 2,09 2,10 2,11 2,12 2,13 2,14 2,15 2,16 2,17 2,18 2,19 2,20 2,21 2,22 2,23 2,24 2,25 2,26 2,27 2,28 2,29 2,30 2,31 et 2,32 Dipesh Ludhwani, Amandeep Goyal et Mandar Jagtap, StatPearls, StatPearls Publishing, (PMID 30725805, lire en ligne)
- ↑ A. Selcuk Adabag, Russell V. Luepker, Véronique L. Roger et Bernard J. Gersh, « Sudden cardiac death: epidemiology and risk factors », Nature Reviews. Cardiology, vol. 7, no 4, , p. 216–225 (ISSN 1759-5010, PMID 20142817, Central PMCID 5014372, DOI 10.1038/nrcardio.2010.3, lire en ligne)
- ↑ Charlotte Glinge, Stefan Sattler, Reza Jabbari et Jacob Tfelt-Hansen, « Epidemiology and genetics of ventricular fibrillation during acute myocardial infarction », Journal of geriatric cardiology: JGC, vol. 13, no 9, , p. 789–797 (ISSN 1671-5411, PMID 27899944, Central PMCID 5122505, DOI 10.11909/j.issn.1671-5411.2016.09.006, lire en ligne)
- ↑ Reza Jabbari, Thomas Engstrøm, Charlotte Glinge et Bjarke Risgaard, « Incidence and risk factors of ventricular fibrillation before primary angioplasty in patients with first ST-elevation myocardial infarction: a nationwide study in Denmark », Journal of the American Heart Association, vol. 4, no 1, , e001399 (ISSN 2047-9980, PMID 25559012, Central PMCID 4330064, DOI 10.1161/JAHA.114.001399, lire en ligne)
- ↑ F. H. Samie et J. Jalife, « Mechanisms underlying ventricular tachycardia and its transition to ventricular fibrillation in the structurally normal heart », Cardiovascular Research, vol. 50, no 2, , p. 242–250 (ISSN 0008-6363, PMID 11334828, DOI 10.1016/s0008-6363(00)00289-3, lire en ligne)
- ↑ Connie R. Bezzina, Raha Pazoki, Abdennasser Bardai et Roos F. Marsman, « Genome-wide association study identifies a susceptibility locus at 21q21 for ventricular fibrillation in acute myocardial infarction », Nature Genetics, vol. 42, no 8, , p. 688–691 (ISSN 1546-1718, PMID 20622880, Central PMCID 3966292, DOI 10.1038/ng.623, lire en ligne)
- ↑ Florence Dumas, Alain Cariou, Stéphane Manzo-Silberman et David Grimaldi, « Immediate percutaneous coronary intervention is associated with better survival after out-of-hospital cardiac arrest: insights from the PROCAT (Parisian Region Out of hospital Cardiac ArresT) registry », Circulation. Cardiovascular Interventions, vol. 3, no 3, , p. 200–207 (ISSN 1941-7632, PMID 20484098, DOI 10.1161/CIRCINTERVENTIONS.109.913665, lire en ligne)
- ↑ Kimia Honarmand, Chantal Mepham, Craig Ainsworth et Zahira Khalid, « Adherence to advanced cardiovascular life support (ACLS) guidelines during in-hospital cardiac arrest is associated with improved outcomes », Resuscitation, vol. 129, , p. 76–81 (ISSN 1873-1570, PMID 29885353, DOI 10.1016/j.resuscitation.2018.06.005, lire en ligne)
- ↑ Paul S. Chan, Harlan M. Krumholz, Graham Nichol et Brahmajee K. Nallamothu, « Delayed time to defibrillation after in-hospital cardiac arrest », The New England Journal of Medicine, vol. 358, no 1, , p. 9–17 (ISSN 1533-4406, PMID 18172170, DOI 10.1056/NEJMoa0706467, lire en ligne)
- ↑ Ageliki Laina, George Karlis, Aris Liakos et Georgios Georgiopoulos, « Amiodarone and cardiac arrest: Systematic review and meta-analysis », International Journal of Cardiology, vol. 221, , p. 780–788 (ISSN 1874-1754, PMID 27434349, DOI 10.1016/j.ijcard.2016.07.138, lire en ligne)
- ↑ Sana M. Al-Khatib, William G. Stevenson, Michael J. Ackerman et William J. Bryant, « 2017 AHA/ACC/HRS Guideline for Management of Patients With Ventricular Arrhythmias and the Prevention of Sudden Cardiac Death: Executive Summary: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines and the Heart Rhythm Society », Journal of the American College of Cardiology, vol. 72, no 14, 10 02, 2018, p. 1677–1749 (ISSN 1558-3597, PMID 29097294, DOI 10.1016/j.jacc.2017.10.053, lire en ligne)
- ↑ Gust H. Bardy, Kerry L. Lee, Daniel B. Mark et Jeanne E. Poole, « Amiodarone or an implantable cardioverter-defibrillator for congestive heart failure », The New England Journal of Medicine, vol. 352, no 3, , p. 225–237 (ISSN 1533-4406, PMID 15659722, DOI 10.1056/NEJMoa043399, lire en ligne)
- ↑ Giacomo Levantesi, Marco Scarano, RosaMaria Marfisi et Giovanna Borrelli, « Meta-analysis of effect of statin treatment on risk of sudden death », The American Journal of Cardiology, vol. 100, no 11, , p. 1644–1650 (ISSN 0002-9149, PMID 18036362, DOI 10.1016/j.amjcard.2007.07.015, lire en ligne)
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/10699695
- ↑ Marina M. Demidova, J. Gustav Smith, Carl-Johan Höijer et Fredrik Holmqvist, « Prognostic impact of early ventricular fibrillation in patients with ST-elevation myocardial infarction treated with primary PCI », European Heart Journal. Acute Cardiovascular Care, vol. 1, no 4, , p. 302–311 (ISSN 2048-8726, PMID 24062921, Central PMCID 3760561, DOI 10.1177/2048872612463553, lire en ligne)
