Torsade de pointes
| Maladie | |||
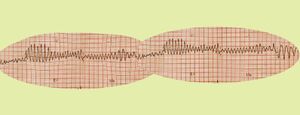
 Torsades de pointes sur l'ECG à 12 dérivations | |||
| Caractéristiques | |||
|---|---|---|---|
| Signes | Pâleur, Apnée, Tachycardie , Tachypnée , Rythme cardiaque irrégulier, Altération de l'état de conscience , Hypoxémie (signe paraclinique), Arrêt cardiaque, Hypotension artérielle , Diaphorèse | ||
| Symptômes |
Nausées, Dyspnée , Vertige , Syncope , Douleur thoracique , Asymptomatique , Palpitations , Diaphorèse | ||
| Diagnostic différentiel |
Fibrillation ventriculaire, Tachycardie ventriculaire | ||
| Informations | |||
| Terme anglais | Torsade de pointes | ||
| Wikidata ID | Q1625433 | ||
| SNOMED CT ID | 31722008 | ||
| Spécialités | Cardiologie, Anesthésie, Soins intensifs, Médecine d'urgence, Médecine interne | ||
| |||
La torsade de pointes est un type de tachycardie ventriculaire polymorphe caractérisée par des amplitudes variables du QRS donnant l'impression que les complexes QRS tournent autour de la ligne isoélectrique sur l'électrocardiogramme. La torsade de pointes est étroitement associée au syndrome du QT long.[1][2][3][4]
Épidémiologie
La prévalence du syndrome du QT long congénital est inconnue. Toutefois, il est estimé qu'entre 1:2000 et 1:20 000 sont atteint de la mutation génétique causant l'allongement de l'intervalle QT. Cliniquement, plus d'hommes que de femmes présentent ce trait. Quant à la prévalence et l'incidence de la torsade de pointes d'origine médicamenteuse, elle reste largement inconnue puisque cette arythmie est souvent transitoire et qu'un diagnostic précis nécessite l'enregistrement d'un ECG pendant l'événement. Néanmoins, plusieurs centres européens estiment que le taux annuel de torsade de pointes d'origine médicamenteuse rapportée se situe entre 0,8 et 1,2 par million personnes-années. L'incidence de la torsade de pointes induite par des médicaments varie également en fonction du médicament en question et de la population étudiée.[5][6][7]
Étiologies
La torsade de pointes est causée par un allongement de l'intervalle QTc qui peut être congénital ou acquis.
Le syndrome du QT long acquis est majoritairement d'origine médicamenteuse (voir section facteurs de risque).
Le syndrome du QT long congénital est la maladie des canaux ioniques la plus commune et a deux variantes génétiques prédominantes : le syndrome de Jervell et Lange-Nielsen et le syndrome de Romano-Ward.[8][4]
| Syndrome | Caractéristique |
|---|---|
| Syndrome de Jervell et de Lange-Nielsen |
|
| Syndrome de Romano-Ward |
|
Physiopathologie
La torsade de pointes est associée à l'allongement de l'intervalle QTc. Le QTc allongé est l'allongement du QT corrigé pour la fréquence cardiaque. On le calcule avec la formule suivante : QTC = QT / √ RR [10]. Un QTc est considéré comme long lorsqu'il est supérieur à 450 ms chez les hommes et à 460 ms chez les femmes. Un QTc supérieur à 500 ms a été associé à une augmentation de deux à trois fois du risque de torsade de pointes.

Le mécanisme proposé pour la torsade de pointes implique l'inhibition du courant potassique à rectification retardée (delayed rectifier potassium current). Cela conduit à un excès d'ions positifs au sein de la membrane cellulaire provoquant une phase de repolarisation prolongée. Si un battement ectopique est généré pendant cette phase de repolarisation prolongée, connue sous le nom de phénomène R sur T, cela peut entraîner une torsade de pointes. L'allongement de l'intervalle QT congénital et médicamenteux affecte la membrane cellulaire de manière similaire en bloquant le canal potassique en question. La torsade de pointes est légèrement différente de la fibrillation ventriculaire parce qu'elle peut se résoudre spontanément. Cependant, la torsades de pointes peut évoluer vers une fibrillation ventriculaire si elle n'est pas traitée.[11][4]
Présentation clinique
Facteurs de risque
Les facteurs de risque de la torsade de pointes sont[4][9][12] :
- l'âge de plus de 65 ans
- le sexe féminin
- des antécédents familiaux de surdité congénitale
- des antécédents familiaux de mort subite chez l'adulte
- des antécédents familiaux de mort subite du nourrisson
- l'hypokaliémie
- l'hypocalcémie
- l'hypomagnésémie
- les troubles du système nerveux central (hémorragie sous-arachnoïdienne, hémorragie intraparenchymateuse, traumatisme crânien, tumeur cérébrale)
- la bradycardie
- les maladies cardiovasculaires
- la myocardite
- le prolapsus de la valve mitrale
- le stress ou l'stress (chez les patients atteints du syndrome du QT long congénital)
- les diurétiques, les antiarythmiques, les antipsychotiques, les antidépresseurs, les antiémétiques, les antifongiques et les antimicrobiens
- les plus courants : amiodarone, procainamide, levofloxacin, clarithromycin, haloperidol, quetiapine, fluoxétine, venlafaxine
- une liste exhaustive des médicaments est disponible ici[note 1].
Questionnaire
Environ 50% des patients atteints sont asymptomatiques. Lorsque les patients sont symptomatiques, les symptômes de la torsade de pointes sont [9]:
- la syncope, des palpitations, des étourdissements (récurrents ou isolés)
- des nausées
- des sueurs
- de la dyspnée
- des douleurs thoraciques peuvent aussi survenir, mais demeurent non spécifiques.
Examen clinique
À l'examen physique, on peut retrouver les signes suivants [9]:
- des signes suggestifs d'arrêt cardiaque
- aux signes vitaux : l'hypotension artérielle, la tachycardie, l'apnée, la tachypnée et la désaturation
- à l'apparence générale : l'altération de l'état de conscience, la pâleur et la diaphorèse
- à l'examen cardiaque :
- un rythme cardiaque irrégulier
- la présence ou l'absence de pouls périphérique.
Examens paracliniques
ECG

L'ECG est l'investigation primordiale permettant le diagnostic d'une torsade de pointes. À l'ECG on peut voir:
- une fluctuation d'amplitude variable des complexes QRS autour de la ligne isoélectrique
- une série d'intervalles R-R courts-longs-courts (qui précède l'apparition des torsades de pointe)
- une extrasystole ventriculaire survenant sur l'onde T précédent le début de la torsade.
Un nomogramme de l'intervalle QT peut fournir une évaluation sensible et spécifique du risque de torsade de pointes dans l'allongement de l'intervalle QTc d'origine médicamenteuse. Pour utiliser ce nomogramme dont l'axe des X est la fréquence cardiaque et l'axe des Y est l'intervalle QT, il suffit de mesurer manuellement l'intervalle QT sur un ECG (du début de l'onde Q jusqu'à la fin de l'onde T) dans 6 dérivations et d'en calculer la moyenne. Ensuite, on place cet intervalle QT en fonction de la fréquence cardiaque sur le nomogramme. [13] Toute valeur tracée au-dessus de la ligne sur le nomogramme expose le patient à un risque de torsade de pointes. [14][15][4]
Bilans sanguins
Le bilan sanguin comprend [9]:
- les électrolytes sanguins : rechercher une hypoglycémie, une hypokaliémie, une hypomagnésémie et une hypocalcémie
- les troponines : permet d'éliminer un infarctus du myocarde lorsque suspecté
- d'autres tests selon l'étiologie suspectée.
Diagnostic différentiel
Le diagnostic différentiel comprend [4]:
- la tachycardie ventriculaire
- la fibrillation ventriculaire
- un problème de monitoring électrique (électrodes, artéfact).
Traitement
Traitement en aigu
| Traitement | Pour qui ? | Explications |
|---|---|---|
| Mesures générales[4] |
|
|
| Magnésium IV |
|
|
| Cardioversion électrique |
|
|
| Défibrillation |
|
|
Traitement chronique
| Type de traitement | Explications |
|---|---|
| Pharmacologique |
|
| Stimulation électrosystolique rapide |
|
Suivi
Les patients qui reçoivent un diagnostic de syndrome du QT allongé congénital doivent malheureusement être informés que l'activité physique peut provoquer une arythmie mortelle. Le pharmacien joue un rôle important quant à l'éducation par rapport à la compliance médicamenteuse afin de prévenir les récurrences. Une attention toute particulière doit être portée lors de la prescription et de l'administration de médicaments prolongeant le QT. Tous les patients devraient savoir prendre leur pouls et leurs proches doivent être formés à prodiguer des soins de réanimation de base. Enfin, un suivi serré est recommandé puisque le risque de mort subite est réel.
Complications
Les complications de la torsade de pointes sont[4] :
- la fibrillation ventriculaire
- la mort subite (10 % des patients).
Évolution
La plupart des épisodes de torsade sont spontanément résolutifs. Cependant, le danger de développer une fibrillation ventriculaire demeure réel.
L'évolution de la maladie dépend grandement de sa cause : congénitale ou acquise.
- Les formes acquises possèdent un très bon pronostic, puisqu'elle peuvent être prise en charge en retirant le facteur déclencheur.
- La forme congénitale possède un pronostic moins favorable. En effet, sans traitement plus de la moitié des patients atteints décéderont dans les 5 ans. Avec un traitement prophylactique, ce taux peut être réduit à moins de 10%.
Prévention
La première étape de la gestion de la torsade de pointes consiste à prévenir leur apparition en ciblant les facteurs de risque modifiables. Cela comprend l’arrêt de tout médicament prolongeant l’intervalle QT et l’optimisation du profil électrolytique d’un patient. La correction de l'hypokaliémie, de l'hypomagnésémie et de l'hypocalcémie peut aider à prévenir l'apparition de torsades. Il existe un petit nombre d'études qui montrent un bénéfice prophylactique possible du magnésium par voie orale ou IV pour les patients présentant un QT allongé d'origine médicamenteuse. Cependant, le bénéfice global n'est pas bien établi et il y a peu de preuves que le magnésium ait un effet sur l'intervalle QT réel.
Notes
- ↑ Il existe une longue liste de médicaments qui peuvent prédisposer une personne à la torsade de pointes. Il est aussi possible de classer les médicaments selon leur potentiel à engendrer une prolongation de l'intervalle QT et donc une torsade de pointes. Un outil utile à cette fin est disponible ici (liste exhaustive et continuellement mise à jour des médicaments pouvant allonger le QT). Les substances qui ralentissent le métabolisme hépatique de ces médicaments peuvent potentialiser l'allongement de l'intervalle QTc, entraînant une probabilité accrue de torsade de pointes.
- ↑ Confusion, hyporéflexie, faiblesse musculaire, hypotension artérielle, dépression respiratoire, coma, arrêt cardiaque.
Références
- Cette page a été modifiée ou créée le 2020/11/07 à partir de Torsade de Pointes (StatPearls / Torsade de Pointes (2020/08/10)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/29083738 (livre).
- ↑ Steven Van Laecke, « Hypomagnesemia and hypermagnesemia », Acta Clinica Belgica, vol. 74, no 1, , p. 41–47 (ISSN 2295-3337, PMID 30220246, DOI 10.1080/17843286.2018.1516173, lire en ligne)
- ↑ Ronald Wilders et Arie O. Verkerk, « Long QT Syndrome and Sinus Bradycardia-A Mini Review », Frontiers in Cardiovascular Medicine, vol. 5, , p. 106 (ISSN 2297-055X, PMID 30123799, Central PMCID 6085426, DOI 10.3389/fcvm.2018.00106, lire en ligne)
- ↑ Qasim Khan, Mohammad Ismail et Iqbal Haider, « High prevalence of the risk factors for QT interval prolongation and associated drug-drug interactions in coronary care units », Postgraduate Medicine, vol. 130, no 8, , p. 660–665 (ISSN 1941-9260, PMID 30145917, DOI 10.1080/00325481.2018.1516106, lire en ligne)
- ↑ 4,0 4,1 4,2 4,3 4,4 4,5 4,6 et 4,7 Brian Cohagan et Dov Brandis, StatPearls, StatPearls Publishing, (PMID 29083738, lire en ligne)
- ↑ M. Salem, T. Reichlin, D. Fasel et A. Leuppi-Taegtmeyer, « Torsade de pointes and systemic azole antifungal agents: Analysis of global spontaneous safety reports », Global Cardiology Science & Practice, vol. 2017, no 2, , p. 11 (ISSN 2305-7823, PMID 29644223, Central PMCID 5871400, DOI 10.21542/gcsp.2017.11, lire en ligne)
- ↑ Andreu Porta-Sánchez, Cameron Gilbert, Danna Spears et Eitan Amir, « Incidence, Diagnosis, and Management of QT Prolongation Induced by Cancer Therapies: A Systematic Review », Journal of the American Heart Association, vol. 6, no 12, (ISSN 2047-9980, PMID 29217664, Central PMCID 5779062, DOI 10.1161/JAHA.117.007724, lire en ligne)
- ↑ Charlotte P. M. Heemskerk, Marieke Pereboom, Karlijn van Stralen et Florine A. Berger, « Risk factors for QTc interval prolongation », European Journal of Clinical Pharmacology, vol. 74, no 2, , p. 183–191 (ISSN 1432-1041, PMID 29167918, DOI 10.1007/s00228-017-2381-5, lire en ligne)
- ↑ Gabrielli, Andrea., Layon, A. Joseph., Yu, Mihae. et Civetta, Joseph M., Civetta, Taylor, & Kirby's critical care, Lippincott Williams & Wilkins, (ISBN 978-0-7817-6869-6 et 0-7817-6869-1, OCLC 253189100, lire en ligne)
- ↑ 9,0 9,1 9,2 9,3 9,4 et 9,5 « Torsade de Pointes: Overview, Pathophysiology, Etiology of Torsade », 24 juillet 2020. https://emedicine.medscape.com/article/1950863-overview#a4.
- ↑ (en-US) « QT Interval • LITFL Medical Blog • ECG Library Basics », sur Life in the Fast Lane • LITFL • Medical Blog, (consulté le 30 décembre 2020)
- ↑ Aksana Baldzizhar, Ekaterina Manuylova, Roman Marchenko et Yury Kryvalap, « Ventricular Tachycardias: Characteristics and Management », Critical Care Nursing Clinics of North America, vol. 28, no 3, , p. 317–329 (ISSN 1558-3481, PMID 27484660, DOI 10.1016/j.cnc.2016.04.004, lire en ligne)
- ↑ Duke, James, 1957-, Anesthesia secrets, Hanley & Belfus, (ISBN 978-1-56053-354-2 et 1-56053-354-4, OCLC 42476269, lire en ligne)
- ↑ (en) A. Chan, G. K. Isbister, C. M. J. Kirkpatrick et S. B. Dufful, « Drug-induced QT prolongation and torsades de pointes: evaluation of a QT nomogram », QJM: An International Journal of Medicine, vol. 100, no 10, , p. 609–615 (ISSN 1460-2725, DOI 10.1093/qjmed/hcm072, lire en ligne)
- ↑ Mariëlle Alders, Hennie Bikker et Imke Christiaans, GeneReviews®, University of Washington, Seattle, (PMID 20301308, lire en ligne)
- ↑ J. Rick Turner, Ignacio Rodriguez, Emily Mantovani et Gary Gintant, « Drug-induced Proarrhythmia and Torsade de Pointes: A Primer for Students and Practitioners of Medicine and Pharmacy », Journal of Clinical Pharmacology, (ISSN 1552-4604, PMID 29672845, DOI 10.1002/jcph.1129, lire en ligne)
