Retard staturo-pondéral
| Maladie | |
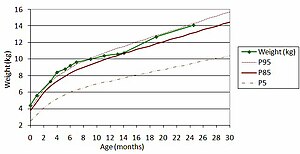 Une courbe de croissance normale pour une fille | |
| Caractéristiques | |
|---|---|
| Signes | Splénomégalie, Chéilite, Koïlonichie, Hépatomégalie, Hypotonie , Cassure de la courbe de croissance, Retard dans la courbe de croissance, Mauvaise hygiène corporelle, Rash, Hématomes, ... [+] |
| Symptômes |
Ronflement, Dysphagie, Régression développementale, Apnée du sommeil, Diarrhée , Vomissement , Perte de poids |
| Diagnostic différentiel |
Malnutrition, Kwashiokor, Marasme, Petite taille constitutionnelle |
| Informations | |
| Autres noms | Retard de croissance |
| Wikidata ID | Q1497481 |
| Spécialité | Pédiatrie |
|
| |
Retard staturo-pondéral (31-2)
Le retard staturo-pondéral (RSP) indique un gain de poids ou de taille insuffisant ou une perte de poids inappropriée chez les enfants ou les nourissons [1]
Le RSP est suggéré par une chute d'un ou plusieurs espaces centiles sur une courbe de croissance en fonction du poids à la naissance ou lorsque le poids est inférieur au 2e centile de poids pour l'âge, quel que soit le poids à la naissance. [2][3] Chez les enfants dont le poids à la naissance se situait entre le 9e et le 91e centile, le RSP est évoqué par une chute sur 2 espaces centiles ou plus.
Épidémiologie
Le retard de croissance est un problème présent courant dans la population pédiatrique. Le retard de croissance est très répandu aux États-Unis, représentant 5 à 10% des enfants considérés comme consultations externes par médecins généralistes. [4] Le retard de croissance est plus fréquent chez les enfants de statut socio-économique inférieur et [4] Le retard de croissance représente 3 à 5% de toutes les admissions à l'hôpital pour les enfants de moins de deux ans.[5][6] Des études rétrospectives suggèrent que les hommes sont légèrement plus susceptibles que les femmes d'être admis à l'hôpital pour échec pour prospérer (53,2% contre 46,7%). [6]
Facteurs de risque
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section contient les facteurs de risque de la maladie. Ces facteurs de risque peuvent être des maladies, des anomalies génétiques, des caractéristiques individuelles (l'âge, le sexe, l'origine ethnique, un certain type d'alimentation), etc. |
| Formats: | Liste à puces, Tableau |
| Balises sémantiques: | Facteur de risque |
| Commentaires: |
|
| Exemple: | Les facteurs de risque de l'infarctus du myocarde sont :
|
Étiologies
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section décrit les étiologies de la maladie, c'est-à-dire ce qui cause la maladie (ex. le diabète de type 2 cause la néphropathie diabétique). Les étiologies doivent être identifiées avec le modèle Étiologies. |
| Formats: | Texte, Liste à puces, Tableau |
| Balises sémantiques: | Étiologie |
| Commentaires: |
|
| Exemple: | Parmi les étiologies les plus courantes d'occlusion de l'intestin grêle, on retrouve :
|
Physiopathologie
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | La physiopathologie traite des mécanismes biologiques qui conduisent à l'apparition d'une maladie. |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: | L'histopathologie doit figurer dans la section Examen paraclinique, et non dans la section physiopathologie. |
| Exemple: | Le VIP est une neurohormone composée de 28 acides aminés et appartenant à la famille des sécrétines-glucagon. Il est produit dans le système nerveux central ainsi que dans les neurones des voies gastro-intestinales, respiratoires et urogénitales. Il agit, via l'expression d'adénylate cyclase cellulaire (AMPc), à titre de vasodilatateur et de régulateur de l'activité des muscles lisses, de stimulateur de la sécrétion d'eau et d'électrolytes par le tractus intestinal, d'inhibiteur de la sécrétion d'acide gastrique et de promoteur du flux sanguin principalement dans le tractus gastro-intestinal. L'ensemble de ces éléments peuvent entraîner une hypokaliémie, une hyperglycémie, une hypomagnésémie et une hypercalcémie qui sont habituellement responsables de la présentation clinique. |
Présentation clinique
Le retard de croissance survient chez les enfants dont l'apport nutritionnel est insuffisant pour soutenir une croissance normale et une prise de poids.[7][8][9] Le retard de croissance se manifeste généralement avant deux ans, lorsque les taux de croissance sont les plus élevés. [8] Les médecins identifient souvent un retard de croissance lors des visites de bureau de routine, lorsque les paramètres de croissance d'un enfant ne suivent pas correctement les courbes de croissance.[8] Les médecins recherchent de nombreux signes à l'examen physique qui peuvent indiquer un cause potentielle de la TTF. Par exemple, des résultats tels que la desquamation de la peau, les ongles en forme de cuillère, la chéilose et la neuropathie peuvent indiquer des carences potentielles en vitamines et en minéraux.[10] Syndrome d'alcoolisme fœtal (SAF) a également été associé à la TTF et peut présente des signes caractéristiques, notamment une microcéphalie, de courtes fissures palpébrales, un philtrum lisse et une fine bordure de vermillon. retard de croissance de l'émaciation, car ils peuvent indiquer différentes causes de TTF. "Gaspillage" fait référence à une décélération de la taille de plus de 2 écarts-types par rapport au poids médian par rapport à la taille, tandis que " retard de croissance" est une baisse de plus de 2 écarts-types de la taille médiane -pour-age.[11] Le schéma caractéristique observé chez les enfants dont l'apport nutritionnel est insuffisant est une décélération initiale de la prise de poids, suivie plusieurs semaines à plusieurs mois plus tard par une décélération de la stature, et enfin une décélération de la circonférence de la tête.[12] Une diminution de la longueur avec une perte de poids proportionnelle peut être liée à des facteurs nutritionnels de longue date ainsi qu'à des causes génétiques ou endocriniennes.[12] Le tour de tête peut également être un indicateur de l'étiologie de la TTF. Si la circonférence de la tête est affectée initialement en plus du poids ou de la longueur, d'autres facteurs sont des causes plus probables qu'un apport insuffisant. Certains d'entre eux comprennent une infection intra-utérine, des tératogènes et certains syndromes congénitaux. [12]
La perte de poids après la naissance est normale et la plupart des bébés retrouvent leur poids à la naissance à l'âge de trois semaines.[2] L'évaluation clinique de la TTF est recommandée pour les bébés qui perdent plus de 10% de leur poids de naissance ou qui ne reviennent pas à leur poids de naissance après trois semaines. semaines.[2]
Examine les paracliniques
Toute contribution serait appréciée.
| Description: | Cette section concerne les tests à demander lorsque la maladie est suspectée et les résultats attendus en présence de la maladie. |
| Formats: | Liste à puces, Tableau |
| Balises sémantiques: | Examen paraclinique, Signe paraclinique |
| Commentaires: |
|
| Exemple: | Les examens suivants sont utiles dans la démarche d'investigation du VIPome :
|
- Investigation 1: signe paraclinique 1, signe paraclinique 2, ...
- Investigation 2: signe paraclinique 3, signe paraclinique 4, ...
- ...
Approche clinique
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Alors que les sections Questionnaire, Examen clinique et Examens paracliniques servent à énumérer, cette section sert à intégrer tous ces éléments pour discuter du raisonnement du clinicien. C'est en quelque sorte la manière dont les cliniciens réfléchissent lorsque confrontés à cette maladie : c'est la section par excellence pour l'enseignement. |
| Formats: | Texte, Liste à puces, Tableau |
| Balises sémantiques: | |
| Commentaires: |
|
| Exemple: | |
Diagnostic
La TTF peut être évaluée par le biais d'un processus à multiples facettes, en commençant par les antécédents du patient qui incluent notamment les antécédents alimentaires, qui est un élément clé pour identifier les causes potentielles de la TTF.[13][14] Ensuite, un examen physique complet peut être effectué, en accordant une attention particulière à l'identification sources organiques possibles de RSP.[13] Cela pourrait inclure la recherche de caractéristique dysmorphique, de bruits respiratoires anormaux et de signes spécifiques carences en vitamines et minéraux. [13] L'examen physique peut également révéler des signes de possible négligence ou maltraitance envers les enfants.[13] Sur la base des informations obtenues à partir de l'historique et de l'examen physique, un bilan peut ensuite être effectué, dans lequel des sources possibles de TTF peuvent être davantage sondées, par des analyses de sang, des radiographies ou d'autres tests. [13] Laboratory devrait être orienté en ce qui concerne les résultats de l’historique et de l’examen physique, car on estime que l'utilité des examens de laboratoire pour les enfants en retard de croissance est de 1,4% .[7] L'analyse sanguine initiale doit être basée sur le tableau clinique de l'enfant. Les analyses sanguines courantes devraient inclure un CBC avec différentiel, un panel métabolique complet pour rechercher des troubles électrolytiques, un test de la fonction thyroïdienne et une analyse d'urine.[15] Si indiqué, des anticorps IgA anti-TTG peuvent être utilisés pour évaluer la maladie coeliaque et un chlorure de sueur test est utilisé pour dépister la mucoviscidose. [15] Si aucune cause n'est découverte, un examen des selles pourrait être indiqué pour rechercher des matières grasses ou réductrices. [15] La protéine C réactive et le taux de sédimentation des érythrocytes (ESR) peuvent également être utilisés pour rechercher des signes de inflammation.[15]
Diagnostic différentiel
Toute contribution serait appréciée.
| Description: | Cette section traite du diagnostic différentiel de la maladie, c'est-à-dire aux autres diagnostics à évoquer lorsque confronté à ce diagnostic. |
| Formats: | Liste à puces |
| Balises sémantiques: | Diagnostic différentiel |
| Commentaires: |
|
| Exemple: | Le diagnostic différentiel de l'appendicite comprend :
|
Traitement
Les nourrissons et les enfants qui ont eu des expériences alimentaires désagréables (par exemple reflux acide ou intolérance alimentaire) peuvent être réticents à manger leurs repas.[14] De plus, le fait de nourrir de force un nourrisson ou un enfant peut décourager une auto-alimentation appropriée. [14] Les interventions psychosociales peuvent viser à encourager l'enfant à se nourrir pendant les repas.[2][14] De plus, faire des heures de repas une expérience positive et agréable grâce à l'utilisation d'un renforcement positif peut également améliorer les habitudes alimentaires des enfants présentant une TTF.[2][14] Si des problèmes de comportement persistent et affectent les habitudes nutritionnelles des enfants atteints de TTF, il est recommandé que l'enfant consulte un psychologue.[14] Si une affection sous-jacente, telle qu'une maladie intestinale inflammatoire, est cause du retard de croissance de l'enfant, le traitement est direct ed vers la condition sous-jacente. Syndrome de réalimentation est causé par un changement de liquide et d'électrolytes chez une personne souffrant de malnutrition lors de la réalimentation artificielle.[16] Elle est potentiellement mortelle et peut survenir en cas de nutrition entérale ou parentérale.[17] L'anomalie électrolytique la plus grave et la plus courante est hypophosphatémie, bien que les anomalies sodiques soient également courantes. Il peut également provoquer des changements dans le métabolisme du glucose, des protéines et des graisses.[18] L'incidence du syndrome de réalimentation est élevée, avec une étude de cohorte prospective montrant que 34% des soins intensifs ont souffert d'hypophosphatémie peu de temps après le redémarrage de l'alimentation.[19]
Suivi
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section traite du suivi de la maladie. |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: |
|
| Exemple: | |
Complications
Toute contribution serait appréciée.
| Description: | Cette section traite des complications possibles de la maladie. |
| Formats: | Liste à puces, Texte |
| Balises sémantiques: | Complication |
| Commentaires: |
|
| Exemple: | Les complications de l'infarctus du myocarde sont :
|
Évolution
Les enfants qui ne parviennent pas à prospérer courent un risque accru de croissance à long terme, de complications cognitives et comportementales.[4] Des études ont montré que les enfants qui ne réussissaient pas à prospérer pendant la petite enfance avaient un poids plus court et plus faible à l'âge scolaire que leurs pairs. Le retard de croissance peut également avoir pour conséquence que les enfants n'atteignent pas leur potentiel de croissance, selon les estimations de taille mi-parentale. [4][20] Études longitudinales ont également démontré une baisse du QI (3 à 5 points) et une performance arithmétique plus faible chez les enfants ayant des antécédents de retard de croissance, par rapport aux pairs recevant une nutrition adéquate en tant que nourrissons et tout-petits. , cependant, des études ont montré que le retard de croissance peut entraîner des problèmes de comportement persistants, malgré un traitement approprié.[4]
Prévention
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section traite des mesures préventives et du dépistage précoce de la maladie (lorsque pertinent). |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: | |
| Exemple: | La prévention primaire consiste à la prise en charge des facteurs de risque :
|
Fait partie de la présentation clinique de ...
Est une complication de ...
Références
- ↑ « Weight faltering and failure to thrive in infancy and early childhood », BMJ, vol. 345, no sep25 1, , e5931 (PMID 23014901, DOI 10.1136/bmj.e5931, lire en ligne)
- ↑ 2,0 2,1 2,2 2,3 et 2,4 National Guideline Alliance (UK), Faltering Growth – recognition and management, London, National Institute for Health and Care Excellence (UK), coll. « National Institute for Health and Care Excellence: Clinical Guidelines », (ISBN 978-1-4731-2693-0, PMID 28991420, lire en ligne)
- ↑ « Weight-for-age Child growth standards », sur World Health Organization
- ↑ 4,0 4,1 4,2 4,3 et 4,4 Larson-Nath C, Biank VF, « Clinical Review of Failure to Thrive in Pediatric Patients », Pediatric Annals, vol. 45, no 2, , e46-9 (PMID 26878182, DOI 10.3928/00904481-20160114-01)
- ↑ Goh LH, How CH, Ng KH, « Failure to thrive in babies and toddlers », Singapore Medical Journal, vol. 57, no 6, , p. 287–291 (PMID 27353148, Central PMCID 4971446, DOI 10.11622/smedj.2016102)
- ↑ 6,0 et 6,1 Thompson RT, Bennett WE, Finnell SM, Downs SM, Carroll AE, « Increased length of stay and costs associated with weekend admissions for failure to thrive », Pediatrics, vol. 131, no 3, , e805-10 (PMID 23439903, DOI 10.1542/peds.2012-2015, lire en ligne)
- ↑ 7,0 et 7,1 Ingo Scholler et S. Nittur, « Understanding failure to thrive », Paediatrics and Child Health, vol. 22, no 10, , p. 438–442 (DOI 10.1016/j.paed.2012.02.007)
- ↑ 8,0 8,1 et 8,2 Basil J Zitelli, Sara C McIntire et Andrew J Nowalk, Zitelli and Davis' atlas of pediatric physical diagnosis, Philadelphia, Pennsylvania, Sixth, (ISBN 978-0-323-07932-7, OCLC 793494374)
- ↑ Robert Kliegman, Patricia S Lye, Brett J Bordini, Heather Toth et Donald Basel, Nelson pediatric symptom-based diagnosis, Philadelphia, Pennsylvania, (ISBN 978-0-323-39956-2, OCLC 986243536)
- ↑ « {{{1}}} »
- ↑ « UNICEF - Definitions », sur www.unicef.org
- ↑ 12,0 12,1 et 12,2 « {{{1}}} »
- ↑ 13,0 13,1 13,2 13,3 et 13,4 « Growth failure in children: a symptom or a disease? », Nutrition in Clinical Practice, vol. 28, no 6, , p. 651–658 (PMID 24170580, DOI 10.1177/0884533613506015)
- ↑ 14,0 14,1 14,2 14,3 14,4 et 14,5 « The toddler who is falling off the growth chart », Paediatrics & Child Health, vol. 17, no 8, , p. 447–54 (PMID 24082808, Central PMCID 3474389, DOI 10.1093/pch/17.8.447)
- ↑ 15,0 15,1 15,2 et 15,3 « {{{1}}} »
- ↑ « Minerva », BMJ, vol. 336, no 7639, , p. 336.2–336 (ISSN 0959-8138, Central PMCID 2234541, DOI 10.1136/bmj.39479.508819.80)
- ↑ « Hyperalimentation, Hypophosphatemia and Coma », Anesthesiology, vol. 38, no 3, , p. 308 (ISSN 0003-3022, DOI 10.1097/00000542-197303000-00032)
- ↑ Stephen D Hearing, « Refeeding syndrome », BMJ, vol. 328, no 7445, , p. 908–909 (ISSN 0959-8138, PMID 15087326, Central PMCID 390152, DOI 10.1136/bmj.328.7445.908)
- ↑ Paul E. Marik, « Refeeding Hypophosphatemia in Critically Ill Patients in an Intensive Care Unit », Archives of Surgery, vol. 131, no 10, , p. 1043–7 (ISSN 0004-0010, PMID 8857900, DOI 10.1001/archsurg.1996.01430220037007)
- ↑ « The developmental sequelae of nonorganic failure to thrive », Journal of Child Psychology and Psychiatry, and Allied Disciplines, vol. 41, no 8, , p. 1003–14 (PMID 11099117, DOI 10.1111/1469-7610.00688)
- Cette page a été modifiée ou créée le 2020/03/24 à partir de Failure_to_thrive (927408879), écrite par les contributeurs de Wikipedia (en) et partagée sous la licence CC-BY-SA 4.0 international. Le contenu original est disponible à https://en.wikipedia.org/wiki/Failure_to_thrive.
