Maladie de Hirschsprung
| Maladie | |
 | |
| Caractéristiques | |
|---|---|
| Signes | Fécalome, Diarrhée explosive à la sortie du doigt, Distension abdominale |
| Symptômes |
Retard staturo-pondéral, Intolérance à l'alimentation, Vomissements bilieux, Obstruction colique, Polyhydramnios, Non-passage du méconium, Abdomen souple et distendu, Dépendance aux lavements sans encoprésie, Diarrhée , Constipation , ... [+] |
| Diagnostic différentiel |
Dysplasie neuronale intestinale, Hypoganglionose isolée, Ganglioneuromatose intestinale, Ganglions immatures, Absence de plexus argyrophile, Achalasie du sphincter anal interne, Syndrome d'hypopéristaltisme intestinal mégacystis-microcolon |
| Informations | |
| Terme anglais | Hirschsprung's disease, Colonic aganglionosis |
| Wikidata ID | Q34733361 |
| SNOMED CT ID | 204739008 |
| Spécialités | Pédiatrie, Chirurgie pédiatrique, Chirurgie générale |
|
| |
La maladie de Hirschsprung (MH) est une maladie congénitale colorectale définie par l'absence de cellules ganglionnaires (GC) dans la paroi du rectum et parfois aussi dans celle du colon plus proximal. Cette maladie est souvent syndromique et diagnostiquée dans les premiers jours de vie.
Épidémiologie
La MH survient chez 1/5000 naissances vivantes et a une prédominance masculine globale de 4: 1.[1] Une inversion de ce ratio est observée dans la littérature lorsque la MH est sous forme pancolique ou étendue.[2] La MH est une maladie congénitale, se présentant principalement dans la période néonatale. Le diagnostic est posé dans 65% des cas avant l'âge de 1 mois et dans 95% des cas avant l'âge d'un an.[3] Il est rarement diagnostiqué à l'âge adulte, bien que, dans la littérature, l'âge le plus âgé au diagnostic est de 74 ans.[4][5] Chez l'adulte, il s'agit du Hirschprung très court qui occasionne un tableau de constipation sévère (et non d'occlusion).
Étiologie
La transmission de la MH est complexe et implique une transmission multigénique. Sa pénétrance est faible, variable et dépendante du sexe. Le principal gène impliqué est le proto-oncogène RET trouvé dans environ 35% des cas sporadiques et 49% des cas familiaux. Des mutations RET[6] peuvent survenir dans l'un des 21 exons du gène. Plus de 100 mutations différentes ont été identifiées. Ceux-ci incluent le non-sens, le faux-sens, les délétions et les insertions.[7][8]
Les autres gènes impliqués dans la pathogénèse de la MH sont impliqués dans seulement 5 à 10% des cas. Il comprend les ligands du récepteur RET[7][5]:
- le facteur neurotrophique dérivé des cellules gliales (GDNF)
- l'endothéline-3
- le récepteur B de l'endothéline (EDNRB)
- le facteur de transcription SOX1
- le gène PHOX2B.
Physiopathologie
Dans la MH, il y a une perturbation du processus de migration et de différenciation des cellules de la crête neurale (CCN) au niveau du système nerveux entérique, qui est sous le contrôle du gène RET et de ses ligands. Vers la 13e semaine de conception, les GC migrent d'abord vers le plexus myentérique, puis vers le plexus sous-muqueux.[9] Les modèles animaux ont mis en évidence un arrêt ou un retard dans la migration des CCN comme facteur derrière la pathogenèse de la MH. [10][5] Cette perturbation entraîne une absence totale de GC dans les plexus nerveux. Cela conduit à une hyperactivité de l'intestin avec la libération persistante d'acétylcholine. Par la suite, il y a une contraction continue du segment colique rétréci (affecté) et une dilatation secondaire progressive du côlon proximal sain.[1] [5] L'absence de ces cellules nécessaires à la transmission des neurotransmetteurs entraîne une non-relaxation de la musculeuse et donc une obstruction fonctionnelle, de l'ordre de la constipation jusqu'à l'obstruction complète.
L'atteinte est habituellement limitée au court segment rectal avec une zone de transition à la jonction rectosigmoïdienne (dans 75% des cas), mais peut atteindre le long segment de la MH (dans 20% des cas), allant jusqu'à l'angle splénique ou au côlon transverse, ou même atteindre tout le colon (dans 5% des cas). L'atteinte varie entre la non-relaxation d'un segment, allant jusqu'à l'obstruction fonctionnelle.
Présentation clinique
Facteurs de risque
Les nourrissons de sexe masculin sont plus à risque d'avoir la MH que ceux de sexe féminin, pour un ratio de 4 garçons pour 1 fille.
De associations avec des anomalies génétiques ont été rapportées[11][5][12] :
- la trisomie 21
- des neurocristopathies:
- le syndrome de Goldberg-Shprintzen
- le syndrome de Smith-Lemli-Opitz
- un MEN 2
- le syndrome d'Ondine (hypoventilation alvéolaire centrale congénitale)
- des anomalies congénitales isolées:
- une maladie cardiaque congénitale
- une malrotation intestinale
- des anomalies des voies urinaires
- des anomalies du système nerveux central
- et autres.
Questionnaire
Ces symptômes sont à rechercher lors du questionnaire chez le nouveau-né:
- un polyhydramnios ou autres indices anormaux du liquide amniotique maternel
- le non-passage du méconium pendant les 48 premières heures de la vie (présent chez 90% des patients atteints)[13] [5]
- des symptômes d'obstruction colique (peut survenir au début de la période néonatale jusqu'à l'âge adulte)[13][5]
- de la constipation
- des vomissements bilieux
- une intolérance à l'alimentation[12].
Les caractéristiques cliniques de l'entérocolite associée à Hirschsprung (HAEC) sont d'autres indicateurs importants dans l'histoire des patients suspectés de MH[12]:
- de la fièvre
- de la diarrhée
- un abdomen souple et distendu.
Un enfant avec une présentation plus tardive aura comme symptômes[12]:
- un antécédent de retard de passage du méconium à la naissance
- un retard de croissance
- une dépendance aux lavements sans encoprésie significative.
Examen clinique
Ces éléments seront retrouvés à l'examen physique du nouveau-né:
- aux signes vitaux et à l'examen général, vérifier les signes de déshydratation
- à l'examen de l'abdomen : une distension abdominale
- au toucher rectal : une diarrhée explosive à la sortie du doigt chez le nouveau-né, un canal anal et une ampoule rectale rétrécis ou vides.
Ces éléments seront retrouvés à l'examen physique chez l'enfant avec une présentation plus tardive:
- à l'examen de l'abdomen : une distension abdominale
- au toucher rectal : un fécalome.
Examens paracliniques
Histopathologie
Pour l'évaluation de la MH, une biopsie rectale jusqu'à la sous-muqueuse est à faire. Ces éléments seront trouvés en histopathologie :
- un absence de GC dans le plexus sous-muqueux et myentérique[14][note 1]
- une hypertrophie des fibres nerveuses dans le segment aganglionnaire.
Pour réduire le taux de résultats non concluants liés à des biopsies inadéquates, le Comité international de gastroentérologie de 2009 a défini des critères pour effectuer des biopsies préopératoires, nécessaires pour assurer une bonne interprétation [15][5] :
- au moins deux biopsies doivent être nécessaires, avec un diamètre minimum de 3 mm.
- la biopsie doit avoir autant de muqueuse que de sous-muqueuse.
- elle doit être bien orientée, incluse dans le bon axe, pour éviter la perte de tissu entre les différents niveaux de coupe.
- les biopsies préopératoires doivent être réalisées à au moins 2 cm au-dessus de la ligne dentelée[note 2].
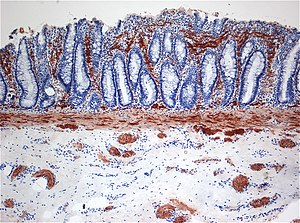
L'histopathologie conventionnelle avec coloration à l'hématoxyline-éosine (H et E) est couramment utilisée dans le diagnostic de la MH.[15][16] [5]La coloration à l'acétylcholinestérase (AChE) est une méthode auxiliaire pour identifier l'activité accrue des fibres nerveuses parasympathiques dans la lamina propria et la musculeuse muqueuse et ainsi, aider au diagnostic, en particulier dans les cas difficiles. L'intestin normalement innervé ne se colore pas avec AChE.[17][18] Cependant, la coloration AChE est une technique laborieuse, prend du temps et nécessite des techniciens et des pathologistes expérimentés. [18][19]
La perte d'expression de la calrétinine à l'absence de GC est caractéristique de la MH.[2] L'immunomarquage avec des anticorps anti-calrétinine entraîne une positivité GC et des fibres nerveuses interstitielles de la lamina propria, de la musculeuse muqueuse et de la sous-muqueuse.[20] Dans les dernières recommandations publiées dans 2009, le Comité international de gastroentérologie a introduit la perte d'expression de la calrétinine comme l'un des critères diagnostiques de la MH.[15]
L'examen des coupes congelées (examen extemporané) est essentiel dans la gestion de la MH. Elle peut être réalisée dans deux circonstances:
- pour établir le diagnostic de la MH
- pour identifier la zone ganglionnaire lors de la résection endoanale.[21][22]
Ce diagnostic est fait sur des biopsies, incluant uniquement la musculature de toutes les parois coliques. Il est de plus en plus recommandé de réaliser des biopsies circonférentielles pour poser un diagnostic définitif. [23][5]
Cependant, plusieurs obstacles ont été bien définis dans le processus d'obtention d'un diagnostic pathologique définitif. Il s'agit notamment du manque d'expertise des pathologistes en raison de la rare exposition aux échantillons, de la qualité inadéquate et inacceptable des échantillons, de la désorientation du tissu soumis vers le service de pathologie et des cellules ganglionnaires immatures normales chez les nouveau-nés.[24] [5]
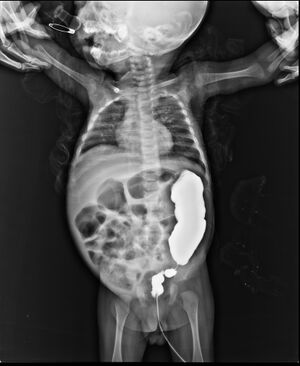
Imagerie
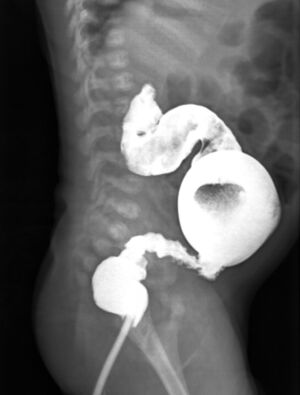
Les signes paracliniques suivants seront retrouvés au lavement de contraste chez un patient ayant la MH[5][25]:

- une zone de transition
- l'inversion du rapport rectosigmoïde[note 3]
- une irrégularité de la muqueuse
- une contraction irrégulière
- une rétention de contraste persistante (>24h).
Autre examen diagnostic
L'absence de RAIR (rectoanal inhibitory reflex) à la manométrie anorectale est diagnostic de la MH. [26][5]
Aucune prise de sang n'est nécessaire chez les patients cliniquement bien et hémodynamiquement stables.
Approche clinique
La suspicion de MH est élevée lorsqu'un enfant âgé de 0 à 6 mois se présente pour constipation et qu'il y a présence d'au moins un autre des signes et symptômes suivants:
- un délai du passage du méconium (>48h)
- une distension abdominale
- une anomalie génétique associée (ex.: Trisomie 21)
- un canal anal et une ampoule rectale rétrécis ou de la diarrhée explosive au toucher rectal.
La suspicion de MH est modérée lorsqu'un enfant de 6 mois à 3 ans se présente avec de la constipation réfractaire et qu'il y a présence d'au moins un autre des signes suivants:
- l'absence de selle dans l'ampoule rectale
- un canal anal et une ampoule rectale rétrécie ou de la diarrhée explosive au toucher rectal.
La suspicion de MH est faible lorsqu'un enfant se présente pour de la constipation réfractaire et qu'il n'y a présence d'aucun de ces signes et symptômes. Il est alors indiqué de faire une radiographie abdominale. S'il y a absence de selle dans le rectum et que ses symptômes sont sévères, ces patients doivent suivre les mêmes investigations que ceux avec suspicion élevée ou modérée.
Lorsque la suspicion de MH est élevée ou modérée, il est important de rechercher la présence de fièvre, de vomissement, de diarrhée et de distension abdominale pour évaluer la présence potentielle d'une complication grave et urgente de la MH: l'entérocolite associée à Hirschsprung (HAEC). Dans ce cas, une évaluation et un traitement en urgence doivent être faits.
Lorsque la possibilité de l'HAEC est éliminée, les patients avec suspicion élevée ou modérée de MH doivent passer un lavement de contraste ou une biopsie rectale avec ou sans manométrie anale (si âgé de > 1 mois). Si les résultats reviennent anormaux, le diagnostic de la MH est confirmé.
Diagnostic
Le diagnostic de la MH est basé sur une combinaison de caractéristiques cliniques, de résultats radiologiques et d'évaluation histopathologique de l'échantillon biopsié. Le diagnostic est confirmé par l'examen histopathologique des biopsies rectales.[5]
Diagnostic différentiel
Le diagnostic différentiel de la MH est [5][27][28][29] :
- la dysplasie neuronale intestinale
- l'hypoganglionose isolée
- la ganglioneuromatose intestinale
- des ganglions immatures
- l'absence de plexus argyrophile
- l'achalasie du sphincter anal interne
- le syndrome d'hypopéristaltisme intestinal mégacystis-microcolon.
Traitement
Préparation préopératoire
Le diagnostic de la MH nécessite presque exclusivement une intervention chirurgicale. Lorsque le diagnostic est posé, il faut traiter l'enfant avec des antibiotiques à large spectre, lui donner des fluides intraveineux, faire un drainage nasogastrique et une décompression rectale (soit par irrigation rectale ou par stimulation rectale). Les patients ayant d'autres anomalies associées doivent être évalués en conséquence[12].
Une fois que l'enfant est stabilisé, l'intervention chirurgicale peut être faite de façon semi-élective. Pendant le temps d'attente pour l'opération, l'enfant peut être retourné à la maison avec une alimentation de lait maternel ou une formule élémentaire, en combinaison avec des irrigations rectales.
L'irrigation rectale avant la chirurgie et dans la gestion des HAEC a quelques avantages cruciaux :
- la décompression de la taille du côlon
- la prévention de la complication la plus dévastatrice : l'entérocolite.
Les parents doivent être bien renseignés sur la bonne procédure pour faire des irrigations rectales et doivent avoir avec eux à la maison le matériel nécessaire pour cela.
Pour les enfants plus vieux ayant un colon extrêmement dilaté, la chirurgie devrait être reportée jusqu'à ce que le diamètre du colon ait diminué suffisamment pour faire la procédure sécuritairement[12].
Interventions chirurgicales
Les différents types de chirurgie visent à faire une résection de la zone atteinte et de descendre le segment non atteint (défini par une extemporanée où il y a présence de cellules ganglionnaires ou d'activité enzymatique) à la marge anale, tout en préservant la fonction normale du sphincter anal. La planification chirurgicale est profondément affectée par la présence de comorbidités. La MH à court segment sans aucune comorbidité peut être soumise à une procédure de pull-through en une seule étape, les autres atteintes de la MH (atteinte du long segment ou totale) ou ayant plusieurs comorbidités doivent commencer par une colostomie de dérivation temporaire.[30] [5] Le moment recommandé pour une procédure définitive varie de 4 à 6 mois après la mise en place de la colostomie.
Une variété de chirurgies pull-through ont été décrites :
- 'swenson :'
- une proctectomie
- tirer le côlon ganglionnaire sain à travers et l'anastomoser à l'anus avec un plan de dissection à l'extérieur du plan musculaire rectal
- 'duhamel :'
- une dissection rétrorectale en laissant le rectum natif en place
- faire une transsection proximale à la zone de transition
- abaisser le segment en rétrorectal
- perforer le rectum natif distalement
- faire une anastomose coloanale
- diviser le septum entre le rectum et le néorectum avec une agrafeuse
- 'soave' :
- une mucosectomie du rectum
- garder l'appareil sphinctérien pour faire l'anastomose coloanale différée ensuite (si immédiat, cela est appelé la technique de Boley).
- la période postopératoire de cette procédure est critique. Des séances régulières fréquentes de dilatations anastomotiques mécaniques, qui peuvent être effectuées à domicile, sont fortement recommandées.
- 'soave transanale' : cette chirurgie est faite en une seule étape au début de la période néonatale, ce qui peut éviter le besoin d'une incision abdominale et d'une colostomie.
Les procédures de Duhamel et de Soave ont l'avantage de préserver l'innervation complexe du rectum et de la vessie.[31] Il est possible d'utiliser l'assistance laparoscopique pour mobiliser le cadre colique avant de faire l'approche périnéale pour les segments malades plus longs.
S'il y a aganglionose complète, il est possible de faire une iléostomie de dérivation puis la procédure de Duhamel 1 an plus tard.
Toutes ces procédures ont des taux de réussite élevés et la morbidité est minime.[32] [5]
Complications
L'une des complications liées à la MH les plus courantes et les plus dévastatrices est l'entérocolite associée à Hirschsprung (HAEC), qui est définie comme un trouble inflammatoire de l'intestin. La sévérité des manifestations cliniques dans HAEC peut varier, les symptômes les plus fréquents sont de la diarrhée, de la distension abdominale et des manifestations systémiques. Il est essentiel de savoir reconnaitre cette condition, car elle peut être mortelle. La prise en charge de chaque patient atteint d'HAEC est basée sur le grade clinique correspondant. Dans l'HAEC de grade I ou suspectée, une prise en charge ambulatoire avec du métronidazole oral accompagné de liquide et d'électrolyte peut être envisagée. Les cas les plus graves, y compris les HAEC définitives et sévères, doivent être admis à l'hôpital et traités par réanimation liquidienne intraveineuse et antibiotiques à large spectre. Une irrigation rectale pour éliminer les selles retenues et réduire la charge bactérienne peut être envisagée chez les personnes présentant une distension abdominale, quel que soit le grade HAEC. Une intervention chirurgicale avec une colostomie proximale peut être envisagée chez les enfants atteints d'HAEC sévère qui ne répondent pas à la prise en charge médicale primaire avec repos intestinal, réanimation liquidienne intraveineuse, irrigations rectales et antibiotiques à large spectre.
Plusieurs autres complications postopératoires moins fréquentes de la MH peuvent survenir:
- une fuite anastomotique (1,5% des patients)
- une sténose anastomotique
- des infections des plaies
- des saignements périanaux
- une incontinence fécale[30][33][34]
- une obstruction tardive (5-10% des patients) : s'il persiste une zone aganglionnaire distalement à l'anastomose
- une difficulté d'évacuation
- une entérocolite fulminante
- un mégacôlon toxique.
Évolution
Autrefois considérée comme une maladie mortelle, le traitement chirurgical a réduit la mortalité par maladie à 3% dans les pays développés. [6] La qualité de vie des patients atteints de MH dépend du degré de continence fécale. Il existe encore une pénurie de littérature mettant en évidence la qualité de vie dans la MH de longue date.
Bien que la conséquence la plus inquiétante de la MH puisse ne pas persister plus tard à l'âge adulte, un taux significatif de patients atteints qui ont subi une intervention chirurgicale définitive pendant la petite enfance pourrait connaître un changement des problèmes d'habitudes intestinales pendant l'âge scolaire. La complication mentionnée peut entraîner des morbidités psychologiques importantes, une altération considérable de la qualité de vie et des problèmes parentaux, y compris un congé de travail. Par conséquent, il est crucial d'utiliser une approche d'équipe interprofessionnelle pour former l'enfant à la propreté, ce qui nécessite quelques étapes essentielles, y compris la formation de compétences de défécation optimales et d'un comportement de toilette optimal.[35] [5]
Prévention
Les parents doivent être conscients de tout symptôme suspect évoquant la MH, y compris un retard dans le passage du méconium pendant plus de 48 heures pendant la période néonatale. De plus, des symptômes non spécifiques, y compris la constipation, la distension abdominale, le reflux, les nausées, les vomissements et la diarrhée, devraient également éveiller les soupçons.[36][5]
Notes
- ↑ Les GC sont des cellules polygonales avec un cytoplasme fibrillaire éosinophile abondant, un noyau excentrique et un gros nucléole.
- ↑ Cette zone est physiologiquement dépourvue de GC et présente une hyperplasie physiologique des fibres nerveuses.
- ↑ Sur un lavement normal, le rectum est plus large que le sigmoïde. Le ratio est inversé lorsque le rectum est étroit dans la MH.
Références
- Cet article a été créé en partie ou en totalité le 2021/01/18 à partir de Chirurgie (application), créée par Dre Hélène Milot, Dr Olivier Mailloux et collaborateurs et partagé sous la licence CC-BY-SA 4.0 international
- Cette page a été modifiée ou créée le 2020/11/07 à partir de Hirschsprung Disease (StatPearls / Hirschsprung Disease (2020/09/03)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/32965813 (livre).
- ↑ 1,0 et 1,1 Naomi E. Butler Tjaden et Paul A. Trainor, « The developmental etiology and pathogenesis of Hirschsprung disease », Translational Research: The Journal of Laboratory and Clinical Medicine, vol. 162, no 1, , p. 1–15 (ISSN 1878-1810, PMID 23528997, Central PMCID 3691347, DOI 10.1016/j.trsl.2013.03.001, lire en ligne)
- ↑ 2,0 et 2,1 I. Barshack, E. Fridman, I. Goldberg et Y. Chowers, « The loss of calretinin expression indicates aganglionosis in Hirschsprung's disease », Journal of Clinical Pathology, vol. 57, no 7, , p. 712–716 (ISSN 0021-9746, PMID 15220363, Central PMCID 1770342, DOI 10.1136/jcp.2004.016030, lire en ligne)
- ↑ M. W. Harrison, D. M. Deitz, J. R. Campbell et T. J. Campbell, « Diagnosis and management of Hirschsprung's disease. A 25 year perspective », American Journal of Surgery, vol. 152, no 1, , p. 49–56 (ISSN 0002-9610, PMID 3728817, DOI 10.1016/0002-9610(86)90138-8, lire en ligne)
- ↑ Maria Menezes, Martin Corbally et Prem Puri, « Long-term results of bowel function after treatment for Hirschsprung's disease: a 29-year review », Pediatric Surgery International, vol. 22, no 12, , p. 987–990 (ISSN 0179-0358, PMID 17006709, DOI 10.1007/s00383-006-1783-8, lire en ligne)
- ↑ 5,00 5,01 5,02 5,03 5,04 5,05 5,06 5,07 5,08 5,09 5,10 5,11 5,12 5,13 5,14 5,15 5,16 5,17 et 5,18 Saran Lotfollahzadeh, Mehran Taherian et Sachit Anand, StatPearls, StatPearls Publishing, (PMID 32965813, lire en ligne)
- ↑ 6,0 et 6,1 Anna Löf Granström et Tomas Wester, « Mortality in Swedish patients with Hirschsprung disease », Pediatric Surgery International, vol. 33, no 11, , p. 1177–1181 (ISSN 1437-9813, PMID 28884210, Central PMCID 5648732, DOI 10.1007/s00383-017-4150-z, lire en ligne)
- ↑ 7,0 et 7,1 G. Martucciello, « Hirschsprung's disease, one of the most difficult diagnoses in pediatric surgery: a review of the problems from clinical practice to the bench », European Journal of Pediatric Surgery: Official Journal of Austrian Association of Pediatric Surgery ... [et Al] = Zeitschrift Fur Kinderchirurgie, vol. 18, no 3, , p. 140–149 (ISSN 0939-7248, PMID 18493886, DOI 10.1055/s-2008-1038625, lire en ligne)
- ↑ Raquel Núñez-Ramos, Raquel M. Fernández, Miguel González-Velasco et Jesús Ruiz-Contreras, « A Scoring System to Predict the Severity of Hirschsprung Disease at Diagnosis and Its Correlation With Molecular Genetics », Pediatric and Developmental Pathology: The Official Journal of the Society for Pediatric Pathology and the Paediatric Pathology Society, vol. 20, no 1, , p. 28–37 (ISSN 1093-5266, PMID 28276298, DOI 10.1177/1093526616683883, lire en ligne)
- ↑ Roshini Dasgupta et Jacob C. Langer, « Hirschsprung disease », Current Problems in Surgery, vol. 41, no 12, , p. 942–988 (ISSN 0011-3840, PMID 15614238, DOI 10.1067/j.cpsurg.2004.09.004, lire en ligne)
- ↑ W. Webster, « Embryogenesis of the enteric ganglia in normal mice and in mice that develop congenital aganglionic megacolon », Journal of Embryology and Experimental Morphology, vol. 30, no 3, , p. 573–585 (ISSN 0022-0752, PMID 4772386, lire en ligne)
- ↑ Ankush Gosain, Philip K. Frykman, Robert A. Cowles et John Horton, « Guidelines for the diagnosis and management of Hirschsprung-associated enterocolitis », Pediatric Surgery International, vol. 33, no 5, , p. 517–521 (ISSN 1437-9813, PMID 28154902, Central PMCID 5395325, DOI 10.1007/s00383-017-4065-8, lire en ligne)
- ↑ 12,0 12,1 12,2 12,3 12,4 et 12,5 Holcomb, George W., III,, Murphy, J. Patrick,, St. Peter, Shawn D., et Gatti, John M.,, Holcomb and Ashcraft's pediatric surgery (ISBN 978-0-323-54976-9, 0-323-54976-4 et 978-0-323-54977-6, OCLC 1107667324, lire en ligne)
- ↑ 13,0 et 13,1 Fleur de Lorijn, Guy E. Boeckxstaens et Marc A. Benninga, « Symptomatology, pathophysiology, diagnostic work-up, and treatment of Hirschsprung disease in infancy and childhood », Current Gastroenterology Reports, vol. 9, no 3, , p. 245–253 (ISSN 1522-8037, PMID 17511924, DOI 10.1007/s11894-007-0026-z, lire en ligne)
- ↑ David Hernandez Gonzalo et Thomas Plesec, « Hirschsprung disease and use of calretinin in inadequate rectal suction biopsies », Archives of Pathology & Laboratory Medicine, vol. 137, no 8, , p. 1099–1102 (ISSN 1543-2165, PMID 23899067, DOI 10.5858/arpa.2012-0220-OA, lire en ligne)
- ↑ 15,0 15,1 et 15,2 Charles H. Knowles, Roberto De Giorgio, Raj P. Kapur et Elisabeth Bruder, « Gastrointestinal neuromuscular pathology: guidelines for histological techniques and reporting on behalf of the Gastro 2009 International Working Group », Acta Neuropathologica, vol. 118, no 2, , p. 271–301 (ISSN 1432-0533, PMID 19360428, DOI 10.1007/s00401-009-0527-y, lire en ligne)
- ↑ S. J. Qualman, R. Jaffe, K. E. Bove et H. Monforte-Muñoz, « Diagnosis of hirschsprung disease using the rectal biopsy: multi-institutional survey », Pediatric and Developmental Pathology: The Official Journal of the Society for Pediatric Pathology and the Paediatric Pathology Society, vol. 2, no 6, , p. 588–596 (ISSN 1093-5266, PMID 10508885, DOI 10.1007/s100249900167, lire en ligne)
- ↑ Maria Mercês Santos, Uenis Tannuri et Maria Cecília M. Coelho, « Study of acetylcholinesterase activity in rectal suction biopsy for diagnosis of intestinal dysganglionoses: 17-year experience of a single center », Pediatric Surgery International, vol. 24, no 6, , p. 715–719 (ISSN 0179-0358, PMID 18408941, DOI 10.1007/s00383-008-2141-9, lire en ligne)
- ↑ 18,0 et 18,1 S. W. Moore et G. Johnson, « Acetylcholinesterase in Hirschsprung's disease », Pediatric Surgery International, vol. 21, no 4, , p. 255–263 (ISSN 0179-0358, PMID 15759143, DOI 10.1007/s00383-005-1383-z, lire en ligne)
- ↑ Nasser Rakhshani, Mohammadreza Araste, Farid Imanzade et Mahshid Panahi, « Hirschsprung Disease Diagnosis: Calretinin Marker Role in Determining the Presence or Absence of Ganglion Cells », Iranian Journal of Pathology, vol. 11, no 4, , p. 409–415 (ISSN 1735-5303, PMID 28855933, Central PMCID 5563939, lire en ligne)
- ↑ Irene de Haro Jorge, Pedro Palazón Bellver, Victoria Julia Masip et Laura Saura García, « Effectiveness of calretinin and role of age in the diagnosis of Hirschsprung disease », Pediatric Surgery International, vol. 32, no 8, , p. 723–727 (ISSN 1437-9813, PMID 27369965, DOI 10.1007/s00383-016-3912-3, lire en ligne)
- ↑ S. I. Ghose, B. R. Squire, M. D. Stringer et G. Batcup, « Hirschsprung's disease: problems with transition-zone pull-through », Journal of Pediatric Surgery, vol. 35, no 12, , p. 1805–1809 (ISSN 0022-3468, PMID 11101741, DOI 10.1053/jpsu.2000.19263, lire en ligne)
- ↑ D. M. Maia, « The reliability of frozen-section diagnosis in the pathologic evaluation of Hirschsprung's disease », The American Journal of Surgical Pathology, vol. 24, no 12, , p. 1675–1677 (ISSN 0147-5185, PMID 11117790, DOI 10.1097/00000478-200012000-00013, lire en ligne)
- ↑ Raj P. Kapur et Amy J. Kennedy, « Transitional zone pull through: surgical pathology considerations », Seminars in Pediatric Surgery, vol. 21, no 4, , p. 291–301 (ISSN 1532-9453, PMID 22985834, DOI 10.1053/j.sempedsurg.2012.07.003, lire en ligne)
- ↑ Leyla Cinel, Bahar Ceyran et Berrin Güçlüer, « Calretinin immunohistochemistry for the diagnosis of Hirschprung disease in rectal biopsies », Pathology, Research and Practice, vol. 211, no 1, , p. 50–54 (ISSN 1618-0631, PMID 25442014, DOI 10.1016/j.prp.2014.08.012, lire en ligne)
- ↑ Mehran Peyvasteh, Shahnam Askarpour, Nasrollah Ostadian et Mohammad-Reza Moghimi, « DIAGNOSTIC ACCURACY OF BARIUM ENEMA FINDINGS IN HIRSCHSPRUNG'S DISEASE », Arquivos brasileiros de cirurgia digestiva: ABCD = Brazilian archives of digestive surgery, vol. 29, no 3, , p. 155–158 (ISSN 2317-6326, PMID 27759777, Central PMCID 5074665, DOI 10.1590/0102-6720201600030007, lire en ligne)
- ↑ Y.-F. Tang, J.-G. Chen, H.-J. An et P. Jin, « High-resolution anorectal manometry in newborns: normative values and diagnostic utility in Hirschsprung disease », Neurogastroenterology and Motility: The Official Journal of the European Gastrointestinal Motility Society, vol. 26, no 11, , p. 1565–1572 (ISSN 1365-2982, PMID 25263969, DOI 10.1111/nmo.12423, lire en ligne)
- ↑ F. Plenat, J. M. Vignaud, J. Floquet et P. Leroux, « [Intestinal ganglioneuromatosis: histochemical, histoenzymological and ultrastructural study of a case] », Annales De Pathologie, vol. 4, no 2, , p. 131–136 (ISSN 0242-6498, PMID 6732905, lire en ligne)
- ↑ V. V. Smith, C. Eng et P. J. Milla, « Intestinal ganglioneuromatosis and multiple endocrine neoplasia type 2B: implications for treatment », Gut, vol. 45, no 1, , p. 143–146 (ISSN 0017-5749, PMID 10369718, Central PMCID 1727575, DOI 10.1136/gut.45.1.143, lire en ligne)
- ↑ M. Torre, G. Martucciello, I. Ceccherini et M. Lerone, « Diagnostic and therapeutic approach to multiple endocrine neoplasia type 2B in pediatric patients », Pediatric Surgery International, vol. 18, no 5-6, , p. 378–383 (ISSN 0179-0358, PMID 12415360, DOI 10.1007/s00383-002-0824-1, lire en ligne)
- ↑ 30,0 et 30,1 Jacob C. Langer, Audrey C. Durrant, Luis de la Torre et Daniel H. Teitelbaum, « One-stage transanal Soave pullthrough for Hirschsprung disease: a multicenter experience with 141 children », Annals of Surgery, vol. 238, no 4, , p. 569–583; discussion 583–585 (ISSN 0003-4932, PMID 14530728, Central PMCID 1360115, DOI 10.1097/01.sla.0000089854.00436.cd, lire en ligne)
- ↑ A. Hadidi, « Transanal endorectal pull-through for Hirschsprung's disease: experience with 68 patients », Journal of Pediatric Surgery, vol. 38, no 9, , p. 1337–1340 (ISSN 1531-5037, PMID 14523816, DOI 10.1016/s0022-3468(03)00392-0, lire en ligne)
- ↑ Waleed Saleh, Khalid Rasheed, Mohammed Al Mohaidly et Hala Kfoury, « Management of Hirschsprung's disease: a comparison of Soave's and Duhamel's pull-through methods », Pediatric Surgery International, vol. 20, no 8, , p. 590–593 (ISSN 0179-0358, PMID 15309470, DOI 10.1007/s00383-004-1237-0, lire en ligne)
- ↑ Kristin Bjørnland, Mikko P. Pakarinen, Pernilla Stenstrøm et Kjetil J. Stensrud, « A Nordic multicenter survey of long-term bowel function after transanal endorectal pull-through in 200 patients with rectosigmoid Hirschsprung disease », Journal of Pediatric Surgery, vol. 52, no 9, , p. 1458–1464 (ISSN 1531-5037, PMID 28094015, DOI 10.1016/j.jpedsurg.2017.01.001, lire en ligne)
- ↑ A. S. Keshtgar, H. C. Ward, G. S. Clayden et N. M. de Sousa, « Investigations for incontinence and constipation after surgery for Hirschsprung's disease in children », Pediatric Surgery International, vol. 19, no 1-2, , p. 4–8 (ISSN 0179-0358, PMID 12721712, DOI 10.1007/s00383-002-0897-x, lire en ligne)
- ↑ E. M. van Kuyk, A. T. Brugman-Boezeman, M. Wissink-Essink et R. S. Severijnen, « Defecation problems in children with Hirschsprung's disease: a biopsychosocial approach », Pediatric Surgery International, vol. 16, no 5-6, , p. 312–316 (ISSN 0179-0358, PMID 10955552, DOI 10.1007/s003830000380, lire en ligne)
- ↑ American Academy of Family Physicians, « Information from your family doctor. Hirschsprung's disease: what you should know », American Family Physician, vol. 74, no 8, , p. 1327–1328 (ISSN 0002-838X, PMID 17087426, lire en ligne)
