Omphalocèle
| Maladie | |
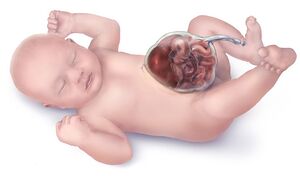 Enfant avec un omphalocèle | |
| Caractéristiques | |
|---|---|
| Signes | Masse abdominale à la base du cordon ombilical, Contenu herniaire viscéral |
| Symptômes |
Masse péri-ombilicale |
| Diagnostic différentiel |
Hernie ombilicale pédiatrique, Syndrome du cordon ombilical court, Gastroschisis |
| Informations | |
| Terme anglais | Omphalocele |
| Wikidata ID | Q1521567 |
| Spécialités | Pédiatrie, Chirurgie générale, Chirurgie pédiatrique, Obstétrique-gynécologie, Génétique, Néonatalogie |
|
| |
L'omphalocèle est un défaut congénital de la paroi abdominale. Il s'agit d'une saillie du contenu viscéral, recouverte d'une membrane, au niveau de la ligne médiane de l'abdomen, à la base du cordon ombilical.
Épidémiologie
La prévalence de l'omphalocèle est de 1 à 2 par 10 000 naissances vivantes[1][2][3] : il s'agit d'une pathologie rare, mais est l'une des anomalies congénitales de la paroi abdominale antérieure les plus fréquemment rencontrées. En prenant en considération les avortements électifs et les décès foetaux, on note une prévalence de 3,38 pour 10 000 grossesses[4]. Cette prévalence a augmenté de 11% entre 1999-2001 et 2005-2007[5].
Le taux de survie dans les cas d'omphalocèles isolées, qui représentent environ 20% de tous les cas d'omphalocèles, peut aller jusqu'à 90%. Ce taux diminue en fonction de la sévérité des atteintes associées[5][1][6].
Étiologies
L'omphalocèle est associé à au moins une anomalie dans 40 à 80% des cas. Les anomalies cardiaques et chromosomiques sont fréquemment associées avec l'omphalocèle[3]. Les foetus avec omphalocèle ont 14-47% de risque d'avoir une anomalie cardiaque et de 3-33% d'avoir une anomalie du système nerveux : ils sont fréquemment associés avec des anomalies congénitales et des syndromes[5][1]. Seul 14% des omphalocèles n'ont aucune autre anomalie associée[7].
Les syndromes congénitaux associés à l'omphalocèle sont les suivants [5]:
- le syndrome de Beckwith-Wiedemann (le plus courant) [5][1][note 1]
- la trisomie 13[8][note 2]
- la trisomie 18[9][note 3]
- la trisomie 21[note 4]
- la pentalogie de Cantrell[10][note 5]
- le syndrome de Shprintzen-Goldberg[11][note 6]
- le syndrome CHARGE[10][note 7]
- le syndrome d'exstrophie cloacale[12][note 8]
- le syndrome de Carpenter[10][note 9]
- le syndrome de Marshall-Smith[10][note 10]
- le syndrome de Meckel-Gruber[5][10][note 11].
Physiopathologie
L'omphalocèle est entraînée par une perturbation de l'organogenèse pendant la période embryonnaire[5].

Dans l'organogenèse normale, vers la sixième semaine de développement, le contenu abdominal devient trop volumineux pour être contenu dans la cavité abdominale. Il fait alors protrusion à la base du cordon ombilical. Cet évènement est connu sous le nom de hernie intestinale physiologique et est identifié à l'échographie prénatale entre la 9e et la 11e semaines de gestation. Le foie n'est jamais présent dans la hernie physiologique de l'intestin moyen. À 12 semaines de gestation, la hernie diminue. Si elle persiste, elle deviendra pathologique[5].
L'omphalocèle se produit lorsque le contenu intestinal ne parvient pas à compléter la rotation et à retourner dans la cavité abdominale. Ceci entraîne un défaut de fermeture de la paroi abdominale à la base du cordon ombilical[5]. Elle peut occasionnellement contenir le foie, la rate et les gonades en présence d'une importante anomalie de la paroi abdominale[1][3]. Les organes herniés sont contenus dans une membrane composée de trois couches, soit la couche externe amniotique, la couche intermédiaire constituée de la gelée de Wharton et la couche interne péritonéale[1][3].
Lorsque le foie fait saillie, sa contribution au développement normal de la cage thoracique est altérée. Ceci peut résulter en un sous-développement de la cage thoracique et amener une morphologie mince et allongée du thorax. Une hypoplasie pulmonaire peut aussi être notée[5][13].
En bref, ce n'est pas un défaut de fermeture de la paroi abdominale comme dans un gastroschisis, mais plutôt un échec au retour des viscères dans la cavité abdominale. Plusieurs voies génétiques d'organogénèse sont impliquées[7].
Présentation clinique
Les nourrisons avec omphalocèle peuvent également présenter une insuffisance respiratoire secondaire à un syndrome restrictif due à l'hypoplasie pulmonaire et au sous-développement de la cage thoracique[5][13].
Facteurs de risque
Les facteurs de risque de l'omphalocèle sont les suivants [5][14]:
- l'âge maternel avancé (>35 ans)
- la grossesse précoce (<20 ans)
- la race noire maternelle
- le sexe masculin
- les naissances multiples
- la fécondation in vitro.
Questionnaire
Le questionnaire chez la femme enceinte est sans particularité. Chez l'enfant qui vient de naître, l'histoire se résume à une masse péri-ombilicale présent depuis la naissance.
Examen clinique
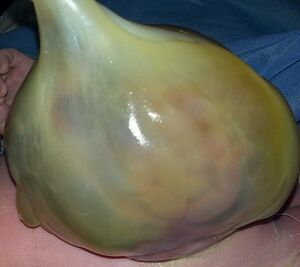
L'examen clinique chez le nourrisson permettra de visualiser l'omphalocèle ainsi que de déterminer la présence d'anomalies associées.
À l'examen abdominal, il y a aura une masse abdominale à la base du cordon ombilical dont le contenu est viscéral [1]. Il faudra alors évaluer :
- le diamètre : supérieur ou inférieur à 5 cm
- la présence du foie à l'intérieur de l'omphalocèle
- la présence d'une rupture du sac herniaire.
L'examen physique permettra de retrouver la présence de certaines anomalies associées en fonction des systèmes atteints et des syndromes associés [5]:
- les anomalies cranio-faciales
- les anomalies cardiaques
- les anomalies du tractus gastro-intestinal
- les anomalies des membres
- les anomalies de la cage thoracique (hypoplasie)[1][5].
Examens paracliniques
Examens prénataux
| Examen paraclinique | Commentaire |
|---|---|
| Monitoring foeto-maternel |
|
| Alpha-foetoprotéine maternelle |
|
| Choriocentèse |
|
| Échographie foetale | |
| IRM foetale |
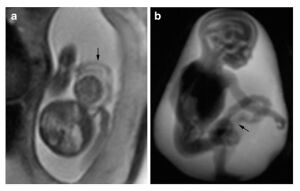
Examens après l'accouchement
Après la stabilisation initiale, on cherche les anomalies associées grâce aux examens suivants [7]:
- l'échographie rénale
- l'échographie cardiaque
- un bilan biochimique.
Diagnostic
La grande majorité (90%) des omphalocèles sont aujourd'hui diagnostiqués avant la naissance. Le diagnostic d'omphalocèle après la naissance est évident à l'examen physique avec l'identification d'une saillie viscérale médiane antérieure, recouverte d'une membrane, au site d'insertion du cordon ombilical.
L'omphalocèle a un diamètre variant entre 2 et 10 cm[1].
Plusieurs systèmes de classification de l'omphalocèle existent. L'omphalocèle peut d'abord être catégorisée selon l'emplacement prédominant: épigastrique, ombilical ou hypogastrique. De plus, l'omphalocèle est également classé selon la grosseur, le contenu de la saillie abdominale et de l'intégrité de la membrane [1]:
- petite: < 5 cm avec seulement quelques anses d'intestin faisant protrusion
- géante: ≥ 5 cm avec le foie partiellement hernié
- rupturée.
Diagnostic différentiel
Les principaux diagnostics différentiels de l'omphalocèle sont les suivants [5][1]:
Traitement
Accouchement
L'accouchement sera vaginal ou par césarienne. La décision sera prise en fonction de la grosseur de l'anomalie, les organes herniés, de l'intégrité de la membrane et de la présence de comorbidités suspectées en anténatal[1]. On prévoit habituellement un accouchement vers la 37e semaine de grossesse[15]. La césarienne n'a pas été démontrée supérieure à l'accouchement vaginal[7].
Prise en charge initiale
La prise en charge du nouveau-né avec une omphalocèle comprend les étapes initiales [5][3]:
- la stabilisation des voies respiratoires
- l'emballage stérile, humide et occlusif de l'intestin pour conserver la chaleur et réduire la perte de liquide (pertes insensibles)[note 12]
- l'insertion d'un tube nasogastrique pour la décompression intestinale
- l'établissement d'un accès intraveineux périphérique.
En cas de compromis vasculaire (suggéré par une tachycardie, une pression artérielle basse ou une apparence intestinale foncée) le patient doit être positionné en décubitus latéral gauche.
Après les étapes initiales, la prise en charge ultérieure implique l'administration de solutés intraveineux et antibiotiques à large spectre intraveineux.
Traitement chirurgical
La base du traitement chirurgical repose sur les principes suivants : retour des viscères dans la cavité abdominale en position de non rotation (équivalent de la procédure de Ladd) et fermeture de la paroi abdominale sans compromettre la physiologie du nouveau-né.
- En présence d'une petite omphalocèle (< 2cm), la réparation chirurgicale définitive doit être envisagée dans les 72 premières heures de vie par fermeture primaire de la peau et de l'aponévrose ombilicale après avoir retiré le sac herniaire[5][3][7].
- En présence d'une omphalocèle plus grosse ou d'autres défauts pariétaux, une approche délicate de réduction du contenu viscéral est préconisée à cause du risque d'augmentation trop élevée de la pression intra-abdominale. Un évaluation du parenchyme hépatique sera à favoriser car une portion du sac peut être adhérente à la capsule de Glisson et on la laissera donc in situ. La membrane qui recouvre aussi la vessie peut être laissée en place pour éviter une rupture de celle-ci. Si la paroi n'est pas refermable, on utilisera une mèche résorbable. Celle-ci peut être graduellement excisée ou on la laissera granuler et s'épithélialiser.
- En présence d'une omphalocèle de plus de 10 centimètres, la scarification du sac amniotique avec application d'une solution de bétadine (providone iodée)/nitrate d'argent, pour permettre l'épithélialisation du sac, est possible[3]. On se retrouvera donc avec une hernie abdominale que l'on pourra réparer ultérieurement quand le patient sera stabilisé et que les comorbidités auront été contrôlées.
- Contrairement au gastroschisis, la technique du Silo n'est pas préconisée[7].
- En cas de rupture de la membrane, le traitement est le même que pour le gastroschisis[3], on favorisera l'approche avec un silo que l'on pourra coudre à la paroi.
Traitement médical
Un traitement conservateur est aussi décrit dans la littérature. Il est utilisé pour les défauts les plus volumineux et/ou chez les nouveaux-nés qui ont de graves atteintes cardiaques ou neurologiques qui limitent leur accès au traitement chirurgical[7]. Les principes sont [19][20]:
- la traction du sac pour éviter la macération contre la peau de l'abdomen
- l'application d'une solution permettant l'épithélialisation et la dessiccation de la membrane
- les produits utilisés pour la scarification ne doivent pas être toxiques à long terme (exemple : nitrate d'argent), doivent idéalement être antibactériens et garder l'intégrité des tissus sous-jacents (éosine aqueuse 2% par exemple)
- l'administration parentérale d'antibiotiques en prophylaxie
- durée des traitements pour une épithélialisation complète : 4-10 semaines
- réparation définitive de la hernie : 1 à 5 ans (technique chirurgicale standard avec prothèse, expanseur tissulaire au besoin, greffe, séparation des composantes, etc.)[7].
Complications
Les complications possibles de l'omphalocèle peuvent être regroupées selon leur moment d'apparition :
Avant la naissance et durant l'accouchement
Les complications pré-natales et périnatales sont les suivantes [5][1][13][6]:
- l'hypoplasie pulmonaire
- la perturbation du développement de la cage thoracique
- le décès foetal
- la rupture de l'omphalocèle
- un traumatisme du foie
- une torsion des viscères.
Après la naissance
Les complications post-natales sont les suivantes [5][1][13]:
- cholestase et hépatomégalie (en cas de nutrition parentérale et déshydratation)
- hypertension pulmonaire
- difficulté d'alimentation
- retard de croissance
- reflux gastro-oesophagien (RGO)
- volvulus intestinal
- ischémie intestinale
- infection de plaie
- syndrome de l'intestin court.
Évolution
Le pronostic dépend en grande partie de la taille du défaut et des anomalies congénitales et syndromes associés. Les grandes omphalocèles avec des anomalies associées ont un taux de mortalité plus élevé. De plus, les nouveau-nés présentant une protrusion hépatique semblent avoir un pronostic plus sombre. Le taux de survie global est près de 80% ce qui reflète l'efficacité du diagnostic prénatal et la décision prise par de nombreuses familles d'interrompre les grossesses avec des anomalies sévères[5][21].
Une ventilation mécanique peut parfois être nécessaire plusieurs semaines avant l'atteinte de la maturité du système respiratoire sous-développé[5].
Les nourrissons atteints d'omphalocèle tolèrent les tétées orales peu de temps après la fermeture[5].
Notes
- ↑ Le syndrome de Beckwith-Wiedemann est un syndrome de prolifération caractérisé par une macrosomie, une hypertrophie de la langue, une hypoglycémie néonatale, des plis et des fosses auriculaires, une hémihypertrophie, une viscéromégalie, une hernie ombilicale, des tumeurs embryonnaires, une omphalocèle, une néphrocalcinose, une maladie du rein en éponge médullaire et une néphromégalie.
- ↑ Trisomie 13 : petits yeux, fente labio-palatine, microcéphalie, cryptorchidie, polydactylie, hypertélorisme, micrognathie, aplasie cutanée et anomalies de l'oreille externe.
- ↑ Trisomie 18 : dolichocéphalie, anomalies de l'oreille externe, micrognathie, fentes palpébrales courtes, petit visage, poing serré avec chevauchement des doigts, hypotonie et pieds en piolets.
- ↑ Trisomie 21 : hypotonie, fentes palpébrales ascendantes, brachycéphalie, oreilles basses, pli palmaire unique, pont nasal plat, taches de Brushfield autour de l'iris, cinquièmes doigts incurvés et un écart entre les premiers et deuxièmes orteils.
- ↑ Pentalogie de Cantrell : Ectopia cordis, anomalie abdominale supra-ombilicale médiane, fente sternale et anomalie intracardiaque.
- ↑ Syndrome de Sphrintzen-Goldberg : craniosynostose, dolichocéphalie, hypertélorisme, exophtalmie, strabisme, doigts et membres allongés, hernies ombilicales et abdominales.
- ↑ Syndrome CHARGE : colobome, malformation cardiaque, atrésie choanale, retard de croissance ou de développement, anomalie génitale et anomalies de l'oreille.
- ↑ Syndrome d'extrophie cloacale : exstrophie de la vessie, anus imperforé, anomalies de la colonne vertébrale.
- ↑ Syndrome de Carpenter: déformation du crâne de Kleeblattschadel (crâne trilobé en feuille de trèfle) due à la pancraniosynostose, syndactylie des mains et des pieds et retard mental.
- ↑ Syndrome de Marshall-Smith : front proéminent, orbites peu profondes, sclères bleues, pont nasal déprimé, micrognathie, maturation squelettique accélérée, difficultés respiratoires, retard mental.
- ↑ Syndrome de Meckel-Gruber : encéphalocèle occipitale, fentes labiale et palatine, microcéphalie, microphtalmie, organes génitaux anormaux, reins polykystiques et polydactylie.
- ↑ Les pansements excessivement humides ou circonférentiels doivent être évités, car ils peuvent macérer l'omphalocèle et compromettre la circulation sanguine.
Références
- Cette page a été modifiée ou créée le 2020/11/07 à partir de Omphalocele (StatPearls / Omphalocele (2020/10/01)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/30085552 (livre).
- Cet article a été créé en partie ou en totalité le 2020/11/07 à partir de Chirurgie (application), créée par Dre. Hélène Milot, Dr. Olivier Mailloux et collaborateurs et partagé sous la licence CC-BY-SA 4.0 international
- ↑ 1,00 1,01 1,02 1,03 1,04 1,05 1,06 1,07 1,08 1,09 1,10 1,11 1,12 1,13 1,14 1,15 1,16 1,17 1,18 1,19 et 1,20 (en) Mariatu A. Verla, Candace C. Style et Oluyinka O. Olutoye, « Prenatal diagnosis and management of omphalocele », Seminars in Pediatric Surgery, vol. 28, no 2, , p. 84–88 (DOI 10.1053/j.sempedsurg.2019.04.007, lire en ligne)
- ↑ Russell S. Kirby, « The prevalence of selected major birth defects in the United States », Seminars in Perinatology, vol. 41, no 6, , p. 338–344 (ISSN 1558-075X, PMID 29037343, DOI 10.1053/j.semperi.2017.07.004, lire en ligne)
- ↑ 3,0 3,1 3,2 3,3 3,4 3,5 3,6 et 3,7 (en) « Application Chirurgie », sur App Store (consulté le 7 décembre 2020)
- ↑ Nathalie Roux, Déborah Jakubowicz, Laurent Salomon et Gilles Grangé, « Early surgical management for giant omphalocele: Results and prognostic factors », Journal of Pediatric Surgery, vol. 53, no 10, , p. 1908–1913 (ISSN 1531-5037, PMID 29803304, DOI 10.1016/j.jpedsurg.2018.04.036, lire en ligne)
- ↑ 5,00 5,01 5,02 5,03 5,04 5,05 5,06 5,07 5,08 5,09 5,10 5,11 5,12 5,13 5,14 5,15 5,16 5,17 5,18 5,19 5,20 5,21 5,22 et 5,23 Tarik Zahouani et Magda D. Mendez, StatPearls, StatPearls Publishing, (PMID 30085552, lire en ligne)
- ↑ 6,0 et 6,1 Annelieke Hijkoop, Nina C. J. Peters, Rosan L. Lechner et Yolande van Bever, « Omphalocele: from diagnosis to growth and development at 2 years of age », Archives of Disease in Childhood. Fetal and Neonatal Edition, vol. 104, no 1, , F18–F23 (ISSN 1468-2052, PMID 29563149, DOI 10.1136/archdischild-2017-314700, lire en ligne)
- ↑ 7,0 7,1 7,2 7,3 7,4 7,5 7,6 7,7 7,8 et 7,9 Holcomb, George W., III,, Murphy, J. Patrick,, St. Peter, Shawn D., et Gatti, John M.,, Holcomb and Ashcraft's pediatric surgery (ISBN 978-0-323-54976-9, 0-323-54976-4 et 978-0-323-54977-6, OCLC 1107667324, lire en ligne)
- ↑ Hui-Fang Hsu et Jia-Woei Hou, « Variable expressivity in Patau syndrome is not all related to trisomy 13 mosaicism », American Journal of Medical Genetics. Part A, vol. 143A, no 15, , p. 1739–1748 (ISSN 1552-4833, PMID 17603803, DOI 10.1002/ajmg.a.31835, lire en ligne)
- ↑ A. Karaman, H. Aydin et K. Göksu, « Concomitant omphalocele, anencephaly and arthrogryposis associated with trisomy 18 », Genetic Counseling (Geneva, Switzerland), vol. 26, no 1, , p. 77–79 (ISSN 1015-8146, PMID 26043511, lire en ligne)
- ↑ 10,0 10,1 10,2 10,3 et 10,4 Chih-Ping Chen, « Syndromes and disorders associated with omphalocele (III): single gene disorders, neural tube defects, diaphragmatic defects and others », Taiwanese Journal of Obstetrics & Gynecology, vol. 46, no 2, , p. 111–120 (ISSN 1875-6263, PMID 17638618, DOI 10.1016/S1028-4559(07)60004-7, lire en ligne)
- ↑ Leopoldo Zelante, Michele Germano, Michele Sacco et Savino Calvano, « Shprintzen-Goldberg omphalocele syndrome: a new patient with an expanded phenotype », American Journal of Medical Genetics. Part A, vol. 140, no 4, , p. 383–384 (ISSN 1552-4825, PMID 16411191, DOI 10.1002/ajmg.a.31064, lire en ligne)
- ↑ Majdouline Boujoual, Hamid Madani, Housain Benhaddou et Mohamed Belahcen, « [Conjoined twins at common omphalocele and cloacal exstrophy with sexual ambiguity] », The Pan African Medical Journal, vol. 17, , p. 243 (ISSN 1937-8688, PMID 25170387, Central PMCID 4145272, DOI 10.11604/pamj.2014.17.243.2418, lire en ligne)
- ↑ 13,0 13,1 13,2 et 13,3 (en) Eileen Duggan et Pramod S. Puligandla, « Respiratory disorders in patients with omphalocele », Seminars in Pediatric Surgery, vol. 28, no 2, , p. 115–117 (DOI 10.1053/j.sempedsurg.2019.04.008, lire en ligne)
- ↑ Polina Frolov, Jasem Alali et Michael D. Klein, « Clinical risk factors for gastroschisis and omphalocele in humans: a review of the literature », Pediatric Surgery International, vol. 26, no 12, , p. 1135–1148 (ISSN 0179-0358 et 1437-9813, DOI 10.1007/s00383-010-2701-7, lire en ligne)
- ↑ 15,0 et 15,1 Robert Resnik et Robert K. Creasy, Creasy and Resnik's Maternal-Fetal Medicine: Principles and Practice, Elsevier, (ISBN 978-1-4160-4224-2, lire en ligne), p. 635–650
- ↑ 16,0 et 16,1 (en) A. Khalil, C. Arnaoutoglou, M. Pacilli et A. Szabo, « Outcome of fetal exomphalos diagnosed at 11–14 weeks of gestation », Ultrasound in Obstetrics & Gynecology, vol. 39, no 4, , p. 401–406 (ISSN 1469-0705, DOI 10.1002/uog.10048, lire en ligne)
- ↑ 17,0 et 17,1 (en) Pp Som et S Naik, « Antenatal Diagnosis of Omphalocele », Medical Journal Armed Forces India, vol. 64, no 3, , p. 276–277 (PMID 27408166, Central PMCID PMC4921613, DOI 10.1016/S0377-1237(08)80118-9, lire en ligne)
- ↑ (en) Teresa Victoria, Savvas Andronikou, Diana Bowen et Pablo Laje, « Fetal anterior abdominal wall defects: prenatal imaging by magnetic resonance imaging », Pediatric Radiology, vol. 48, no 4, , p. 499–512 (ISSN 1432-1998, DOI 10.1007/s00247-017-3914-x, lire en ligne)
- ↑ M. Grob, « Conservative Treatment of Exomphalos », Archives of Disease in Childhood, vol. 38, no 198, , p. 148–150 (ISSN 0003-9888, PMID 13950613, Central PMCID 2019004, lire en ligne)
- ↑ (en) A. Binet, A. Scalabre, S. Amar et K. Alzahrani, « Operative versus conservative treatment for giant omphalocele: Study of French and Ivorian management », Annales de Chirurgie Plastique Esthétique, vol. 65, no 2, , p. 147–153 (ISSN 0294-1260, DOI 10.1016/j.anplas.2019.03.004, lire en ligne)
- ↑ Peter Conner, Jenny Hammarqvist Vejde et Carmen Mesas Burgos, « Accuracy and impact of prenatal diagnosis in infants with omphalocele », Pediatric Surgery International, vol. 34, no 6, , p. 629–633 (ISSN 1437-9813, PMID 29637257, Central PMCID 5954074, DOI 10.1007/s00383-018-4265-x, lire en ligne)
