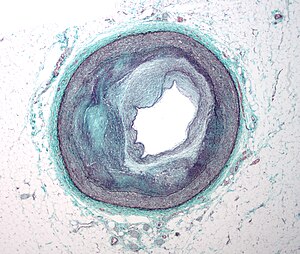
Maladie artérielle périphérique infra-iliaque
La maladie artérielle périphérique (MAP) infra-iliaque est une maladie athérosclérotique des vaisseaux sanguins commençant au niveau des artères fémorales et s'étendant distalement.
Épidémiologie
Dans le monde, plus de 230 millions de personnes sont touchées par la MAP. Au Canada, on estime qu'environ 800 000 personnes sont touchées par cette maladie. La prévalence est plus élevée dans les populations plus âgées; jusqu'à 20 % chez les personnes de plus de 70 ans. Au Canada, la communauté autochtone est plus touchée par la maladie artérielle périphérique. Bien que des données limitées ne permettent pas une quantification précise, on estime que plus de 13 % de la communauté autochtone est probablement touchée en raison de son taux accru de facteurs de risque. Il est également important de noter que la prévalence de la maladie artérielle périphérique chez les Afro-Américains est le double de celle des Blancs non hispaniques. Bien que l'on pense historiquement que cette maladie est plus fréquente chez les hommes, des données récentes peuvent démontrer que le taux chez les hommes et les femmes peut être assez similaire.[1][2][3][4]
Étiologies
Les étiologies sont:[1][5][6][7]
- L'athérosclérose: l'étiologie la plus fréquente.
- La radiothérapie: peut provoquer des changements vasculaires qui entraînent des changements dans le flux sanguin.
- Une endofibrose de l'artère iliaque: affecte généralement une population de patients différente; des patients plus jeunes et physiquement actifs et même des athlètes professionnels.
- Une blessure vasculaire: toute lésion traumatique d'un vaisseau sous-inguinal, et même leur réparation pourrait entraîner des modifications du flux sanguin.
- Des vasculites.
Ces différentes étiologies peuvent affecter une ou plusieurs artères:
- fémorale (commune, superficielle, profonde)
- poplitée
- tronc tibiopéronéal
- tibial antérieur
- tibial postérieur
- péronier
- dorsale pédieuse.
Physiopathologie
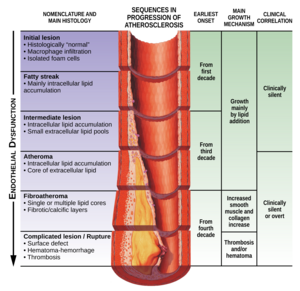
Cette section se concentrera sur la physiopathologie de la maladie lorsque l'athérosclérose en est la cause.
La physiopathologie de l'athérosclérose implique des interactions complexes entre le cholestérol et les cellules vasculaires dont les détails dépassent le cadre de cet article. La plaque d'athérosclérose s'accumule lentement à l'intérieur des artères. L'athérosclérose entraîne le rétrécissement des vaisseaux sanguins, et donc des limitations du flux sanguin. La limitation spécifique du flux sanguin dépend de l'étendue du rétrécissement des vaisseaux sanguins. Pour les personnes atteintes d'athérosclérose des vaisseaux, mais qui ne subissent pas de claudication, cela est dû aux artères qui compensent l'accumulation de plaque en se dilatant pour préserver le flux à travers le vaisseau. Pour ceux qui souffrent de claudication intermittente, le débit sanguin est encore suffisant pour alimenter les muscles au repos avec suffisamment de sang car l'étendue de la sténose n'est pas significative. Pendant la marche, les muscles ont besoin de plus de flux sanguin et, à leur tour, les vaisseaux essaieront de se dilater pour fournir suffisamment de sang. Cependant, pour les personnes atteintes de MAP, l'artère ne peut plus se dilater et l'inadéquation entre l'offre et la demande du sang déclenche les symptômes de claudication. La diminution des demandes énergétiques du muscle (en ralentissant ou en s'arrêtant) permet à l'apport sanguin de «rattraper» et les symptômes ischémiques disparaissent. Au fur et à mesure que la sténose se poursuit, même parfois en pleine occlusion, cela entraîne une douleur au repos a cause d'une mauvaise perfusion des nerfs. Les plaies non cicatrisantes et les ulcères ischémiques représentent une perte de tissu due à une mauvaise circulation sanguine. Dans les cas les plus graves, les orteils ou tout l'avant-pied peuvent devenir noirs et momifiés à mesure que la gangrène se développe. [1][8]
Au fur et à mesure que le rétrécissement progresse ou obstrue complètement l'artère, le flux sanguin se déplace vers des artères plus petites parallèles à l'artère malade et forme ainsi une circulation collatérale. Bien que ce flux collatéral préserve la perfusion distale, le réseau de vaisseaux plus petits n'achemine jamais autant de flux sanguin que l'artère principale. [1][8]
Présentation clinique
Facteurs de risque
Les facteurs de risque de la maladie artérielle périphérique sont globalement assez similaires à ceux de la plupart des maladies cardiovasculaires. Néanmoins, il est utile de les diviser en deux catégories ; modifiable et non modifiable[9][10][11][12] :
- Modifiables
- le tabagisme[RR: 3-4] (facteur de risque modifiable le plus important)
- le diabète sucré (relation claire avec les niveaux d'A1c)
- l'HTA
- les dyslipidémies
- Non-modifiables
Questionnaire
Les symptômes typiques de cette maladie sont:
- Asymptomatique.
- La claudication[9][1] :
- La présentation initiale typique de MAP.
- Classiquement décrit comme une fatigue musculaire, des douleurs ou des crampes reproductibles à l'effort qui sont soulagées par le repos. Cela se produit le plus souvent dans le mollet[note 1].
- Elle entraîne une capacité de marche limitées et une réduction de la qualité de vie.
- Parfois, les patients atteints de MAP ne se plaignent pas de claudication. Cela peut être dû au fait que leur maladie n'est pas avancée et qu'ils ne s'exercent pas à l'intensité qui entraînerait des symptômes. Certains vont normaliser ces douleurs aussi.
- Des plaies chroniques ou qui prennent beaucoup de temps à guérir.
- Une douleur de repos ischémique :
- Présent que lorsque la gravité de la maladie progresse.
- Se produit généralement la nuit et se situe dans les parties les plus distales du pied.
- Les patients décriront souvent avoir été réveillés par la douleur, parfois décrite comme brûlante, avoir besoin de se frotter les pieds, de se promener dans la pièce ou, un signe classique de MAP, de suspendre leur pied au bord du lit[note 2] pour bien dormir.
- La limitation d'exercice :
- La claudication ne se produit pas chez tous les patients. Certains patients, en particulier ceux qui présentent certaines comorbidités ou dont la fonction d'exercice de base est faible, peuvent subir une diminution de leur fonction physique sans claudication.
Examen clinique
À l'examen clinique:
- Il est possible qu'il n'y ait pas de signes cliniques.
- La partie la plus importante de l'examen est l'examen vasculaire périphérique ou l'on pourra trouver:
- Une diminution ou perte du pouls aux membres inférieurs (poul femoral absent[Se: 7 %[13]][Sp: 99 %[14]][LR+: 6,1[15]], tibial postérieur et pédieux absent[Se: 63-73 %[16]][Sp: 91-99 %[17]][LR+: 8,8[18]]).
- La hauteur ou l'on retrouve un pouls normal indique que l'obstruction est distale à cette hauteur.
- Une augmentation du refill capillaire ≥ 5s[Se: 28 %[19]][Sp: 85 %[20]][LR+: 1,9[21]].
- Une augmentation du remplissage veineux > 20s[Se: 22 %[22]][Sp: 94 %[23]][LR+: 3,6[24]][25].
- Un test de Buerger[Se: 100 %[26]] positif[note 3].
- Des souffles[Se: 20-50 %[27]][Sp: 92-99 %[28]][LR+: 5,6[29]][LR-: 0,7[30]][note 4].
- Une diminution ou perte du pouls aux membres inférieurs (poul femoral absent[Se: 7 %[13]][Sp: 99 %[14]][LR+: 6,1[15]], tibial postérieur et pédieux absent[Se: 63-73 %[16]][Sp: 91-99 %[17]][LR+: 8,8[18]]).
- À l'examen des membres inférieurs[9] :
- Une ou des ulcérations cutanées[Se: 2 %[31]][Sp: 100 %[32]][LR+: 7[33]] et des plaies: généralement, toute forme de perte de tissu se présentera après que le patient ait déjà ressenti une douleur au repos[note 5].
- Il est important de noter que la perte de tissu est généralement précédée d'une forme de traumatisme; un coup de pied ou une pression due à des chaussures mal ajustées.
- De la gangrène qui implique généralement les orteils ou les zones de pression pour les patients alités.
- Une froideur[Se: 10 %[34]][Sp: 98 %[35]][LR+: 6,1][LR-: 0,9[36]].
- Une perte de pilosité[Se: 48 %[37]][Sp: 71 %[38]][LR+: 1,7[39]] et une atrophie cutanée[Se: 50 %[40]][Sp: 70 %[41]][LR+: 1,7[42]]
- Un érythème, pâleur, couleur bleu[Se: 35 %[43]][Sp: 87 %[44]][LR+: 2,8[45]][LR-: 0,7[46]].
- Il est également important de rechercher des complications, notamment une cellulite ou de la gangrène infectée.
- examen cardiovasculaire: à la recherche de souffle ou de signes d'insuffisance cardiaque (la MCAS étant très co-morbide).
- examen abdominal: à la recherche d'un souffle abdominale, évocateur d'une MAP aorto-iliaque.
-
Ulcère artériel.
-
Une nécrose secondaire à une MAP avancée
-
Une gangrène sèche secondaire à une MAP avancée
Examens paracliniques
Laboratoires
Il n'y a pas de tests sanguins qui peuvent être utilisés directement pour le diagnostic de MAP. Cependant, certains tests sanguins peuvent être utiles:
- la FSC et la CRP en cas d'infection
- un bilan lipidique pour le contrôle des facteurs de risques
- la créatinine pour dépister une maladie rénale co-morbide (comme la néphroangiosclérose).
Pressions
| Examen | Précisions |
|---|---|
| Index cheville-bras[Se: 90 %[47]][Sp: 98 %[48]][note 6][49] |
|
| Test de stress[50] |
|
Imagerie
| Examen | Précisions | |
|---|---|---|
| Duplex artériel[51] |
|
|
| Angio-TDM des membres inférieurs[52] |
|
 |
| Angiographie endovasculaire |
|
 |
| Radiographie du genou, de la jambe, cuisse, cheville et pied |
|
 |
Approche clinique
Le diagnostic de la MAP est établi avec l'anamnèse, l'examen physique et l'ITB. Compte tenu des complications possibles associées à la MAP, il est alors important d'examiner les plaies ou les infections qui nécessitent un traitement urgent.
Une MAP peut-être asymptomatique et le patient peut claudiquer sur d'autres pathologies comme les hernies lombaires, sténoses spinales et autres problèmes musculosquelettiques limitant la marche. Il faut également questionnaire les maladies rhumatologiques comme une vasculite.
Diagnostic différentiel
Les diagnostics différentiels de la maladie artérielle périphérique sont principalement composés d'entités qui imitent la douleur de la claudication, soit des troubles musculo-squelettiques et neurologiques tels que: [1][9][53]
- la sciatalgie
- les troubles lombo-sacrés: hernie discale lombaire, sténose spinale (peuvent causer des douleurs dans les jambes lors de la marche en raison de la claudication neurogénique)
- une gonarthose ou une arthrose de la cheville
- une neuropathie périphérique
- un syndrome chronique des loges
- un kyste de Baker
- une thrombose veineuse profonde du membre inférieur
- une insuffisance veineuse
- une thromboangéite oblitérante
- une thrombophlébite superficielle du membre inférieur
- un phénomène de Raynaud.
Il existe des causes vasculaires périphériques plus rares de claudication qui justifient une consultation en chirurgie vasculaire. Ceux-ci inclus:[9]
- une coarctation congénitale et acquise de l'aorte
- une endofibrose de l'artère iliaque externe (syndrome de l'artère iliaque chez les cyclistes)
- une dysplasie fibromusculaire
- un anévrisme poplité (avec thromboembolie secondaire)
- un piégeage poplité
- des tumeurs vasculaires
- de la radiothérapie.
Traitement
Le traitement de la MAP dépend de la gravité de la maladie et de la manière dont elle est classée en fonction de cette gravité.
Dessous sont deux systèmes de classification pour MAP. Le premier est le Classement de Fontaine [54]. Il s'agit d'un système de classification plus ancien et qui n'est plus utilisé aussi souvent maintenant. Le second est le système de classification le plus couramment utilisé, le système de Classification de Rutherford de l'ischémie chronique menaçante des membres [55]. Cette classification utilise une combinaison de symptômes et de résultats d'examens paracliniques pour classer la MAP en 6 catégories. Typiquement, après le développement d'une douleur de repos, c'est-à-dire au minimum la classification de Rutherford 4, la maladie est appelée ischémie chronique menaçant les membres (anciennement ischémie critique des membres).
| Stade | Description | Image |
|---|---|---|
| 1 | abolition d'un ou plusieurs pouls périphériques sans aucun retentissement fonctionnel | |
| 2 | «claudication intermittente» se manifestant par des douleurs à la marche apparaissant au-delà d'un certain périmètre, signe d'une ischémie musculaire à l'effort.
Ce stade est parfois subdivisé en stade 2a (ou faible) et stade 2b (ou fort) selon le degré invalidant ou non de la claudication |
|
| 3 | douleur de repos | |
| 4 | présence de troubles trophiques ou de nécrose des membres inférieurs comme un ulcère ou une gangrène, signant une ischémie critique | 
|
| Grade | Catégorie | Description clinique | Critères objectifs |
|---|---|---|---|
| 0 | 0 | Asymptomatique - pas de maladie occlusive significative sur le plan hémodynamique | Tapis roulant normal |
| I | 1 | Légère claudication | Complète l'exercice sur tapis roulant; pression de la cheville après exercice > 50 mm Hg mais au moins 20 mm Hg inférieur à la valeur de repos |
| 2 | Claudication modérée | Entre les catégories 1 et 3 | |
| 3 | Claudication sévère | Impossible de terminer l'exercice standard sur tapis roulant et la pression de la cheville après l'exercice <50 mm Hg | |
| II | 4 | Douleur de repos ischémique | Pression de la cheville au repos < 40 mm Hg, volume du pouls de la cheville ou du métatarse plat ou à peine pulsatile ; pression des orteils <30 mm Hg |
| III | 5 | Perte tissulaire mineure - ulcère non cicatrisant, gangrène focale avec ischémie pédieuse diffuse | Pression de la cheville au repos < 60 mm Hg, volume du pouls de la cheville ou du métatarse plat ou à peine pulsatile ; pression des orteils <40 mm Hg |
| 6 | Perte tissulaire majeure - s'étendant au-dessus du niveau transmétatarsien, le pied fonctionnel n'est plus récupérable | Identique à la catégorie 5 |
Maladie asymptomatique
Il n'existe aucune preuve démontrant l'avantage du dépistage de la MAP asymptomatique. Lorsque la MAP est causée par l'athérosclérose (ces patients seront probablement atteints de MCAS également) [58][59]:
- prendre en charge les facteurs de risques de la MAP
- discuter avec le patient la pertinence d'initier une statine.
Claudication intermittente
Ce niveau de maladie limite principalement la capacité fonctionnelle du patient et ne menace pas directement le membre (autre que l'évolution naturelle de cette maladie vers une aggravation). Par conséquent, les objectifs du traitement seront d'améliorer la capacité fonctionnelle des patients ainsi que d'assurer une bonne modification du risque afin de limiter l'évolution de la maladie.
La modification des facteurs de risque est également nécessaire en raison du fait que ces patients sont souvent comorbides avec une coronaropathie et une maladie de l'artère carotide et souffrent d'une mortalité élevée par infarctus du myocarde et accidents vasculaires cérébraux. Par conséquent, la modification des facteurs de risque d'athérosclérose peut également réduire ces sources de mortalité:[9][58][60]
- Arrêt du tabac
- Traitement de la dyslipidémie
- Optimisation diabétique
- Gestion de la tension artérielle
- Thérapie antiplaquettaire:
- Acide acétylsalicylique 80 mg PO DIE (Clopidogrel 75 mg PO DIE en alternative; warfarine non indiquée)
L'autre composante de la prise en charge à ce stade de la maladie est l'amélioration de la capacité fonctionnelle. La thérapie de base est un programme d'exercice[note 7].
- La durée idéale de cette thérapie est de 30 à 60 minutes 3 fois par semaine sur une durée de 3 à 6 mois.
- Les patients doivent subir de la claudication pendant la thérapie[note 8].
- Bien qu'un programme d'exercices supervisés avec accès à un tapis roulant soit idéal, cela n'est sans aucun doute pas réalisable pour tous les patients.
Il existe d'autres médicaments qui peuvent être utilisés pour améliorer la capacité fonctionnelle. Cependant, bon nombre d'entre eux ne sont pas disponibles au Canada et ne sont donc pas du tout disponibles pour nos patients, ou à un prix raisonnable. Voici une liste non exhaustive:
- Cilostazol
- Naftidrofuryl
- Pentoxifylline 400 mg PO TID (prend généralement 2 à 4 semaines pour commencer à fonctionner).
Ischémie chronique menaçant les membres
Une fois que la maladie atteint cette gravité, alors que l'objectif est toujours d'améliorer la capacité fonctionnelle, il existe maintenant un risque pour le membre et il faut donc le gérer, généralement avec une forme de revascularisation opératoire. Le choix de la méthode de revascularisation est très complexe. Les options de revascularisation comprennent la chirurgie ouverte, la chirurgie endovasculaire ou un hybride des deux.[9]
Ce stade de la maladie peut également entraîner une perte de tissu sous forme d'ulcères artériels. Ces ulcères s'accompagnent d'un risque d'infection, de propagation et d'un risque accru de perte de membre. Avant la revascularisation, guérir les ulcères peut être difficile en raison du manque d'un flux sanguin suffisant vers l'ulcère, c'est pourquoi après la revascularisation, il y a plus de chances que cet objectif puisse être atteint.[9]
Il y a des moments où les patients ne sont pas candidats à la revascularisation malgré une maladie grave.
- Les comorbidités du patient l'empêchent de subir une revascularisation en toute sécurité.
- Déjà subi des revascularisations sans succès et n'a plus de vaisseau cible à revasculariser.
À ce stade, il existe principalement deux options en fonction de l'état du patient:
- Douleur stable et bien contrôlée avec des médicaments, perte de tissu/lésion stable et non infectée: prise en charge et suivi médical.
- Douleur pas tolérable ou propagation incontrôlable de l'infection provoquant des tissus non viables: l'amputation doit être explorée avec les patients.[9]
Planification du Traitement
Il existe de nombreuses méthodes différentes que les chirurgiens vasculaires utilisent pour aider à planifier le traitement, cet article se concentrera sur deux systèmes validés de la Society for Vascular Surgery.
WIfI
Le système de classification "WIfI" est un système de stratification des risques créé par la Society for Vascular Surgery. Il prend en compte la plaie, l'ischémie et l'infection du pied des patients. Chacun de ces trois aspects est noté en fonction de certains aspects, comme indiqué ci-dessous dans les tableaux. Ensuite, la combinaison de ces grades peut être utilisée pour déterminer l'estimation du risque d'amputation à 1 an, et l'estimation de la probabilité du bénéfice/nécessité de la revascularisation. Il s'agit d'un outil très utile et normalisé qui peut aider à déterminer le risque du patient et le besoin d'intervention.[61]
| Grade | Ulcère | Gangrène |
|---|---|---|
| 0 | Pas d'ulcère | Pas de gangrène |
| Description clinique : douleur de repos ischémique (nécessite symptômes typiques + ischémie grade 3); pas de blessure. | ||
| 1 | Petit(s) ulcère(s) peu profond(s) sur la partie distale de la jambe ou du pied ; pas d'os exposé, sauf si limité à la phalange distale | Pas de gangrène |
| Description clinique : perte tissulaire mineure. Récupérable avec simple amputation numérique (1 ou 2 doigts) ou couverture cutanée. | ||
| 2 | Ulcère plus profond avec os, articulation ou tendon exposés ; n'impliquant généralement pas le talon ; ulcère peu profond du talon, sans atteinte calcanéenne | Modifications gangréneuses limitées aux doigts |
| Description clinique : perte tissulaire majeure récupérable avec plusieurs (≥3) amputations digitales ou amputation transmétatarsienne standard ± couverture cutanée. | ||
| 3 | Ulcère étendu et profond touchant l'avant-pied et/ou le médio-pied ; ulcère du talon profond et de pleine épaisseur ± atteinte calcanéenne | Gangrène étendue impliquant l'avant-pied et/ou le médio-pied ; nécrose du talon pleine épaisseur ± atteinte calcanéenne |
| Description clinique : perte tissulaire importante récupérable uniquement avec une reconstruction complexe du pied ou une MAT non traditionnelle (Chopart ou Lisfranc) ; couverture par lambeau ou prise en charge complexe de la plaie nécessaire pour un grand défaut des tissus mous | ||
| Grade | ABI | Pression systolique cheville | Pression orteil, oxymétrie transcutanée |
|---|---|---|---|
| 0 | ≥0.80 | >100 mm Hg | ≥60 mm Hg |
| 1 | 0.6-0.79 | 70-100 mm Hg | 40-59 mm Hg |
| 2 | 0.4-0.59 | 50-70 mm Hg | 30-39 mm Hg |
| 3 | ≤0.39 | <50 mm Hg | <30 mm Hg |
| Manifestation clinique de l'infection | Grade | IDSA/PEDIS Gravité de l'infection |
|---|---|---|
| Aucun symptôme ou signe d'infection | 0 | Non infecté |
| Infection présente, définie par la présence d'au moins 2 des éléments suivants :
• Gonflement ou induration locale • Érythème > 0,5 à ≤ 2 cm autour de l'ulcère • Sensibilité ou douleur locale • Chaleur locale • Écoulement purulent (sécrétion épaisse, opaque à blanche ou sanguine) ________________________________________________________________ Infection locale impliquant uniquement la peau et le tissu sous-cutané (sans atteinte des tissus plus profonds et sans signes systémiques comme décrit ci-dessous). Exclure les autres causes d'une réponse inflammatoire de la peau (p. ex., traumatisme, goutte, neuro-ostéoarthropathie aiguë de Charcot, fracture, thrombose, stase veineuse) |
1 | Légère |
| Infection locale (telle que décrite ci-dessus) avec érythème > 2 cm, ou impliquant des structures plus profondes que la peau et les tissus sous-cutanés (p. ex., abcès, ostéomyélite, arthrite septique, fasciite) et
Aucun signe de réponse inflammatoire systémique (comme décrit ci-dessous) |
2 | Modéré |
| Infection locale (telle que décrite ci-dessus) avec les signes du SRIS, se manifestant par au moins deux des éléments suivants :
• Température >38° ou <36°C • Fréquence cardiaque > 90 battements/min • Fréquence respiratoire > 20 respirations/min ou PaCO2 < 32 mm Hg • Nombre de globules blancs > 12 000 ou < 4 000 cu/mm ou 10 % de formes immatures (bande) |
3 | Sévère |
| Ischémie-0 | Ischémie-1 | Ischémie-2 | Ischémie-3 | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| W-0 | TB | TB | B | M | TB | B | M | H | B | B | M | H | B | M | M | H | |
| W-1 | TB | TB | B | M | TB | B | M | H | B | M | H | H | M | M | H | H | |
| W-2 | B | B | M | H | M | M | H | H | M | H | H | H | H | H | H | H | |
| W-3 | M | M | H | H | H | H | H | H | H | H | H | H | H | H | H | H | |
| fI-0 | fI-1 | fI-2 | fI-3 | fI-0 | fI-1 | fI-2 | fI-3 | fI-0 | fI-1 | fI-2 | fI-3 | fI-0 | fI-1 | fI-2 | fI-3 | ||
| Très faible = TB = stade clinique 1
Bas = B = stade clinique 2 Modéré = M = Stade clinique 3 Élevé = H = Stade clinique 4 | |||||||||||||||||
| Ischémie-0 | Ischémie-1 | Ischémie-2 | Ischémie-3 | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| W-0 | TB | TB | TB | TB | TB | B | B | M | B | B | M | M | M | H | H | H | |
| W-1 | TB | TB | TB | TB | B | M | M | M | H | H | H | H | H | H | H | H | |
| W-2 | TB | TB | TB | TB | M | M | H | H | H | H | H | H | H | H | H | H | |
| W-3 | TB | TB | TB | TB | M | M | M | H | H | H | H | H | H | H | H | H | |
| fI-0 | fI-1 | fI-2 | fI-3 | fI-0 | fI-1 | fI-2 | fI-3 | fI-0 | fI-1 | fI-2 | fI-3 | fI-0 | fI-1 | fI-2 | fI-3 | ||
| Très faible = TB = stade clinique 1
Bas = B = stade clinique 2 Modéré = M = Stade clinique 3 Élevé = H = Stade clinique 4 | |||||||||||||||||
GLASS
Le "Global Limb Anatomic Staging System" (GLASS) est un système de stadification basé sur l'anatomie fémoro-poplitée et infra-poplitée spécifique au patient. Il comprend également des modificateurs basés sur l'anatomie vasculaire du pied. Ces facteurs sont combinés pour former un score GLASS global. Ceci peut ensuite être utilisé en conjonction avec le score WIfI pour déterminer si un patient sera susceptible de bénéficier d'une absence d'intervention, d'une intervention endovasculaire ou d'une procédure ouverte. Il s'agit d'une manière fondée sur des preuves de choisir la méthode de revascularisation pour les patients.[62]
Options de revascularisation
Endovasculaire
Le traitement endovasculaire est une modalité peu invasive et bien établie pour traiter la MAP. Il existe deux principaux types de traitements endovasculaires, l'angioplastie[note 9] et le stenting[note 10]. Ces traitements endovasculaires donnent les meilleurs résultats lorsqu'ils sont appliqués sur des lésions occlusives focales des artères iliaques et fémorales superficielles. Le succès technique et la durabilité du traitement endovasculaire diminuent chez les patients présentant des occlusions totales de segments longs et une artériopathie occlusive sous-poplitée.
Les complications du traitement endovasculaire comprennent l'échec du traitement, qu'il soit immédiat ou à plus long terme, l'hématome au site opératoire et toutes les autres complications habituelles associées à la chirurgie.
| % de perméabilité à 1 an
(intervalle) |
% de perméabilité à 3 ans
(intervalle) |
% de perméabilité à 5 ans
(intervalle) | |
|---|---|---|---|
| Sténose d'angioplastie | 77 (76–80) | 61 (55–68) | 55 (52–62) |
| Occlusion d'angioplastie | 65 (55–71) | 48 (40–55) | 42 (33–51) |
| Angioplastie + sténose du stent | 75 (73–79) | 66 (64–70) | |
| Angioplastie + occlusion de stent | 73 (69–75) | 64 (59–67) |
Ouverte
Les options chirurgicales comprennent:
- Greffes de pontage pour détourner le flux autour du blocage.
- Par exemple, d'une fémorale à l'autre (fem-fem), de la fémorale à la poplitée (fem-pop), de la poplitée à un tibial (fem-tib), etc.
- endartérectomie pour éliminer par segment la plaque obstructive.
- angioplastie de patch afin d'augmenter le diamètre de l'artère.
Les pontages peuvent être classés comme anatomiques ou non anatomiques[note 11]. Les pontages peuvent être réalisés avec différents matériaux, tels que la propre veine du patient, une veine cryoconservée ou des greffons synthétiques. Le matériau et l'emplacement du pontage détermineront sa perméabilité sur une période de temps[note 12][9].
Hybride
La chirurgie hybride est toute chirurgie qui combine des techniques endovasculaires et ouvertes. Ces opérations peuvent transmettre les bénéfices de chaque type de chirurgie, mais aussi leurs complications.
Suivi
Le suivi de ces patients dépend fortement de la gravité de la maladie et de la présence ou non d'interventions. Cependant, quelle que soit la gravité de la maladie, il est toujours important de passer en revue les facteurs de risque modifiables, comme l'arrêt du tabac, et d'assurer une prise en charge médicale optimale. Il est aussi important de s'assurer que le patient se sente à l'aise pour retourner à la clinique si des symptômes se développent/aggravent[63][64][65]
Maladie asymptomatique
Pour la maladie asymptomatique[64]:
- Un suivi est sans doute nécessaire car l'évolution naturelle est qu'elle s'aggrave avec le temps.
- Aucune preuve pour suggérer à quelle fréquence ce suivi devrait être fait.
- Il été suggéré que les patients présentant un risque plus élevé de progression soient suivis de plus près.
Maladie symptomatique
Pour la maladie symptomatique[65]:
- Les patients qui participent à la thérapie par la marche doivent être suivis à un intervalle régulier convenu entre le patient et le médecin.
- Pour les patients présentant un risque élevé de progression vers une maladie pouvant nécessiter une intervention, ou une maladie grave avec un risque élevé d'intervention, un suivi plus étroit est recommandé.
- Des ITB lors des suivis sont recommandés.
Revascularisation endovasculaire
Pour la revascularisation endovasculaire[63]
- Le suivi dépend de la procédure, principalement de l'anatomie et du type d'intervention.
- Généralement être effectué à 1, 3 et 6 mois, puis tous les 6 mois.
- Il est important d'évaluer les symptômes des patients et de faire un examen clinique approfondi.
- Obtenir des ITB réguliers ainsi que des duplex est aussi important.
- Les vitesses systoliques maximales dérivées du duplex sont utiles pour indiquer s'il y a une resténose ou une occlusion, ce qui n'est pas rare, en particulier dans les maladies les plus graves.
Revascularisation ouverte
Pour la revascularisation ouverte[63]
- Le suivi commence généralement avec une évaluation initiale postopératoire précoce.
- Puis à 3 (pas toujours nécessaire pour les pontages prothétiques sous-inguinaux ; principalement pour les pontages veineux), 6 et 12 mois, suivi d'un suivi régulier de 6 à 12 mois.
- Un examen physique, un ITB et un duplex sont nécessaires.
- L'utilisation de duplex peut aider à évaluer la perméabilité du segment artériel traité ou du pontage via la vitesse systolique maximale et le rapport de vitesse.
- Le tableau ci-dessous est un exemple de la manière dont l'échodoppler peut être utilisé pour déterminer le risque de thrombose du greffon veineux sous-inguinal..
| Catégorie | Vitesse systolique maximale (cm/s) | Rapport de vitesse | Critères de basse vitesse (cm/s) | ITB |
|---|---|---|---|---|
| Risque le plus élevé | >300 | >3.5 | <45 | <0.15 |
| Risque élevé | >300 | >3.5 | <45 | >0.15 |
| Risque modéré | 180-300 | >2.0 | >45 | >0.15 |
| Faible risque | <180 | <2.0 | >45 | >0.15 |
Complications
La maladie artérielle périphérique a une progression naturelle qui expose les patients à un risque élevé de complications. Les complications de cette maladie sont:[1][64]
- l'ischémie critique du membre inférieur
- gangrène des orteils
- S'ils restent sous forme de gangrène sèche, c'est-à-dire sans infection, et qu'il y a une bonne circulation, que ce soit au départ ou après l'intervention, il peut se former une escarre qui va rétrécir et éventuellement se momifier et une auto-amputation peut se produire.
- S'ils sont infectés, des antibiotiques peuvent être nécessaires et s'il y a une mauvaise circulation avec un risque de propagation gangréneuse, une amputation chirurgicale est à envisager..
- l'amputation AK, BK, transmétatarsienne, d'un rayon, d'un orteil ou de l'hallux
- une cellulite, un érysipèle, une bactériémie
- une douleur chronique causée par l'ischémie
- un ulcère artériel
- une diminution de la qualité de vie.
-
Nécrose de plusieurs orteils.
-
Ulcère artériel
Évolution
Même avec un traitement, le pronostic de la MAP est généralement réservé. Si le patient ne change pas son mode de vie, la maladie est évolutive. De plus, la plupart des patients atteints d'AOMI ont également une coexistence de maladies cérébrovasculaires ou coronariennes, ce qui augmente également le taux de mortalité. Les résultats chez les femmes ont tendance à être pires que chez les hommes, principalement en raison du petit diamètre des artères. De plus, les femmes sont plus susceptibles de développer des complications et des événements emboliques. Les taux de morbidité et de mortalité à 5, 10 et 15 ans, toutes causes confondues, sont respectivement d'environ 30 %, 50 % et 70 %. Les patients atteints d'ischémie chronique menaçant les membres ont une mortalité de 20 % au cours de la première année suivant la présentation. [1][60][9]
Prévention
Le pilier de la prévention primaire de la maladie artérielle périphérique est l'atténuation des facteurs de risque cardiovasculaire: [66]
- arrêt tabagique
- contrôle du diabète
- exercice (au moins 150 minutes par semaine d'activité aérobique d'intensité modérée ou 75 minutes par semaine d'activité aérobique vigoureuse, ou une combinaison des deux, de préférence réparties sur toute la semaine[67])
- contrôle adéquat de la pression artérielle et du cholestérol (que ce soit avec une prise en charge conservatrice ou médicale) [1]
Il n'y a pas d'avantage à dépister les patients asymptomatiques.[59]
La prévention tertiaire de la maladie artérielle périphérique a un fort chevauchement avec le traitement lui-même. Pour les patients qui n'ont pas un niveau de maladie nécessitant une intervention chirurgicale, la thérapie par la marche est extrêmement importante. Elle peut grandement améliorer les symptômes et les troubles fonctionnels dans cette population. [68]
Notes
- ↑ Car ce groupe musculaire est situé à un niveau distal des artères sous-inguinales obstruées.
- ↑ La gravité augmente le flux sanguin.
- ↑ Attention, les cellulites sont fréquentes chez les patients atteint de MAP et pourraient causer un test de Buerger négatif.
- ↑ Souffles fémoraux, iliaques ou poplités. Rarement fait en clinique.
- ↑ Cependant, ce n'est pas toujours le cas, par exemple ceux qui souffrent de neuropathie diabétique peuvent ne remarquer qu'il y a un problème qu'une fois qu'il y a une perte de tissu.
- ↑ Les valeurs de Se et Sp sont pPour des sténoses hémodynamiquement significatives (> 50%).
- ↑ Certaines réflexions sur le mécanisme incluent l'élargissement des vaisseaux collatéraux existants, l'angiogenèse induite par l'exercice, l'augmentation de la vasodilatation dépendante de l'endothélium de l'oxyde nitrique de la microcirculation, l'amélioration de la bioénergétique du muscle squelettique et l'amélioration de l'hémorrhéologie.
- ↑ Ce paramètre est un élément clé dans le mécanisme de la thérapie par l'exercice.
- ↑ L'angioplastie est le processus de gonflage d'un ballon dans une artère sténosée dans l'espoir d'éclaircir le flux dans l'artère. Il existe différents types et tailles de ballons pour l'angioplastie, et peuvent donc être utilisés dans différentes artères. De plus, certains médicaments peuvent être ajoutés à ces ballons qui sont censés limiter l'hyperplasie intimale et donc la récidive de la sténose.
- ↑ Le stent implique le placement d'un stent dans une artère sténosée pour agir comme un échafaudage pour maintenir l'artère ouverte.
- ↑ Des exemples de pontages anatomiques comprennent :
- Pontage fémoro-poplité
- Pontage aorto-iliaque
- Pontage du poplité à tronc tibiopéronier
- Pontage axillo-fémoral
- Pontage fémoral-fémoral
- ↑
Taux de perméabilité à 5 ans du pontage fémoral poplité au-dessus du genou Conduite Perméabilité Veine 74–76% Polytétrafluoroéthylène (synthétique) 39–52% - ↑ Avec une sténose supplémentaire du greffon, il est logique que l'ITB diminue en raison d'une baisse de la perfusion. En ce qui concerne la vitesse systolique maximale, elle augmente dans cette situation car la sténose provoque un flux plus turbulent qui augmente la vitesse. Cette mesure est fréquemment utilisée par les chirurgiens vasculaires pour mieux comprendre le degré de sténose indépendamment de la diminution de la perfusion.
Références
- Cette page a été modifiée ou créée le 2022/09/10 à partir de Peripheral Arterial Disease (StatPearls / Peripheral Arterial Disease (2022/07/07)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/28613496 (livre).
- ↑ 1,0 1,1 1,2 1,3 1,4 1,5 1,6 1,7 1,8 et 1,9 Michael R. Zemaitis, Julia M. Boll et Mark A. Dreyer, StatPearls, StatPearls Publishing, (PMID 28613496, lire en ligne)
- ↑ Qurat-Ul-Ain Jelani, Mikhail Petrov, Sara C. Martinez et Lene Holmvang, « Peripheral Arterial Disease in Women: an Overview of Risk Factor Profile, Clinical Features, and Outcomes », Current Atherosclerosis Reports, vol. 20, no 8, , p. 40 (ISSN 1534-6242, PMID 29858704, Central PMCID 5984648, DOI 10.1007/s11883-018-0742-x, lire en ligne)
- ↑ Marge Lovell, Kenneth Harris, Thomas Forbes et Gwen Twillman, « Peripheral arterial disease: Lack of awareness in Canada », The Canadian Journal of Cardiology, vol. 25, no 1, , p. 39–45 (ISSN 0828-282X, PMID 19148341, Central PMCID 2691879, lire en ligne)
- ↑ Christopher Bonneau, Nadine R. Caron, Mohamad A. Hussain et Ahmed Kayssi, « Peripheral artery disease among Indigenous Canadians: What do we know? », Canadian Journal of Surgery, vol. 61, no 5, , p. 305–310 (ISSN 0008-428X, PMID 30246980, Central PMCID 6153097, DOI 10.1503/cjs.013917, lire en ligne)
- ↑ F. Simon, A. Oberhuber, N. Floros et P. Düppers, « Pathophysiology of chronic limb ischemia », Gefasschirurgie: Zeitschrift Fur Vaskulare Und Endovaskulare Chirurgie: Organ Der Deutschen Und Der Osterreichischen Gesellschaft Fur Gefasschirurgie Unter Mitarbeit Der Schweizerischen Gesellschaft Fur Gefasschirurgie, vol. 23, no Suppl 1, , p. 13–18 (ISSN 0948-7034, PMID 29950791, Central PMCID 5997105, DOI 10.1007/s00772-018-0380-1, lire en ligne)
- ↑ Javier A. Jurado, Riyaz Bashir et Mark W. Burket, « Radiation-induced peripheral artery disease », Catheterization and Cardiovascular Interventions: Official Journal of the Society for Cardiac Angiography & Interventions, vol. 72, no 4, , p. 563–568 (ISSN 1522-726X, PMID 18819153, DOI 10.1002/ccd.21681, lire en ligne)
- ↑ G.F. VERALDI, M. MACRÌ, P. CRISCENTI et L. SCORSONE, « Arterial endofibrosis in professional cyclists », Il Giornale di Chirurgia, vol. 36, no 6, , p. 267–271 (ISSN 0391-9005, PMID 26888703, Central PMCID 4767374, DOI 10.11138/gchir/2015.36.6.267, lire en ligne)
- ↑ 8,0 et 8,1 Naomi M. Hamburg et Mark A. Creager, « Pathophysiology of Intermittent Claudication in Peripheral Artery Disease », Circulation Journal: Official Journal of the Japanese Circulation Society, vol. 81, no 3, , p. 281–289 (ISSN 1347-4820, PMID 28123169, DOI 10.1253/circj.CJ-16-1286, lire en ligne)
- ↑ 9,00 9,01 9,02 9,03 9,04 9,05 9,06 9,07 9,08 9,09 9,10 et 9,11 (en) L. Norgren, W. R. Hiatt, J. A. Dormandy et M. R. Nehler, « Inter-Society Consensus for the Management of Peripheral Arterial Disease (TASC II) », Journal of Vascular Surgery, série TASC II, vol. 45, no 1, Supplement, , S5–S67 (ISSN 0741-5214, DOI 10.1016/j.jvs.2006.12.037, lire en ligne)
- ↑ Iftikhar J. Kullo, Kent R. Bailey, Sharon L. R. Kardia et Thomas H. Mosley, « Ethnic differences in peripheral arterial disease in the NHLBI Genetic Epidemiology Network of Arteriopathy (GENOA) study », Vascular Medicine (London, England), vol. 8, no 4, , p. 237–242 (ISSN 1358-863X, PMID 15125483, DOI 10.1191/1358863x03vm511oa, lire en ligne)
- ↑ W. T. Meijer, D. E. Grobbee, M. G. Hunink et A. Hofman, « Determinants of peripheral arterial disease in the elderly: the Rotterdam study », Archives of Internal Medicine, vol. 160, no 19, , p. 2934–2938 (ISSN 0003-9926, PMID 11041900, DOI 10.1001/archinte.160.19.2934, lire en ligne)
- ↑ Smriti Murali Krishna, Joseph V. Moxon et Jonathan Golledge, « A Review of the Pathophysiology and Potential Biomarkers for Peripheral Artery Disease », International Journal of Molecular Sciences, vol. 16, no 5, , p. 11294–11322 (ISSN 1422-0067, PMID 25993296, Central PMCID 4463701, DOI 10.3390/ijms160511294, lire en ligne)
- ↑ https://doi.org/10.1177/0272989x9701700107
- ↑ https://doi.org/10.1177/0272989x9701700107
- ↑ https://doi.org/10.1177/0272989x9701700107
- ↑ ISBN: 978-0-323392761
- ↑ ISBN: 978-0-323392761
- ↑ ISBN: 978-0-323392761
- ↑ https://doi.org/10.1177/014107688908201209
- ↑ https://doi.org/10.1177/014107688908201209
- ↑ https://doi.org/10.1177/014107688908201209
- ↑ https://doi.org/10.1177/014107688908201209
- ↑ https://doi.org/10.1177/014107688908201209
- ↑ https://doi.org/10.1177/014107688908201209
- ↑ Steven R. McGee, Evidence-based physical diagnosis, (ISBN 978-0-323-50871-1 et 0-323-50871-5, OCLC 959371826, lire en ligne)
- ↑ 10.1001/archinte.158.12.1357
- ↑ ISBN: 978-0-323392761
- ↑ ISBN: 978-0-323392761
- ↑ ISBN: 978-0-323392761
- ↑ ISBN: 978-0-323392761
- ↑ https://doi.org/10.1177/0272989x9701700107
- ↑ https://doi.org/10.1177/0272989x9701700107
- ↑ https://doi.org/10.1177/0272989x9701700107
- ↑ https://doi.org/10.1177/0272989x9701700107
- ↑ https://doi.org/10.1177/0272989x9701700107
- ↑ https://doi.org/10.1177/0272989x9701700107
- ↑ https://doi.org/10.1177/014107688908201209
- ↑ https://doi.org/10.1177/014107688908201209
- ↑ https://doi.org/10.1177/014107688908201209
- ↑ https://doi.org/10.1177/014107688908201209
- ↑ https://doi.org/10.1177/014107688908201209
- ↑ https://doi.org/10.1177/014107688908201209
- ↑ https://doi.org/10.1177/0272989x9701700107
- ↑ https://doi.org/10.1177/0272989x9701700107
- ↑ https://doi.org/10.1177/0272989x9701700107
- ↑ https://doi.org/10.1177/0272989x9701700107
- ↑ https://doi.org/10.1067%2Fmva.2000.108640
- ↑ https://doi.org/10.1067%2Fmva.2000.108640
- ↑ Kaylan N. McClary et Patrick Massey, StatPearls, StatPearls Publishing, (PMID 31334946, lire en ligne)
- ↑ Inge I. de Liefde, Jan Klein, Jeroen J. Bax et Hence J. M. Verhagen, « Exercise ankle brachial index adds important prognostic information on long-term out-come only in patients with a normal resting ankle brachial index », Atherosclerosis, vol. 216, no 2, , p. 365–369 (ISSN 1879-1484, PMID 21397231, DOI 10.1016/j.atherosclerosis.2010.10.051, lire en ligne)
- ↑ Ameena Zubair et Saran Lotfollahzadeh, StatPearls, StatPearls Publishing, (PMID 35015455, lire en ligne)
- ↑ Dominik Fleischmann, Richard L. Hallett et Geoffrey D. Rubin, « CT angiography of peripheral arterial disease », Journal of vascular and interventional radiology: JVIR, vol. 17, no 1, , p. 3–26 (ISSN 1051-0443, PMID 16415129, DOI 10.1097/01.RVI.0000191361.02857.DE, lire en ligne)
- ↑ Matthew K. Walsworth, Rob de Bie, Stephen F. Figoni et Jessica B. O'Connell, « Peripheral Artery Disease: What You Need to Know », The Journal of Orthopaedic and Sports Physical Therapy, vol. 47, no 12, , p. 957–964 (ISSN 1938-1344, PMID 28992768, DOI 10.2519/jospt.2017.7442, lire en ligne)
- ↑ R. Fontaine, M. Kim et R. Kieny, « [Surgical treatment of peripheral circulation disorders] », Helvetica Chirurgica Acta, vol. 21, no 5-6, , p. 499–533 (ISSN 0018-0181, PMID 14366554, lire en ligne)
- ↑ R. B. Rutherford, J. D. Baker, C. Ernst et K. W. Johnston, « Recommended standards for reports dealing with lower extremity ischemia: revised version », Journal of Vascular Surgery, vol. 26, no 3, , p. 517–538 (ISSN 0741-5214, PMID 9308598, DOI 10.1016/s0741-5214(97)70045-4, lire en ligne)
- ↑ R. Fontaine, M. Kim, R. Kieny: «Die chirugische Behandlung der peripheren Durchblutungsstörungen», in:Helvetica Chirurgica Acta, Basel, 1954, 21 (5/6): 499-533
- ↑ Erreur de référence : Balise
<ref>incorrecte : aucun texte n’a été fourni pour les références nommées:212 - ↑ 58,0 et 58,1 (en) Michael S. Conte, Frank B. Pomposelli, Daniel G. Clair et Patrick J. Geraghty, « Society for Vascular Surgery practice guidelines for atherosclerotic occlusive disease of the lower extremities: Management of asymptomatic disease and claudication », Journal of Vascular Surgery, vol. 61, no 3, , p. 2S–41S.e1 (ISSN 0741-5214 et 1097-6809, PMID 25638515, DOI 10.1016/j.jvs.2014.12.009, lire en ligne)
- ↑ 59,0 et 59,1 US Preventive Services Task Force, Susan J. Curry, Alex H. Krist et Douglas K. Owens, « Screening for Peripheral Artery Disease and Cardiovascular Disease Risk Assessment With the Ankle-Brachial Index: US Preventive Services Task Force Recommendation Statement », JAMA, vol. 320, no 2, , p. 177–183 (ISSN 1538-3598, PMID 29998344, DOI 10.1001/jama.2018.8357, lire en ligne)
- ↑ 60,0 et 60,1 D. L. Clement, H. Boccalon, J. Dormandy et I. Durand-Zaleski, « A clinical approach to the management of the patient with coronary (Co) and/or carotid (Ca) artery disease who presents with leg ischaemia (Lis) », International Angiology: A Journal of the International Union of Angiology, vol. 19, no 2, , p. 97–125 (ISSN 0392-9590, PMID 10905794, lire en ligne)
- ↑ (en) Joseph L. Mills, Michael S. Conte, David G. Armstrong et Frank B. Pomposelli, « The Society for Vascular Surgery Lower Extremity Threatened Limb Classification System: Risk stratification based on Wound, Ischemia, and foot Infection (WIfI) », Journal of Vascular Surgery, vol. 59, no 1, , p. 220–234.e2 (ISSN 0741-5214 et 1097-6809, PMID 24126108, DOI 10.1016/j.jvs.2013.08.003, lire en ligne)
- ↑ Michael S. Conte, Andrew W. Bradbury, Philippe Kolh et John V. White, « Global vascular guidelines on the management of chronic limb-threatening ischemia », Journal of Vascular Surgery, vol. 69, no 6S, , p. 3S–125S.e40 (ISSN 1097-6809, PMID 31159978, Central PMCID 8365864, DOI 10.1016/j.jvs.2019.02.016, lire en ligne)
- ↑ 63,0 63,1 63,2 et 63,3 R. Eugene Zierler, William D. Jordan, Brajesh K. Lal et Firas Mussa, « The Society for Vascular Surgery practice guidelines on follow-up after vascular surgery arterial procedures », Journal of Vascular Surgery, vol. 68, no 1, , p. 256–284 (ISSN 1097-6809, PMID 29937033, DOI 10.1016/j.jvs.2018.04.018, lire en ligne)
- ↑ 64,0 64,1 et 64,2 (en) Conte Ms, Pomposelli Fb, Clair Dg et Geraghty Pj, « Society for Vascular Surgery practice guidelines for atherosclerotic occlusive disease of the lower extremities: management of asymptomatic disease and claudication », Journal of vascular surgery, vol. 61, no 3 Suppl, 2015 mar (ISSN 1097-6809, PMID 25638515, DOI 10.1016/j.jvs.2014.12.009, lire en ligne)
- ↑ 65,0 et 65,1 (en) Marie D. Gerhard-Herman, Heather L. Gornik, Coletta Barrett et Neal R. Barshes, « 2016 AHA/ACC Guideline on the Management of Patients With Lower Extremity Peripheral Artery Disease: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines », Journal of the American College of Cardiology, vol. 69, no 11, , e71–e126 (ISSN 0735-1097, DOI 10.1016/j.jacc.2016.11.007, lire en ligne)
- ↑ (en) Rachelle L. Muir, « Peripheral arterial disease: Pathophysiology, risk factors, diagnosis, treatment, and prevention », Journal of Vascular Nursing, vol. 27, no 2, , p. 26–30 (ISSN 1062-0303, DOI 10.1016/j.jvn.2009.03.001, lire en ligne)
- ↑ (en) « American Heart Association Recommendations for Physical Activity in Adults and Kids », sur www.heart.org (consulté le 12 septembre 2022)
- ↑ (en-US) Mary M. McDermott, « Exercise Rehabilitation for Peripheral Artery Disease: A REVIEW », Journal of Cardiopulmonary Rehabilitation and Prevention, vol. 38, no 2, , p. 63–69 (ISSN 1932-7501, DOI 10.1097/HCR.0000000000000343, lire en ligne)