Thrombose veineuse profonde du membre inférieur
| Maladie | |||
 TVP gauche | |||
| Caractéristiques | |||
|---|---|---|---|
| Signes | Douleur à la palpation, Chaleur, Œdème unilatéral, Signe de Homans, Signe de Payr, Signe de Meyer, État subfébrile , Distension veineuse, Érythème cutané , Température corporelle élevée | ||
| Symptômes |
Douleur, Oedème local, Température corporelle élevée | ||
| Diagnostic différentiel |
Insuffisance cardiaque, Insuffisance veineuse, Syndrome néphrotique, Cirrhose hépatique, Claquage musculaire, Lymphangite, Obstruction lymphatique, Varices, Pathologie du genou, Kyste poplité, ... [+] | ||
| Informations | |||
| Autres noms | Phlébite | ||
| Spécialités | Médecine interne, hématologie | ||
| |||
Prévention des thromboses veineuses (15-2)
La thrombose veineuse profonde du membre inférieur correspond à un caillot de sang (thrombus) qui obstrue la lumière des veines profondes de la jambe. Lorsque le thrombus se détache ou se fragmente et migre dans la circulation systémique, on parle d'embolie.
La maladie thromboembolique veineuse (TEV) comprend la thrombose veineuse profonde (TVP) et l'embolie pulmonaire (EP).
Physiopathologie
La stase veineuse, les lésions endothéliales et l'inflammation conduisent à un état d'hypercoagulabilité. L'activation de la cascade de coagulation active la libération de facteurs prothrombotiques. Simultanément, l'agrégation des plaquettes et de cellules sanguines entrainent la formation d'un thrombus. Le thrombus peut provoquer une occlusion complète ou partielle de la veine entraînant une stase veineuse, un lymphœdème et éventuellement une ischémie des tissus environnants. Un TVP peut se propager et conduire à une embolie pulmonaire[1].
La majorité des thromboses veineuses surviennent aux membres inférieurs. Le thrombus commence à se former dans les veines du mollet (thrombose veineuse distale), puis peut migrer en 2 à 5 jours aux veines de la cuisse.
- Lorsque le thrombus demeure distal (après la veine poplitée) : pas de risque d'embolie pulmonaire
- Lorsque le thrombus touche la veine poplitée ou les veines de la cuisse ou du bassin: risque d'embolisation aux poumons.
- 50% des patients avec thrombose veineuse profonde ont une embolie pulmonaire radiologique
- 70-90% des patients avec embolie pulmonaire ont une thrombose veineuse profonde associée
À noter que les thromboses veineuses du membre supérieur, bien que rares, sont tout autant à risque d'embolie pulmonaire.
Présentation clinique
Facteurs de risque
Les principaux facteurs de risques comprennent tous les facteurs menant à la triade de Virchow, soit la triade de stase veineuse (ou turbulence veineuse), coagulopathie et lésion endothéliale.[2][3][4][5]
| Mécanisme | Facteurs de risque |
|---|---|
| 1) Stase veineuse |
|
| 2) Lésion endothéliale |
|
| 3) État d'hypercoagulabilité |
|
| Autres |
Questionnaire
Il est important de questionner spécifiquement la présence des facteurs de risque de thrombose veineuse ainsi que la présence de :
- douleur au membre atteint
- oedème local du membre atteint
- fièvre
- Symptôme d'embolie pulmonaire (douleur thoracique, dyspnée, syncope)
Examen clinique
L'examen physique peut présenter les signes cliniques suivant:
- signes vitaux: fièvre, subfébrile
- examen du membre inférieur
- Œdème unilatéral
- chaleur du membre atteint
- Érythème localisé
- distension veineuse ("cordon palpable")
- douleur à la palpation du trajet des veines profondes
- signe de Homans : douleur au mollet à la dorsiflexion de la cheville
- signe de Payr : douleur à la pression de la plante médiale du pied
- signe de Meyer : douleur à la compression du mollet
Approche clinique
Le diagnostic de la TVP est difficile, à cet effet, le score de Wells pour la thrombose veineuse profonde peut être utile et permettra d'orienter les investigations subséquentes.
| Critères | Points |
|---|---|
| Cancer actif dans les 6 derniers mois en Tx actif ou palliatif | 1 |
| Paralyse, parésie ou immobilisation plâtrée récente du membre inférieur | 1 |
| Alitement récent pendant plus de 3 jours et/ou chirurgie majeure depuis moins de 12 semaines requérant une anesthésie régionale ou générale | 1 |
| Douleur à la pression sur le trajet du système veineux profond | 1 |
| Œdème de tout le membre inférieur | 1 |
| Circonférence du mollet > 3 cm vs autre mollet mesuré à 10 cm sous la tubérosité tibiale | 1 |
| Œdème à godet unilatéral | 1 |
| Veines collatérales superficielles non variqueuses | 1 |
| Antécédent de TVP documenté[note 1] | 1 |
| Diagnostic alternatif aussi probable ou plus probable (par exemple: Kyste de Baker, cellulite, dommage musculaire, syndrome post-phlébitique, lymphadénopathie inguinale, compression veineuse externe) | -2 |
Niveau de probabilité selon les critères de Wells[7]:
- 3-8: élevé (70 à 80%)
- 1-2: modéré (30%)
- 0 ou moins: faible (5 à 10%)
Niveau de probabilité selon les critères de Wells modifiés:
- si <= 1 point: risque, faible 6 %
- si >= 2 points: risque élevé 28 %
Il est également important de faire le dépistage de néoplasie approprié pour l'âge ou de rechercher une néoplasie si le patient présente des symptômes B, une atteinte bilatérale ou un examen physique ou paraclinique suspect.
Examens paracliniques
Laboratoires
Les investigations de base sont[8]:
- Formule sanguine complète
- INR, TCA
- D-dimères sériques: augmentés
- bilan rénal
- D'autres investigations peuvent être demandées selon la suspicion clinique et le jugement du clinicien.
On peut considérer le dépistage de thrombophilie (controversé) s'il y a : TVP bilatérale, récidivante, premier épisode idiopathique chez un jeune patient (< 60 ans), un site inhabituel, une association de thromboses veineuse et artérielle, des avortements spontanés répétés, des antécédents familiaux significatifs de TVP, EP ou thrombophilie connue[9]. Le bilan inclut:
- antithrombine
- Protéine C
- Protéine S
- Mutation du Facteur V Leiden
- Mutation prothrombine
- Recherche des anticorps antiphospholipides
Il est également important de faire le dépistage de néoplasie approprié pour l'âge ou de rechercher une néoplasie si le patient présente des symptômes B, une atteinte bilatérale ou un examen physique ou paraclinique suspect.
Imagerie
Les modalités d'imagerie disponibles pour évaluer la TVP comprennent:
- l'échographie doppler
- l'échographie au point de service (POCUS)
- les études vasculaires (angiographie par IRM ou tomodensitométrie, phlébographies).
Diagnostic
Après avoir stratifié le risque sur la base des critères de Wells, on suit l'algorithme diagnostique suivant [8]:
| TVP peu probable | TVP probable |
|---|---|
Mesurer les D-dimères
|
Faire une échographie Doppler des veines proximales du membre inférieur avec compression veineuse
|
Diagnostic différentiel
Le diagnostic différentiel de la TVP comprend :
- Étirement ou déchirure musculaire avec œdème secondaire
- Kyste poplité (de Baker) rupturé
- Cellulite
- Lymphangite ou obstruction lymphatique
- Varices et insuffisance veineuse
- Pathologie du genou (p. ex: entorse, arthrite septique, synovite, rupture de ligament croisé)
- Insuffisance cardiaque, cirrhose, syndrome néphrotique (mais habituellement ces pathologies se présentent par un œdème bilatéral)
- Pathologie compressive des du membre inférieur ou iliaques (néoplasies, abcès, hématomes)
Traitement
Il faut d'abord déterminer si le patient devra être hospitalisé ou peut être renvoyé à la maison sous anticoagulation avec un suivi adéquat.
Considérer une hospitalisation si[8][10]:
- Instabilité hémodynamique (SaO2 < 90% AA)
- Insuffisance rénale sévère
- Risque hémorragique élevé (p. ex: post-op récent)
- Douleurs sévères mal soulagées (nécessitant une analgésie intraveineuse)
- Complications (atteinte menaçante du membre)
- Risque de non-compliance aux médicaments, fiabilité du suivi
Anticoagulation
L'anticoagulation doit être initiée rapidement, dès le diagnostic de TVP ou si la suspicion clinique est élevée et que le délai d'investigations est long (> 4h) afin de réduire la mortalité et morbidité associées[11][12]:
- 1er choix: anticoagulants oraux directs (AOD)
- Contre-indications: insuffisance rénale (Rivaroxaban et Édoxaban : eDFG < 15 ; Apixaban et Dabigatran : eDFG < 30), insuffisance hépatique avec coagulopathie, > 120 kg
- rivaroxaban (Xarelto) et apixaban (Eliquis): débuter d'emblée en monothérapie
- Rivaroxaban 15mg po bid pour 21 jours, puis 20mg po die pour le reste du traitement
- Apixaban 10mg po bid pour 7 jours, puis 5mg po bid pour le reste du traitement
- dabigatran (Pradaxa) et Édoxaban : nécessite un pont avec un autre anticoagulant (souvent une HBPM) pendant 5-10 jours
- Dabigatran 150mg po bid
- Edoxaban 30mg po die
- 2e choix: antagonistes de la vitamine K (warfarine)
- Indications: dialyse, insuffisance rénale sévère, obésité
- Nécessite un pont avec de l'héparine non fractionnée ou l'héparine de bas poids moléculaire en même temps : poursuivre ≥ 5 jours et cesser lorsque 2 INR de suite (à 24h d'intervalle) sont ≥ 2.0
- Dose: typiquement, débuter avec 5mg po die puis ajuster en fonction de l'INR
- Déconseillé chez le patient avec néoplasie
- 3e choix: héparine de bas poids moléculaire (HBPM)
- Contre-indications: eDFG < 30 ou antécédent de HIT
- Doses:
- daltéparine (Fragmin) 200U/kg sc die ou 100U/kg sc bid si >100kg
- Énoxaparine (Lovenox) 1.5mg/kg sc die ou 1mg/kg sc die si >100kg
- nadroparine (Fraxiparine) 171U/kg sc die ou 86U/kg sc bid
- tinzaparine (Innohep) 175U/kg sc die
- Seul anticoagulant utilisé en grossesse (1er choix, non tératogène)
- Historiquement préférée pour les patients avec cancer, mais de plus en plus de données ont démontré l'utilisation sécuritaire des AOD pour les néoplasies non digestives[13]
- 'héparine'
- Indications: si la capacité d'arrêter l'anticoagulation rapidement est requise
- Si TVP provoquée par un facteur de risque isolé transitoire : 3 mois après disparition du facteur de risque
- 1ère récidive provoquée: idem, considérer traitement prolongé
- Si TVP idiopathique : Minimum 3 mois et considérer un traitement long terme si faible risque hémorragique
- 1ère récidive idiopathique: idem, forte recommandation de traitement à vie
- Néoplasie active : prolongée
Thrombolyse
Les indications pour le traitement thrombolytique de la TVP sont[14]:
- La thrombose proximale massive des membres inférieurs (soit une TVP poplitée ou fémorale)
- La thrombose ilio-fémorale associée à l'un ou aux deux des éléments suivants:
- Gonflement symptomatique sévère (donc à risque d'ischémie)
- Ischémie menaçant les membres (Phlegmasia cerulea dolens)
L'agent thrombolytique rt-PA (alteplase) est débuté en plus de l'anticoagulation avec de l'héparine standard.
Autres
Le 'filtre de la VCI' est réservé aux patients ayant[11]:
- TVP proximale et dont l'anticoagulation est contre-indiquée
- les patients avec une embolie pulmonaire malgré une anticoagulation thérapeutique.
- Le port de 'bas compressifs' peut aider à prévenir le syndrome post-phlébite[15].
Complications
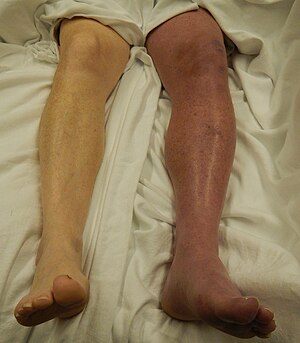
Les complications:
- embolie pulmonaire (complication la plus redoutable)
- embolie paradoxale
- thrombophlébite septique
- phlegmesia cerulea dolens et phlegmesia alba dolens
- syndrome post-phlébite
- insuffisance veineuse chronique
Prévention
Prévention des thromboses veineuses (15-2)
Chez les patients hospitalisés, l'indication est déterminée par le score de Padua.
| Facteur de risque | Points |
|---|---|
| Cancer actif[note 2] | 3 |
| Antécédents de TVP (sauf superficielles) | 3 |
| Mobilité réduite[note 3] | 3 |
| Thombophilie[note 4] | 3 |
| Trauma ou chirurgie récente ( ≤ 1 mois) | 2 |
| Âge ≥ 70 ans | 1 |
| Défaillance cardiaque ou respiratoire | 1 |
| Infarctus du myocarde ou AVC ischémique | 1 |
| Infection aiguë et/ou maladie rhumatologique | 1 |
| Obésité (IMC ≥ 30) | 1 |
| Traitement hormonal | 1 |
| Interprétation | |
| Haut risque - prophylaxie nécessaire[note 5] | ≥ 4 points |
| Faible risque | ≤ 3 points |
Thromboprophylaxie
| Pharmacologique | Non-pharmacologique |
|---|---|
La dose est à individualiser selon le poids et la clairance de la créatinine. |
|
La thromboprophylaxie est cessée au congé de l'hôpital sauf dans certains situations particulières (post-opératoire de chirurgie pour un cancer ou chirurgies orthopédiques).
Contre-indications
Absolues:
- Saignement actif ou risque élevé de saignement (ulcère actif, AVC massif)
- Coagulopathie
- Thrombocytopénie (plaquettes < 50 x 109/L)
- Antécédent de HIT ou sensibilité à l'héparine ou HBPM
Relatives:
- Chirurgie ou AVC < 3mois
- Antécédents de malformation artérioveineuse, de diathèse hémorragique, de saignement intracrânien
- Anévrisme cérébral, lésion cérébrale ou néoplasie intracrânienne
- Hypertension non maîtrisée
- Rétinopathie diabétique hémorragique
- Thrombolyse < 7 jours
- Présence dans les 3 derniers mois de: saignement gastro-intestinal, analgésie épidurale ou rachidienne
- Chirurgie majeure < 14 jours
Notes
- ↑ Ce critère a été rajouté dans les critères de Wells modifiés.
- ↑ Patient avec cancer local ou métastases à distance et/ou chez qui une chimiothérapie ou radiothérapie a été effectuée dans les 6 mois précédents.
- ↑ Immobilisation au lit anticipée (avec mobilisation pour les toilettes) pour au moins 3 jours. Cette immobilisation peut être du fait de la condition du patient ou par ordre du médecin traitant.
- ↑ Mutation de l'antihrombine, déficits en protéines C ou S, facteur V Leiden, mutation de la prothrombine, syndrome antiphospholipides.
- ↑ 11% de MTE chez les patients à haut risque vs 0.3% chez les patients à faible risque (HR: 32.0; 95% CI, 4.1 - 251.0). Dans la population à haut risque, le risque de TVP était de 6.7%, d'EP non fatale de 3.9% et d'EP fatale à 0.4%.
Références
- Cette page a été modifiée ou créée le 2021/04/14 à partir de Deep Venous Thrombosis Of The Lower Extremity (StatPearls / Deep Venous Thrombosis Of The Lower Extremity (2020/11/24)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/29262179 (livre).
- ↑ (en) Huyen A Tran, Harry Gibbs, Eileen Merriman et Jennifer L Curnow, « New guidelines from the Thrombosis and Haemostasis Society of Australia and New Zealand for the diagnosis and management of venous thromboembolism », Medical Journal of Australia, vol. 210, no 5, 2019-03-xx, p. 227–235 (ISSN 0025-729X et 1326-5377, DOI 10.5694/mja2.50004, lire en ligne)
- ↑ (pt) Gustavo Muçouçah Sampaio Brandão, Raissa Carolina Fonseca Cândido, Hamilton de Almeida Rollo et Marcone Lima Sobreira, « Anticoagulantes orais diretos para o tratamento da trombose venosa profunda: revisão de revisões sistemáticas », Jornal Vascular Brasileiro, vol. 17, no 4, 2018-12-xx, p. 310–317 (ISSN 1677-5449, PMID 30787949, Central PMCID PMC6375259, DOI 10.1590/1677-5449.005518, lire en ligne)
- ↑ (en) L. Jara-Palomares, N. van Es, J. M. Praena-Fernandez et G. Le Gal, « Relationship between type of unprovoked venous thromboembolism and cancer location: An individual patient data meta-analysis », Thrombosis Research, vol. 176, , p. 79–84 (ISSN 0049-3848 et 1879-2472, PMID 30780008, DOI 10.1016/j.thromres.2019.02.011, lire en ligne)
- ↑ (en) Sheng Xu, Jerry Yongqiang Chen, Qishi Zheng et Ngai Nung Lo, « The safest and most efficacious route of tranexamic acid administration in total joint arthroplasty: A systematic review and network meta-analysis », Thrombosis Research, vol. 176, 2019-04-xx, p. 61–66 (DOI 10.1016/j.thromres.2019.02.006, lire en ligne)
- ↑ (en) Junxun Li, Fan Zhang, Chujia Liang et Zhuangjian Ye, « The Diagnostic Efficacy of Age-Adjusted D-Dimer Cutoff Value and Pretest Probability Scores for Deep Venous Thrombosis », Clinical and Applied Thrombosis/Hemostasis, vol. 25, , p. 1076029619826317 (ISSN 1076-0296, PMID 30754991, Central PMCID PMC6715010, DOI 10.1177/1076029619826317, lire en ligne)
- ↑ (en) Alessandro Di Minno, Pasquale Ambrosino, Ilenia Calcaterra et Matteo Nicola Dario Di Minno, « COVID-19 and Venous Thromboembolism: A Meta-analysis of Literature Studies », Seminars in Thrombosis and Hemostasis, vol. 46, no 07, , p. 763–771 (ISSN 0094-6176 et 1098-9064, PMID 32882719, Central PMCID PMC7645842, DOI 10.1055/s-0040-1715456, lire en ligne)
- ↑ Philip S. Wells, David R. Anderson, Marc Rodger et Melissa Forgie, « Evaluation of D-dimer in the diagnosis of suspected deep-vein thrombosis », The New England Journal of Medicine, vol. 349, no 13, , p. 1227–1235 (ISSN 1533-4406, PMID 14507948, DOI 10.1056/NEJMoa023153, lire en ligne)
- ↑ 8,0 8,1 et 8,2 Tobias Tritschler, Noémie Kraaijpoel, Grégoire Le Gal et Philip S. Wells, « Venous Thromboembolism », JAMA, vol. 320, no 15, , p. 1583 (ISSN 0098-7484, DOI 10.1001/jama.2018.14346, lire en ligne)
- ↑ (en) « La recherche de thrombophilie héréditaire et son impact thérapeutique dans la maladie thromboembolique veineuse : résultats d’une étude monocentrique rétrospective sur 162 patients », La Revue de Médecine Interne, vol. 37, no 10, , p. 661–666 (ISSN 0248-8663, DOI 10.1016/j.revmed.2016.01.001, lire en ligne)
- ↑ (en) Thomas L. Ortel, Ignacio Neumann, Walter Ageno et Rebecca Beyth, « American Society of Hematology 2020 guidelines for management of venous thromboembolism: treatment of deep vein thrombosis and pulmonary embolism », Blood Advances, vol. 4, no 19, , p. 4693–4738 (ISSN 2473-9529 et 2473-9537, PMID 33007077, Central PMCID PMC7556153, DOI 10.1182/bloodadvances.2020001830, lire en ligne)
- ↑ 11,0 11,1 et 11,2 (en) Romain Chopard, Ida Ehlers Albertsen et Gregory Piazza, « Diagnosis and Treatment of Lower Extremity Venous Thromboembolism: A Review », JAMA, vol. 324, no 17, , p. 1765 (ISSN 0098-7484, DOI 10.1001/jama.2020.17272, lire en ligne)
- ↑ 12,0 et 12,1 (en) « Clinical Guides », sur Thrombosis Canada - Thrombose Canada, (consulté le 9 mai 2021)
- ↑ (en) J. J. López‐Núñez, J. Trujillo‐Santos et M. Monreal, « Management of venous thromboembolism in patients with cancer », Journal of Thrombosis and Haemostasis, vol. 16, no 12, , p. 2391–2396 (ISSN 1538-7836, DOI 10.1111/jth.14305, lire en ligne)
- ↑ « UpToDate », sur www.uptodate.com (consulté le 27 avril 2021)
- ↑ (en) « The effectiveness of graduated compression stockings for prevention of venous thromboembolism in orthopedic and abdominal surgery patients requiring extended pharmacologic thromboprophylaxis », Journal of Vascular Surgery: Venous and Lymphatic Disorders, vol. 6, no 6, , p. 766–777.e2 (ISSN 2213-333X, DOI 10.1016/j.jvsv.2018.05.020, lire en ligne)
- ↑ (en) S. BARBAR, F. NOVENTA, V. ROSSETTO et A. FERRARI, « A risk assessment model for the identification of hospitalized medical patients at risk for venous thromboembolism: the Padua Prediction Score », Journal of Thrombosis and Haemostasis, vol. 8, no 11, , p. 2450–2457 (ISSN 1538-7933, DOI 10.1111/j.1538-7836.2010.04044.x, lire en ligne)
