Sténose du pylore
| Maladie | |||
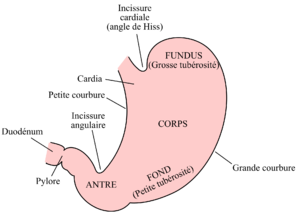 Schéma de l'estomac | |||
| Vidéo | |||
|---|---|---|---|
| Caractéristiques | |||
| Signes | Muqueuses sèches, Pli cutané, Refill capillaire allongé, Fontanelles déprimées, Yeux creux, Diminution du larmoiement, Ondes péristaltiques inversées, Olive pylorique | ||
| Symptômes |
Diminution du débit urinaire, Somnolence, Absence de satiété, Teint ictérique, Diminution du poids, Vomissements projectiles bilieux, Vomissements post-prandiaux, Constipation | ||
| Diagnostic différentiel |
Septicémie, Volvulus, Hernie, Appendicite, Insuffisance rénale aiguë, Constipation chronique, Infection des voies urinaires, Pancréas annulaire, Entérocolite nécrosante, Atrésie et sténose duodénale, ... [+] | ||
| Informations | |||
| Terme anglais | Pyloric Stenosis | ||
| Autres noms | Sténose pylorique hypertrophique infantile | ||
| Wikidata ID | Q18554354 | ||
| Spécialités | Chirurgie générale, Pédiatrie, Chirurgie pédiatrique, Médecine familiale, Médecine d'urgence | ||
| |||
La sténose du pylore, ou SPHI hypertrophique infantile (SPHI), est caractérisée par un épaississement anormal des muscles du pylore de l'estomac, ce qui entraîne une obstruction de la vidange gastrique.[1][2]
Épidémiologie
La SPHI touche 2 à 3 naissances vivantes sur 1000 par an, avec un ratio homme-femme de 6 : 1. Elle touche des individus âgés de 3 à 6 semaines de vie de façon préférentielle, et demeure rare après 12 semaines de vie. [3]
Cette maladie affecte principalement des individus caucasiens (incidence de 2,4 personnes sur 1000).[2] Elle est moins fréquente dans les populations indiennes, asiatiques et noires. [1][2][4] Il est estimé que 30% des nourrissons qui développent une sténose sont les premiers nés de leur fratrie.[3][5]
Étiologies
L'étiologie exacte de la SPHI hypertrophique infantile est inconnue. Cependant, une composante génétique est fortement soupçonnée. En effet, le risque de contracter cette atteinte est 20 fois plus important si un membre de la même fratrie développe cette pathologie. De la même façon, si un enfant a un jumeau identique qui a cette maladie, son risque de la développer se multiplie par 200.[3]
Une étiologie environnementale, en lien avec une exposition à des facteurs spécifiques, semble aussi probable. [3]
Physiopathologie
La SPHI se caractérise par une hypertrophie et une hyperplasie marquées des couches musculaires circulaires et longitudinales du pylore. Par conséquent, le canal pylorique s'allonge et les muscles du pylore s'épaississent. En réponse à ce remodelage, un oedème peut se développer. Ce phénomène entraine un rétrécissement de la lumière de l'antre gastrique.[4]
Si l'atteinte devient sévère, l'estomac se dilate suite à une obstruction de la sortie gastrique. C'est cette obstruction qui induit les épisodes de vomissement projectiles non biliaires.[2]
Ces vomissements répétés peuvent précipiter une déshydratation de même que des désordres métaboliques et électrolytiques chez l'enfant.[5][6]
Présentation clinique
Facteurs de risque
Les facteurs de risque de la SPHI sont [1][3][5][6] :
- une histoire familiale de SPHI
- un petit poids de naissance
- une alimentation à la bouteille
- un tabagisme maternel lors de la grossesse
- une prise d'antibiotiques de type macrolide
- être le premier enfant né d'une fratrie
- la prématurité
- le sexe masculin.
Questionnaire
Les manifestations cliniques de la SPHI sont les suivantes [5][6]:
- des vomissements projectiles non bilieux qui surviennent en post-prandial immédiat
- l'absence de satiété après le boire
- la constipation
- la diminution du débit urinaire
- la somnolence
- l'ictère
- la perte de poids.
L'atteinte se présente principalement entre la 3ème et la 6ème semaines de vie d'un nourrisson.[2][3]
Examen clinique
À l'inspection générale, des signes de déshydratation peuvent être présents[2][7] :
- des fontanelles déprimées
- des yeux creux
- des muqueuses sèches
- une diminution du larmoiement
- un pli cutané
- le refill capillaire allongé.
À l'examen abdominal d'une SPHI, les constatations suivantes peuvent être notées[2] :
- des ondes péristaltiques inversées
- une olive pylorique : correspond à un pylore induré de 1 à 2 cm, palpable à l'hypocondre droit.
Examens paracliniques
Laboratoires
Les examens suivants sont utiles dans la démarche d'investigation :
- une FSC
- les ions :
- les patients avec des vomissements sévères développent parfois une hypokaliémie et/ou une hypochlorydie[2][7]
- un gaz veineux :
- des vomissements répétés peuvent entrainer une alcalose métabolique[2][7]
- la créatininémie et l'urée :
- elle permet d'évaluer si le patient présente une déshydratation de même que la fonction rénale[5].
Imageries

Voici les imageries susceptible de mener au diagnostic d'une SPHI :
- Une échographie abdominale est le gold standard.
- Elle permet de diagnostiquer une SPHI lorsque l'épaisseur de la paroi pylorique de 3 mm ou plus, que la longueur du canal pylorique de 15 mm ou plus, et que le diamètre du canal soit de 10 à 14mm. Cet examen peut aussi démontrer le signe de la chenille, ce qui correspond à une dilatation de l'estomac secondaire à des contractions gastriques contre un pylore hypertrophié.[3][8]
- Une radiographie abdominale est moins sensible et spécifique qu'une échographie, mais elle permet d'identifier des signes en faveur du diagnostic de la SPHI. Ces signes sont :
- un élargissement de la bulle gastrique
- une absence de gaz au niveau de l'intestin grêle ou du côlon
- le signe de la chenille peut aussi être présent.[2]
- Une radiographie abdominale avec utilisation de baryum permet de mettre en lumière les signes cliniques suivants[2] :
- le signe du fil[note 1][9]
- le signe du double track[note 2][10]
- le signe du bec[note 3][11]
- le signe de l'épaule[note 4][12].
Diagnostic
Le diagnostic de SPHI est posé lorsque le tableau clinique de même que des trouvailles à l'imagerie médicale concordent avec cette pathologie. C'est typiquement l'échographie abdominale qui est utilisée dans ce contexte. [5]
Diagnostic différentiel
Le diagnostic différentiel de la SPHI comprend[2][5] :
- le volvulus intestinal
- la maladie de Hirschsprung
- la hernie
- la gastro-entérite
- les coliques
- la constipation
- l'entérocolite nécrosante
- l'appendicite
- le mégacôlon toxique
- l'infection des voies urinaires
- l'insuffisance rénale aiguë
- la torsion testiculaire
- la septicémie
- une Atrésie et sténose duodénale
- pancréas annulaire.
Traitement
Prise en charge initiale
Un traitement médical est nécessaire et consiste généralement en une réhydratation et une correction des déséquilibres électrolytiques. Le patient se présente classiquement avec une alcalose métabolique hypochlorémique. Si une réhydratation est nécessaire, un bolus de 20 cc/kg de NS suivi d'un M1/2F + 20 mEq KCL à 1,25-2X les besoins de base. Si le patient présente une déshydratation modérée ou sévère, des quantités plus importantes de cristalloïdes seront utilisées.[2][3]
Le tube NG doit être envisagé chez un patient qui présente des vomissements conséquents. [2][6] Le patient est NPO en vue de l'intervention chirurgicale.
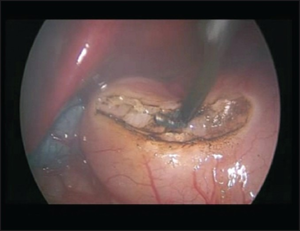
Prise en charge chirurgicale
La prise en charge chirurgicale est uniquement effectuée après la correction de toute déshydratation, soit typiquement 12 à 48 heures après l'admission. [13] Une pyloromyotomie chirurgicale de Ramstedt est l'intervention privilégiée. Cette intervention implique d'effectuer un incision longitudinale puis une dissection mousse jusqu'à la sous-muqueuse, soit de la veine de Mayo jusqu'à 1 à 2 cm sur l'antre gastrique. Cette procédure peut être réalisée par laparoscopie ou de façon ouverte (incision transversale haute ou péri-ombilicale). Elle consiste à inciser de façon longitudinale puis à disséquer le muscle pylorique jusqu'à la sous-muqueuse.[3]
L'opération est curative et présente une très faible morbidité.[13] En cas de transsection de la muqueuse, on referme la pyloromyotomie et on procède à une seconde incision musculaire sur l'autre versant.
Suivi
Le seul soin postopératoire est une continuation des liquides intraveineux jusqu'à ce que le patient tolère l'alimentation par voie orale. L'alimentation peut commencer 4 à 8 heures après la récupération de l'anesthésie.[2][14]
En postopératoire, les nourrissons doivent être observés à l'hôpital pour des complications chirurgicales telles qu'une pyloromyotomie incomplète, une perforation muqueuse et des saignements.[2]
Les nourrissons peuvent être renvoyés à la maison lorsqu'ils sont hydratés et tolèrent bien les tétées.[2]
Étant donné les vomissements, il faut effectuer un suivi de l'équilibre acido-basique du patient.
Complications
Les complications potentielles de la SPHI sont les suivantes[2][15] :
- une insuffisance rénale aigüe pré-rénale
- une hyperbilirubinémie non conjuguée : le syndrome ictéropylorique
- une alcalose métabolique
- une déshydratation
- un choc hypovolémique.
Évolution
Le pronostic est excellent lorsqu'il est diagnostiqué tôt. La chirurgie est curative. Il y a une mortalité minime.
Jusqu'à 80% des patients continuent à avoir une forme plus légère de vomissements après la chirurgie. Le plus souvent, ces derniers correspondent à des régurgitations. Si les vomissements persistent plus de 5 jours après l'opération, des études radiologiques complémentaires, telle qu'une série gastro-intestinales supérieure, seraient indiquées.[2][3][15]
Prévention
À ce jour, il n'existe aucune recommandation pour la prévention de la SPHI.
Notes
- ↑ Une dispersion linéaire et étroite du produit de contraste au niveau de la lumière du système gastro-intestinal, ce qui démontre une sténose
- ↑ Deux stries de baryum au niveau du pylore
- ↑ Une projection du baryum qui traverse le pylore étroit, ressemblant un bec d'oiseau
- ↑ Protrusion du pylore hypertrophiée au niveau de l'antre gastrique
Références
- Cette page a été modifiée ou créée le 2020/11/07 à partir de Pyloric Stenosis (StatPearls / Pyloric Stenosis (2020/03/26)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/32310391 (livre).
- Cet article a été créé en partie ou en totalité le 2021/04/08 à partir de Chirurgie (application), créée par Dre Hélène Milot, Dr Olivier Mailloux et collaborateurs et partagé sous la licence CC-BY-SA 4.0 international
- ↑ 1,0 1,1 et 1,2 Roberto Galea et Edith Said, « Infantile Hypertrophic Pyloric Stenosis: An Epidemiological Review », Neonatal network: NN, vol. 37, no 4, , p. 197–204 (ISSN 1539-2880, PMID 30567916, DOI 10.1891/0730-0832.37.4.197, lire en ligne)
- ↑ 2,00 2,01 2,02 2,03 2,04 2,05 2,06 2,07 2,08 2,09 2,10 2,11 2,12 2,13 2,14 2,15 2,16 2,17 et 2,18 Karen Garfield et Shane R. Sergent, StatPearls, StatPearls Publishing, (PMID 32310391, lire en ligne)
- ↑ 3,0 3,1 3,2 3,3 3,4 3,5 3,6 3,7 3,8 et 3,9 (en) « Chirurgie », sur App Store (consulté le 23 février 2021)
- ↑ 4,0 et 4,1 Yael S. Rosenthal, Gabriel Chodick, Zachi Grossman et Varda Shalev, « The incidence of infantile hypertrophic pyloric stenosis and its association with folic acid supplementation during pregnancy: A nested case-control study », Journal of Pediatric Surgery, vol. 54, no 4, , p. 701–706 (ISSN 1531-5037, PMID 29884554, DOI 10.1016/j.jpedsurg.2018.05.005, lire en ligne)
- ↑ 5,0 5,1 5,2 5,3 5,4 5,5 et 5,6 « Pyloric stenosis - WikEM », sur wikem.org (consulté le 25 février 2021)
- ↑ 6,0 6,1 6,2 et 6,3 « Sténose du pylore », Wikipédia, (lire en ligne)
- ↑ 7,0 7,1 et 7,2 Philip Kaye, « Acquired pyloric stenosis resulting in hypokalaemic, hyperchloraemic normal anion gap metabolic acidosis. Persistent vomiting in an adult: cause and effect », BMJ case reports, vol. 2018, (ISSN 1757-790X, PMID 29348282, Central PMCID 5778228, DOI 10.1136/bcr-2017-222800, lire en ligne)
- ↑ Karen Garfield et Shane R. Sergent, StatPearls, StatPearls Publishing, (PMID 32310391, lire en ligne)
- ↑ (en) « String sign », Wikipedia, (lire en ligne)
- ↑ (en-US) Mohammad Taghi Niknejad, « Double track sign (pyloric stenosis) | Radiology Reference Article | Radiopaedia.org », sur Radiopaedia (consulté le 25 février 2021)
- ↑ (en-US) M. Venkatesh, « Beak sign (pyloric stenosis) | Radiology Reference Article | Radiopaedia.org », sur Radiopaedia (consulté le 25 février 2021)
- ↑ (en-US) Frank Gaillard, « Shoulder sign (pyloric stenosis) | Radiology Reference Article | Radiopaedia.org », sur Radiopaedia (consulté le 25 février 2021)
- ↑ 13,0 et 13,1 M. Bašković, B. Župančić, N. Lesjak et I. Vukasović, « [Hypertrophic Pyloric Stenosis - Five-Year Retrospective Analysis] », Acta Medica Croatica: Casopis Hravatske Akademije Medicinskih Znanosti, vol. 70, no 2, , p. 103–106 (ISSN 1330-0164, PMID 28722837, lire en ligne)
- ↑ Bo Wei et Hongbo Wei, « [Surgical treatment strategy for advanced gastric cancer] », Zhonghua Wei Chang Wai Ke Za Zhi = Chinese Journal of Gastrointestinal Surgery, vol. 21, no 10, , p. 1099–1102 (ISSN 1671-0274, PMID 30370506, lire en ligne)
- ↑ 15,0 et 15,1 Kaja Mørk, Hans Skari, Ole Schistad et Pål Aksel Næss, « [Surgical treatment of pyloric stenosis] », Tidsskrift for Den Norske Laegeforening: Tidsskrift for Praktisk Medicin, Ny Raekke, vol. 138, no 7, (ISSN 0807-7096, PMID 29663766, DOI 10.4045/tidsskr.17.0619, lire en ligne)
