Entérocolite nécrosante
| Maladie | |
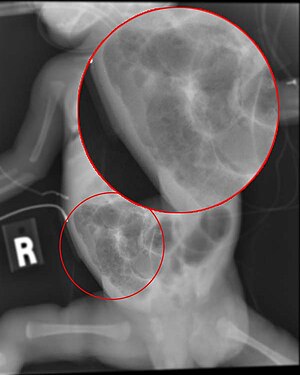
 Pneumatose intestinale chez un nouveau-né atteint d'entérocolite nécrosante | |
| Caractéristiques | |
|---|---|
| Signes | Diminution des bruits intestinaux, Sensibilité abdominale à la palpation, Érythème de l'abdomen, Diminution de la perfusion périphérique, Anses intestinales visibles, Empâtement abdominal, Asthénie , Cyanose , Distension abdominale |
| Symptômes |
Diminution de l'appétit, Baisse de l'activité, Intolérance à l'alimentation, Fatigue , Douleur abdominale, Diarrhée , Hématochézie , Vomissement |
| Diagnostic différentiel |
Septicémie, Maltraitance, Fistule trachéo-œsophagienne, Malrotation avec ou sans volvulus du mésogastre, Infection des voies urinaires, Iléus méconial, Invagination intestinale, Atrésie intestinale, Atrésie et sténose duodénale, Maladie de Hirschsprung, ... [+] |
| Informations | |
| Wikidata ID | Q10859678 |
| SNOMED CT ID | 206525008 |
| Spécialités | Chirurgie générale, pédiatrie |
|
| |
L'entérocolite nécrosante est une inflammation à degré variable de l'intestin conduisant à une nécrose de la muqueuse ou transmurale ; ceci favorise la perte d'intégrité de la paroi intestinale par la mort cellulaire et donc la translocation bactérienne, voire la péritonite [1][2][3]. Plus précisément, l'iléon distal ainsi que le côlon sont les parties généralement touchées. [4] Cette maladie potentiellement mortelle et d'origine multifactorielle touche presque exclusivement les nouveau-nés, particulièrement les bébés prématurés. [1][2][3]
Épidémiologie
L'entérocolite nécrosante est une maladie affectant les nouveau-nés et elle constitue l'urgence potentiellement mortelle la plus courante affectant le tractus gastro-intestinal des nourrissons dans l'unité de soins intensifs néonatals. Cette maladie survient généralement entre la deuxième et la troisième semaines de vie. L'incidence dans le monde varie entre 0,3 et 2,4 nourrissons pour 1000 naissances vivantes. Près de 70% de ces cas surviennent chez des bébés prématurés nés avant 36 semaines de gestation. L'entérocolite nécrosante affecte 2% à 5% de tous les nourrissons prématurés et elle est responsable de près de 8% de toutes les admissions en néonatalogie. [3]
Bien que l'entérocolite nécrosante survienne principalement chez les prématurés, elle a été documentée chez les nourrissons nés à terme. En effet, environ 15% des nourrissons sont à terme. [4] Chez les nourrissons nés à terme, l'incidence est d'environ 0,5 nouveaux-nés atteints de l'entérocolite nécrosante pour 1000 naissances vivantes. [5] Dans cette population, le début survient généralement au cours des premiers jours de la vie et il est généralement associé à un événement hypoxique comme une malformation cardiaque congénitale. [3]
Physiopathologie
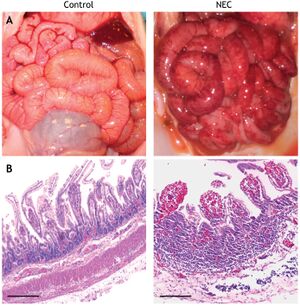
L'entérocolite nécrosante est causée par une invasion bactérienne dans la paroi intestinale. Cela conduit à une inflammation et à une destruction cellulaire de la paroi de l'intestin. Il y a une ischémie muqueuse , puis une nécrose et finalement une accumulation de gaz dans la sous-muqueuse (pneumatose intestinale).[6] Si elle n'est pas reconnue et traitée, une perforation intestinale peut survenir, entraînant un déversement du contenu intestinal dans la cavité abdominale, ce que l'on appelle une péritonite.
Le mécanisme spécifique et la cause de cette invasion bactérienne ne sont pas encore connus. Chez les nouveau-nés prématurés, l'immaturité du tractus gastro-intestinal jouerait un rôle dans la pathogenèse de l'entérocolite nécrosante. [3] En effet, la principale théorie est que cette immaturité associée à des insultes telles que des facteurs génétiques ou un débalancement de la flore intestinale pourrait initier une réponse immunitaire. Ensuite, la libération de cytokines augmenterait la perméabilité intestinale et permettrait la translocation de certaines bactéries. Alors, il en résulterait une inflammation et finalement une nécrose. L'immunité passive qui est moins développée chez le nouveau-né prématuré pourrait favoriser l'inflammation au sein de l'intestin. Toutefois, l'administration oral d'anticorps chez cette population n'a pas diminué le risque. [5]
Quoique l'iléon terminal et le colon proximal soient les segments les plus atteints, il est possible d'avoir une gangrène de l'estomac jusqu'au rectum que l'on appelle NEC totalis[6], pathologie habituellement fatale.
Présentation clinique
Facteurs de risque
Trois facteurs de risque principaux ont été retenus : [1][2][4][5]
- la prématurité (âge gestationnel plus petit ou faible poids à la naissance)
- la prématurité est le seul facteur de risque dont le lien de causalité avec l'entérocolite nécrosante est réellement démontré
- une alimentation préparée à haute force osmotique, soit un lait non-maternel
- des facteurs génétiques.
Il existe aussi d'autres facteurs de risque, qui explique notamment que l'on peut avoir un NEC chez un enfant à terme[6] :
- la trisomie 21
- la maladie de Hirschprung
- l'asphyxie périnatale
- le rotavirus
- le gastroschisis
- les cardiopathies congénitales.
Questionnaire
Les signes et symptômes de l'entérocolite nécrosante sont très variables, non spécifiques et subtils. [7] Typiquement, les symptômes débutent dans les premiers jours de vie en même temps que le début de l'alimentation. En effet, 80% de nourrissons affectés par l'entérocolite nécrosante sont âgés de moins de 1 mois. [4]
Les cliniciens doivent donc rester méfiants lorsqu'un nouveau-né se présente avec les signes et symptômes suivants : [1][2][3]
- une diminution de l'appétit et une intolérance à l'alimentation
- une baisse de l'activité
- de la fatigue
- des hématochézie
- de la diarrhée
- une douleur abdominale
- des vomissements.
Examen clinique

L'examen physique comprend : [3][5]
- la prise des signes vitaux
- bradycardie
- instabilité de la température
- l'examen de l'abdomen :
- l'examen des extrémités :
- l'observation des signes systémiques liés à une insuffisance respiratoire et à un état de choc distributif :
Examens paracliniques
Laboratoires
Les analyses de laboratoire ont une utilité limitée et elles ne sont pas spécifiques. [3]
Voici différents tests et leurs utilités : [3][4][5]
- une formule sanguine complète :
- le taux d'hémoglobine : il permet de vérifier la présence d'une anémie
- le nombre de globules blancs : une leucopénie laisserait suspecter la présence d'une septicémie
- la mesure de la protéine C réactive : elle permet d'objectiver la présence d'une inflammation
- des tests de coagulation : ils permettent de vérifier la présence d'une coagulation intravasculaire disséminée (CIVD)
- la mesure des gaz du sang artériel : elle permet de vérifier la présence d'une acidose métabolique
- un ionogramme sanguin : une hyponatrémie et un faible taux de bicarbonate sérique pourraient être présents
- la mesure de l'urée et de la créatinine
- des hémocultures : elles sont généralement négatives dans ce cas-ci
- la calprotectine fécale a une utilité limitée, mais elle permet d'objectiver une inflammation intestinale
- un test d'hydrogène respiratoire : ce dernier peut être positif, mais il est rarement effectué
- la mesure des lactates : elle permet de vérifier la présence d'un choc septique
- variation de la glycémie.
Radiographie simple de l'abdomen
La radiographie simple de l'abdomen est l'examen paraclinique le plus important afin de poser le diagnostic. Cette dernière comprend des vues en décubitus antérieur-postérieur et en décubitus latéral gauche (pour obtenir un niveau hydro-aérique). [3][4]
Les résultats qui orientent vers une entérocolite nécrosante sont les suivants : [3][4][5]
- une pneumatose intestinale (signe pathognomonique)
- ce signe serait le résultat de l'invasion bactérienne causant une augmentation de la production de gaz par les bactéries ainsi qu'une atteinte de la barrière intestinale
- des anses dilatées de l'intestin
- de l'air libre (visible surtout en décubitus latéral gauche)
- de l'aéroportie (signe de mauvais pronostic)
- de l'ascite.
Une radiographie abdominale est également un outil précieux pour suivre la progression de la maladie. Dans la plupart des cas, elle doit être répétée en série toutes les 6 heures jusqu'à ce que le traitement définitif ait eu lieu. [3]
Échographie
L'échographie adominale semblerait également être une bonne option afin de diagnostiquer l'entérocolite nécrosante, mais cette dernière est actuellement à l'étude. [4] Actuellement, elle n'est pas couramment utilisée afin de poser le diagnostic de cette pathologie. [5] Elle permet néanmoins d'évaluer la présence de liquide libre, l'épaisseur de la paroi des anses intestinales, l'échogénicité, la vascularisation et la présence d'une pneumatose intestinale ainsi que d'un pneumopéritoine. [4][5]
L'échographie pourrait être utile dans les cas cliniques suivants : [5]
- si le médecin a des inquiétudes face à une entérocolite nécrosante sans pneumatose à la radiographie abdominale
- si le nouveau-né n'a aucun symptôme, mais que les radiographies abdominales sont douteuses
- si le médecin désire opérer un nouveau-né qui a une pneumatose intestinale, mais peu d'éléments cliniques à l'histoire.
Spectroscopie dans l'infrarouge proche
Cet examen paraclinique permet d'évaluer la perfusion intestinale. Il a été démontré que la spectroscopie dans l'infrarouge proche pourrait être effectuée chez les nouveau-nés et elle serait sécuritaire. Toutefois, cet outil n'est pas utilisé actuellement chez les nourrissons et plusieurs études sont en cours. [5]
Histopathologie


Chez un patient atteint d'une entérocolite nécrosante, l'histopathologie révèle un tissu de la paroi intestinale avec une inflammation et une invasion bactérienne. Par conséquent, il sera également possible d'observer un ischémie, une nécrose, et finalement une perforation. [9] L'intestin peut avoir de l'air au sein de sa paroi (pneumatose) témoignant de la perte d'intégrité de sa muqueuse. Ceci peut entraîner par la suite une ischémie transmurale et une perforation qui mènera à une péritonite.
Diagnostic
La classification de Bell modifiée permet de définir si l'entérocolite nécrosante est suspectée (stade I) ou prouvée (stades II et III). [4] Cette dernière permet également de juger la gravité de la maladie. [5]
| Stade | Signes généraux | Signes au niveau intestinal | Signes radiologiques | |
|---|---|---|---|---|
| I
Suspectée |
A | Température instable, apnées, bradycardie | Résidus gastriques, légère distension abdominale, sang occulte dans les selles | Iléus et dilatation légers |
| B | Idem à IA | Idem à IA, selles sanglantes | Idem à IA | |
| II
Prouvée |
A | Idem à IA | Idem à IB, bruits intestinaux absents, abdomen tendu et douloureux | Iléus, pneunomatose intestinale |
| B | Idem à IA, acidose métabolique, légère thrombocytopénie | Idem à IB, bruits intestinaux absents, abdomen tendu et très douloureux, cellulite abdominale, masse dans le quadrant inférieur droit | Idem à IIA, aéroportie avec ou sans ascite | |
| III
Avancée |
A | Idem à IIB, acidose respiratoire, neutropénie, hypotension, coagulation intravasculaire disséminée | Idem à I et II, signes de péritonite, douleur marquée à l'abdomen, distension abdominale | Idem à IIB, ascite plus intense |
| B | Idem à IIIA | Idem à IIIA | Idem à IIB, pneumopéritoine | |
Cette classification a quelques limites : [5]
- le stade I est totalement non spécifique
- plusieurs diagnostics ayant la même présentation peuvent être évoqués à partir des critères
- par exemple, la classification de Bell ne permet pas de différencier l'entérocolite nécrosante d'une perforation intestinale spontanée.
Diagnostic différentiel
Avec la présentation potentiellement vague de l'entérocolite nécrosante, le diagnostic différentiel est large. [3]
Les symptômes d'entérocolite nécrosante dans cette population, y compris les nausées et les vomissements, peuvent être le résultat d'anomalies congénitales : [3][5]
- une sténose du pylore
- une atrésie duodénale ou atrésie iléale
- une fistule trachéo-œsophagienne
- une malrotation avec ou sans volvulus du mésogastre
- la maladie de Hirschsprung
- un iléus méconial.
Le diagnostic différentiel doit également comprendre diverses causes infectieuses : [3]
- une gastro-entérite
- une infection des voies urinaires
- une septicémie
- une méningite
- une pneumonie.
D'autres possibilités incluent : [3]
- une intussusception
- une torsion testiculaire
- la maltraitance des enfants, y compris des blessures intracrâniennes.
Traitement
Le traitement doit être débuté rapidement car l'évolution peut être fulgurante. Il n'y a pas de traitement définitif, on vise à corriger les paramètres, assurer l'alimentation autrement que par voie orale et mitiger les complications. On doit suivre étroitement le patient et faire des examens physiques et paracliniques (ex : bilan de coagulation, gaz artériel, radiographie abdominale) fréquemment. De plus, on doit isoler l'enfant pour éviter qu'une épidémie ne se propage au sein de l'unité néonatale[6].
Réanimation standard
Le traitement commence par une réanimation standard basée sur les signes vitaux du patient. Les voies respiratoires, la respiration et la circulation doivent être surveillées de près. Voici quelques actions à poser s'il y a une altération des signes vitaux : [3]
- En cas d'hypotension, la réanimation liquidienne (hypotension) est indiquée
- En cas d'insuffisance respiratoire, le patient peut avoir besoin d'une intubation endotrachéale (insuffisance respiratoire) et d'une ventilation mécanique (insuffisance respiratoire). Les directives de maintien de la vie pédiatrique avancé doivent être suivies pour la réanimation en cas de choc septique.
Interventions médicales
La première intervention en cas de suspicion d'entérocolite nécrosante est d'arrêter toute alimentation entérale et de ne rien administrer au patient par voie orale (nil per os). Voici les différentes procédures à effectuer : [3][4]
- Placer une sonde nasogastrique (suspicion d'entérocolite nécrosante) pour la décompression de l'estomac et des anses intestinales dilatées.
- Débuter des antibiotiques intraveineux (suspicion d'entérocolite nécrosante) avec une couverture à large spectre pour une durée de 10 à 14 jours. Le schéma antibiotique suggéré comprend l'ampicilline (suspicion d'entérocolite nécrosante), la gentamicine (suspicion d'entérocolite nécrosante) et la clindamycine (suspicion d'entérocolite nécrosante) ou le métronidazole (suspicion d'entérocolite nécrosante).
- Tant que le patient ne peut rien recevoir par voie orale, fournir une nutrition parentérale totale (suspicion d'entérocolite nécrosante) (hyperalimentation intra-veineuse).
Si ce traitement conservateur est efficace, les nourrissons peuvent reprendre l'alimentation entérale une fois que les signes d'infection ont disparu et que le transit semble repris. Dans certains cas, cela peut prendre de plusieurs jours à une semaine. En effet, généralement, ces interventions médicales ont un succès de 50% à 70% en 7 à 10 jours. [4] La présence de selles normales détermine le retour de la fonction intestinale. [3]
Interventions chirurgicales
Le chirurgien pédiatrique doit être consulté rapidement dès la suspicion du diagnostic. En effet, il pourra suivre étroitement l'évolution de la maladie et la réponse favorable ou non au traitement médical instauré. Le premier critère pour aller en salle d'opération est le pneumopéritoine prouvé à la radiographie. Or, seulement 50% des patients avec perforation ont ce signe paraclinique. Les autres critères chirurgicaux relatifs sont[4][6][10] :
- un traitement médical maximal sans amélioration
- une anse intestinale dilatée et fixe à la radiographie sériée
- échec de réponse au traitement médical
- une augmentation de l'acidose ou une diminution des globules blancs et des plaquettes
- une masse abdominale palpable
- érythème de la paroi abdominale.
Il existe 2 options chirurgicales : [3][4][11][10][12]
- la résection (un aggravation de leur état, une perforation intestinale, l'absence de réponse au traitement médical) par laparotomie est l'approche standard :
- la chirurgie est aussi conservatrice que possible
- elle consiste à enlever uniquement les parties de l'intestin incontestablement nécrotiques ou perforées dans une tentative de préserver le plus d'intestin possible
- la valve iléocæcale est idéalement préservée si possible
- une stomie de dérivation (nourrisson en état de choc ou qui a une péritonite importante) est généralement utilisée chez le nourrisson en état de choc ou qui a une péritonite importante et elle peut être renversée après la guérison (réanastomose)
- une réanastomose en 8 à 12 semaines (faire un lavement avant)
- la chirurgie est aussi conservatrice que possible
- les patients extrêmement petits (< 1000-1500 grammes) et malades pourraient ne pas être suffisamment stables pour tolérer une laparotomie, donc un drain péritonéal (patients extrêmement petits (< 1000-1500 grammes) et malades) et un lavage (patients extrêmement petits (< 1000-1500 grammes) et malades) seront effectués
- ces interventions sont réalisées sous anesthésie locale
- s'il n'y a pas d'amélioration après 48 heures, une laparotomie doit être effectuée (40%)
- il y a plusieurs facteurs de risque : prématurité, stade de Bell et comorbidités.
Des études randomisées[13][14] et une revue Cochrane[15] ont été faites pour déterminer la meilleure conduite chirurgicale, et aucune des deux options ne s'est montrée supérieure (décès, statut neurodéveloppemental). Une grande étude de cohorte multicentrique de 8935 patients a démontré que les deux tiers des patients avaient eu une laparotomie. Le taux de mortalité était de 30%, alors que le taux de décès de drainage péritonéal (éventuellement 46% a été converti en laparotomie) avait le même taux de mortalité. Seulement 27% des patients avec drainage péritonéal seul a survécu.[6]
Futurs traitements
Les traitements suivants sont actuellement à l'étude : [3][5][16][17][18][19][20]
- les probiotiques
- ces derniers sont déjà utilisés dans plusieurs régions
- ils permettent de modifier la composition en micro-organismes de la flore intestinale
- leur utilité serait de réduire le risque d'infections et de décès
- des agents bloquant la production de protoxyde d'azote
- des agents bloquant la production de monoxyde de carbone à faible dose.
Suivi
Après le début des interventions médicales, il est important de faire des analyses de laboratoire ainsi que des radiographies abdominales sériées à toutes les 8 à 12 heures. [4] Un examen physique de l'abdomen par la même équipe traitante est primordiale pour évaluer une dégradation dans la palpation.
Suite à une intervention chirurgicale pour une entérocolite nécrosante, les nourrissons doivent recevoir des antibiotiques par voie intraveineuse et une nutrition parentérale totale pendant au moins 2 semaines. Il peut y avoir une récidive de l'entérocolite nécrosante sur l'intestin résiduel et un suivi étroit est primordial. Les soins médicaux de routine, y compris la surveillance et la correction des anomalies électrolytiques ou de l'anémie, doivent également se poursuivre pendant cette période. Une assistance ventilatoire doit être fournie si nécessaire. [3] Le séjour à l'hôpital peut durer plusieurs mois. [5]
Complications
À mesure que l'entérocolite nécrosante progresse, elle peut entraîner une perforation intestinale. La perforation intestinale peut entraîner diverses complications telles que : [1][2][3]
- une péritonite
- une septicémie
- le décès.
Les complications suivantes peuvent résulter d'une hospitalisation et d'un traitement prolongés, ainsi que d'une intervention chirurgicale : [3][4][5]
- une insuffisance hépatique peut être causée par une nutrition parentérale totale prolongée
- une sténose et une obstruction peuvent être causées par les adhérences, une cicatrisation fibrotique dans une zone ischémique et des cicatrices postopératoires
- 10% des cas après le traitement ou la chirurgie
- le site le plus fréquent est l'angle splénique
- le traitement est chirurgical et il est diagnostiqué par un lavement hydrosoluble avant la fermeture de la stomie
- le syndrome de l'intestin court (la chirurgie est la première cause)
- l'insuffisance intestinale
- les carences nutritionnelles
- les retards de croissance et retards de développement
- 2 fois plus de risque chez les patients traités avec une chirurgie
- il est important de suivre le développement neurologique (échelle Hayley ou IRM fonctionnelle)
- le décès (50% des enfants qui devront être opérés décèdent de la maladie).
Évolution
Le pronostic de l'entérocolite nécrosante dépend de la gravité de la maladie au moment où elle est reconnue et où le traitement est commencé. [3] La mortalité est similaire chez les nourrissons nés à terme et ceux prématurés. La mortalité globale varie de 20% pour le traitement médical jusqu'à 50% pour le traitement chirurgical. [5] Cependant, pour les nourrissons atteints d'entérocolite nécrosante avancée, soit lorsqu'il y a une destruction complète de la paroi intestinale qui entraîne une perforation et une péritonite, la mortalité approche les 100%. [3]
Le taux de récidive est d'environ 10% et les facteurs de risque sont un faible poids à la naissance et la présence d'anomalies congénitales. [5]
Prévention
Chez les nourrissons de très faible poids à la naissance, les nourrissons allaités ont une incidence plus faible d'entérocolite nécrosante. Les mères de ces nourrissons devraient être informées des avantages de l'allaitement, en particulier en ce qui concerne sa relation avec le développement de l'entérocolite nécrosante. [3] Le lait maternel de la mère ou de la banque de lait maternel peut être administré par voie entérale pour diminuer le risque de développer l'entérocolite. Ce dernier contient différentes protéines qui ont des effets bénéfiques. En effet, certaines ont des effets anti-microbiens ainsi qu'anti-inflammatoires et d'autres permettent la regénération des cellules. Par exemple, la caséine empêche les bactéries d'adhérer à l'épithélium et elle stimule la production de mucine qui est contenue dans dans le mucus. [5]
Les suppléments de lactoferrine semblent avoir des propriétés anti-microbiennes qui permettraient de diminuer les risques d'entérocolite nécrosante, de septicémie et de décès. Afin d'obtenir des résultats optimaux, les suppléments devraient être commencés dans les trois jours suivant l'accouchement. D'autres études sur le sujet sont nécessaires. [5]
Les conditions prénatales et postnatales qui provoquent une diminution du flux sanguin intestinal ont été impliquées dans le risque accru de développement d'entérocolite nécrosante. Par exemple, des conditions provoquant une insuffisance placentaire pendant la période prénatale, telles que l'hypertension, la prééclampsie et la consommation de cocaïne, peuvent diminuer le flux sanguin intestinal du nourrisson. Pour les nourrissons nés dans ces conditions, une alimentation entérale prudente est justifiée. Les affections postnatales provoquant une diminution similaire du flux sanguin splanchnique et donc un risque accru d'entérocolite nécrosante, comprennent une persistance du canal artériel, d'autres maladies cardiaques ou une hypotension générale et une atteinte cardiovasculaire. [1][2][3] L'utilisation d'IPP ou d'antihistaminique dans la période post-natale, de même qe les antibiotiques prophylactiques, sont déconseillés car ils peuvent augmenter le risque de NEC[6].
Références
- Cette page a été modifiée ou créée le 2020/11/07 à partir de Necrotizing Enterocolitis (StatPearls / Necrotizing Enterocolitis (2020/08/13)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/30020729 (livre).
- Cet article a été créé en partie ou en totalité le 2020/11/19 à partir de Chirurgie (application), créée par Dre Hélène Milot, Dr Olivier Mailloux et collaborateurs et partagé sous la licence CC-BY-SA 4.0 international
- ↑ 1,0 1,1 1,2 1,3 1,4 et 1,5 Alain Cuna, Lovya George et Venkatesh Sampath, « Genetic predisposition to necrotizing enterocolitis in premature infants: Current knowledge, challenges, and future directions », Seminars in Fetal & Neonatal Medicine, vol. 23, no 6, , p. 387–393 (ISSN 1878-0946, PMID 30292709, Central PMCID 6626706, DOI 10.1016/j.siny.2018.08.006, lire en ligne)
- ↑ 2,0 2,1 2,2 2,3 2,4 et 2,5 B. Afzal, V. Elberson, C. McLaughlin et V. H. S. Kumar, « Early onset necrotizing enterocolitis (NEC) in premature twins », Journal of Neonatal-Perinatal Medicine, vol. 10, no 1, , p. 109–112 (ISSN 1878-4429, PMID 28304317, DOI 10.3233/NPM-1616, lire en ligne)
- ↑ 3,00 3,01 3,02 3,03 3,04 3,05 3,06 3,07 3,08 3,09 3,10 3,11 3,12 3,13 3,14 3,15 3,16 3,17 3,18 3,19 3,20 3,21 3,22 3,23 3,24 3,25 3,26 et 3,27 Jacob G. Ginglen et Nikolai Butki, StatPearls, StatPearls Publishing, (PMID 30020729, lire en ligne)
- ↑ 4,00 4,01 4,02 4,03 4,04 4,05 4,06 4,07 4,08 4,09 4,10 4,11 4,12 4,13 4,14 4,15 et 4,16 (en) « Chirurgie », sur App Store (consulté le 20 décembre 2020)
- ↑ 5,00 5,01 5,02 5,03 5,04 5,05 5,06 5,07 5,08 5,09 5,10 5,11 5,12 5,13 5,14 5,15 5,16 5,17 5,18 et 5,19 (en) Holcomb, George W., III,, Murphy, J. Patrick,, St. Peter, Shawn D., et Gatti, John M.,, Holcomb and Ashcraft's pediatric surgery, 1316 p. (ISBN 978-0-323-54976-9, 0-323-54976-4 et 978-0-323-54977-6, OCLC 1107667324, lire en ligne), p. 536-550
- ↑ 6,0 6,1 6,2 6,3 6,4 6,5 et 6,6 Kliegman, Robert,, Stanton, Bonita,, St. Geme, Joseph W., III, et Schor, Nina Felice,, Nelson textbook of pediatrics (ISBN 978-0-323-56888-3, 0-323-56888-2 et 978-0-323-52950-1, OCLC 1096283151, lire en ligne)
- ↑ Sheila M. Gephart, Corrine Hanson, Christine M. Wetzel et Michelle Fleiner, « NEC-zero recommendations from scoping review of evidence to prevent and foster timely recognition of necrotizing enterocolitis », Maternal Health, Neonatology and Perinatology, vol. 3, , p. 23 (ISSN 2054-958X, PMID 29270303, Central PMCID 5733736, DOI 10.1186/s40748-017-0062-0, lire en ligne)
- ↑ RadsWiki, necrotizing enterocolitis, (lire en ligne)
- ↑ S. Rugolotto, M. Gruber, P. D. Solano et L. Chini, « Necrotizing enterocolitis in a 850 gram infant receiving sorbitol-free sodium polystyrene sulfonate (Kayexalate): clinical and histopathologic findings », Journal of Perinatology: Official Journal of the California Perinatal Association, vol. 27, no 4, , p. 247–249 (ISSN 0743-8346, PMID 17377608, DOI 10.1038/sj.jp.7211677, lire en ligne)
- ↑ 10,0 et 10,1 Peter J. Fagenholz et Marc A. de Moya, « Acute inflammatory surgical disease », The Surgical Clinics of North America, vol. 94, no 1, , p. 1–30 (ISSN 1558-3171, PMID 24267493, DOI 10.1016/j.suc.2013.10.008, lire en ligne)
- ↑ Qiankun Geng, Yongming Wang, Lei Li et Chunbao Guo, « Early postoperative outcomes of surgery for intestinal perforation in NEC based on intestinal location of disease », Medicine, vol. 97, no 39, , e12234 (ISSN 1536-5964, PMID 30278493, Central PMCID 6181543, DOI 10.1097/MD.0000000000012234, lire en ligne)
- ↑ D. P. Craven, J. S. Fowler et M. E. Foster, « Management of a neonate with necrotizing entero-colitis and eight prolapsed stomas in a dehisced wound », Journal of Wound, Ostomy, and Continence Nursing: Official Publication of The Wound, Ostomy and Continence Nurses Society, vol. 26, no 4, , p. 214–220 (ISSN 1071-5754, PMID 10476178, DOI 10.1016/s1071-5754(99)90046-3, lire en ligne)
- ↑ (en) R. Lawrence Moss, Reed A. Dimmitt, Douglas C. Barnhart et Karl G. Sylvester, « Laparotomy versus Peritoneal Drainage for Necrotizing Enterocolitis and Perforation », New England Journal of Medicine, vol. 354, no 21, , p. 2225–2234 (ISSN 0028-4793 et 1533-4406, DOI 10.1056/NEJMoa054605, lire en ligne)
- ↑ (en) Clare M. Rees, Simon Eaton, Edward M. Kiely et Angie M. Wade, « Peritoneal Drainage or Laparotomy for Neonatal Bowel Perforation?: A Randomized Controlled Trial », Annals of Surgery, vol. 248, no 1, , p. 44–51 (ISSN 0003-4932, DOI 10.1097/SLA.0b013e318176bf81, lire en ligne)
- ↑ (en) « Peritoneal drainage versus laparotomy as initial surgical treatment for perforated necrotizing enterocolitis or spontaneous intestinal perforation in preterm low birth weight infants », sur www.cochrane.org (consulté le 24 janvier 2021)
- ↑ Thad Wilkins et Jacqueline Sequoia, « Probiotics for Gastrointestinal Conditions: A Summary of the Evidence », American Family Physician, vol. 96, no 3, , p. 170–178 (ISSN 1532-0650, PMID 28762696, lire en ligne)
- ↑ Peter A. Bron, Michiel Kleerebezem, Robert-Jan Brummer et Patrice D. Cani, « Can probiotics modulate human disease by impacting intestinal barrier function? », The British Journal of Nutrition, vol. 117, no 1, , p. 93–107 (ISSN 1475-2662, PMID 28102115, Central PMCID 5297585, DOI 10.1017/S0007114516004037, lire en ligne)
- ↑ Sylvia Cruchet, Raquel Furnes, Aldo Maruy et Eduardo Hebel, « The use of probiotics in pediatric gastroenterology: a review of the literature and recommendations by Latin-American experts », Paediatric Drugs, vol. 17, no 3, , p. 199–216 (ISSN 1179-2019, PMID 25799959, Central PMCID 4454830, DOI 10.1007/s40272-015-0124-6, lire en ligne)
- ↑ James Versalovic, « The human microbiome and probiotics: implications for pediatrics », Annals of Nutrition & Metabolism, vol. 63 Suppl 2, , p. 42–52 (ISSN 1421-9697, PMID 24217035, DOI 10.1159/000354899, lire en ligne)
- ↑ Katarzyna Dylag, Magdalena Hubalewska-Mazgaj, Marcin Surmiak et Jakub Szmyd, « Probiotics in the mechanism of protection against gut inflammation and therapy of gastrointestinal disorders », Current Pharmaceutical Design, vol. 20, no 7, , p. 1149–1155 (ISSN 1873-4286, PMID 23755726, DOI 10.2174/13816128113199990422, lire en ligne)
