« Gastrectomie pariétale » : différence entre les versions
(→Suivi) |
|||
| (36 versions intermédiaires par 4 utilisateurs non affichées) | |||
| Ligne 1 : | Ligne 1 : | ||
{{Information procédure | {{Information procédure | ||
| image = Gastrectomie partielle - application d’une deuxième cartouche d’autosuture.jpeg | |||
| image = | | spécialités = Chirurgie générale, endocrinologie, gastro-entérologie, chirurgie bariatrique | ||
| spécialités = Chirurgie générale, endocrinologie, gastro-entérologie | |||
| systèmes = Digestif | | systèmes = Digestif | ||
| vidéo = | | vidéo = | ||
| wikidata_id = | | wikidata_id = | ||
|autres_noms=gastrectomie verticale, gastrectomie en manchon}}La gastrectomie pariétale (ou verticale) est une intervention bariatrique qui consiste à retirer de façon longiligne le fundus et les portions latérales gauches du corps et de l'antre gastrique ; laissant un volume résiduel d'environ 100 mL le long de la petite courbure gastrique <ref name=":1">{{Citation d'un ouvrage|nom1=Reavis, Kevin M.,|nom2=Barrett, Allison M.,|nom3=Kroh, Matthew,|nom4=Society of American Gastrointestinal Endoscopic Surgeons,|titre=The SAGES manual of bariatric surgery|isbn=978-3-319-71282-6|isbn2=3-319-71282-9|oclc=1031089500|lire en ligne=https://www.worldcat.org/oclc/1031089500|consulté le=2020-11-11}}</ref>. Ainsi, il s'agit d'une intervention bariatrique | | autres_noms = gastrectomie verticale, gastrectomie en manchon, sleeve gastrectomy | ||
| version_de_classe = 2 | |||
}}La '''gastrectomie pariétale''' (ou verticale) est une [[intervention bariatrique]] qui consiste à retirer de façon longiligne le fundus et les portions latérales gauches du corps et de l'antre gastrique ; laissant un volume résiduel d'environ 100 mL le long de la petite courbure gastrique <ref name=":1">{{Citation d'un ouvrage|nom1=Reavis, Kevin M.,|nom2=Barrett, Allison M.,|nom3=Kroh, Matthew,|nom4=Society of American Gastrointestinal Endoscopic Surgeons,|titre=The SAGES manual of bariatric surgery|isbn=978-3-319-71282-6|isbn2=3-319-71282-9|oclc=1031089500|lire en ligne=https://www.worldcat.org/oclc/1031089500|consulté le=2020-11-11}}</ref>. Ainsi, il s'agit d'une intervention bariatrique dite '''restrictive''', mais également '''métabolique''' par les changements neurohormonaux imputables au retrait des cellules pariétales gastriques et une rapidité du transit accrue avec un feedback négatif au niveau duodénal.<ref name=":1" />. La perte de poids attendue est d'environ 25%.<ref name=":1" /> | |||
== Avantages et limitations == | |||
Globalement, on retient les '''avantages''' suivants pour la gastrectomie verticale<ref name=":1" /> : | Globalement, on retient les '''avantages''' suivants pour la gastrectomie verticale<ref name=":1" /> : | ||
* intervention de courte durée | * intervention de courte durée | ||
* faible morbidité | * faible morbidité<ref group="note">Par rapport à d'autres chirurgies de perte de poids, la gastrectomie pariétale est techniquement plus facile avec relativement moins de morbidité et est donc devenue la chirurgie de perte de poids la plus courante pratiquée aux États-Unis. Actuellement, il y a 3 gastrectomies pour un Y-de-Roux aux États-Unis. </ref><ref name=":0">{{Citation d'un ouvrage|prénom1=Kevin|nom1=Seeras|prénom2=Senthilkumar|nom2=Sankararaman|prénom3=Peter P.|nom3=Lopez|titre=StatPearls|éditeur=StatPearls Publishing|date=2020|pmid=30085577|lire en ligne=http://www.ncbi.nlm.nih.gov/books/NBK519035/|consulté le=2020-10-26}}</ref> | ||
** moins de déficit nutritionnel et vitaminiques à long terme | |||
** moins de complication chirurgicale | |||
* profil d'effets secondaires faible | * profil d'effets secondaires faible | ||
* bonne qualité de vie | * bonne qualité de vie | ||
| Ligne 22 : | Ligne 24 : | ||
== Indications == | == Indications == | ||
Les indications de la gastrectomie pariétale sont celles de la [[chirurgie bariatrique]] en général. | |||
Les indications de la gastrectomie | {{Inclure une section d'une page|page=Chirurgie bariatrique|section=Indications}} | ||
== Contre-indications == | == Contre-indications == | ||
Les contre-indications absolues | Les indications, ainsi que les contre-indications absolues et relatives de la gastrectomie pariétales sont les critères usuels d'une [[Chirurgie bariatrique|candidature bariatrique]]'''.''' | ||
{{Inclure une section d'une page|page=Chirurgie bariatrique|section=Contre-indications}} | |||
== Évaluation == | == Évaluation == | ||
{{Page principale|lien=Chirurgie bariatrique#Évaluation}} | |||
L'évaluation bariatrique est multidisciplinaire. La sélection des patients a été établie pour minimiser les complications chirurgicales et maximiser les bénéfices d'une ressource limitée. L'évaluation devra donc statuer sur la santé mentale, médicale et nutritionnelle, ainsi qu'optimiser les comorbidités pour diminuer les complications chirurgicales. | |||
== Anatomie == | == Anatomie == | ||
La gastrectomie pariétale est une intervention bariatrique qui consiste à retirer de façon longiligne le fundus de l'estomac et les portions latérales gauches du corps et de l'antre gastrique: | |||
[[Fichier:Stomach-fr.svg|vignette]] | |||
L'estomac est divisé en cardia (juste distal à la jonction gastro-oesophagienne), le fundus (attenant au diaphragme gauche et partageant les vaisseaux courts de la rate), le corps, l'antre et le pylore. La petite courbure se trouve sous les segments médiaux du foie et comprend l'incisura angularis qui peut être identifiée comme la jonction des axes vertical et horizontal de la petite courbure. La grande courbure est le long bord latéral gauche de l'estomac et supporte l'épiploon. Le bord gauche de l'œsophage intra-abdominal et le fundus se rencontrent à un angle aigu appelé «angle de His». Postérieurement à l'estomac se trouve l'arrière-cavité qui est un espace potentiel antérieur au pancréas et bordé par l'artère splénique, la rate, le rein gauche et le mésocôlon transverse. | |||
=== Ligaments | === Ligaments === | ||
* Ligament gastro-hépatique | Les ligaments de l'estomac sont les suivants: | ||
* Ligament gastrophrénique | * Ligament gastro-hépatique: petite courbure vers le bord médial du foie, contient les artères gastriques gauche et droite. Peut contenir une artère hépatique gauche récurrente. | ||
* Ligament gastrosplénique | * Ligament gastrophrénique : relie le fundus vers l'hémidiaphragme gauche. | ||
* Ligament gastro-colique | * Ligament gastrosplénique : grande courbure de la rate et contient les vaisseaux gastriques courts. | ||
* Ligament gastro-colique : estomac inférieur au côlon transverse, considéré comme faisant partie du grand épiploon et contenant les vaisseaux gastro-épiploïques | |||
=== Vascularisation | === Vascularisation === | ||
[[ | [[Fichier:Approvisionnement sanguin de l'estomac.svg|vignette|Approvisionnement sanguin de l'estomac]] | ||
Le tronc coeliaque a trois branches : artères gastrique gauche, hépatique commune et splénique. L'artère gastrique gauche longe la petite courbure supérieure et s'anastomose avec l'artère gastrique droite. L'artère gastrique gauche est le principal apport sanguin à l'estomac après une gastrectomie verticale et elle dégage de nombreuses branches postérieures qui doivent rester ininterrompues pendant la dissection de la surface postérieure de l'estomac. L'artère hépatique commune donne l'artère gastroduodénale qui passe derrière la première partie du duodénum. L'artère gastrique droite est une branche de l'artère hépatique propre et rejoint l'artère gastrique gauche le long de la petite courbure. L'artère gastro-épiploïque droite se branche ensuite à partir de l'artère gastroduodénale et passe dans le ligament gastrocolique (épiploon) le long de la grande courbure pour rejoindre l'artère gastroépiploïque gauche qui est une branche de l'artère splénique courant le long de la plus grande courbure de latéral à médial. L'artère splénique dégage également 3 à 5 artères gastriques courtes circulant dans le ligament gastrosplénique vers le fundus gastrique. | |||
== | == Préparation == | ||
D'abord, tel que discuté ci-haut, plusieurs patients bénéficieront d'un régime faible en calories et élevés en protéines afin de diminuer le volume hépatique pour favoriser une exposition de l'estomac (il s'agit d'une diète liquide uniformisée sur 10 à 14 jours). Le patient recevra une antibioprophylaxie (ex. : céfazoline 2 ou 3g) pondérée selon son poids. Finalement, le patient doit recevoir une thromboprophylaxie ajustée à son poids sous forme d'héparine sous-cutanée et on lui installera des jambières à compression séquentielle. | |||
Le patient sera placé en décubitus dorsal. Selon la préférence du chirurgien, il sera les jambes fermées ou écartées (''split-leg''). L'opérateur principal sera à droite ou entre les jambes. L'assistant se placera à gauche du patient. | |||
Après l'induction anesthésique, on placera le patient en Fowler (Tredelenburg inversé). Une sonde orogastrique pour décomprimée l'estomac sera installée puis retirée avant la manipulation de celui-ci par le chirurgien. | |||
=== Équipement === | === Équipement === | ||
L'équipement laparoscopique de base est nécessaire pour cette opération qui comprendra l'insufflation avec du gaz | L'équipement laparoscopique de base est nécessaire pour cette opération qui comprendra l'insufflation avec du gaz CO<sub>2</sub>, des champs chirurgicaux, des moniteurs, des instruments laparoscopiques, l'électrocautérisation et des trocarts. Contrairement aux procédures laparoscopiques conventionnelles, avec les patients bariatriques, vous aurez besoin de trocarts plus longs ainsi que d'instruments laparoscopiques plus longs pour s'adapter à la paroi abdominale plus épaisse.<ref name=":0" /> | ||
Sont également requis: <ref name=":0" /> | Sont également requis: <ref name=":0" /> | ||
* | * 3 trocarts de 5 mm pour les instruments et l'écarteur hépatique, 1 trocart Optiview pour le laparoscope (10-12 mm), 1 ou 2 trocarts de 12 mm pour l'agrafeuse | ||
* | * 1 aiguille de Veress standard ou extra-longue | ||
* | * écarteur hépatique (ex. : écarteur de Nathanson) | ||
* | * laparoscope 30 degrés, lentille 5 ou 10 mm | ||
* | * agrafeuse linéaire endoscopique avec différentes épaisseurs de cartouche (en moyenne 5 à 6 applications) | ||
* | * bougie de 34 Fr (selon la préférence du chirurgien) | ||
* | * endoscope flexible au besoin | ||
* dispositif d'énergie laparoscopique (appareil d'électrochirurgie pour sceller et couper les tissus) | |||
* porte-aiguille laparoscopique | |||
* clippeuse vasculaire | |||
* sutures à peau | |||
* un sac endoscopique pour l'extraction de l'estomac. | |||
== Technique == | == Technique == | ||
Il existe de nombreuses façons d'effectuer une gastrectomie laparoscopique en manchon, une procédure type est présentée ici. | |||
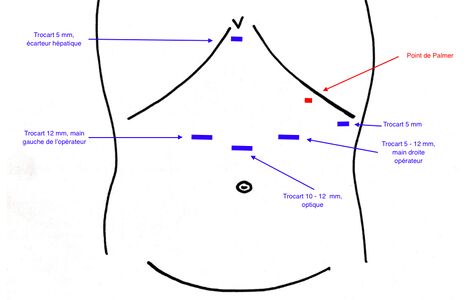
Il existe de nombreuses façons d'effectuer une gastrectomie laparoscopique en manchon, | [[Fichier:Trocartssleeve.jpg|vignette|469x469px|Exemples de positionnement des trocarts laparoscopiques pour une gastrectomie pariétale]] | ||
=== Entrée et mise en place === | |||
L'entrée dans l'abdomen commence dans le quadrant supérieur gauche ('''point de Palmer''') et la technique utilisée est à la discrétion du chirurgien. | |||
Habituellement: | |||
# L'aiguille de '''Veress''' est utilisée puis le trocart Optiview est introduit avec le laparoscope | |||
# L'abdomen est insufflé à une pression de 15 mmHg et l'abdomen est exploré visuellement avec un laparoscope. Un pneumopéritoine de 12 mmHg a été proposé dans les protocoles ERAS, mais le patient doit être fortement curarisé. | |||
Le placements des trocarts sera le suivant: | |||
* trocart de 5 mm dans le quadrant supérieur gauche, ligne axillaire antérieure (port de l'assistant) | |||
* trocart de 5 ou 12 mm dans la ligne médio-claviculaire supérieure gauche pour la main droite du chirurgien | |||
* trocart de 5 ou 12 mm dans la ligne médio-claviculaire paramédiane supérieure droite pour la main gauche du chirurgien | |||
* trocart de 12 mm placé au niveau ou juste au-dessus de l'ombilic (habituellement une longueur de main sous l'apophyse xyphoïde) pour la caméra | |||
* écarteur de foie placé dans la zone sous-xiphoïde via un trocart 5 mm (l'écarteur Nathanson est habituellement utilisé) | |||
* une fois tous les ports insérés et le foie rétracté, le patient est placé en Trendelenburg inversé, le patient est en ''split-leg'' et donc le chirurgien est entre les jambes du patient, l'assistant est à gauche de celui-ci. | |||
=== Mobilisation de la grande courbure === | |||
La dissection commence par la division de '''l'[[épiploon]]''' à quelques centimètres en amont du [[pylore]]. On divise l'épiploon en tentant de préserver le plus possible sa vascularisation en utilisant un appareil d'électrochirurgie. On monte le long de la grande courbure jusqu'à rencontrer les vaisseaux courts du pôle supérieur de la [[rate]]. D'ailleurs, celui-ci peut devenir ischémique (bleuté) en cours de procédure car la rate a une circulation terminale. La dissection est poursuivie pour diviser complètement le ligament gastrophrénique jusqu'à mobiliser l'''<nowiki/>'angle de His'''. On doit bien voir le '''pilier gauche''' du diaphragme. | |||
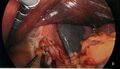
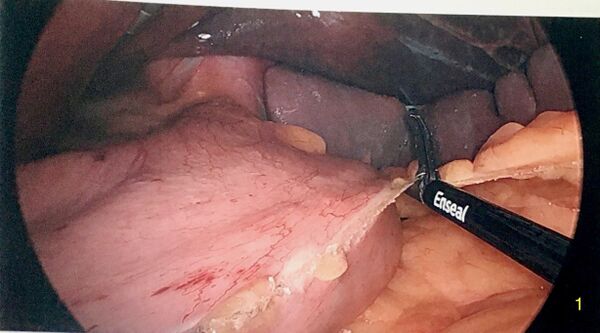
[[Fichier:Gastrectomie pariétale - mobilisation de la grande courbure (photo).jpg|centré|vignette|600x600px|Dissection de la grande courbure en décrochant l’épiploon avec un appareil d’électrochirurgie. Foie surélevé par l’écarteur Nathason. Rate lobulée au fond à droite de l’image.]] | |||
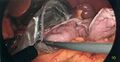
[[Fichier:Gastrectomie partielle - ligature du ligament gastrosplénique.jpg|centré|vignette|600x600px|Ligature du ligament gastrosplénique contenant les vaisseaux courts.]] | |||
=== Identification et réparation d'une hernie hiatale === | |||
Après avoir exposé le pilier gauche du diaphragme, on doit évaluer s'il y a une hernie hiatale. Si tel est le cas, il est recommandé d'en réduire le contenu et le sac et de réparer la hernie avec un rapprochement des piliers. On utilise des sutures en X interrompues en arrière de l'oesophage. | |||
L'épiploon | === Mobilisation postérieure === | ||
L'épiploon étant séparé complètement de la grande courbure, on accède à l'arrière-cavité des épiploons. L'estomac est soulevé antérieurement pour exposer sa paroi postérieure. Toutes les '''adhérences''' doivent être défaites, en prenant soin de ne pas transmettre de chaleur de l'appareil d'électrochirurgie sur la capsule pancréatique. On doit visualiser la petite courbure. La vascularisation de celle-ci servira de point de repère pour l'application des recharges de l'agrafeuse. | |||
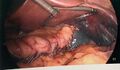
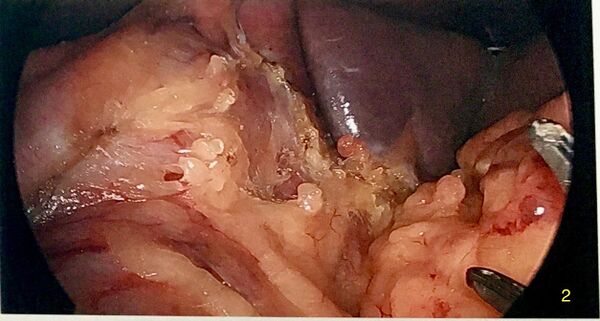
[[Fichier:Gastrectomie partielle - mobilisation postérieure.jpg|centré|vignette|600x600px|Mobilisation postérieure de l’estomac en divisant les adhérences dans l’arrière-cavité.]] | |||
=== Placement de la bougie === | |||
Une bougie orogastrique de 32 à 40 Fr est placée sous visualisation laparoscopique. L'anesthésiste pousse la bougie jusqu'au pylore de sorte que l'on mette légèrement en tension la zone pré-pylorique où les dernières attaches épiploïques ont été divisées. | |||
*'''Taille de la bougie''' : la bougie sert de guide pour l'application des cartouches d'autosuture pour créer un manchon autour de la bougie. Une bougie trop petite créé une gastrectomie trop étroite et donc augmente la résistance et la pression intra-luminale. Ceci augmenterait le risque de fuite. A contrario, une bougie trop large créerait un réservoir trop flasque et la perte de poids ne serait pas optimale. Lors de la cinquième conférence internationale, il a été recommandé d'utiliser une grande bougie (la '''médiane était de 36 Fr''').<ref name=":11">{{Citation d'un article|prénom1=Michel|nom1=Gagner|prénom2=Colleen|nom2=Hutchinson|prénom3=Raul|nom3=Rosenthal|titre=Fifth International Consensus Conference: current status of sleeve gastrectomy|périodique=Surgery for Obesity and Related Diseases: Official Journal of the American Society for Bariatric Surgery|volume=12|numéro=4|date=2016-05|issn=1878-7533|pmid=27178618|doi=10.1016/j.soard.2016.01.022|lire en ligne=https://pubmed.ncbi.nlm.nih.gov/27178618/|consulté le=2020-11-26|pages=750–756}}</ref> | |||
*'''Longueur du pylore''' : il y a débat sur le point de départ de la première charge d'agrafes en terme de distance du pylore. Des distances de 2 à 6 cm sont pratiquées aujourd'hui et la quantité d'antre retenu détermine sa signification clinique. Avec une distance de 2 cm, plus d'antre est réséqué et le reste gastrique est relativement plus petit. Ceci, en théorie, produira une augmentation de la perte de poids excessive mais peut conduire à plus de complications de l'augmentation de la pression intragastrique distale. Des études comparant une distance de 2 cm et une distance de 4 à 6 cm ont montré des résultats mitigés. L'un a montré des résultats égaux en considérant la perte de poids et les complications<ref name=":8">{{Citation d'un article|prénom1=Ahmed|nom1=ElGeidie|prénom2=Mohamed|nom2=ElHemaly|prénom3=Emad|nom3=Hamdy|prénom4=Mohamed|nom4=El Sorogy|titre=The effect of residual gastric antrum size on the outcome of laparoscopic sleeve gastrectomy: a prospective randomized trial|périodique=Surgery for Obesity and Related Diseases: Official Journal of the American Society for Bariatric Surgery|volume=11|numéro=5|date=2015-09|issn=1878-7533|pmid=25638594|doi=10.1016/j.soard.2014.12.025|lire en ligne=https://pubmed.ncbi.nlm.nih.gov/25638594/|consulté le=2020-11-27|pages=997–1003}}</ref>, et l'autre a démontré une perte de poids accrue sans augmentation des complications pour la longueur de 2 cm.<ref name=":9">{{Citation d'un article|prénom1=Emad|nom1=Abdallah|prénom2=Ayman|nom2=El Nakeeb|prénom3=Tamer|nom3=Youssef|prénom4=Tamer|nom4=Yousef|titre=Impact of extent of antral resection on surgical outcomes of sleeve gastrectomy for morbid obesity (a prospective randomized study)|périodique=Obesity Surgery|volume=24|numéro=10|date=2014-10|issn=1708-0428|pmid=24728866|doi=10.1007/s11695-014-1242-x|lire en ligne=https://pubmed.ncbi.nlm.nih.gov/24728866/|consulté le=2020-11-27|pages=1587–1594}}</ref> L'opinion de la conférence internationale était de commencer la résection à '''au moins 3 cm du pylore'''.<ref name=":0" /> | |||
* | * | ||
=== Résection gastrique === | |||
Une agrafeuse endoscopique de 60 mm de long est utilisée pour suturer et trancher l'estomac dans son axe vertical. La mise à feu est commencée à environ 5 cm proximal au pylore le long de la bougie et avec un angle parallèle à la petite courbure. Il faut s'assurer que l'agrafeuse englobe des longueurs égales de l'estomac antérieur et postérieur pour éviter la «spirale» du manchon - la mise en tension de la grande courbure par l'assistant est essentielle pour ce faire. Les lignes d'agrafes sont tirées séquentiellement le long de la bougie vers l'angle de His. En moyenne, l'épaisseur de paroi de l'antre, du corps et des fonds est respectivement de 3,1, 2,4 et 1,7 mm<ref name=":13">{{Citation d'un article|prénom1=Hazem|nom1=Elariny|prénom2=Hamilton|nom2=González|prénom3=Bingshi|nom3=Wang|titre=Tissue thickness of human stomach measured on excised gastric specimens from obese patients|périodique=Surgical Technology International|volume=14|date=2005|issn=1090-3941|pmid=16525963|lire en ligne=https://pubmed.ncbi.nlm.nih.gov/16525963/|consulté le=2020-11-27|pages=119–124}}</ref>. Le but est d'utiliser une agrafeuse avec des agrafes suffisamment hautes pour accueillir l'antre le plus épais par opposition au fundus plus fin. Certains ont préconisé des résultats supérieurs en utilisant une hauteur d'agrafe plus haute en distal et une hauteur d'agrafe plus courte en proximal à l'approche du fundus<ref name=":14">{{Citation d'un article|prénom1=David L.|nom1=Warner|prénom2=Kent C.|nom2=Sasse|titre=Technical Details of Laparoscopic Sleeve Gastrectomy Leading to Lowered Leak Rate: Discussion of 1070 Consecutive Cases|périodique=Minimally Invasive Surgery|volume=2017|date=2017|issn=2090-1445|pmid=28761766|pmcid=5518516|doi=10.1155/2017/4367059|lire en ligne=https://pubmed.ncbi.nlm.nih.gov/28761766/|consulté le=2020-11-27|pages=4367059}}</ref>. On utilise des agrafes de plus en plus petites (exemples avec Echelon, on utilise d'abord des agrafes noires ou vertes, puis dorées, et finalement bleues). De 5 à 6 applications sont nécessaires (moyenne de 5,6). | |||
Il ne doit plus rester de cardia à la dernière application de cartouche. | |||
* Renforcement de la ligne d'agrafage - les principaux objectifs du renforcement de la ligne d'agrafage sont de réduire les taux de fuite et d'hémorragie de la ligne d'agrafage. Il existe de nombreuses techniques pour ce faire et se divisent en deux catégories principales, la surpiqûre et le | *'''Renforcement de la ligne d'agrafage''' - les principaux objectifs du renforcement de la ligne d'agrafage sont de réduire les taux de fuite et d'hémorragie de la ligne d'agrafage. Il existe de nombreuses techniques pour ce faire et se divisent en deux catégories principales, la surpiqûre (clips endoscopiques ou surjet de Maxon) et le renforcement. Dans une méta-analyse récente en 2016, en comparant le renforcement à l'absence de renforcement, il n'y avait pas de différence statistiquement significative dans le taux de fuite, mais il a été démontré une diminution des complications globales, y compris le saignement de la ligne d'agrafage. Lors de la comparaison entre le surjet et le renforcement, le surjet a révélé des avantages plus faibles avec des temps de fonctionnement plus longs et un taux de complications plus élevé ; mais est moins coûteuse. Néanmoins, le concensus jusqu'à ce jour est d'utiliser une technique ou l'autre, afin de diminuer le risque de saignement. | ||
<gallery> | |||
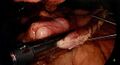
Fichier:Gastrectomie partielle - application de la première cartouche d’autosuture (image).jpeg|Application de la 1<sup>ère</sup> cartouche d’autosutures, bougie 34 Fr en place. | |||
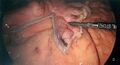
Fichier:Gastrectomie partielle - visualisation de la première application d’agrafes .jpeg|Visualisation de la 1<sup>ère</sup> application d’agrafes. | |||
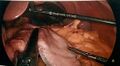
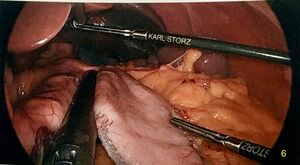
Fichier:Gastrectomie partielle - application d’une deuxième cartouche d’autosuture.jpeg|Application d’une 2<sup>e</sup> cartouche d’autosutures. Le foie toujours surélevé. | |||
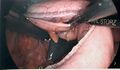
Fichier:Gastrectomie partielle - application de la dernière cartouches d’autosutures.jpeg|Application de la 5<sup>e</sup> et dernière cartouches d’autosutures. On regarde sous l’estomac pour bien visualiser le pilier gauche du diaphragme (à gauche de l’image). On entrevoit la rate qui est ischémique en son pôle supérieur (après la division des vaisseaux courts). | |||
Fichier:Gastrectomie partielle - renforcement la ligne d’agrafes avec des clips endoscopiques.jpeg|On renforce la ligne d’agrafes avec des clips endoscopiques après avoir retiré la bougie. | |||
</gallery> | |||
=== Endoscopie === | |||
Cette étape est optionnelle. Elle est suggérée lors des reprises de gastrectomie verticale ou si on a un doute sur l'intégrité de la ligne d'agrafe. Un endoscope flexible est soigneusement inséré dans l'œsophage et la ligne d'agrafage est visualisée pour l'intégrité et l'hémostase. L'estomac restant peut être immergé dans le liquide d'irrigation, puis insufflé avec l'endoscope pour rechercher une fuite. Il est aussi possible d'instiller une solution colorée par du bleu de méthylène. | |||
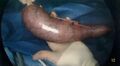
Le test de fuite peropératoire est à la discrétion du chirurgien car il y a eu des résultats incohérents<ref group="note">Une analyse rétrospective multicentrique en 2017 a démontré une faible sensibilité du test de fuite peropératoire pour prédire les fuites postopératoires. Ils ont démontré que le test de fuite peropératoire était négatif chez 91% des patients qui ont finalement développé une fuite de la ligne d'agrafes.</ref><ref name=":15">{{Citation d'un article|prénom1=Jason|nom1=Bingham|prénom2=Jedediah|nom2=Kaufman|prénom3=Kai|nom3=Hata|prénom4=James|nom4=Dickerson|titre=A multicenter study of routine versus selective intraoperative leak testing for sleeve gastrectomy|périodique=Surgery for Obesity and Related Diseases: Official Journal of the American Society for Bariatric Surgery|volume=13|numéro=9|date=2017-09|issn=1878-7533|pmid=28629729|doi=10.1016/j.soard.2017.05.022|lire en ligne=https://pubmed.ncbi.nlm.nih.gov/28629729/|consulté le=2020-11-27|pages=1469–1475}}</ref>.[[Fichier:Gastrectomie partielle - vérification de la ligne d'agrafes (photo).jpg|centré|vignette|600x600px|On observe toute la ligne d’agrafes pour s’assurer de son intégrité et de l’absence de saignement.]] | |||
=== Retrait de l'estomac === | |||
L'estomac est mis dans un sac endoscopique afin de diminuer la contamination de la paroi du trou de trocart qui servira de site d'extraction. Habituellement, on utilise le site de trocart de 12 mm paramédian droit. | |||
<gallery> | |||
Fichier:Gastrectomie partielle - estomac dans le sac endoscopique.jpg|On met l’estomac excisé dans un sac endoscopique et on le retire par le site de trocart de travail qu’on agrandit. On refermera l’aponévrose de celui-ci ensuite. | |||
Fichier:Gastrectomie - dernier regard (photo).jpg|Dernier regard sur le site chirurgical. Pôle supérieur de la rate clairement ischémique. Hémostase adéquate. On retire l’écarteur hépatique sous vision directe. Il y a une hépatomégalie du foie gauche secondaire à la stéatose. | |||
Fichier:Gastrectomie partielle - vérification de l'estomac (photo).jpg|Estomac retiré dans lequel on a insufflé du CO<sub>2</sub> pour visualiser la ligne d’agrafes (absence de torsion). | |||
</gallery> | |||
=== Fermeture === | |||
Une fermeture aponévrotique avec un passe-fil est effectuée sur le site du port de travail élargi pour l'extraction et la fermeture cutanée est effectuée sur tous les sites. | |||
Une fermeture | |||
== Complications == | == Complications == | ||
{{ | Le tableau suivant illustre les complications suivant une gastrectomie pariétale par laparoscopie. | ||
Actuellement, la morbidité et la mortalité à 30 jours d'une gastrectomie en manchon laparoscopique dans la littérature varient respectivement de 0 à 17,5% et de 0 à 1,2 %.<ref name=":16">https:// | {| class="wikitable" | ||
!Critères | |||
!HUTTER | |||
!BIRKMEYER | |||
!CARLIN | |||
!INGE | |||
|- | |||
|Nombre de patients | |||
|944 | |||
|854 | |||
|2949 | |||
|67 | |||
|- | |||
|Âge (années) | |||
|moyenne = 47 | |||
|37-55 | |||
|moyenne = 46 | |||
|13-19 | |||
|- | |||
|{{Complication|nom=Décès}} | |||
|0.11 | |||
|0 | |||
|0.07 | |||
|0 | |||
|- | |||
|{{Complication|nom=Fuite anastomotique|affichage=Fuite par perforation}} | |||
|0.74 | |||
|0.35 | |||
|0.9 | |||
|1.5 | |||
|- | |||
|{{Complication|nom=Infection d'un site chirurgical}} | |||
|2.0 | |||
|2.2 | |||
|2.2 | |||
|3 | |||
|- | |||
|{{Complication|nom=Embolie pulmonaire}} / {{Complication|nom=Thrombose veineuse profonde du membre inférieur|affichage=thrombose veineuse profonde}} | |||
|0.32 | |||
|0.9 | |||
|0.5 | |||
|0 | |||
|- | |||
|Réoperation | |||
|3.0 | |||
|0.6 | |||
|1.4 | |||
|1.5 | |||
|- | |||
|{{Complication|nom=Saignement intra-abdominal}} | |||
|0.6 | |||
|0.6 | |||
|1.1 | |||
|0 | |||
|} | |||
Actuellement, la morbidité et la mortalité à 30 jours d'une gastrectomie en manchon laparoscopique dans la littérature varient respectivement de 0 à 17,5% et de 0 à 1,2 %.<ref name=":16">{{Citation d'un article|prénom1=Mohamed|nom1=Ali|prénom2=Maher|nom2=El Chaar|prénom3=Saber|nom3=Ghiassi|prénom4=Ann M.|nom4=Rogers|titre=American Society for Metabolic and Bariatric Surgery updated position statement on sleeve gastrectomy as a bariatric procedure|périodique=Surgery for Obesity and Related Diseases: Official Journal of the American Society for Bariatric Surgery|volume=13|numéro=10|date=2017-10|issn=1878-7533|pmid=29054173|doi=10.1016/j.soard.2017.08.007|lire en ligne=https://pubmed.ncbi.nlm.nih.gov/29054173/|consulté le=2022-04-08|pages=1652–1657}}</ref><ref name=":0" /> | |||
Comme pour de nombreuses opérations, les complications peuvent être divisées entre précoces et tardives. | Comme pour de nombreuses opérations, les complications peuvent être divisées entre précoces et tardives. | ||
=== Précoces === | |||
Hémorragie <ref name=":0" /> | ==== Hémorragie ==== | ||
L'incidence rapportée est comprise entre 1 et 6% en postopératoire et peut être intraluminale ou intraabdominale.<ref name=":17">{{Citation d'un article|prénom1=Eldo E.|nom1=Frezza|titre=Laparoscopic vertical sleeve gastrectomy for morbid obesity. The future procedure of choice?|périodique=Surgery Today|volume=37|numéro=4|date=2007|issn=0941-1291|pmid=17387557|doi=10.1007/s00595-006-3407-2|lire en ligne=https://pubmed.ncbi.nlm.nih.gov/17387557/|consulté le=2022-05-05|pages=275–281}}</ref> Les saignements extraluminaux proviennent généralement de la ligne d'agrafage, de la rate, du foie ou de la paroi abdominale. Ceci est traité avec une réopération à la discrétion du chirurgien. Pour les saignements intraluminaux, le patient peut présenter du [[méléna]] ou de l'[[hématémèse]] avec une diminution d'hématocrite concomitante. Cela peut être traité par des moyens endoscopiques et plus rarement une intervention chirurgicale. <ref name=":0" /> | |||
Il existe des preuves pour soutenir le renforcement de la ligne d'agrafage pour éviter les saignements. Il y a eu plus de succès lors de la comparaison des matériaux de contrefort par opposition au renforcement des sutures de ligne d'agrafes. Il y a encore une controverse dans ce domaine, et une conclusion définitive n'a pas encore été tirée. <ref name=":18">{{Citation d'un article|prénom1=Theodoros|nom1=Diamantis|prénom2=Konstantinos G.|nom2=Apostolou|prénom3=Andreas|nom3=Alexandrou|prénom4=John|nom4=Griniatsos|titre=Review of long-term weight loss results after laparoscopic sleeve gastrectomy|périodique=Surgery for Obesity and Related Diseases: Official Journal of the American Society for Bariatric Surgery|volume=10|numéro=1|date=2014-01|issn=1878-7533|pmid=24507083|doi=10.1016/j.soard.2013.11.007|lire en ligne=https://pubmed.ncbi.nlm.nih.gov/24507083/|consulté le=2022-05-05|pages=177–183}}</ref><ref name=":0" /> | |||
==== Fuite ==== | |||
L'incidence des fuites postopératoires lors de la gastrectomie par manchon laparoscopique est comprise entre 2 et 3% .<ref name=":19">{{Citation d'un article|prénom1=Scott A.|nom1=Shikora|prénom2=Christine B.|nom2=Mahoney|titre=Clinical Benefit of Gastric Staple Line Reinforcement (SLR) in Gastrointestinal Surgery: a Meta-analysis|périodique=Obesity Surgery|volume=25|numéro=7|date=2015-07|issn=1708-0428|pmid=25968078|pmcid=4460272|doi=10.1007/s11695-015-1703-x|lire en ligne=https://pubmed.ncbi.nlm.nih.gov/25968078/|consulté le=2022-05-05|pages=1133–1141}}</ref> La cause de la fuite chez les patients souffrant de gastrectomie par manchon est une augmentation de la pression relayée sur la ligne d'agrafage en cas d'ischémie relative. Ceci est généralement situé juste en dessous de la jonction GE où il y a une ischémie relative en raison de la dépendance aux vaisseaux gastriques courts sacrifiés. L'augmentation de la pression peut être due à un rétrécissement distal causé par une bougie de petit calibre, un rétrécissement ou une erreur de technique de tir de l'agrafeuse trop près de l'incisura angularis. Il y a eu des résultats et des opinions mitigés sur la question de savoir si le renforcement de la ligne d'agrafage peut réduire le taux de fuite postopératoire et des études supplémentaires sont nécessaires. Il a été démontré qu'une plus grande taille de bougie réduira l'incidence des fuites. | |||
Fuite | |||
L'incidence des fuites postopératoires lors de la gastrectomie par manchon laparoscopique est comprise entre 2 et 3% .<ref name=":19">https:// | |||
Les patients peuvent être asymptomatiques mais présentent fréquemment de la fièvre, une tachycardie et une tachypnée, une fréquence cardiaque élevée étant le premier signe. Le test diagnostique de choix est un scanner avec contraste oral et IV qui démontre une sensibilité et une spécificité relativement élevées. Une série de contraste UGI a une spécificité élevée, mais une faible sensibilité et n'est donc pas recommandée comme imagerie diagnostique de première intention. <ref name=":0" /> | Les patients peuvent être asymptomatiques mais présentent fréquemment de la fièvre, une tachycardie et une tachypnée, une fréquence cardiaque élevée étant le premier signe. Le test diagnostique de choix est un scanner avec contraste oral et IV qui démontre une sensibilité et une spécificité relativement élevées. Une série de contraste UGI a une spécificité élevée, mais une faible sensibilité et n'est donc pas recommandée comme imagerie diagnostique de première intention. <ref name=":0" /> | ||
Les fuites doivent être classées comme aiguë (<5 jours après l'opération) ou chronique (> 4 semaines après l'opération). Chez le patient aigu et instable, l'exploration avec drainage de la fuite et mise en place d'une sonde d'alimentation distale est la gestion de choix. Chez le patient chronique, la prise en charge chirurgicale est moins réussie. S'ils sont instables, le patient nécessitera une opération comme décrit pour une fuite aiguë. Pour une fuite / fistule chronique chez un patient stable, le traitement est conservateur en utilisant le drainage de l'abcès s'il est présent, des antibiotiques, | Les fuites doivent être classées comme aiguë (<5 jours après l'opération) ou chronique (> 4 semaines après l'opération). Chez le patient aigu et instable, l'exploration avec drainage de la fuite et mise en place d'une sonde d'alimentation distale est la gestion de choix. Chez le patient chronique, la prise en charge chirurgicale est moins réussie. S'ils sont instables, le patient nécessitera une opération comme décrit pour une fuite aiguë. Pour une fuite / fistule chronique chez un patient stable, le traitement est conservateur en utilisant le drainage de l'abcès s'il est présent, des antibiotiques, le [[nil-per-os]], une [[HAIV]] et un stenting endoluminal. La plupart des fistules / fuites chroniques se referment en 4 semaines à 3 mois.<ref name=":20">{{Citation d'un article|prénom1=Ana Maria|nom1=Burgos|prénom2=Italo|nom2=Braghetto|prénom3=Attila|nom3=Csendes|prénom4=Fernando|nom4=Maluenda|titre=Gastric leak after laparoscopic-sleeve gastrectomy for obesity|périodique=Obesity Surgery|volume=19|numéro=12|date=2009-12|issn=1708-0428|pmid=19506979|doi=10.1007/s11695-009-9884-9|lire en ligne=https://pubmed.ncbi.nlm.nih.gov/19506979/|consulté le=2022-05-05|pages=1672–1677}}</ref><ref name=":0" /> Finalement, un endo-VAC, des drainages internes, d'une septotomie endoscopique et en dernier recours, une réintervention chirurgicale de type Y-de-Roux peuvent être nécessaires. | ||
=== Tardives === | |||
Stricture <ref name=":0" /> | ==== Stricture ==== | ||
Cette {{Complication|nom=Stricture de l'estomac|affichage=complication}} a une incidence allant jusqu'à 4% et peut se présenter de manière aiguë secondaire à un œdème ou plus souvent de manière chronique. Les symptômes courants sont la [[dysphagie]], les [[nausées]] et les [[vomissements]] et la localisation la plus fréquente est l'incisura angularis. Dans le contexte aigu, cela est probablement secondaire à un œdème ou à une torsion due à des problèmes techniques. L'image diagnostique de choix est une étude de contraste UGI. Le traitement de la sténose aiguë est conservateur et ne nécessite une intervention chirurgicale qu'en cas de non-résolution. Les patients qui présentent des sténoses chroniques doivent subir des dilatations endoscopiques au ballon (long ballon utilisé pour traiter l'achalasie) et peuvent nécessiter plusieurs interventions pour une amélioration à long terme. L'échec de la prise en charge endoscopique nécessitera une intervention chirurgicale avec soit une [[séromyotomie laparoscopique]], soit une conversion en une procédure de [[pontage gastrique Roux-en-Y]].<ref name=":21">{{Citation d'un article|prénom1=Amit|nom1=Parikh|prénom2=Joshua B.|nom2=Alley|prénom3=Richard M.|nom3=Peterson|prénom4=Michael C.|nom4=Harnisch|titre=Management options for symptomatic stenosis after laparoscopic vertical sleeve gastrectomy in the morbidly obese|périodique=Surgical Endoscopy|volume=26|numéro=3|date=2012-03|issn=1432-2218|pmid=22044967|doi=10.1007/s00464-011-1945-1|lire en ligne=https://pubmed.ncbi.nlm.nih.gov/22044967/|consulté le=2022-05-05|pages=738–746}}</ref><ref name=":0" /> | |||
==== Reflux gastro-œsophagien ==== | |||
Le {{Complication|nom=RGO}} sévère est une contre-indication relative à la gastrectomie en manchon. Il y a eu des résultats contradictoires dans la littérature, mais beaucoup ont préconisé le développement ou l'aggravation des symptômes de reflux. Les traitements de première intention sont des IPP, mais si le patient présente des symptômes sévères et est réfractaire au traitement médical, ils peuvent nécessiter une conversion en pontage gastrique Roux-en-Y.<ref name=":22">{{Citation d'un article|prénom1=Simone|nom1=Gehrer|prénom2=Beatrice|nom2=Kern|prénom3=Thomas|nom3=Peters|prénom4=Caroline|nom4=Christoffel-Courtin|titre=Fewer nutrient deficiencies after laparoscopic sleeve gastrectomy (LSG) than after laparoscopic Roux-Y-gastric bypass (LRYGB)-a prospective study|périodique=Obesity Surgery|volume=20|numéro=4|date=2010-04|issn=1708-0428|pmid=20101473|doi=10.1007/s11695-009-0068-4|lire en ligne=https://pubmed.ncbi.nlm.nih.gov/20101473/|consulté le=2022-05-05|pages=447–453}}</ref><ref name=":0" /> En long terme, il est possible que ces patients présentent davantage d'oesophage de Barret. | |||
==== Carences nutritionnelles ==== | |||
Toutes les procédures bariatriques présentent des carences en nutriments et sont largement évitées par des tests de routine et une supplémentation quotidienne: | |||
*{{Complication|nom=Déficit en vitamine C|affichage=vitamine C}} | |||
*{{Complication|nom=Déficit en fer|affichage=fer}} | |||
Carences nutritionnelles | *{{Complication|nom=Déficit en vitamine B12|affichage=vitamine B12}} | ||
*Vitamines liposolubles | |||
Toutes les procédures bariatriques présentent des carences en nutriments et sont largement évitées par des tests de routine et une supplémentation quotidienne | *{{Complication|nom=Déficit en folates|affichage=folates}} | ||
*{{Complication|nom=Déficit en thiamine|affichage=thiamine}} | |||
Il existe des données montrant une diminution de l'incidence de la carence en nutriments par rapport au patient ayant subi un pontage gastrique, à l'exception du folate.<ref name=":0" /> | |||
== Suivi == | == Suivi == | ||
=== Alimentation | === Alimentation et habitudes de vie === | ||
{{Inclure une section d'une page|page=Chirurgie bariatrique|section=Alimentation et habitudes de vie}} | |||
=== | === Analyses de laboratoire === | ||
{| class="wikitable" | |||
|+ | |||
! rowspan="2" |Valeur à analyser | |||
! colspan="2" |Fréquence | |||
|- | |||
= | !Durant la 1<sup>ère</sup> année post-opératoire | ||
!Par la suite | |||
|- | |||
|Formule sanguine complète | |||
| rowspan="9" |Chaque 3 à 6 mois | |||
| rowspan="9" |Annuellement | |||
|- | |||
|Ions | |||
|- | |||
|Albumine | |||
|- | |||
|Ferritine | |||
|- | |||
|Vitamine B12 | |||
|- | |||
|Acide folique | |||
|- | |||
|Calcium | |||
|- | |||
|Vitamine D | |||
|- | |||
|Parathyroïde | |||
|} | |||
== Signification clinique == | == Signification clinique == | ||
=== Résultats attendus === | === Résultats attendus === | ||
Des données à long terme sont maintenant disponibles sur les résultats de la gastrectomie. La perte de poids moyenne en excès («excess weight loss») après | Des données à long terme sont maintenant disponibles sur les résultats de la gastrectomie. La perte de poids moyenne en excès («excess weight loss») après 5 ans pour une gastrectomie laparoscopique pariétale serait d'environ 60%, la perte de poids moyenne étant de 25% et la résolution des comorbidités est excellente. Une méta-analyse réalisée en 2017 a comparé les résultats à mi-parcours et à long terme entre la gastrectomie pariétale et le Y-de-Roux La conclusion était qu'à mi-parcours (3 à 5 ans après l'opération) les deux chirurgies avaient des résultats similaires en termes de perte de poids excessive et de résolution ou d'amélioration des comorbidités. Les données à long terme ont démontré que le bypass gastrique a finalement entraîné une perte de poids supérieure, mais l'amélioration des comorbidités est restée la même entre les deux procédures.<ref name=":23">{{Citation d'un article|prénom1=Saeed|nom1=Shoar|prénom2=Alan A.|nom2=Saber|titre=Long-term and midterm outcomes of laparoscopic sleeve gastrectomy versus Roux-en-Y gastric bypass: a systematic review and meta-analysis of comparative studies|périodique=Surgery for Obesity and Related Diseases: Official Journal of the American Society for Bariatric Surgery|volume=13|numéro=2|date=2017-02|issn=1878-7533|pmid=27720197|doi=10.1016/j.soard.2016.08.011|lire en ligne=https://pubmed.ncbi.nlm.nih.gov/27720197/|consulté le=2020-11-11|pages=170–180}}</ref><ref name=":0" /> | ||
Voici un résumé de la résolution | Voici un résumé de la résolution des comorbidités associées à l'obésité en fonction de la procédure effectuée : | ||
{| class="wikitable" | {| class="wikitable" | ||
|+Résolution des comorbidités en fonction de la procédure bariatrique | |+Résolution des comorbidités en fonction de la procédure bariatrique<ref name=":12">{{Citation d'un lien web|langue=en-US|nom1=Pearce|prénom1=Nicole|titre=Canadian Adult Clinical Practice Guideline Chapters|url=https://obesitycanada.ca/guidelines/chapters/|site=Obesity Canada|consulté le=2020-11-11}}</ref> | ||
! | ! | ||
!Gastrectomie pariétale | !Gastrectomie pariétale | ||
| Ligne 231 : | Ligne 297 : | ||
|40 | |40 | ||
|- | |- | ||
|Taux de résolution du diabète de type 2 | |Taux de résolution du diabète de type 2 (%) | ||
|30 | |30 | ||
|40 | |40 | ||
| Ligne 241 : | Ligne 307 : | ||
|60 | |60 | ||
|- | |- | ||
|Taux de résolution de l'apnée/hypopnée du sommeil | |Taux de résolution de l'apnée/hypopnée du sommeil (%) | ||
|40 | |40 | ||
|50 | |50 | ||
|70 | |70 | ||
|- | |- | ||
|Taux de résolution du | |Taux de résolution du RGO (%) | ||
| | | | ||
| | | | ||
| | | | ||
|- | |- | ||
|Taux de résolution de la | |Taux de résolution de la dyslipidémie (%) | ||
| | | | ||
|65 | |65 | ||
| | |95 | ||
|} | |} | ||
=== | === La gastrectomie verticale comme pont vers la dérivation bilio-pancréatique === | ||
Vu l'importante incidence de morbidité et de mortalité, 23% et 7% respectivement, chez les patients avec un IMC supérieur à 60 kg/m<sup>2</sup> qui subissent une [[Dérivation biliopancréatique avec switch duodénal|dérivation biliopancréatique avec switch duodénal (BPD-DS)]], les chirurgiens ont développé une procédure en deux temps, ayant comme première étape la gastrectomie pariétale pour le taux de morbidité. Le ''Clinical Issues Committee'' du ASMBS a analysé 13 études incluant 821 patients à haut risque ayant subi ce type de procédure. En moyenne, l'IMC préopératoire était de 60, puis 4 à 60 mois en suivi post-opératoire, leur IMC était à 45. Les complications observés chez cette population à haut risque a démontré un taux de fuite à 1,2%, un taux de saignement à 1,6%, et une mortalité à 0,24%. Le ASMBS conclut donc que la gastrectomie pariétale est de valeur en tant qu'étape initiale d'une chirurgie bariatrique chez une population à haut risque. | |||
== Fonctionnement<!-- à retravailler avec source et schéma --> == | |||
La gastrectomie verticale est une chirurgie pour contrer l'obésité par différents mécanismes. D'abord, il s'agit d'une '''procédure restrictive''' puisque le volume gastrique est diminué significativement. Le patient aura un volume post-opératoire d'environ 100 mL (½ tasse), puis environ 250 mL à deux ans post-opératoire. Il y a également une composante '''neurohormonale'''. La vidange gastrique est accélérée par un relâchement plus précoce de la GLP-1 et de la PYY3-36 (un sous-type de neuropeptide Y très orexigène). Le bolus alimentaire arrivant plus rapidement dans l'intestin, la satiété est obtenue plus rapidement par rétroaction négative. L'estomac amputé de son fundus et de la majorité de son corps sécrète moins de ghreline gastrique - hormone orexigène sécrétée par les cellules pariétales du fundus et du corps gastrique et donc le patient a moins d'appétit globalement. | |||
== Notes == | == Notes == | ||
<references group="note" /> | <references group="note" /> | ||
== Références == | == Références == | ||
{{Article importé d'une source | {{Article importé d'une source | ||
| Ligne 269 : | Ligne 338 : | ||
| révision = 2020/06/28 | | révision = 2020/06/28 | ||
| url = https://www.ncbi.nlm.nih.gov/books/NBK519035/ | | url = https://www.ncbi.nlm.nih.gov/books/NBK519035/ | ||
| révisé = | | révisé = 1 | ||
| pmid = 30085577 | | pmid = 30085577 | ||
}} | }} | ||
<references | <references /> | ||
Version du 18 juin 2022 à 18:18
| Procédure | |
 | |
| Procédure | |
|---|---|
| Système | Digestif |
| Informations | |
| Autres noms | gastrectomie verticale, gastrectomie en manchon, sleeve gastrectomy |
| Spécialités | Chirurgie générale, endocrinologie, gastro-entérologie, chirurgie bariatrique |
|
| |
La gastrectomie pariétale (ou verticale) est une intervention bariatrique qui consiste à retirer de façon longiligne le fundus et les portions latérales gauches du corps et de l'antre gastrique ; laissant un volume résiduel d'environ 100 mL le long de la petite courbure gastrique [1]. Ainsi, il s'agit d'une intervention bariatrique dite restrictive, mais également métabolique par les changements neurohormonaux imputables au retrait des cellules pariétales gastriques et une rapidité du transit accrue avec un feedback négatif au niveau duodénal.[1]. La perte de poids attendue est d'environ 25%.[1]
Avantages et limitations
Globalement, on retient les avantages suivants pour la gastrectomie verticale[1] :
- intervention de courte durée
- faible morbidité[note 1][2]
- moins de déficit nutritionnel et vitaminiques à long terme
- moins de complication chirurgicale
- profil d'effets secondaires faible
- bonne qualité de vie
Les limitations de la gastrectomie sont toutefois les suivants :
- moins de perte de poids que les autres procédures
- moins de correction des comorbidités métaboliques que les autres procédures
- augmentation du risque de reflux gastro-oesophagien (5-10%)[1]
Indications
Les indications de la gastrectomie pariétale sont celles de la chirurgie bariatrique en général. Les indications d'une chirurgie bariatrique comprennent[2]:
- Un IMC > 40 ou IMC ≥ 35 avec au moins un état comorbide lié à l'obésité:
- l'hypertension artérielle primaire
- une dyslipidémie
- un diabète de type 2
- du reflux gastro-oesophagien sévère
- de l'apnée du sommeil
- une maladie cardiaque athérosclérotique
- une insuffisance veineuse sévère
- une cirrhose hépatique non-alcoolique (NASH)
- de l'incontinence urinaire
- un pseudotumor cerebri
- des problèmes musculosquelettiques invalidants
- des tentatives infructueuses à perdre du poids de manière non chirurgicale
- une autorisation en termes de santé mentale.
Les lignes directrices canadiennes incluent aussi des critères pour les adolescents :
- IMC ≥ 35 avec au moins un état comorbide lié à l'obésité de l'adolescence et réfractaire au traitement médical et aux changements d'habitude de vie : apnée du sommeil (index d'apnée >15 épisodes), pseudotumor cerebri, NASH, diabète de type 2.
- IMC ≥ 40 avec de l'hypertension, une résistance à l'insuline ou intolérance au glucose, qualité de vie diminuée, diminution de l'autonomie (AVQ, AVD), apnée du sommeil avec index de 5 à 15
Des mises à jour récentes ont inclus des patients ayant un IMC de 30-35 avec un diabète de type 2 incontrôlable ou un syndrome métabolique comme indication pour une gastrectomie pariétale.
Contre-indications
Les indications, ainsi que les contre-indications absolues et relatives de la gastrectomie pariétales sont les critères usuels d'une candidature bariatrique.
Absolues
Les contre-indications absolues comprennent[3] :
- l'incapacité à tolérer une anesthésie générale
- une coagulopathie incontrôlable
- une néoplasie active
- une cirrhose Child-C
- une maladie psychiatrique sévère ou instable
- un tabagisme, une toxicomanie ou un alcoolisme
- une boulimie ou une hyperphagie boulimique non traitée.
D'un point de vue cognitif, le patient doit être apte à comprendre les risques et bénéfices de la chirurgie, et il doit avoir les capacités pour instaurer les changements d'habitude de vie requis pour la chirurgie. Le patient doit également être compliant avec sa médication.
Relatives
Les contre-indications relatives sont[3] :
- la maladie cœliaque
- les allergies multiples
- le syndrome de Prader-Willi
- une maladie de Crohn duodénale
- la narcodépendance
- un âge < 18 ans ou âge > 65 ans (relatif selon l'état de santé global du patient).
Évaluation
L'évaluation bariatrique est multidisciplinaire. La sélection des patients a été établie pour minimiser les complications chirurgicales et maximiser les bénéfices d'une ressource limitée. L'évaluation devra donc statuer sur la santé mentale, médicale et nutritionnelle, ainsi qu'optimiser les comorbidités pour diminuer les complications chirurgicales.
Anatomie
La gastrectomie pariétale est une intervention bariatrique qui consiste à retirer de façon longiligne le fundus de l'estomac et les portions latérales gauches du corps et de l'antre gastrique:

L'estomac est divisé en cardia (juste distal à la jonction gastro-oesophagienne), le fundus (attenant au diaphragme gauche et partageant les vaisseaux courts de la rate), le corps, l'antre et le pylore. La petite courbure se trouve sous les segments médiaux du foie et comprend l'incisura angularis qui peut être identifiée comme la jonction des axes vertical et horizontal de la petite courbure. La grande courbure est le long bord latéral gauche de l'estomac et supporte l'épiploon. Le bord gauche de l'œsophage intra-abdominal et le fundus se rencontrent à un angle aigu appelé «angle de His». Postérieurement à l'estomac se trouve l'arrière-cavité qui est un espace potentiel antérieur au pancréas et bordé par l'artère splénique, la rate, le rein gauche et le mésocôlon transverse.
Ligaments
Les ligaments de l'estomac sont les suivants:
- Ligament gastro-hépatique: petite courbure vers le bord médial du foie, contient les artères gastriques gauche et droite. Peut contenir une artère hépatique gauche récurrente.
- Ligament gastrophrénique : relie le fundus vers l'hémidiaphragme gauche.
- Ligament gastrosplénique : grande courbure de la rate et contient les vaisseaux gastriques courts.
- Ligament gastro-colique : estomac inférieur au côlon transverse, considéré comme faisant partie du grand épiploon et contenant les vaisseaux gastro-épiploïques
Vascularisation

Le tronc coeliaque a trois branches : artères gastrique gauche, hépatique commune et splénique. L'artère gastrique gauche longe la petite courbure supérieure et s'anastomose avec l'artère gastrique droite. L'artère gastrique gauche est le principal apport sanguin à l'estomac après une gastrectomie verticale et elle dégage de nombreuses branches postérieures qui doivent rester ininterrompues pendant la dissection de la surface postérieure de l'estomac. L'artère hépatique commune donne l'artère gastroduodénale qui passe derrière la première partie du duodénum. L'artère gastrique droite est une branche de l'artère hépatique propre et rejoint l'artère gastrique gauche le long de la petite courbure. L'artère gastro-épiploïque droite se branche ensuite à partir de l'artère gastroduodénale et passe dans le ligament gastrocolique (épiploon) le long de la grande courbure pour rejoindre l'artère gastroépiploïque gauche qui est une branche de l'artère splénique courant le long de la plus grande courbure de latéral à médial. L'artère splénique dégage également 3 à 5 artères gastriques courtes circulant dans le ligament gastrosplénique vers le fundus gastrique.
Préparation
D'abord, tel que discuté ci-haut, plusieurs patients bénéficieront d'un régime faible en calories et élevés en protéines afin de diminuer le volume hépatique pour favoriser une exposition de l'estomac (il s'agit d'une diète liquide uniformisée sur 10 à 14 jours). Le patient recevra une antibioprophylaxie (ex. : céfazoline 2 ou 3g) pondérée selon son poids. Finalement, le patient doit recevoir une thromboprophylaxie ajustée à son poids sous forme d'héparine sous-cutanée et on lui installera des jambières à compression séquentielle.
Le patient sera placé en décubitus dorsal. Selon la préférence du chirurgien, il sera les jambes fermées ou écartées (split-leg). L'opérateur principal sera à droite ou entre les jambes. L'assistant se placera à gauche du patient.
Après l'induction anesthésique, on placera le patient en Fowler (Tredelenburg inversé). Une sonde orogastrique pour décomprimée l'estomac sera installée puis retirée avant la manipulation de celui-ci par le chirurgien.
Équipement
L'équipement laparoscopique de base est nécessaire pour cette opération qui comprendra l'insufflation avec du gaz CO2, des champs chirurgicaux, des moniteurs, des instruments laparoscopiques, l'électrocautérisation et des trocarts. Contrairement aux procédures laparoscopiques conventionnelles, avec les patients bariatriques, vous aurez besoin de trocarts plus longs ainsi que d'instruments laparoscopiques plus longs pour s'adapter à la paroi abdominale plus épaisse.[2]
Sont également requis: [2]
- 3 trocarts de 5 mm pour les instruments et l'écarteur hépatique, 1 trocart Optiview pour le laparoscope (10-12 mm), 1 ou 2 trocarts de 12 mm pour l'agrafeuse
- 1 aiguille de Veress standard ou extra-longue
- écarteur hépatique (ex. : écarteur de Nathanson)
- laparoscope 30 degrés, lentille 5 ou 10 mm
- agrafeuse linéaire endoscopique avec différentes épaisseurs de cartouche (en moyenne 5 à 6 applications)
- bougie de 34 Fr (selon la préférence du chirurgien)
- endoscope flexible au besoin
- dispositif d'énergie laparoscopique (appareil d'électrochirurgie pour sceller et couper les tissus)
- porte-aiguille laparoscopique
- clippeuse vasculaire
- sutures à peau
- un sac endoscopique pour l'extraction de l'estomac.
Technique
Il existe de nombreuses façons d'effectuer une gastrectomie laparoscopique en manchon, une procédure type est présentée ici.
Entrée et mise en place
L'entrée dans l'abdomen commence dans le quadrant supérieur gauche (point de Palmer) et la technique utilisée est à la discrétion du chirurgien.
Habituellement:
- L'aiguille de Veress est utilisée puis le trocart Optiview est introduit avec le laparoscope
- L'abdomen est insufflé à une pression de 15 mmHg et l'abdomen est exploré visuellement avec un laparoscope. Un pneumopéritoine de 12 mmHg a été proposé dans les protocoles ERAS, mais le patient doit être fortement curarisé.
Le placements des trocarts sera le suivant:
- trocart de 5 mm dans le quadrant supérieur gauche, ligne axillaire antérieure (port de l'assistant)
- trocart de 5 ou 12 mm dans la ligne médio-claviculaire supérieure gauche pour la main droite du chirurgien
- trocart de 5 ou 12 mm dans la ligne médio-claviculaire paramédiane supérieure droite pour la main gauche du chirurgien
- trocart de 12 mm placé au niveau ou juste au-dessus de l'ombilic (habituellement une longueur de main sous l'apophyse xyphoïde) pour la caméra
- écarteur de foie placé dans la zone sous-xiphoïde via un trocart 5 mm (l'écarteur Nathanson est habituellement utilisé)
- une fois tous les ports insérés et le foie rétracté, le patient est placé en Trendelenburg inversé, le patient est en split-leg et donc le chirurgien est entre les jambes du patient, l'assistant est à gauche de celui-ci.
Mobilisation de la grande courbure
La dissection commence par la division de l'épiploon à quelques centimètres en amont du pylore. On divise l'épiploon en tentant de préserver le plus possible sa vascularisation en utilisant un appareil d'électrochirurgie. On monte le long de la grande courbure jusqu'à rencontrer les vaisseaux courts du pôle supérieur de la rate. D'ailleurs, celui-ci peut devenir ischémique (bleuté) en cours de procédure car la rate a une circulation terminale. La dissection est poursuivie pour diviser complètement le ligament gastrophrénique jusqu'à mobiliser l'angle de His. On doit bien voir le pilier gauche du diaphragme.
Identification et réparation d'une hernie hiatale
Après avoir exposé le pilier gauche du diaphragme, on doit évaluer s'il y a une hernie hiatale. Si tel est le cas, il est recommandé d'en réduire le contenu et le sac et de réparer la hernie avec un rapprochement des piliers. On utilise des sutures en X interrompues en arrière de l'oesophage.
Mobilisation postérieure
L'épiploon étant séparé complètement de la grande courbure, on accède à l'arrière-cavité des épiploons. L'estomac est soulevé antérieurement pour exposer sa paroi postérieure. Toutes les adhérences doivent être défaites, en prenant soin de ne pas transmettre de chaleur de l'appareil d'électrochirurgie sur la capsule pancréatique. On doit visualiser la petite courbure. La vascularisation de celle-ci servira de point de repère pour l'application des recharges de l'agrafeuse.
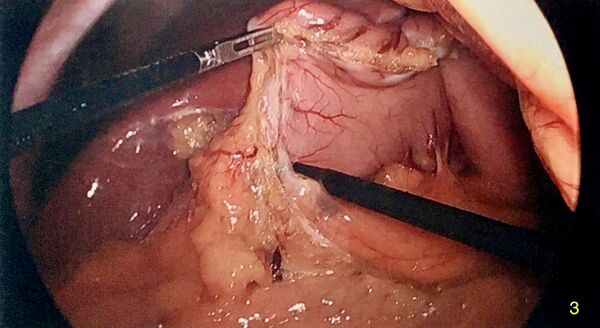
Placement de la bougie
Une bougie orogastrique de 32 à 40 Fr est placée sous visualisation laparoscopique. L'anesthésiste pousse la bougie jusqu'au pylore de sorte que l'on mette légèrement en tension la zone pré-pylorique où les dernières attaches épiploïques ont été divisées.
- Taille de la bougie : la bougie sert de guide pour l'application des cartouches d'autosuture pour créer un manchon autour de la bougie. Une bougie trop petite créé une gastrectomie trop étroite et donc augmente la résistance et la pression intra-luminale. Ceci augmenterait le risque de fuite. A contrario, une bougie trop large créerait un réservoir trop flasque et la perte de poids ne serait pas optimale. Lors de la cinquième conférence internationale, il a été recommandé d'utiliser une grande bougie (la médiane était de 36 Fr).[4]
- Longueur du pylore : il y a débat sur le point de départ de la première charge d'agrafes en terme de distance du pylore. Des distances de 2 à 6 cm sont pratiquées aujourd'hui et la quantité d'antre retenu détermine sa signification clinique. Avec une distance de 2 cm, plus d'antre est réséqué et le reste gastrique est relativement plus petit. Ceci, en théorie, produira une augmentation de la perte de poids excessive mais peut conduire à plus de complications de l'augmentation de la pression intragastrique distale. Des études comparant une distance de 2 cm et une distance de 4 à 6 cm ont montré des résultats mitigés. L'un a montré des résultats égaux en considérant la perte de poids et les complications[5], et l'autre a démontré une perte de poids accrue sans augmentation des complications pour la longueur de 2 cm.[6] L'opinion de la conférence internationale était de commencer la résection à au moins 3 cm du pylore.[2]
Résection gastrique
Une agrafeuse endoscopique de 60 mm de long est utilisée pour suturer et trancher l'estomac dans son axe vertical. La mise à feu est commencée à environ 5 cm proximal au pylore le long de la bougie et avec un angle parallèle à la petite courbure. Il faut s'assurer que l'agrafeuse englobe des longueurs égales de l'estomac antérieur et postérieur pour éviter la «spirale» du manchon - la mise en tension de la grande courbure par l'assistant est essentielle pour ce faire. Les lignes d'agrafes sont tirées séquentiellement le long de la bougie vers l'angle de His. En moyenne, l'épaisseur de paroi de l'antre, du corps et des fonds est respectivement de 3,1, 2,4 et 1,7 mm[7]. Le but est d'utiliser une agrafeuse avec des agrafes suffisamment hautes pour accueillir l'antre le plus épais par opposition au fundus plus fin. Certains ont préconisé des résultats supérieurs en utilisant une hauteur d'agrafe plus haute en distal et une hauteur d'agrafe plus courte en proximal à l'approche du fundus[8]. On utilise des agrafes de plus en plus petites (exemples avec Echelon, on utilise d'abord des agrafes noires ou vertes, puis dorées, et finalement bleues). De 5 à 6 applications sont nécessaires (moyenne de 5,6).
Il ne doit plus rester de cardia à la dernière application de cartouche.
- Renforcement de la ligne d'agrafage - les principaux objectifs du renforcement de la ligne d'agrafage sont de réduire les taux de fuite et d'hémorragie de la ligne d'agrafage. Il existe de nombreuses techniques pour ce faire et se divisent en deux catégories principales, la surpiqûre (clips endoscopiques ou surjet de Maxon) et le renforcement. Dans une méta-analyse récente en 2016, en comparant le renforcement à l'absence de renforcement, il n'y avait pas de différence statistiquement significative dans le taux de fuite, mais il a été démontré une diminution des complications globales, y compris le saignement de la ligne d'agrafage. Lors de la comparaison entre le surjet et le renforcement, le surjet a révélé des avantages plus faibles avec des temps de fonctionnement plus longs et un taux de complications plus élevé ; mais est moins coûteuse. Néanmoins, le concensus jusqu'à ce jour est d'utiliser une technique ou l'autre, afin de diminuer le risque de saignement.
-
Application de la 1ère cartouche d’autosutures, bougie 34 Fr en place.
-
Visualisation de la 1ère application d’agrafes.
-
Application d’une 2e cartouche d’autosutures. Le foie toujours surélevé.
-
Application de la 5e et dernière cartouches d’autosutures. On regarde sous l’estomac pour bien visualiser le pilier gauche du diaphragme (à gauche de l’image). On entrevoit la rate qui est ischémique en son pôle supérieur (après la division des vaisseaux courts).
-
On renforce la ligne d’agrafes avec des clips endoscopiques après avoir retiré la bougie.
Endoscopie
Cette étape est optionnelle. Elle est suggérée lors des reprises de gastrectomie verticale ou si on a un doute sur l'intégrité de la ligne d'agrafe. Un endoscope flexible est soigneusement inséré dans l'œsophage et la ligne d'agrafage est visualisée pour l'intégrité et l'hémostase. L'estomac restant peut être immergé dans le liquide d'irrigation, puis insufflé avec l'endoscope pour rechercher une fuite. Il est aussi possible d'instiller une solution colorée par du bleu de méthylène.
Le test de fuite peropératoire est à la discrétion du chirurgien car il y a eu des résultats incohérents[note 2][9].
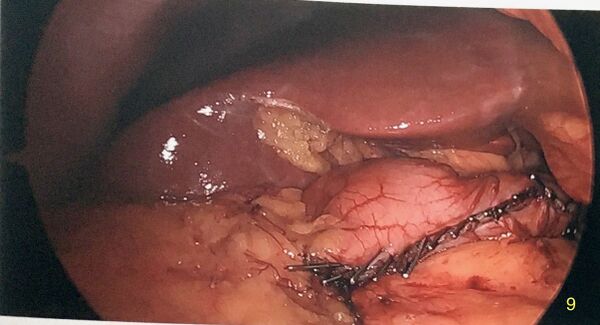
Retrait de l'estomac
L'estomac est mis dans un sac endoscopique afin de diminuer la contamination de la paroi du trou de trocart qui servira de site d'extraction. Habituellement, on utilise le site de trocart de 12 mm paramédian droit.
-
On met l’estomac excisé dans un sac endoscopique et on le retire par le site de trocart de travail qu’on agrandit. On refermera l’aponévrose de celui-ci ensuite.
-
Dernier regard sur le site chirurgical. Pôle supérieur de la rate clairement ischémique. Hémostase adéquate. On retire l’écarteur hépatique sous vision directe. Il y a une hépatomégalie du foie gauche secondaire à la stéatose.
-
Estomac retiré dans lequel on a insufflé du CO2 pour visualiser la ligne d’agrafes (absence de torsion).
Fermeture
Une fermeture aponévrotique avec un passe-fil est effectuée sur le site du port de travail élargi pour l'extraction et la fermeture cutanée est effectuée sur tous les sites.
Complications
Le tableau suivant illustre les complications suivant une gastrectomie pariétale par laparoscopie.
| Critères | HUTTER | BIRKMEYER | CARLIN | INGE |
|---|---|---|---|---|
| Nombre de patients | 944 | 854 | 2949 | 67 |
| Âge (années) | moyenne = 47 | 37-55 | moyenne = 46 | 13-19 |
| décès | 0.11 | 0 | 0.07 | 0 |
| Fuite par perforation | 0.74 | 0.35 | 0.9 | 1.5 |
| infection d'un site chirurgical | 2.0 | 2.2 | 2.2 | 3 |
| embolie pulmonaire / thrombose veineuse profonde | 0.32 | 0.9 | 0.5 | 0 |
| Réoperation | 3.0 | 0.6 | 1.4 | 1.5 |
| saignement intra-abdominal | 0.6 | 0.6 | 1.1 | 0 |
Actuellement, la morbidité et la mortalité à 30 jours d'une gastrectomie en manchon laparoscopique dans la littérature varient respectivement de 0 à 17,5% et de 0 à 1,2 %.[10][2]
Comme pour de nombreuses opérations, les complications peuvent être divisées entre précoces et tardives.
Précoces
Hémorragie
L'incidence rapportée est comprise entre 1 et 6% en postopératoire et peut être intraluminale ou intraabdominale.[11] Les saignements extraluminaux proviennent généralement de la ligne d'agrafage, de la rate, du foie ou de la paroi abdominale. Ceci est traité avec une réopération à la discrétion du chirurgien. Pour les saignements intraluminaux, le patient peut présenter du méléna ou de l'hématémèse avec une diminution d'hématocrite concomitante. Cela peut être traité par des moyens endoscopiques et plus rarement une intervention chirurgicale. [2]
Il existe des preuves pour soutenir le renforcement de la ligne d'agrafage pour éviter les saignements. Il y a eu plus de succès lors de la comparaison des matériaux de contrefort par opposition au renforcement des sutures de ligne d'agrafes. Il y a encore une controverse dans ce domaine, et une conclusion définitive n'a pas encore été tirée. [12][2]
Fuite
L'incidence des fuites postopératoires lors de la gastrectomie par manchon laparoscopique est comprise entre 2 et 3% .[13] La cause de la fuite chez les patients souffrant de gastrectomie par manchon est une augmentation de la pression relayée sur la ligne d'agrafage en cas d'ischémie relative. Ceci est généralement situé juste en dessous de la jonction GE où il y a une ischémie relative en raison de la dépendance aux vaisseaux gastriques courts sacrifiés. L'augmentation de la pression peut être due à un rétrécissement distal causé par une bougie de petit calibre, un rétrécissement ou une erreur de technique de tir de l'agrafeuse trop près de l'incisura angularis. Il y a eu des résultats et des opinions mitigés sur la question de savoir si le renforcement de la ligne d'agrafage peut réduire le taux de fuite postopératoire et des études supplémentaires sont nécessaires. Il a été démontré qu'une plus grande taille de bougie réduira l'incidence des fuites.
Les patients peuvent être asymptomatiques mais présentent fréquemment de la fièvre, une tachycardie et une tachypnée, une fréquence cardiaque élevée étant le premier signe. Le test diagnostique de choix est un scanner avec contraste oral et IV qui démontre une sensibilité et une spécificité relativement élevées. Une série de contraste UGI a une spécificité élevée, mais une faible sensibilité et n'est donc pas recommandée comme imagerie diagnostique de première intention. [2]
Les fuites doivent être classées comme aiguë (<5 jours après l'opération) ou chronique (> 4 semaines après l'opération). Chez le patient aigu et instable, l'exploration avec drainage de la fuite et mise en place d'une sonde d'alimentation distale est la gestion de choix. Chez le patient chronique, la prise en charge chirurgicale est moins réussie. S'ils sont instables, le patient nécessitera une opération comme décrit pour une fuite aiguë. Pour une fuite / fistule chronique chez un patient stable, le traitement est conservateur en utilisant le drainage de l'abcès s'il est présent, des antibiotiques, le nil-per-os, une HAIV et un stenting endoluminal. La plupart des fistules / fuites chroniques se referment en 4 semaines à 3 mois.[14][2] Finalement, un endo-VAC, des drainages internes, d'une septotomie endoscopique et en dernier recours, une réintervention chirurgicale de type Y-de-Roux peuvent être nécessaires.
Tardives
Stricture
Cette complication a une incidence allant jusqu'à 4% et peut se présenter de manière aiguë secondaire à un œdème ou plus souvent de manière chronique. Les symptômes courants sont la dysphagie, les nausées et les vomissements et la localisation la plus fréquente est l'incisura angularis. Dans le contexte aigu, cela est probablement secondaire à un œdème ou à une torsion due à des problèmes techniques. L'image diagnostique de choix est une étude de contraste UGI. Le traitement de la sténose aiguë est conservateur et ne nécessite une intervention chirurgicale qu'en cas de non-résolution. Les patients qui présentent des sténoses chroniques doivent subir des dilatations endoscopiques au ballon (long ballon utilisé pour traiter l'achalasie) et peuvent nécessiter plusieurs interventions pour une amélioration à long terme. L'échec de la prise en charge endoscopique nécessitera une intervention chirurgicale avec soit une séromyotomie laparoscopique, soit une conversion en une procédure de pontage gastrique Roux-en-Y.[15][2]
Reflux gastro-œsophagien
Le RGO sévère est une contre-indication relative à la gastrectomie en manchon. Il y a eu des résultats contradictoires dans la littérature, mais beaucoup ont préconisé le développement ou l'aggravation des symptômes de reflux. Les traitements de première intention sont des IPP, mais si le patient présente des symptômes sévères et est réfractaire au traitement médical, ils peuvent nécessiter une conversion en pontage gastrique Roux-en-Y.[16][2] En long terme, il est possible que ces patients présentent davantage d'oesophage de Barret.
Carences nutritionnelles
Toutes les procédures bariatriques présentent des carences en nutriments et sont largement évitées par des tests de routine et une supplémentation quotidienne:
- vitamine C
- fer
- vitamine B12
- Vitamines liposolubles
- folates
- thiamine
Il existe des données montrant une diminution de l'incidence de la carence en nutriments par rapport au patient ayant subi un pontage gastrique, à l'exception du folate.[2]
Suivi
Alimentation et habitudes de vie
Le suivi du patient bariatrique est la pierre angulaire du succès à long terme. Les lignes directrices canadiennes[2] suggèrent :
- Alimentation post-opératoire :
- transition liquide à molle pendant 2 semaines, puis si bien tolérée introduire les solides
- recommandé de manger 3 à 5 petits repas par jour en débutant toujours avec les sources de protéines[note 3]
- manger lentement et bien mastiquer, éviter la suralimentation[note 4]
- non recommandé de boire et de manger simultanément
- éviter les liquides 30 minutes après le repas
- bien s'hydrater, éviter les boissons gazeuses[note 5].
- Changement des habitudes de vie :
- Fertilité :
- la grossesse est recommandée après 18 mois post-opératoires[note 10]
- une contraception doit être proposée pendant la période charnière.
- Vitamines et minéraux: à moins d'un déficit documenté en pré-opératoire, une multi-vitamine extra-forte 1 ou 2 comprimés par jour ainsi qu'un supplément de fer et/ou de vitamine D couvrent les besoins du patient opéré.
| Supplément | Prise suggérée |
|---|---|
| Vitamine B1 |
|
| Vitamine B12 |
|
| Acide folique |
|
| Fer |
|
| Vitamine E |
|
| Citrate de calcium |
|
| Vitamine D3 |
|
| Vitamine A |
|
| Vitamine K |
|
| Zinc |
|
| Cuivre |
|
Analyses de laboratoire
| Valeur à analyser | Fréquence | |
|---|---|---|
| Durant la 1ère année post-opératoire | Par la suite | |
| Formule sanguine complète | Chaque 3 à 6 mois | Annuellement |
| Ions | ||
| Albumine | ||
| Ferritine | ||
| Vitamine B12 | ||
| Acide folique | ||
| Calcium | ||
| Vitamine D | ||
| Parathyroïde | ||
Signification clinique
Résultats attendus
Des données à long terme sont maintenant disponibles sur les résultats de la gastrectomie. La perte de poids moyenne en excès («excess weight loss») après 5 ans pour une gastrectomie laparoscopique pariétale serait d'environ 60%, la perte de poids moyenne étant de 25% et la résolution des comorbidités est excellente. Une méta-analyse réalisée en 2017 a comparé les résultats à mi-parcours et à long terme entre la gastrectomie pariétale et le Y-de-Roux La conclusion était qu'à mi-parcours (3 à 5 ans après l'opération) les deux chirurgies avaient des résultats similaires en termes de perte de poids excessive et de résolution ou d'amélioration des comorbidités. Les données à long terme ont démontré que le bypass gastrique a finalement entraîné une perte de poids supérieure, mais l'amélioration des comorbidités est restée la même entre les deux procédures.[18][2]
Voici un résumé de la résolution des comorbidités associées à l'obésité en fonction de la procédure effectuée :
| Gastrectomie pariétale | Y-de-Roux | Dérivation bilio-pancréatique
avec switch duodénal | |
|---|---|---|---|
| Perte de poids total (%) | 25 | 30 | 40 |
| Taux de résolution du diabète de type 2 (%) | 30 | 40 | 80 |
| Taux de résolution de l'hypertension (%) | 30 | 40 | 60 |
| Taux de résolution de l'apnée/hypopnée du sommeil (%) | 40 | 50 | 70 |
| Taux de résolution du RGO (%) | |||
| Taux de résolution de la dyslipidémie (%) | 65 | 95 |
La gastrectomie verticale comme pont vers la dérivation bilio-pancréatique
Vu l'importante incidence de morbidité et de mortalité, 23% et 7% respectivement, chez les patients avec un IMC supérieur à 60 kg/m2 qui subissent une dérivation biliopancréatique avec switch duodénal (BPD-DS), les chirurgiens ont développé une procédure en deux temps, ayant comme première étape la gastrectomie pariétale pour le taux de morbidité. Le Clinical Issues Committee du ASMBS a analysé 13 études incluant 821 patients à haut risque ayant subi ce type de procédure. En moyenne, l'IMC préopératoire était de 60, puis 4 à 60 mois en suivi post-opératoire, leur IMC était à 45. Les complications observés chez cette population à haut risque a démontré un taux de fuite à 1,2%, un taux de saignement à 1,6%, et une mortalité à 0,24%. Le ASMBS conclut donc que la gastrectomie pariétale est de valeur en tant qu'étape initiale d'une chirurgie bariatrique chez une population à haut risque.
Fonctionnement
La gastrectomie verticale est une chirurgie pour contrer l'obésité par différents mécanismes. D'abord, il s'agit d'une procédure restrictive puisque le volume gastrique est diminué significativement. Le patient aura un volume post-opératoire d'environ 100 mL (½ tasse), puis environ 250 mL à deux ans post-opératoire. Il y a également une composante neurohormonale. La vidange gastrique est accélérée par un relâchement plus précoce de la GLP-1 et de la PYY3-36 (un sous-type de neuropeptide Y très orexigène). Le bolus alimentaire arrivant plus rapidement dans l'intestin, la satiété est obtenue plus rapidement par rétroaction négative. L'estomac amputé de son fundus et de la majorité de son corps sécrète moins de ghreline gastrique - hormone orexigène sécrétée par les cellules pariétales du fundus et du corps gastrique et donc le patient a moins d'appétit globalement.
Notes
- ↑ Par rapport à d'autres chirurgies de perte de poids, la gastrectomie pariétale est techniquement plus facile avec relativement moins de morbidité et est donc devenue la chirurgie de perte de poids la plus courante pratiquée aux États-Unis. Actuellement, il y a 3 gastrectomies pour un Y-de-Roux aux États-Unis.
- ↑ Une analyse rétrospective multicentrique en 2017 a démontré une faible sensibilité du test de fuite peropératoire pour prédire les fuites postopératoires. Ils ont démontré que le test de fuite peropératoire était négatif chez 91% des patients qui ont finalement développé une fuite de la ligne d'agrafes.
- ↑ Les recommandations d'apport en protéines sont de 1.2 à 1.5 g/kg/jr.
- ↑ Le dépassement de la capacité de l'estomac provoque des nausées et des vomissements.
- ↑ Les boissons gazeuses sont fortement déconseillées pour leur piètre aspect nutritionnel et pour l'inconfort causé par le gaz carbonique.
- ↑ Il n'est pas recommandé de consommer de l'alcool puisqu'il s'agit d'un ulcérogène et d'une source de calories vides. L'effet peut être plus rapide car la vidange gastrique est accélérée. Malheureusement, 7% des patients opérés développeront une dépendance à l'alcool.
- ↑ L'activité physique permet de stabiliser la perte de poids, d'augmenter la masse maigre et d'améliorer la santé mentale.
- ↑ Le tabac est ulcérogène, tout comme l'alcool.
- ↑ Cependant, la marijuana est orexigène (stimulant à l'appétit) et contrevient donc aux vertus de la chirurgie bariatrique
- ↑ Les femmes opérées en-deçà d'un an de la procédure bariatrique avaient un taux de perte foetale plus élevée contrairement à celles qui étaient opérées il y a plus d'un an (35.5% vs 16.3%).
- ↑ L'observance aux suppléments diminue avec le temps et des rappels doivent souvent être faits. De plus, les suppléments peuvent occasionner une constipation, effet secondaire de certaines chirurgies bariatriques également, dont la gastrectomie pariétale.
- ↑ Recommended Dietary Allowance
Références
- Cette page a été modifiée ou créée le 2020/10/25 à partir de Sleeve Gastrectomy (StatPearls / Sleeve Gastrectomy (2020/06/28)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/30085577 (livre).
- ↑ 1,0 1,1 1,2 1,3 et 1,4 Reavis, Kevin M.,, Barrett, Allison M.,, Kroh, Matthew, et Society of American Gastrointestinal Endoscopic Surgeons,, The SAGES manual of bariatric surgery (ISBN 978-3-319-71282-6 et 3-319-71282-9, OCLC 1031089500, lire en ligne)
- ↑ 2,00 2,01 2,02 2,03 2,04 2,05 2,06 2,07 2,08 2,09 2,10 2,11 2,12 2,13 et 2,14 Kevin Seeras, Senthilkumar Sankararaman et Peter P. Lopez, StatPearls, StatPearls Publishing, (PMID 30085577, lire en ligne) Erreur de référence : Balise
<ref>incorrecte : le nom « :0 » est défini plusieurs fois avec des contenus différents. - ↑ 3,0 et 3,1 Jeffrey I. Mechanick, Adrienne Youdim, Daniel B. Jones et W. Timothy Garvey, « Clinical practice guidelines for the perioperative nutritional, metabolic, and nonsurgical support of the bariatric surgery patient--2013 update: cosponsored by American Association of Clinical Endocrinologists, The Obesity Society, and American Society for Metabolic & Bariatric Surgery », Obesity (Silver Spring, Md.), vol. 21 Suppl 1, , S1–27 (ISSN 1930-739X, PMID 23529939, Central PMCID 4142593, DOI 10.1002/oby.20461, lire en ligne)
- ↑ Michel Gagner, Colleen Hutchinson et Raul Rosenthal, « Fifth International Consensus Conference: current status of sleeve gastrectomy », Surgery for Obesity and Related Diseases: Official Journal of the American Society for Bariatric Surgery, vol. 12, no 4, , p. 750–756 (ISSN 1878-7533, PMID 27178618, DOI 10.1016/j.soard.2016.01.022, lire en ligne)
- ↑ Ahmed ElGeidie, Mohamed ElHemaly, Emad Hamdy et Mohamed El Sorogy, « The effect of residual gastric antrum size on the outcome of laparoscopic sleeve gastrectomy: a prospective randomized trial », Surgery for Obesity and Related Diseases: Official Journal of the American Society for Bariatric Surgery, vol. 11, no 5, , p. 997–1003 (ISSN 1878-7533, PMID 25638594, DOI 10.1016/j.soard.2014.12.025, lire en ligne)
- ↑ Emad Abdallah, Ayman El Nakeeb, Tamer Youssef et Tamer Yousef, « Impact of extent of antral resection on surgical outcomes of sleeve gastrectomy for morbid obesity (a prospective randomized study) », Obesity Surgery, vol. 24, no 10, , p. 1587–1594 (ISSN 1708-0428, PMID 24728866, DOI 10.1007/s11695-014-1242-x, lire en ligne)
- ↑ Hazem Elariny, Hamilton González et Bingshi Wang, « Tissue thickness of human stomach measured on excised gastric specimens from obese patients », Surgical Technology International, vol. 14, , p. 119–124 (ISSN 1090-3941, PMID 16525963, lire en ligne)
- ↑ David L. Warner et Kent C. Sasse, « Technical Details of Laparoscopic Sleeve Gastrectomy Leading to Lowered Leak Rate: Discussion of 1070 Consecutive Cases », Minimally Invasive Surgery, vol. 2017, , p. 4367059 (ISSN 2090-1445, PMID 28761766, Central PMCID 5518516, DOI 10.1155/2017/4367059, lire en ligne)
- ↑ Jason Bingham, Jedediah Kaufman, Kai Hata et James Dickerson, « A multicenter study of routine versus selective intraoperative leak testing for sleeve gastrectomy », Surgery for Obesity and Related Diseases: Official Journal of the American Society for Bariatric Surgery, vol. 13, no 9, , p. 1469–1475 (ISSN 1878-7533, PMID 28629729, DOI 10.1016/j.soard.2017.05.022, lire en ligne)
- ↑ Mohamed Ali, Maher El Chaar, Saber Ghiassi et Ann M. Rogers, « American Society for Metabolic and Bariatric Surgery updated position statement on sleeve gastrectomy as a bariatric procedure », Surgery for Obesity and Related Diseases: Official Journal of the American Society for Bariatric Surgery, vol. 13, no 10, , p. 1652–1657 (ISSN 1878-7533, PMID 29054173, DOI 10.1016/j.soard.2017.08.007, lire en ligne)
- ↑ Eldo E. Frezza, « Laparoscopic vertical sleeve gastrectomy for morbid obesity. The future procedure of choice? », Surgery Today, vol. 37, no 4, , p. 275–281 (ISSN 0941-1291, PMID 17387557, DOI 10.1007/s00595-006-3407-2, lire en ligne)
- ↑ Theodoros Diamantis, Konstantinos G. Apostolou, Andreas Alexandrou et John Griniatsos, « Review of long-term weight loss results after laparoscopic sleeve gastrectomy », Surgery for Obesity and Related Diseases: Official Journal of the American Society for Bariatric Surgery, vol. 10, no 1, , p. 177–183 (ISSN 1878-7533, PMID 24507083, DOI 10.1016/j.soard.2013.11.007, lire en ligne)
- ↑ Scott A. Shikora et Christine B. Mahoney, « Clinical Benefit of Gastric Staple Line Reinforcement (SLR) in Gastrointestinal Surgery: a Meta-analysis », Obesity Surgery, vol. 25, no 7, , p. 1133–1141 (ISSN 1708-0428, PMID 25968078, Central PMCID 4460272, DOI 10.1007/s11695-015-1703-x, lire en ligne)
- ↑ Ana Maria Burgos, Italo Braghetto, Attila Csendes et Fernando Maluenda, « Gastric leak after laparoscopic-sleeve gastrectomy for obesity », Obesity Surgery, vol. 19, no 12, , p. 1672–1677 (ISSN 1708-0428, PMID 19506979, DOI 10.1007/s11695-009-9884-9, lire en ligne)
- ↑ Amit Parikh, Joshua B. Alley, Richard M. Peterson et Michael C. Harnisch, « Management options for symptomatic stenosis after laparoscopic vertical sleeve gastrectomy in the morbidly obese », Surgical Endoscopy, vol. 26, no 3, , p. 738–746 (ISSN 1432-2218, PMID 22044967, DOI 10.1007/s00464-011-1945-1, lire en ligne)
- ↑ Simone Gehrer, Beatrice Kern, Thomas Peters et Caroline Christoffel-Courtin, « Fewer nutrient deficiencies after laparoscopic sleeve gastrectomy (LSG) than after laparoscopic Roux-Y-gastric bypass (LRYGB)-a prospective study », Obesity Surgery, vol. 20, no 4, , p. 447–453 (ISSN 1708-0428, PMID 20101473, DOI 10.1007/s11695-009-0068-4, lire en ligne)
- ↑ (en) « Canadian Guidelines for Vitamin Supplementation »
- ↑ Saeed Shoar et Alan A. Saber, « Long-term and midterm outcomes of laparoscopic sleeve gastrectomy versus Roux-en-Y gastric bypass: a systematic review and meta-analysis of comparative studies », Surgery for Obesity and Related Diseases: Official Journal of the American Society for Bariatric Surgery, vol. 13, no 2, , p. 170–180 (ISSN 1878-7533, PMID 27720197, DOI 10.1016/j.soard.2016.08.011, lire en ligne)
- ↑ (en-US) Nicole Pearce, « Canadian Adult Clinical Practice Guideline Chapters », sur Obesity Canada (consulté le 11 novembre 2020)