Entérite à Campylobacter
| Maladie | |
| Caractéristiques | |
|---|---|
| Signes | Hypotension orthostatique, Muqueuse buccale sèche, Oligurie, Diminution de l'état général, Pli cutané, Tachycardie , Tachypnée , Hépatosplénomégalie, Refill capillaire allongé, Sensibilité abdominale diffuse, ... [+] |
| Symptômes |
Frissons, Courbatures, Crampes abdominales, Vertige , Douleur abdominale, Diarrhée , Hématochézie , Perte de poids |
| Diagnostic différentiel |
Appendicite, Saignement gastro-intestinal, Malabsorption, Syndrome du colon irritable, Cytomégalovirus, Colite ulcéreuse, Herpes simplex, Norovirus, Salmonella, Shigella, ... [+] |
| Informations | |
| Wikidata ID | Q131488 |
|
| |
Toute contribution serait appréciée.
| Description: | Cette section contient la définition du concept et devrait se résumer à quelques phrases au maximum : il ne s'agit pas d'une introduction. S'il existe des pages alternatives ou des nuances qui seraient susceptibles d'intéresser le lecteur, elles seront mentionnées dans cette section avec des liens. Le format attendu est le texte. |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: | Une erreur fréquente est de mettre des signes, des symptômes et le traitement dans l'introduction. Dans un soucis de concision, et considérant que votre page sera consultée autant sur ordinateur que sur les téléphones intelligents, la définition sert à définir à la manière d'un dictionnaire. |
| Exemple: | L'appendicite est l'inflammation et l'infection de l'appendice. |
Les espèces de Campylobacter représentent l'une des causes les plus courantes de maladies diarrhéiques bactériennes dans le monde.
Épidémiologie
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section contient les données épidémiologiques sur la maladie (ex. incidence, prévalence, coûts en hospitalisation, proportion d'hommes-femmes, régions où la prévalence est plus élevée, etc.). Chaque donnée épidémiologique doit être appuyée par une référence. Idéalement, des statistiques canadiennes et québécoises sont mentionnées lorsque disponibles. |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: | Les facteurs de risque ne sont pas présentés ici, mais bien dans la sous-section Facteurs de risque (Présentation clinique). Le pronostic et l'évolution naturelle de la maladie sont décrits dans la section Évolution. |
| Exemple: | La FRP est une maladie relativement rare qui affecte le plus souvent les patients âgés de 40 à 60 ans. Une prédominance masculine est observée avec un ratio H : F estimé à environ 2:1 ou 3:1. L'incidence de la FRP est inconnue, mais est estimée à 1 pour 200 000 à 500 000 par an. |
Campylobacter est une cause majeure de diarrhée dans les pays en développement et dans les pays développés, qui est devenue de plus en plus répandue. Selon les « Centers for Disease Control » (CDC) des États-Unis, il y a environ 1,3 million de cas d'infection à Campylobacter chaque année aux États-Unis seulement. Cela entraîne un coût économique compris entre 1,3 et 6,8 milliards de dollars par an aux États-Unis.[1] En mars 2013, le CDC a signalé une augmentation de 14% des cas de C. jejuni aux États-Unis. Un pour cent de la population humaine européenne est touché chaque année par la campylobactériose. Dans les pays en développement, les taux d'isolement de Campylobacter pour les maladies d'origine alimentaire se situent entre 5% et 20%. La campylobactériose peut survenir dans tous les groupes d'âge, bien qu'elle affecte principalement les patients pédiatriques dans les pays en développement. Malgré la mise en place de modalités de traitement et d'éradication dans les réservoirs d'animaux, il y a eu une augmentation dramatique des cas dans les régions développées et sous-développées du monde.[1][2] Dans les pays développés, 90% des cas surviennent pendant les mois d'été, ce qui serait lié à la viande insuffisamment cuite dans les installations extérieures. La maladie affecte le plus souvent les enfants de moins de 4 ans et les jeunes adultes âgés de 15 à 44 ans.[3][2]
La prévalence mondiale de la maladie met en évidence la capacité de Campylobacter à survivre dans un large éventail d'environnements. Les voies de transmission aux humains comprennent la consommation d'aliments et d'eau contaminés, le contact avec les animaux et le contact de personne à personne.[4] Avec la popularité croissante des voyages internationaux du bétail et des humains, la propagation de Campylobacter est difficile à contrôler. Le CDC a fait des efforts pour éduquer le public sur les signes et les symptômes de la maladie et la prévention des maladies pour ceux qui voyagent dans des pays qui présentent un risque élevé de contact avec des sources infectées. Ces efforts comprennent l'hygiène des mains, la séparation des viandes crues des autres aliments lors de la cuisson, la cuisson minutieuse des aliments et l'évitement des produits laitiers crus et de l'eau non traitée.[2]
Étiologies
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section décrit les étiologies de la maladie, c'est-à-dire ce qui cause la maladie (ex. le diabète de type 2 cause la néphropathie diabétique). Les étiologies doivent être identifiées avec le modèle Étiologies. |
| Formats: | Texte, Liste à puces, Tableau |
| Balises sémantiques: | Étiologie |
| Commentaires: |
|
| Exemple: | Parmi les étiologies les plus courantes d'occlusion de l'intestin grêle, on retrouve :
|
Les voies de transmission aux humaines de l'infection à Campylobacter comprennent:
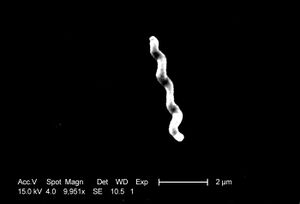
La bactérie Campylobacter est une tige à Gram négatif mobile en forme de tire-bouchon. Ils varient en taille de 0,5 à 5 microns de longueur sur 0,2 à 0,9 microns de largeur. Alors qu'il existe des dizaines d'espèces, 3 représentent les principales sources d'infection humaine: Campylobacter jejuni, Campylobacter coli et Campylobacter lari. C. jejuni est l'espèce la plus souvent impliquée. [1][2]
Des études contrôlées par des volontaires ont mis en évidence la virulence relative de Campylobacter. Une infection à des doses aussi faibles que 800 UFC[note 1] peut provoquer des symptômes.[5] Cette virulence met en évidence le besoin de propreté chez ceux qui sont en contact avec des réservoirs d'infection, tels que la volaille, l'eau contaminée et les produits laitiers crus.[2]
Physiopathologie
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | La physiopathologie traite des mécanismes biologiques qui conduisent à l'apparition d'une maladie. |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: | L'histopathologie doit figurer dans la section Examen paraclinique, et non dans la section physiopathologie. |
| Exemple: | Le VIP est une neurohormone composée de 28 acides aminés et appartenant à la famille des sécrétines-glucagon. Il est produit dans le système nerveux central ainsi que dans les neurones des voies gastro-intestinales, respiratoires et urogénitales. Il agit, via l'expression d'adénylate cyclase cellulaire (AMPc), à titre de vasodilatateur et de régulateur de l'activité des muscles lisses, de stimulateur de la sécrétion d'eau et d'électrolytes par le tractus intestinal, d'inhibiteur de la sécrétion d'acide gastrique et de promoteur du flux sanguin principalement dans le tractus gastro-intestinal. L'ensemble de ces éléments peuvent entraîner une hypokaliémie, une hyperglycémie, une hypomagnésémie et une hypercalcémie qui sont habituellement responsables de la présentation clinique. |
Les selles sanglantes et muqueuses sont fréquentes et résultent de l'invasion de l'épithélium par les bactéries de l'intestin. Cela conduit à des lésions inflammatoires et à des lésions muqueuses. Bien que la pathogenèse soit mal comprise, le plasmide pVir est associé à une maladie plus invasive et à une probabilité accrue de diarrhée sanglante.
Présentation clinique
Toute contribution serait appréciée.
| Description: | Cette section contient la sous-section optionnelle Facteurs de risque et les sous-sections obligatoires Questionnaire et Examen clinique. |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: |
|
| Exemple: |
(Aucun texte)
(Texte)
(Texte)
(Texte) |
Facteurs de risque
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section contient les facteurs de risque de la maladie. Ces facteurs de risque peuvent être des maladies, des anomalies génétiques, des caractéristiques individuelles (l'âge, le sexe, l'origine ethnique, un certain type d'alimentation), etc. |
| Formats: | Liste à puces, Tableau |
| Balises sémantiques: | Facteur de risque |
| Commentaires: |
|
| Exemple: | Les facteurs de risque de l'infarctus du myocarde sont :
|
Les patients immunodéprimés et âgés sont les plus à risque de morbidité, de mortalité et de maladie prolongée.
Questionnaire
Toute contribution serait appréciée.
| Description: | Cette section traite des symptômes à rechercher à l'anamnèse (questionnaire). Les symptômes sont ressentis et exprimés par les patients. |
| Formats: | Liste à puces |
| Balises sémantiques: | Symptôme, Élément d'histoire |
| Commentaires: |
|
| Exemple: | Les symptômes de l'infarctus du myocarde sont :
D'autres éléments à rechercher au questionnaire de l'infarctus sont :
Il est parfois pertinent de mentionner des symptômes qui sont absents, comme dans la pharyngite à streptocoque. Les symptômes de la pharyngite à streptocoque sont :
|
L'infection à Campylobacter se manifeste généralement par une entérite avec diarrhée volumineuse (plus de 10 selles par jour peuvent survenir). Les individus peuvent éprouver une phase prodromique des symptômes durant 1 à 3 jours. Les symptômes de la phase prodromique comprennent:
- forte fièvre
Cette phase prodromique est associée à une évolution de la maladie plus sévère. L'apparition des symptômes survient généralement 24 à 72 heures après l'ingestion de la bactérie; bien que cela puisse prendre plus de temps à se développer chez les individus infectés par de plus petites quantités de bactéries. Le pic de maladie dure généralement de 24 à 48 heures. La durée moyenne de la phase diarrhéique aiguë de l'entérite à Campylobacter est d'environ 7 jours. Il n'est pas rare que les symptômes de douleurs abdominales persistent pendant des jours à des semaines après la résolution de la diarrhée.[6][2]
Pendant la phase aiguë de la maladie, les symptômes les plus fréquents sont:
Examen clinique
Toute contribution serait appréciée.
| Description: | Cette section traite des signes à rechercher lors de l'examen clinique. |
| Formats: | Liste à puces |
| Balises sémantiques: | Examen clinique, Signe clinique |
| Commentaires: |
|
| Exemple: | L'examen physique de l'appendicite démontrera les éléments suivants :
|
Examens paracliniques
Toute contribution serait appréciée.
| Description: | Cette section concerne les tests à demander lorsque la maladie est suspectée et les résultats attendus en présence de la maladie. |
| Formats: | Liste à puces, Tableau |
| Balises sémantiques: | Examen paraclinique, Signe paraclinique |
| Commentaires: |
|
| Exemple: | Les examens suivants sont utiles dans la démarche d'investigation du VIPome :
|
- Investigation 1: signe paraclinique 1, signe paraclinique 2, ...
- Investigation 2: signe paraclinique 3, signe paraclinique 4, ...
- ...
La culture de selles, le dosage immunoenzymatique (EIA) ou la PCR peuvent diagnostiquer une infection à Campylobacter. Pour une culture de selles, des colonies d'espèces de Campylobacter sont cultivées en utilisant des techniques de culture sélectives conçues pour améliorer l'isolement de C. coli et C. jejuni. C. jejuni et C. coli sont thermophiles, se développent mieux à 42 degrés Celsius et sont microaérophiles, poussant mieux dans un environnement contenant 5% à 10% d'oxygène.[3] L'EIA et la PCR ont montré une sensibilité accrue par rapport à la culture de selles. Les développements utilisant la réaction de transcription inverse-polymérase en chaîne (RT-PCR), ont permis le développement de tests plus sensibles pour le dépistage de sources alimentaires potentiellement infectées. [7][2]
Approche clinique
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Alors que les sections Questionnaire, Examen clinique et Examens paracliniques servent à énumérer, cette section sert à intégrer tous ces éléments pour discuter du raisonnement du clinicien. C'est en quelque sorte la manière dont les cliniciens réfléchissent lorsque confrontés à cette maladie : c'est la section par excellence pour l'enseignement. |
| Formats: | Texte, Liste à puces, Tableau |
| Balises sémantiques: | |
| Commentaires: |
|
| Exemple: | |
Diagnostic
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section traite de la manière dont on peut diagnostiquer une maladie en tenant compte de l'histoire, de l'examen clinique et des investigations. C'est dans cette section que se retrouveront les critères permettant d'infirmer ou de confirmer la présence de la maladie (lorsqu'ils existent). |
| Formats: | Texte, Liste à puces, Tableau |
| Balises sémantiques: | |
| Commentaires: |
|
| Exemple: | L'asystolie est un diagnostic électrocardiographique. L'absence d'activité électrique chez un patient inconscient sans pouls permet de confirmer le diagnostic, tout en s'assurant qu'il n'y a pas de cable débranché et que la calibration du moniteur est adéquate.
Selon le Fourth Universal Definition of Myocardial Infarction, l'infarctus aigu du myocarde est diagnostiqué lorsqu'il y a :
|
Diagnostic différentiel
Toute contribution serait appréciée.
| Description: | Cette section traite du diagnostic différentiel de la maladie, c'est-à-dire aux autres diagnostics à évoquer lorsque confronté à ce diagnostic. |
| Formats: | Liste à puces |
| Balises sémantiques: | Diagnostic différentiel |
| Commentaires: |
|
| Exemple: | Le diagnostic différentiel de l'appendicite comprend :
|
- Diagnostic différentiel 1
- Diagnostic différentiel 2
- Diagnostic différentiel 3
- Appendicite
- Iléocolite aigue
Le diagnostic différentiel comprend d'autres sources de diarrhée bactérienne infectieuse telles que Salmonella, Shigella, Escherichia coli, Listeria et Clostridium difficile. Une gastro-entérite virale telle que le norovirus peut également se présenter de manière similaire.[8] Une intoxication alimentaire à médiation toxique peut présenter des symptômes similaires. Les causes parasitaires de diarrhée, y compris Giardia lamblia, Cryptosporidium parvum et Entamoeba histolytica, peuvent provoquer une diarrhée prolongée chez les voyageurs et les patients immunodéprimés imitant Campylobacter.[9][2]
La douleur abdominale de Campylobacter peut imiter l'appendicite et nécessiter une imagerie avancée telle qu'une échographie, une tomodensitométrie ou une IRM pour se différencier. La maladie inflammatoire de l'intestin, la maladie de Crohn et la colite ulcéreuse, peut également se manifester par des douleurs abdominales et des selles sanglantes. La culture de selles, l'imagerie diagnostique, la biopsie et la coloscopie permettent de diagnostiquer ces maladies chroniques.[10][2]
Traitement
Toute contribution serait appréciée.
| Description: | Cette section décrit le traitement de la maladie. |
| Formats: | Liste à puces, Tableau, Texte |
| Balises sémantiques: | Traitement, Traitement pharmacologique |
| Commentaires: |
|
| Exemple: | |
L'infection par Campylobacter est généralement spontanément résolutive et légère. Les interventions chez les patients en bonne santé sont axées sur l'hydratation et la reconstitution des électrolytes. L'hydratation peut être orale ou parentérale selon la gravité de la maladie et le degré de déshydratation. Évitez les agents anti-motilité car ils peuvent entraver la résolution de l'infection.[11] Les antibiotiques ne sont pas un pilier du traitement chez les patients en bonne santé. Envisagez des antibiotiques pour les patients à haut risque tels que les immunodéprimés et les personnes âgées. Les personnes atteintes d'une maladie plus grave comme de la fièvre, des selles sanglantes ou des douleurs abdominales sévères peuvent également justifier des antibiotiques. Les patients immunodéprimés peuvent nécessiter plusieurs cycles d'antibiotiques.[12][2]
Les infections à Campylobacter sont mieux traitées avec des antibiotiques macrolides.[13] Cela est dû aux multiples schémas de résistance aux antibiotiques apparus ces dernières années. On pense que l'utilisation d'antibiotiques chez les animaux d'élevage est la source de souches résistantes. Les souches de Campylobacter au Canada présentaient auparavant une résistance de 8,6% aux tétracyclines en 1981; ce taux est passé à 56% dans des études plus récentes.[14] Un profil de résistance significatif à la thérapie aux fluoroquinolones est apparu. Alors qu'au début des années 1990, il n'y avait presque pas de résistance aux fluoroquinolones décrite dans la littérature, des données plus récentes aux États-Unis montrent une résistance aux fluoroquinolones de 40% sur un site de la région de Pennsylvanie. % aux États-Unis, on s'inquiète du développement éventuel de souches résistantes.[15] Les patients qui échouent à une antibiothérapie nécessitent des tests de sensibilité aux médicaments. Les recherches suggèrent que l'émergence de souches résistantes provient de l'utilisation généralisée d'antibiotiques chez les animaux d'élevage. Le plaidoyer pour une utilisation judicieuse des antibiotiques dans les environnements agricoles à grande échelle s'est intensifié dans les efforts de contrôle de la résistance aux antibiotiques.[16][2]
Suivi
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section traite du suivi de la maladie. |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: |
|
| Exemple: | |
Complications
Toute contribution serait appréciée.
| Description: | Cette section traite des complications possibles de la maladie. |
| Formats: | Liste à puces, Texte |
| Balises sémantiques: | Complication |
| Commentaires: |
|
| Exemple: | Les complications de l'infarctus du myocarde sont :
|
Il existe de nombreuses complications médicales associées à l'infection à Campylobacter, dont beaucoup ont un pronostic pire que l'infection aiguë elle-même. Les infections à Campylobacter peuvent provoquer des maladies extra-intestinales touchant les systèmes neurologique, pulmonaire, immunologique et cardiaque. [2]
En 1859, le scientifique français Jean-Baptiste Octave Landry a signalé pour la première fois la maladie connue aujourd'hui sous le nom de syndrome de Guillain-Barré (SGB). Le SGB est une maladie auto-immune qui présente une paralysie flasque ascendante symétrique due à la démyélinisation des nerfs périphériques. Ce n'est qu'au 20e siècle qu'une forte association entre GBS et Campylobacter a été établie. Aujourd'hui, on estime que Campylobacter, en particulier C. jejuni, provoque environ 30% de tous les SGB. Environ 1 personne sur 1000 infectée par Campylobacter développera le SGB. Il survient 1 à 3 semaines après l'infection par Campylobacter. On pense que le mécanisme de la maladie auto-immune se fait par mimétisme moléculaire créant des auto-anticorps qui réagissent avec les nerfs périphériques. L'évolution clinique de ceux qui souffrent de SGB varie. Environ 20% des patients atteints de SGB ont une évolution clinique compliquée nécessitant des soins intensifs prolongés. Malgré les progrès réalisés dans la prise en charge des soins intensifs du SGB, sa mortalité se situe entre 3% et 7% .[7][2]
Des rapports de cas ont émergé de myocardite et de péricardite associées à Campylobacter. Ceci est le plus souvent décrit chez les hommes jeunes et en bonne santé ayant des antécédents de maladie diarrhéique associée aux voyages. Les patients peuvent présenter des symptômes allant d'un léger inconfort thoracique à une douleur intense qui imite un infarctus du myocarde. Les tests en laboratoire montrent souvent des taux élevés de troponine, de CK, de BNP et de CRP. Des niveaux accrus de troponine T ont été associés à un pire pronostic. Cependant, une valeur normale n'exclut pas le diagnostic de myocardite. L'échocardiographie est utilisée pour identifier les épanchements péricardiques associés et les anomalies du mouvement de la paroi associées à l'affection. Chez la plupart des patients, l'évolution clinique des symptômes et des résultats est bénigne. Environ 30% des personnes atteintes développent une cardiomyopathie dilatée. Dans les cas graves, des arythmies menaçant le pronostic vital et un collapsus cardiovasculaire nécessitant une oxygénation extracorporelle de la membrane (ECMO) ont été décrits.[17][2]
Environ 1% à 5% des patients souffriront d'arthrite réactive aiguë avec une incidence annuelle de 4,3 pour 100 000. Les jeunes adultes sont le groupe le plus souvent touché. C. jejuni et C. coli sont tous deux associés à la maladie. Les symptômes commencent dans les 4 semaines suivant l'infection aiguë et les symptômes prédominants sont une inflammation articulaire stérile. Les symptômes varient d'une oligo-arthralgie légère à une polyarthrite invalidante. Les symptômes musculo-squelettiques sont la présentation la plus courante, bien que les patients puissent également présenter des symptômes oculaires, dermatologiques et urinaires. Alors que les symptômes affectent le plus souvent les genoux et les chevilles, une atteinte des petites articulations et des tendons est également observée. La durée des symptômes de l'arthrite réactive aiguë est variable. Les patients peuvent présenter des symptômes qui durent de plusieurs mois à un an. Il n'y a pas d'association avec HLA B27 au niveau de la population. [18][19][2]
Dans le système gastro-intestinal (GI), il y a eu une association accrue de maladies œsophagiennes et colorectales avec les infections à Campylobacter. Dans la phase aiguë de la maladie, des infections sévères peuvent se manifester par une colite qui peut entraîner une morbidité importante nécessitant parfois une intervention chirurgicale. Le mégacôlon toxique est une complication rare de la colite à Campylobacter et doit être envisagé chez les patients gravement malades. Les patients qui développent un mégacôlon toxique ont une morbidité et une mortalité élevées en dépit des interventions.[20][2]
Plusieurs autres manifestations gastro-entérologiques sont associées à Campylobacter, notamment le reflux gastro-œsophagien (RGO), l'œsophage de Barrett (BE) et l'adénocarcinome de l'œsophage. La recherche a également montré qu'il existe un risque accru de carcinome colorectal et de maladie du côlon irritable suite à des infections à Campylobacter.[21][2]
Une forme de lymphome, la maladie immunoproliférative du petit intestin, a montré une association avec les infections à Campylobacter. Des échantillons de biopsie plusieurs patients ont noté la présence de C. jejuni et un traitement antimicrobien ciblant cet organisme a conduit à la rémission rapide de la maladie immunoproliférative du petit intestin. [22][2]
Évolution
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section contient le pronostic et évolution naturelle de la maladie. Le pronostic est lié à la survie du patient atteint de la maladie. L'évolution naturelle est la manière dont évoluera la maladie du patient dans le temps. |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: | |
| Exemple: | La dissection aortique est associée une mortalité très élevée. Au moins 30% des patients décèdent après leur arrivée à l'urgence, et ce, même après une intervention chirurgicale. Pour ceux qui survivent à la chirurgie, la morbidité est également très élevée et la qualité de vie est mauvaise. La mortalité la plus élevée d'une dissection aortique aiguë est dans les 10 premiers jours. Les patients qui ont une dissection chronique ont tendance à avoir un meilleur pronostic, mais leur espérance de vie est raccourcie par rapport à la population générale.[1] Sans traitement, la mortalité est de 1 à 3% par heure au cours des 24 premières heures, 30% à une semaine, 80% à deux semaines et 90% à un an. |
La mortalité globale pour l'infection à Campylobacter est de 24 pour 10 000 cas confirmés par culture. Chez les patients en bonne santé, les infections à Campylobacter ont une évolution auto-limitée avec d'excellents résultats cliniques. Ces patients nécessitent des soins de soutien tels que la replétion électrolytique, la réhydratation orale et parentérale. Les antibiotiques doivent être envisagés chez les patients immunodéprimés et ceux présentant de la fièvre, une diarrhée sanglante, de nombreuses selles ou une aggravation des symptômes. Environ 10,8% des patients nécessitent une hospitalisation, ce qui en fait la troisième cause d'hospitalisation pour gastro-entérite. Les patients immunodéprimés et âgés présentent les risques les plus élevés de maladie prolongée et mortelle. La plupart des patients connaissent une résolution de la maladie sans complications.[12][2]
Moins de 1% des patients présentent une bactériémie transitoire, qui survient au cours de l'infection aiguë. La bactériémie est associée à une mortalité comprise entre 2,5 et 12,5% .[23] Les patients immunodéprimés et les patients âgés sont plus susceptibles de présenter une bactériémie.[24] Les patients VIH / SIDA ont une incidence accrue d'infection par Campylobacter et une évolution plus virulente. Ces patients peuvent nécessiter plusieurs doses d'antibiothérapie. Ils sont plus susceptibles de présenter des symptômes extra-intestinaux et d'avoir une mortalité plus élevée. [25][2]
Prévention
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section traite des mesures préventives et du dépistage précoce de la maladie (lorsque pertinent). |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: | |
| Exemple: | La prévention primaire consiste à la prise en charge des facteurs de risque :
|
Les sources les plus fréquemment signalées d'infections à Campylobacter sont la volaille insuffisamment cuite dans les pays développés et l'eau contaminée dans les pays en développement. S'assurer que la volaille et la viande sont bien cuites à 70 ° C avant l'ingestion réduit le risque d'infection. Le CDC recommande de laver les articles qui entrent en contact avec de la volaille crue. Ils recommandent également des planches à découper séparées pour la viande crue et le nettoyage des ustensiles après leur contact avec la viande crue.[1] Le lait et le fromage non pasteurisés doivent être évités. L'eau non traitée ne doit pas être consommée. Pratiquer une hygiène de base des mains diminue le risque d'infection. [26][2]
Concepts clés
- Campylobacter est l'une des principales causes de maladies d'origine alimentaire dans le monde. C. jejuni est le plus souvent identifié comme étant le coupable le plus courant des infections humaines
- Campylobacter est une espèce robuste de bactéries qui peut survivre dans un large éventail d'environnements. Un petit nombre de bactéries peut provoquer une infection.
- Les personnes les plus exposées au risque d'infection sont les voyageurs internationaux, les personnes qui entrent fréquemment en contact avec le bétail, en particulier la volaille, et les consommateurs d'eau non traitée ou de lait non pasteurisé.
- Cliniquement, l'infection à Campylobacter se manifeste généralement par une diarrhée (parfois sanglante) qui culmine généralement 1 à 2 jours après son apparition. La phase d'entérite aiguë de l'infection est généralement spontanément résolutive et disparaît après 7 jours.
- La culture de selles, PCR ou EIA établit le diagnostic.
- Campylobacter est généralement autolimitant, et certains cas nécessitent un réapprovisionnement en liquide et en électrolytes. Lorsque des antibiotiques sont nécessaires, les macrolides tels que l'azithromycine sont le traitement de choix.
- Il existe de multiples complications liées à l'infection à Campylobacter; plus particulièrement, il existe un associé à l'infection et au syndrome de Guillain-Barré.[2]
Références
- Cette page a été modifiée ou créée le 2020/11/11 à partir de Campylobacter (StatPearls / Campylobacter (2020/08/11)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/30725718 (livre).
- ↑ 1,0 1,1 1,2 et 1,3 Nadeem O. Kaakoush, Natalia Castaño-Rodríguez, Hazel M. Mitchell et Si Ming Man, « Global Epidemiology of Campylobacter Infection », Clinical Microbiology Reviews, vol. 28, no 3, , p. 687–720 (ISSN 1098-6618, PMID 26062576, Central PMCID 4462680, DOI 10.1128/CMR.00006-15, lire en ligne)
- ↑ 2,00 2,01 2,02 2,03 2,04 2,05 2,06 2,07 2,08 2,09 2,10 2,11 2,12 2,13 2,14 2,15 2,16 2,17 2,18 2,19 2,20 et 2,21 Greg H. Fischer et Elizabeth Paterek, StatPearls, StatPearls Publishing, (PMID 30725718, lire en ligne)
- ↑ 3,0 et 3,1 Sharon V. R. Epps, Roger B. Harvey, Michael E. Hume et Timothy D. Phillips, « Foodborne Campylobacter: infections, metabolism, pathogenesis and reservoirs », International Journal of Environmental Research and Public Health, vol. 10, no 12, , p. 6292–6304 (ISSN 1660-4601, PMID 24287853, Central PMCID 3881114, DOI 10.3390/ijerph10126292, lire en ligne)
- ↑ Nompilo Sibanda, Aaron McKenna, Anne Richmond et Steven C. Ricke, « A Review of the Effect of Management Practices on Campylobacter Prevalence in Poultry Farms », Frontiers in Microbiology, vol. 9, , p. 2002 (ISSN 1664-302X, PMID 30197638, Central PMCID 6117471, DOI 10.3389/fmicb.2018.02002, lire en ligne)
- ↑ R. E. Black, M. M. Levine, M. L. Clements et T. P. Hughes, « Experimental Campylobacter jejuni infection in humans », The Journal of Infectious Diseases, vol. 157, no 3, , p. 472–479 (ISSN 0022-1899, PMID 3343522, DOI 10.1093/infdis/157.3.472, lire en ligne)
- ↑ G. Kapperud, J. Lassen, S. M. Ostroff et S. Aasen, « Clinical features of sporadic Campylobacter infections in Norway », Scandinavian Journal of Infectious Diseases, vol. 24, no 6, , p. 741–749 (ISSN 0036-5548, PMID 1287808, DOI 10.3109/00365549209062459, lire en ligne)
- ↑ 7,0 et 7,1 Paolo Bonilauri, Lia Bardasi, Roberto Leonelli et Mattia Ramini, « Detection of Food Hazards in Foods: Comparison of Real Time Polymerase Chain Reaction and Cultural Methods », Italian Journal of Food Safety, vol. 5, no 1, , p. 5641 (ISSN 2239-7132, PMID 27800434, Central PMCID 5076710, DOI 10.4081/ijfs.2016.5641, lire en ligne)
- ↑ P. Rohner, D. Pittet, B. Pepey et T. Nije-Kinge, « Etiological agents of infectious diarrhea: implications for requests for microbial culture », Journal of Clinical Microbiology, vol. 35, no 6, , p. 1427–1432 (ISSN 0095-1137, PMID 9163457, DOI 10.1128/JCM.35.6.1427-1432.1997, lire en ligne)
- ↑ Andrew Slack, « Parasitic causes of prolonged diarrhoea in travellers - diagnosis and management », Australian Family Physician, vol. 41, no 10, , p. 782–786 (ISSN 0300-8495, PMID 23210100, lire en ligne)
- ↑ A. S. Mee, M. Shield et M. Burke, « Campylobacter colitis: differentiation from acute inflammatory bowel disease », Journal of the Royal Society of Medicine, vol. 78, no 3, , p. 217–223 (ISSN 0141-0768, PMID 3973886, Central PMCID 1289637, DOI 10.1177/014107688507800309, lire en ligne)
- ↑ C. M. Nolan, K. E. Johnson, M. B. Coyle et K. Faler, « Campylobacter jejuni enteritis: efficacy of antimicrobial and antimotility drugs », The American Journal of Gastroenterology, vol. 78, no 10, , p. 621–626 (ISSN 0002-9270, PMID 6624735, lire en ligne)
- ↑ 12,0 et 12,1 Guillermo M. Ruiz-Palacios, « The health burden of Campylobacter infection and the impact of antimicrobial resistance: playing chicken », Clinical Infectious Diseases: An Official Publication of the Infectious Diseases Society of America, vol. 44, no 5, , p. 701–703 (ISSN 1537-6591, PMID 17278063, DOI 10.1086/509936, lire en ligne)
- ↑ Taradon Luangtongkum, Byeonghwa Jeon, Jing Han et Paul Plummer, « Antibiotic resistance in Campylobacter: emergence, transmission and persistence », Future Microbiology, vol. 4, no 2, , p. 189–200 (ISSN 1746-0921, PMID 19257846, Central PMCID 2691575, DOI 10.2217/17460913.4.2.189, lire en ligne)
- ↑ Dobryan M. Tracz, Monika Keelan, Jasmine Ahmed-Bentley et Amera Gibreel, « pVir and bloody diarrhea in Campylobacter jejuni enteritis », Emerging Infectious Diseases, vol. 11, no 6, , p. 838–843 (ISSN 1080-6040, PMID 15963277, Central PMCID 3367571, DOI 10.3201/eid1106.041052, lire en ligne)
- ↑ Amita Gupta, Jennifer M. Nelson, Timothy J. Barrett et Robert V. Tauxe, « Antimicrobial resistance among Campylobacter strains, United States, 1997-2001 », Emerging Infectious Diseases, vol. 10, no 6, , p. 1102–1109 (ISSN 1080-6040, PMID 15207064, Central PMCID 3323172, DOI 10.3201/eid1006.030635, lire en ligne)
- ↑ B. M. Allos, « Campylobacter jejuni Infections: update on emerging issues and trends », Clinical Infectious Diseases: An Official Publication of the Infectious Diseases Society of America, vol. 32, no 8, , p. 1201–1206 (ISSN 1058-4838, PMID 11283810, DOI 10.1086/319760, lire en ligne)
- ↑ Faisal Inayat, Nouman Safdar Ali, Iqra Riaz et Hafeez Ul Hasan Virk, « From the Gut to the Heart: Campylobacter jejuni Enteritis Leading to Myopericarditis », Cureus, vol. 9, no 6, , e1326 (ISSN 2168-8184, PMID 28690959, Central PMCID 5501719, DOI 10.7759/cureus.1326, lire en ligne)
- ↑ Janet E. Pope, Adriana Krizova, Amit X. Garg et Heather Thiessen-Philbrook, « Campylobacter reactive arthritis: a systematic review », Seminars in Arthritis and Rheumatism, vol. 37, no 1, , p. 48–55 (ISSN 0049-0172, PMID 17360026, Central PMCID 2909271, DOI 10.1016/j.semarthrit.2006.12.006, lire en ligne)
- ↑ T. Hannu, L. Mattila, H. Rautelin et P. Pelkonen, « Campylobacter-triggered reactive arthritis: a population-based study », Rheumatology (Oxford, England), vol. 41, no 3, , p. 312–318 (ISSN 1462-0324, PMID 11934969, DOI 10.1093/rheumatology/41.3.312, lire en ligne)
- ↑ Michael Kwok, Andrew Maurice, Carl Lisec et Jason Brown, « Campylobacter colitis: Rare cause of toxic megacolon », International Journal of Surgery Case Reports, vol. 27, , p. 141–143 (ISSN 2210-2612, PMID 27614338, Central PMCID 5018068, DOI 10.1016/j.ijscr.2016.08.030, lire en ligne)
- ↑ Sandra Macfarlane, Elizabeth Furrie, George T. Macfarlane et John F. Dillon, « Microbial colonization of the upper gastrointestinal tract in patients with Barrett's esophagus », Clinical Infectious Diseases: An Official Publication of the Infectious Diseases Society of America, vol. 45, no 1, , p. 29–38 (ISSN 1537-6591, PMID 17554697, DOI 10.1086/518578, lire en ligne)
- ↑ Marc Lecuit, Eric Abachin, Antoine Martin et Claire Poyart, « Immunoproliferative small intestinal disease associated with Campylobacter jejuni », The New England Journal of Medicine, vol. 350, no 3, , p. 239–248 (ISSN 1533-4406, PMID 14724303, DOI 10.1056/NEJMoa031887, lire en ligne)
- ↑ H. Nielsen, K. K. Hansen, K. O. Gradel et B. Kristensen, « Bacteraemia as a result of Campylobacter species: a population-based study of epidemiology and clinical risk factors », Clinical Microbiology and Infection: The Official Publication of the European Society of Clinical Microbiology and Infectious Diseases, vol. 16, no 1, , p. 57–61 (ISSN 1469-0691, PMID 19673969, DOI 10.1111/j.1469-0691.2009.02900.x, lire en ligne)
- ↑ Jérôme Pacanowski, Valérie Lalande, Karine Lacombe et Cherif Boudraa, « Campylobacter bacteremia: clinical features and factors associated with fatal outcome », Clinical Infectious Diseases: An Official Publication of the Infectious Diseases Society of America, vol. 47, no 6, , p. 790–796 (ISSN 1537-6591, PMID 18699745, DOI 10.1086/591530, lire en ligne)
- ↑ W. Tee et A. Mijch, « Campylobacter jejuni bacteremia in human immunodeficiency virus (HIV)-infected and non-HIV-infected patients: comparison of clinical features and review », Clinical Infectious Diseases: An Official Publication of the Infectious Diseases Society of America, vol. 26, no 1, , p. 91–96 (ISSN 1058-4838, PMID 9455515, DOI 10.1086/516263, lire en ligne)
- ↑ A. Facciolà, R. Riso, E. Avventuroso et G. Visalli, « Campylobacter: from microbiology to prevention », Journal of Preventive Medicine and Hygiene, vol. 58, no 2, , E79–E92 (ISSN 1121-2233, PMID 28900347, Central PMCID 5584092, lire en ligne)
- ↑ Unité formant colonie
