Dissection aortique
| Maladie | |
| Caractéristiques | |
|---|---|
| Signes | Faiblesse musculaire, Paresthésie, Tamponnade cardiaque, Altération de l'état de conscience , Syncope , Masse pulsatile, Insuffisance aortique, Tension artérielle différentielle augmentée, Signes neurologiques focaux , Enrouement de la voix, ... [+] |
| Symptômes |
Douleur thoracique sévère, Douleur thoracique à début soudain, Douleur thoracique déchirante, Douleur thoracique transfixiante, Douleur thoracique antérieure |
| Diagnostic différentiel |
Embolie pulmonaire, Pneumothorax, Anévrismes de l'aorte, Spasme oesophagien, Syndrome coronarien aigu, Accident ischémique transitoire, Accident vasculaire cérébral, Tamponnade cardiaque, Rupture de l'œsophage, Pancréatite aiguë, ... [+] |
| Informations | |
| Wikidata ID | Q594660 |
|
| |
Toute contribution serait appréciée.
| Description: | Cette section contient la définition du concept et devrait se résumer à quelques phrases au maximum : il ne s'agit pas d'une introduction. S'il existe des pages alternatives ou des nuances qui seraient susceptibles d'intéresser le lecteur, elles seront mentionnées dans cette section avec des liens. Le format attendu est le texte. |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: | Une erreur fréquente est de mettre des signes, des symptômes et le traitement dans l'introduction. Dans un soucis de concision, et considérant que votre page sera consultée autant sur ordinateur que sur les téléphones intelligents, la définition sert à définir à la manière d'un dictionnaire. |
| Exemple: | L'appendicite est l'inflammation et l'infection de l'appendice. |
Bien que peu commune, la dissection aortique aiguë (DAA) est une maladie rare, mais catastrophique. Elle est due à la séparation des couches de la paroi aortique. Une déchirure dans la couche intimale entraîne la progression de la dissection (proximale ou rétrograde) principalement en raison de l'entrée de sang entre l'intima et la média. La DAA est associée à un taux de mortalité très élevé; la majorité des patients décèdent avant même d'arriver aux urgences. Les patients ayant une dissection aortique chronique (plus de deux semaines) ont un pronostic légèrement meilleur. [1]
Épidémiologie
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section contient les données épidémiologiques sur la maladie (ex. incidence, prévalence, coûts en hospitalisation, proportion d'hommes-femmes, régions où la prévalence est plus élevée, etc.). Chaque donnée épidémiologique doit être appuyée par une référence. Idéalement, des statistiques canadiennes et québécoises sont mentionnées lorsque disponibles. |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: | Les facteurs de risque ne sont pas présentés ici, mais bien dans la sous-section Facteurs de risque (Présentation clinique). Le pronostic et l'évolution naturelle de la maladie sont décrits dans la section Évolution. |
| Exemple: | La FRP est une maladie relativement rare qui affecte le plus souvent les patients âgés de 40 à 60 ans. Une prédominance masculine est observée avec un ratio H : F estimé à environ 2:1 ou 3:1. L'incidence de la FRP est inconnue, mais est estimée à 1 pour 200 000 à 500 000 par an. |
L'incidence de la dissection aortique serait de 5 à 30 cas pour 1 million de personnes par an. En ce qui concerne les présentations aux urgences, trois DAA sont diagnostiquées sur 1000 patients présentant des douleurs aiguës au dos, à la poitrine ou à l'abdomen. L'âge est un facteur de risque pour environ 75% des dissections aortiques survenant chez des patients âgés de 40 à 70 ans, la majorité se produisant entre 50 et 65 ans. L'AAD est trois fois plus fréquente chez les hommes que chez les femmes, bien que les femmes aient tendance à se présenter plus tard et à connaître de pires résultats.[1]
Différences entre les patients plus âgés et plus jeunes se présentant avec une dissection de l'aorte ascendante:
Patients adultes plus âgés:
- Plus susceptibles de présenter:
- Une athérosclérose
- Un anévrisme aortique antérieur
- Une dissection iatrogène
- Un hématome intramural.
Patients plus jeunes:
- Moins susceptibles d'antécédents d'hypertension
- Plus susceptible de trouble de tissu conjonctif comme le syndrome de Marfan.
Étiologies
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section décrit les étiologies de la maladie, c'est-à-dire ce qui cause la maladie (ex. le diabète de type 2 cause la néphropathie diabétique). Les étiologies doivent être identifiées avec le modèle Étiologies. |
| Formats: | Texte, Liste à puces, Tableau |
| Balises sémantiques: | Étiologie |
| Commentaires: |
|
| Exemple: | Parmi les étiologies les plus courantes d'occlusion de l'intestin grêle, on retrouve :
|

Les causes les plus courantes de la dissection aortique aiguë sont:
- Hypertension (76%)
- L'athérosclérose (27%)
- Une altération préexistante de la média aortique, histoire de chirurgie cardiaque (16%)
- Anévrysme aortique (16%)
- Un trouble du tissu conjonctif (acquis, congénital ou héréditaire) (5%)
- Traumatique
- Usage de cocaïne (1,8%)
- Iatrogénique (4) [2]
Physiopathologie
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | La physiopathologie traite des mécanismes biologiques qui conduisent à l'apparition d'une maladie. |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: | L'histopathologie doit figurer dans la section Examen paraclinique, et non dans la section physiopathologie. |
| Exemple: | Le VIP est une neurohormone composée de 28 acides aminés et appartenant à la famille des sécrétines-glucagon. Il est produit dans le système nerveux central ainsi que dans les neurones des voies gastro-intestinales, respiratoires et urogénitales. Il agit, via l'expression d'adénylate cyclase cellulaire (AMPc), à titre de vasodilatateur et de régulateur de l'activité des muscles lisses, de stimulateur de la sécrétion d'eau et d'électrolytes par le tractus intestinal, d'inhibiteur de la sécrétion d'acide gastrique et de promoteur du flux sanguin principalement dans le tractus gastro-intestinal. L'ensemble de ces éléments peuvent entraîner une hypokaliémie, une hyperglycémie, une hypomagnésémie et une hypercalcémie qui sont habituellement responsables de la présentation clinique. |

La paroi aortique se compose de trois couches: l'intima, les médias et l'adventice. Une exposition constante à une pression pulsatile élevée et à une contrainte de cisaillement entraîne un affaiblissement de la paroi aortique chez les patients sensibles, pouvant provoquer une déchirure intimale. Suite à cette déchirure, le sang coule dans l'espace intima-médiatique, créant une fausse lumière. La plupart de ces déchirures ont lieu dans l'aorte ascendante, généralement dans la paroi latérale droite où se produit la plus grande force de cisaillement sur l'aorte. Une DAA peut se propager antérograde et / ou rétrograde et, selon la direction de la dissection, provoquer une obstruction de la branche qui produit une ischémie du territoire affecté (coronaire, cérébral, rachidien ou viscéral). Pour les dissections proximales de type A, elles peuvent provoquer une tamponnade aiguë, une insuffisance aortique ou une rupture aortique. [3][1]
Dans une dissection aortique aiguë, la vraie lumière est bordée par l'intima tandis que la fausse lumière est dans la média. Dans la plupart des cas, la vrai lumière est plus petite que la fausse. Souvent, le sang circulant à travers la fausse lumière conduit au développement d'un anévrisme avec un potentiel de rupture. Les trois sites communs pour une DAA sont les suivants: [1]
- Près de 2 à 2,5 cm au-dessus de la racine aortique (le site le plus courant)
- Juste en distal de l'origine de l'artère sous-clavière gauche
- Dans l'arc aortique [1]
Présentation clinique
Toute contribution serait appréciée.
| Description: | Cette section contient la sous-section optionnelle Facteurs de risque et les sous-sections obligatoires Questionnaire et Examen clinique. |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: |
|
| Exemple: |
(Aucun texte)
(Texte)
(Texte)
(Texte) |
Facteurs de risque
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section contient les facteurs de risque de la maladie. Ces facteurs de risque peuvent être des maladies, des anomalies génétiques, des caractéristiques individuelles (l'âge, le sexe, l'origine ethnique, un certain type d'alimentation), etc. |
| Formats: | Liste à puces, Tableau |
| Balises sémantiques: | Facteur de risque |
| Commentaires: |
|
| Exemple: | Les facteurs de risque de l'infarctus du myocarde sont :
|
Les facteurs à haut risque prédisposant à la dissection aortique non traumatique comprennent: [1]
- Hypertension (survient chez 70% des patients atteints de DAA distale de Standford de type B)
- Une augmentation brutale, transitoire et sévère de la pression artérielle (par exemple, une musculation intense et l'utilisation d'agents sympathomimétiques tels que la cocaïne, l'ecstasy ou les boissons énergisantes)
- Affections génétiques incluant le syndrome de Marfan (présent chez 50% des moins de 40 ans, contre seulement 2% des patients plus âgés), le syndrome d'Ehlers-Danlos, le syndrome de Turner et le syndrome de Loeys-Dietz.
- La Valve aortique bicuspide,
- La Coarctation de l'aorte.
- Anévrisme aortique préexistant, ou histoire familiale de dissection aortique
- Athérosclérose
- Grossesse et accouchement (risque aggravé chez les femmes enceintes atteintes de troubles du tissu conjonctif tels que le syndrome de Marfan)
- Instrumentation ou chirurgie aortique (pontage coronarien, remplacement de la valve aortique ou mitrale et pose d'un stent percutané ou insertion d'un cathéter)
- Maladies inflammatoires ou infectieuses à l'origine de vascularites (syphilis, consommation de cocaïne) [1]
Questionnaire
Toute contribution serait appréciée.
| Description: | Cette section traite des symptômes à rechercher à l'anamnèse (questionnaire). Les symptômes sont ressentis et exprimés par les patients. |
| Formats: | Liste à puces |
| Balises sémantiques: | Symptôme, Élément d'histoire |
| Commentaires: |
|
| Exemple: | Les symptômes de l'infarctus du myocarde sont :
D'autres éléments à rechercher au questionnaire de l'infarctus sont :
Il est parfois pertinent de mentionner des symptômes qui sont absents, comme dans la pharyngite à streptocoque. Les symptômes de la pharyngite à streptocoque sont :
|
À son arrivée à l'hôpital, le patient doit être questionné sur trois aspects fondamentaux de sa douleur, c'est-à-dire la qualité, l'irradiation et l'intensité de sa douleur initiale. Classiquement, la dissection aortique aiguë se présente de façon suivante :
- Début brutal des douleurs thoraciques
- Douleurs maximales
- Nature déchirante
- Douleur localisée dans la poitrine antérieure, si la dissection est plus ascendante,
- Irradiant vers le dos, si la dissection est descendante.
Diverses études ont identifié l'intensité d'apparition de la douleur comme le facteur historique le plus fiable. Il peut y avoir un caractère migrateur, car la dissection se propage caudalement. [1] La présentation de la DAA représente l'ampleur de la dissection, avec des plaintes correspondant aux structures cardiovasculaires touchées. Chez environ 10% des patients, la DAA est indolore, ce qui est plus fréquent rencontré chez les patients présentant un syndrome de Marfan.
La présence de douleurs thoraciques accompagnées de signes neurologiques, la combinaison de douleurs thoraciques et abdominales, ou encore la présence de douleurs thoraciques accompagnées d'une faiblesse des membres ou d'une paresthésie doivent alerter le clinicien sur la possibilité d'une DAA. En effet, au moment de la présentation, des déficits neurologiques sont présents chez 20% des patients. La syncope est également fréquente et peut être due à une hypovolémie, des arythmies, un infarctus du myocarde ou une augmentation du tonus vagal. Si la dissection est antérograde, elle peut impliquer les vaisseaux des extrémités entraînant une perte de pouls, des paresthésies et de la douleur.[1] Les médecins soupçonnent correctement le diagnostic de DAA dans aussi peu que 15% à 43% des cas de DAA vérifiés. Si elle n'est pas traitée, la mortalité approche les 50% dans les 48 premières heures suivant son apparition. Malgré une abondance de littérature, un nombre important de dissections aortiques sont manquées au service des urgences.[4][5][6][1]
| Probabilité de Dissection Aortique[7][8] | ||
|---|---|---|
| Symptômes positifs (présents chez le patient) |  | |
| Augmentation de probabilité de la maladie | ||
| Symptômes | ||
| Douleurs déchirantes
Douleurs irradiées Douleurs thoraciques soudaines Histoire d'hypertension |
10,8x
7,6x 2,6x 1,5x | |
| Signes cliniques à l'examen physique | ||
| Déficit neurologique focal
Souffle cardiaque diastolique Différence de pouls |
33x
4.9x 2,7x | |
| Résultats laboratoires | ||
| Aorte ou médiastin élargis
Hypertrophie ventriculaire gauche à l'ECG |
3,4
3,2 | |
| Symptômes négatifs (absents chez le patient) | ||
| Diminution de probabilités de la maladie | ||
| Symptômes | ||
| Douleurs thoraciques soudaines
Histoire d'hypertension Douleurs déchirantes Douleurs irradiées. |
0,3x
0,4x 0,4x 0,6x | |
| Signes cliniques à l'examen physique | ||
| Déficit neurologique focal
Souffle cardiaque diastolique Différence de pouls |
0,87x
1,1x 0,63x | |
| Résultats laboratoires | ||
| Aorte ou médiastin élargis
Hypertrophie ventriculaire gauche à l'ECG |
0,13x
0,84x | |
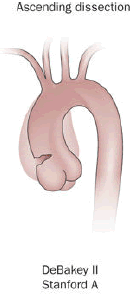
Il existe deux principales classifications anatomiques utilisées pour classifier la dissection aortique: [1]
Le système de Stanford est plus fréquemment utilisé. Il classe les dissections aortiques en deux types selon que la partie ascendante ou descendante de l'aorte est impliquée. [1]
- Le type A concerne l'aorte ascendante, quel que soit le site de la déchirure intimale primaire. La dissection de type A est définie comme une dissection proximale à l'artère brachiocéphalique.
- Le type B concerne une dissection partant de l'artère sous-clavière gauche et n'impliquant que l'aorte descendante.[1]
La classification DeBakey est basée sur le site d'origine de la dissection.[1]
- Le type 1 provient de l'aorte ascendante et au moins de l'arc aortique.
- Le type 2 provient et est limité à l'aorte ascendante.
- Le type 3 commence dans l'aorte descendante et s'étend distalement au-dessus du diaphragme (type 3a) ou en dessous du diaphragme (type 3b) .[1]
Les dissections aortiques ascendantes sont presque deux fois plus fréquentes que les dissections descendantes.[9][1] 67% des DAA sont de type A selon la classification de Stanford contre 33% de type B.
Examen clinique
Toute contribution serait appréciée.
| Description: | Cette section traite des signes à rechercher lors de l'examen clinique. |
| Formats: | Liste à puces |
| Balises sémantiques: | Examen clinique, Signe clinique |
| Commentaires: |
|
| Exemple: | L'examen physique de l'appendicite démontrera les éléments suivants :
|
Certains signes physiques associés sont classiquement cités, mais présents dans moins de 50% des cas confirmés de DAA. L'hypertension est très courante dans la DAA. Si le patient présente une hypotension, il s'agit d'un signe grave indiquant très probablement une rupture. Une différence de tension artérielle de plus de 20 mmHg entre les bras devrait éveiller la suspicion d'une dissection aortique. Les autres caractéristiques comprennent: [1]
- Une masse pulsatile palpable sur l'abdomen
- Une insuffisance aortique
- Un souffle / murmure diastolique
- Des bruits cardiaques étouffés (suggérant une tamponnade cardiaque)
- Une syncope
- Un état mental altéré
- Une perte des pouls périphériques
- Un Syndrome de Horner [1]
- Un enrouement de la voix
Examens paraclinique
Toute contribution serait appréciée.
| Description: | Cette section concerne les tests à demander lorsque la maladie est suspectée et les résultats attendus en présence de la maladie. |
| Formats: | Liste à puces, Tableau |
| Balises sémantiques: | Examen paraclinique, Signe paraclinique |
| Commentaires: |
|
| Exemple: | Les examens suivants sont utiles dans la démarche d'investigation du VIPome :
|
Des études de routine comme un ECG et une radiographie thoracique peuvent aider à différencier d'autres causes possibles de douleurs thoraciques, mais peuvent être trompeuses. Un ECG à 12 dérivations est obligatoire pour exclure un MI.[1]
La confirmation de la DAA nécessite une imagerie cardiovasculaire pour identifier la présence d'une déchirure intimale, établir la classification de Stanford et détecter une atteinte valvulaire ou de branche. La plupart des directives recommandent soit l'aortographie par tomodensitométrie, soit l'échocardiographie transoesophagienne (ETO) pour le diagnostic de la DAA. Le choix de la modalité à utiliser comme écran de première ligne doit être basé sur la disponibilité et l'expertise institutionnelles. Pour la plupart des services des urgences (SU), l'angiographie par tomodensitométrie sera probablement la première technique d'imagerie avancée en raison de sa large disponibilité.[10][1]
Les analyses de sang doivent inclure la FSC, les électrolytes, la troponine, le D-dimère et la fonction rénale.
La radiographie thoracique peut montrer un médiastin élargi (> 8 cm) ou une collection de liquide dans l'hémithorax en raison d'une rupture. Les caractéristiques de radiographie suggérant la DAA comprennent: [1]
- Cap apical gauche
- Épanchement pleural
- Déviation de l'œsophage
- Déviation de la trachée vers la droite
- Dépression de la bronche principale gauche
- Perte de la bande paratrachéale [1]
Si le patient est stable, un Angio-TDM est recommandé. Le scanner en spirale peut détecter rapidement l'emplacement de la déchirure intimale et aider le chirurgien à planifier la procédure. Les résultats suggérés par la DAA incluent: [1]
- Volet de dissection intimale
- Double lumière
- Dilatation aortique et hématome
- Régions de malperfusion
- Une fuite de contraste indique une rupture aortique [1]
L'échocardiographie est également une modalité utile pour détecter la DAA. L'EDU est la technique préférée qui peut être pratiquée au chevet du patient et utilisée pour la visualisation peropératoire. [1]
- Volet de dissection avec flux Doppler différentiel
- Vraie et fausse lumière dans l'aorte ascendante
- Thrombose dans la fausse lumière
- Déplacement central de la calcification intimale
- Épanchement péricardique [1]
Histopathologie
La dissection aortique est un processus aigu dans lequel une déchirure de la face interne de l'aorte conduit à une dissection à travers les laminas et à la formation d'une nouvelle lumière (fausse lumière) et à une chute aiguë de la pression artérielle systémique, pouvant conduire à l'hémopéricarde et à la tamponnade cardiaque [11] avec mort subite. C'est le point final d'un long processus de blessure et de réparation dans la paroi aortique, généralement dû à des forces hémodynamiques telles que l'hypertension systémique chronique. La déchirure dissèque généralement les médias en deux parties, formant une lumière entre l'intima-média et la média-adventice. La dissection dans le tiers externe des médias [12] est plus courante dans ce contexte. Par conséquent, la fragilité de cette couche a diminué la distensibilité aortique et a un potentiel de dissection aortique.[1]
La couche médiatique est formée de cellules musculaires lisses, de fibres élastiques, de fibres de collagène et d'acide hyaluronique. Chacun de ces composants peut être altéré et affaiblir la structure conduisant à un vaisseau moins résistant. Certains changements histologiques sont énumérés ici:
- Matrice extracellulaire: l'accumulation mucoïde qui augmente l'espace intralamellaire ou translamellaire, créant la soi-disant «dégénérescence kystique» du milieu qui diminue la résistance des vaisseaux. Le principal composant de l'accumulation de mucine est la chondroïtine-6-sulfate [13].
- Altération des fibres élastiques: fragmentation, amincissement, désorganisation. Une aorte normale a un maillage dense de fibres élastiques qui contribuent substantiellement à sa résistance à la pression artérielle. La fragmentation des fibres élastiques étend les espaces translamellaires en diminuant l'élasticité de l'aorte. L'amincissement élargit les espaces intralamellaires. La désorganisation fait référence à la disposition non parallèle de fibres qui sont disposées au hasard d'une manière non fonctionnelle.
- Cellules musculaires lisses altérées: perte nucléaire, désorganisation. La perte de cellules nucléaires, dite «nécrose des cellules musculaires lisses» peut apparaître en bandes ou en larges zones où seuls les contours des cellules fantômes sont visibles. Le trouble des cellules musculaires lisses peut être focal ou nodulaire.
- Effondrement médial laminaire: l'effondrement des fibres élastiques représente ce que l'on appelle la «nécrose médiale laminaire» et s'accompagne d'une perte significative de cellules musculaires lisses interposées.
- Fibres de collagène: fibrose. Il s'agit du processus le moins courant dans les maladies dégénératives de l'aorte.[1]
Ces résultats sont généralement associés les uns aux autres et doivent être reconnus pour classer avec précision la dégénérescence médiale (comme légère / modérée / sévère) à partir de la gravité et de la distribution des lésions dégénératives [14][15].[1]
Vasa Vasorum[1]
Le vasa vasorum est un réseau vasculaire distribué autour des couches externes du média et de l'adventice de l'aorte. Son rôle est crucial dans le maintien de l'apport en oxygène et en nutriments de l'aorte elle-même. Une efficacité vasculaire réduite du vasa vasorum entraîne une altération médiale et une nécrose. Comme prouvé empiriquement, l'obstruction du vasa vasorum induit des changements dégénératifs dans le milieu avec dissection aortique ultérieure [16]. Cela peut être physiologiquement causé par un épaississement vasculaire, une tortuosité et une obstruction.[1]
Hypertension [1]
C'est le facteur de risque le plus important pour le développement de la dégénérescence médiale [17][18]. L'hypertension provoque une modification des forces hémodynamiques agissant sur la paroi aortique et provoque des dommages directs au milieu aortique, un épaississement intimal et une raideur aortique conséquente. [1]
Vieillissement[1]
Avec le vieillissement, il y a une perte d'élastine et une augmentation du collagène, une fragmentation et un désordre des fibres élastiques avec différents degrés d'altérations des cellules musculaires lisses [19]. C'est la principale raison physiologique de la forte corrélation épidémiologique entre l'âge et les maladies aortiques telles que les anévrismes et la dissection [13]. De plus, la fibrose s'accompagne souvent d'une microcalcification dans la partie acellulaire interne des médias chez les personnes âgées. [1]
Prédisposition génétique[1]
Syndrome de Marfan: dans ce syndrome génétique, le maillage des fibres est altéré et les vaisseaux sont plus sujets à la formation d'anévrismes.D'autres syndromes sont associés à une paroi aortique altérée: Ehlers-Danlos, syndrome de Loeys-Dietz (SDL) et syndrome de Turner.[1]
Maladies congénitales [1]
Tétralogie de Fallot, coarctation de l'aorte, valve aortique bicuspide. [1]
Approche clinique
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Alors que les sections Questionnaire, Examen clinique et Examens paracliniques servent à énumérer, cette section sert à intégrer tous ces éléments pour discuter du raisonnement du clinicien. C'est en quelque sorte la manière dont les cliniciens réfléchissent lorsque confrontés à cette maladie : c'est la section par excellence pour l'enseignement. |
| Formats: | Texte, Liste à puces, Tableau |
| Balises sémantiques: | |
| Commentaires: |
|
| Exemple: | |
Diagnostic
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section traite de la manière dont on peut diagnostiquer une maladie en tenant compte de l'histoire, de l'examen clinique et des investigations. C'est dans cette section que se retrouveront les critères permettant d'infirmer ou de confirmer la présence de la maladie (lorsqu'ils existent). |
| Formats: | Texte, Liste à puces, Tableau |
| Balises sémantiques: | |
| Commentaires: |
|
| Exemple: | L'asystolie est un diagnostic électrocardiographique. L'absence d'activité électrique chez un patient inconscient sans pouls permet de confirmer le diagnostic, tout en s'assurant qu'il n'y a pas de cable débranché et que la calibration du moniteur est adéquate.
Selon le Fourth Universal Definition of Myocardial Infarction, l'infarctus aigu du myocarde est diagnostiqué lorsqu'il y a :
|
Diagnostic différentiel
Toute contribution serait appréciée.
| Description: | Cette section traite du diagnostic différentiel de la maladie, c'est-à-dire aux autres diagnostics à évoquer lorsque confronté à ce diagnostic. |
| Formats: | Liste à puces |
| Balises sémantiques: | Diagnostic différentiel |
| Commentaires: |
|
| Exemple: | Le diagnostic différentiel de l'appendicite comprend :
|
Les diagnostics alternatifs sur le différentiel de la dissection aortique comprennent les conditions potentiellement mortelles suivantes:
- Infarctus du myocarde
- Anévrisme de l'aorte
- Tamponnade cardiaque (d'une autre cause)
- Rupture de l'œsophage (syndrome de Boerhaave)
- Pneumothorax spontané
- Embolie pulmonaire
- Accident vasculaire cérébral / accident ischémique transitoire
Si un patient présente des douleurs abdominales, des coliques rénales ou biliaires, une occlusion intestinale / perforation, une ischémie mésentérique non liée à la dissection doit être envisagée. Le déficit du pouls peut être le signe de phénomènes emboliques ou d'occlusion artérielle non liés à la dissection. [20][1]
Traitement
Toute contribution serait appréciée.
| Description: | Cette section décrit le traitement de la maladie. |
| Formats: | Liste à puces, Tableau, Texte |
| Balises sémantiques: | Traitement, Traitement pharmacologique |
| Commentaires: |
|
| Exemple: | |
Une fois le diagnostic de DAA confirmé ou hautement suspecté, une consultation urgente en chirurgie cardiothoracique ou vasculaire doit être obtenue, quel que soit le lieu de dissection. Les dissections aiguës impliquant l'aorte ascendante sont considérées comme des urgences chirurgicales. Le patient doit avoir une ligne artérielle et un cathéter veineux central pour la surveillance. Une foley doit être insérée pour évaluer la production d'urine.[1] Le temps est un facteur clé lors d'un diagnostic de DAA; en effet le taux de mortalité augmente de 1à 2 % par heure suivant l'apparition des symptômes dans les premiers 24 heures. Environ 20% des patients qui présentent une DAA décéderont avant leur arrivée à l'hôpital. Sans traitement médical, 30% décéderont à une semaine, 80% à 2 semaines et 90% à 1 an.
Le traitement médical consiste avant tout à stabiliser le patient.
- S'assurer que le patient est Nil per os et qu'il a une ligne artérielle.
- Analgésie avec opiacés (la morphine est l'analgésique préféré, car elle diminue également la production sympathique)
- Ralentir le Rythme cardiaque à 60 Bpm avec bêtabloquant IV courte durée (réduction de la fréquence cardiaque et de la pression artérielle réduit la tension de la paroi aortique et limite l'étendue de la dissection).
- Ensuite, réduire la tension artérielle < 120 mmHg en utilisant des agents antihypertenseurs.
- Chirurgie vasculaire pour réparation une. fois le patient stabilisé
La stratégie à 2 agents pharmacologiques consiste à d'abord un Bêtabloquant, suivi de l'antihypertenseur:
- Esmolo IV, 500 microgrammes / kilo en bolus sur 1 minute, suivi de 50 microgramme/kg/min en continu.
- Agent antihypertenseurs les plus utilisés sont:
- Nicarpidine IV
- Clevidipine IV
- Nitroprusside de sodium IV
- Fenoldopam IV
D'autres agents qui peuvent être utilisés pour abaisser la tension artérielle comprennent le labétalol,véramipril, le diltiazem ou bloquer des canaux calciques, Les B-bloquants doivent être utilisés avec prudence dans les situations de régurgitation aortique aiguë, car ils bloquent la tachycardie compensatrice.[1]
Chez les patients hypotendus, l'administration intraveineuse de liquides est une première approche raisonnable. Des vasopresseurs peuvent être ajoutés, si nécessaire, pour maintenir une perfusion adéquate, mais peuvent provoquer une propagation de fausse lumière supplémentaire. Les agents inotropes doivent être évités car ils sont susceptibles d'augmenter la force et le taux de contraction ventriculaire et par conséquent d'aggraver la tension de la paroi aortique.[1]
La thérapie chirurgicale pour la DAA de type A implique l'excision de la déchirure intimale, l'oblitération de l'entrée dans la fausse lumière de manière proximale et la reconstitution de l'aorte avec l'interposition d'une greffe vasculaire synthétique.
L'intervention chirurgicale pour la DAA de type B a tendance à être réservée aux patients qui ont un cours compliqué. La greffe d'endoprothèse vasculaire (TEVAR) a été utilisée comme alternative moins invasive à la chirurgie, principalement pour les patients présentant des dissections compliquées de type B. [5][21][16][1]
Pour la DAA impliquant l'aorte ascendante, l'aorte doit être remplacée et la valve aortique doit être évaluée. Dans la plupart des cas, la valve aortique peut également devoir être excisée et remplacée par une valve prosthétique.
Les dissections impliquant l'aorte descendante sont complexes et il existe un risque de paraplégie. Les dissections les plus difficiles sont celles qui impliquent l'arc aortique. La mortalité chirurgicale varie de 5 à 20%. Même ceux qui survivent ont un long rétablissement. [1]
En raison de la mortalité chirurgicale élevée, des procédures endovasculaires sont aujourd'hui effectuées pour la DAA. La mise en place d'un stent endovasculaire est associée à une morbidité significativement plus faible par rapport à la chirurgie, mais la clé est la sélection du patient.
Suivi
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section traite du suivi de la maladie. |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: |
|
| Exemple: | |
- Une fois que le patient est traité chirurgicalement ou médicalement, la pression artérielle doit être contrôlée
- Le patient doit être étroitement surveillé pour la progression de la dissection aortique
- Une tomodensitométrie thoracique régulière ou une IRM est recommandée tous les 3 à 6 mois pour vérifier la progression de la maladie [1]
Complications
Toute contribution serait appréciée.
| Description: | Cette section traite des complications possibles de la maladie. |
| Formats: | Liste à puces, Texte |
| Balises sémantiques: | Complication |
| Commentaires: |
|
| Exemple: | Les complications de l'infarctus du myocarde sont :
|
Les délais de diagnostique ou encore l'omission de considérer une DAA contribuent à un taux de mortalité très élevé. Les dissections aiguës et celles < 2 semaines sont les plus à risque de présenter ces complications mortelles. La mortalité peut ainsi se présenter selon 4 voies différentes:
- Tamponade cardiaque aigue
- Insuffisance aortique aiguë (choc cardiogénique)
- Rupture aortique
- Ischémie des organes terminaux (intestinales, rénal)
Le risque de mortalité diminue après 2 semaines, lorsque des signes radiologiques montrent une thrombose de la dissection et une perte de la communication entre la vraie et fausse lumière du vaisseau sanguin. Certaines complications peuvent toutefois survenir:
- Infarctus du myocarde
- Paraplégie
- Insuffisance rénale
- Amputation des extrémités
- Ischémie intestinale
- Compression de la veine cave supérieure[1]
Évolution
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section contient le pronostic et évolution naturelle de la maladie. Le pronostic est lié à la survie du patient atteint de la maladie. L'évolution naturelle est la manière dont évoluera la maladie du patient dans le temps. |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: | |
| Exemple: | La dissection aortique est associée une mortalité très élevée. Au moins 30% des patients décèdent après leur arrivée à l'urgence, et ce, même après une intervention chirurgicale. Pour ceux qui survivent à la chirurgie, la morbidité est également très élevée et la qualité de vie est mauvaise. La mortalité la plus élevée d'une dissection aortique aiguë est dans les 10 premiers jours. Les patients qui ont une dissection chronique ont tendance à avoir un meilleur pronostic, mais leur espérance de vie est raccourcie par rapport à la population générale.[1] Sans traitement, la mortalité est de 1 à 3% par heure au cours des 24 premières heures, 30% à une semaine, 80% à deux semaines et 90% à un an. |
La dissection aortique entraîne toujours une mortalité très élevée. Au moins 30% des patients décèdent après leur arrivée à l'urgence, et ce, même après une intervention chirurgicale. Pour ceux qui survivent à la chirurgie, la comorbidité fait également des ravages et la qualité de vie est mauvaise. La mortalité la plus élevée d'une dissection aortique aiguë est dans les 10 premiers jours. Les patients qui ont une dissection chronique ont tendance à avoir un meilleur pronostic, mais même leur espérance de vie est raccourcie par rapport à la population générale.[1] Sans traitement, la mortalité est de 1 à 3%/h au cours des 24 premières heures, 30% à 1 semaine, 80% à 2 semaines et 90% à 1 an.
La mortalité hospitalière chez le patient traité est d'environ 30% pour les dissections proximales et 10% pour les dissections distales. La survie des patients qui survivent à l'épisode aigu est d'environ 60% à 5 ans et 40% à 10 ans. Environ 1/3 des décès tardifs sont dus à des complications de la dissection; le reste est dû à d'autres troubles.
Prévention
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section traite des mesures préventives et du dépistage précoce de la maladie (lorsque pertinent). |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: | |
| Exemple: | La prévention primaire consiste à la prise en charge des facteurs de risque :
|
Dans la population en général, la prévention consiste à:
- Contrôler l'hypertension
- Contrôler l'hyperlipidémie
- Cesser l'usage du tabac
- Éviter l'utilisation d'agents sympathomimétique (cocaïne, méthamphétamine)
Pour les patients qui sont à risque de maladies touchant le collagène et les parois des artères, ou avec risques génétiques ou anatomiques, la prévention consiste à avoir un suivi régulier avec un cardiologue afin de:
- Contrôler la tension artérielle
- Maintenir le poids santé et éviter l'obésité
- Surveiller l'excès de cholestérol
- Offrir un support afin de cesser de fumer [1]
- Et éviter l'utilisation de drogues illicites.
Concepts clés
Références
- Cette page a été modifiée ou créée le 2021/01/30 à partir de Aortic Dissection (StatPearls / Aortic Dissection (2020/12/17)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/28722992 (livre).
- ↑ 1,00 1,01 1,02 1,03 1,04 1,05 1,06 1,07 1,08 1,09 1,10 1,11 1,12 1,13 1,14 1,15 1,16 1,17 1,18 1,19 1,20 1,21 1,22 1,23 1,24 1,25 1,26 1,27 1,28 1,29 1,30 1,31 1,32 1,33 1,34 1,35 1,36 1,37 1,38 1,39 1,40 1,41 1,42 1,43 1,44 1,45 1,46 1,47 et 1,48 David Levy, Amandeep Goyal, Yulia Grigorova et Fabiola Farci, StatPearls, StatPearls Publishing, (PMID 28722992, lire en ligne)
- ↑ « Dissection aortique - Troubles cardiovasculaires », sur Édition professionnelle du Manuel MSD (consulté le 5 février 2021)
- ↑ Tao Zeng, Lei Shi, Qingwei Ji et Ying Shi, « Cytokines in aortic dissection », Clinica Chimica Acta; International Journal of Clinical Chemistry, vol. 486, , p. 177–182 (ISSN 1873-3492, PMID 30086263, DOI 10.1016/j.cca.2018.08.005, lire en ligne)
- ↑ Domenico Spinelli, Filippo Benedetto, Rocco Donato et Gabriele Piffaretti, « Current evidence in predictors of aortic growth and events in acute type B aortic dissection », Journal of Vascular Surgery, vol. 68, no 6, , p. 1925–1935.e8 (ISSN 1097-6809, PMID 30115384, DOI 10.1016/j.jvs.2018.05.232, lire en ligne)
- ↑ 5,0 et 5,1 Christopher Lau, Jeremy R. Leonard, Erin Iannacone et Mario Gaudino, « Surgery for Acute Presentation of Thoracoabdominal Aortic Disease », Seminars in Thoracic and Cardiovascular Surgery, vol. 31, no 1, , p. 11–16 (ISSN 1532-9488, PMID 30071280, DOI 10.1053/j.semtcvs.2018.07.018, lire en ligne)
- ↑ Lifei Wu, « The pathogenesis of thoracic aortic aneurysm from hereditary perspective », Gene, vol. 677, , p. 77–82 (ISSN 1879-0038, PMID 30030203, DOI 10.1016/j.gene.2018.07.047, lire en ligne)
- ↑ (en) Graham Walker and The NNT Group, « Homepage », sur TheNNT (consulté le 22 février 2021)
- ↑ Michael Klompas, « Does this patient have an acute thoracic aortic dissection? », JAMA, vol. 287, no 17, , p. 2262–2272 (ISSN 0098-7484, PMID 11980527, DOI 10.1001/jama.287.17.2262, lire en ligne)
- ↑ Paolo Berretta, Mariano Cefarelli, Andrea Montalto et Carlo Savini, « [Surgical indications for thoracic aortic disease: beyond the "magic numbers" of aortic diameter] », Giornale Italiano Di Cardiologia (2006), vol. 19, no 7, , p. 429–436 (ISSN 1827-6806, PMID 29989600, DOI 10.1714/2938.29539, lire en ligne)
- ↑ R. Erbel, « [Aortic diseases : Modern diagnostic and therapeutic strategies] », Herz, vol. 43, no 3, , p. 275–290 (ISSN 1615-6692, PMID 29569149, DOI 10.1007/s00059-018-4694-2, lire en ligne)
- ↑ J. C. Leonard, P. S. Hasleton, P. S. Hasleton et J. C. Leonard, « Dissecting aortic aneurysms: a clinicopathological study. I. Clinical and gross pathological findings », The Quarterly Journal of Medicine, vol. 48, no 189, , p. 55–63 (ISSN 0033-5622, PMID 482591, lire en ligne)
- ↑ Hiroaki Osada, Masahisa Kyogoku, Motonori Ishidou et Manabu Morishima, « Aortic dissection in the outer third of the media: what is the role of the vasa vasorum in the triggering process? », European Journal of Cardio-Thoracic Surgery: Official Journal of the European Association for Cardio-Thoracic Surgery, vol. 43, no 3, , e82–88 (ISSN 1873-734X, PMID 23277437, DOI 10.1093/ejcts/ezs640, lire en ligne)
- ↑ 13,0 et 13,1 Motoji Sawabe, « Vascular aging: from molecular mechanism to clinical significance », Geriatrics & Gerontology International, vol. 10 Suppl 1, , S213–220 (ISSN 1447-0594, PMID 20590836, DOI 10.1111/j.1447-0594.2010.00603.x, lire en ligne)
- ↑ O. Leone, L. Agozzino, A. Angelini et G. Bartoloni, « Criteria for histopathologic diagnosis of aortic disease consensus statement from the SIAPEC-IAP study group of "cardiovascular pathology" in collaboration with the association for Italian cardiovascular pathology », Pathologica, vol. 104, no 1, , p. 1–33 (ISSN 0031-2983, PMID 22799053, lire en ligne)
- ↑ Marc K. Halushka, Annalisa Angelini, Giovanni Bartoloni et Cristina Basso, « Consensus statement on surgical pathology of the aorta from the Society for Cardiovascular Pathology and the Association For European Cardiovascular Pathology: II. Noninflammatory degenerative diseases - nomenclature and diagnostic criteria », Cardiovascular Pathology: The Official Journal of the Society for Cardiovascular Pathology, vol. 25, no 3, , p. 247–257 (ISSN 1879-1336, PMID 27031798, DOI 10.1016/j.carpath.2016.03.002, lire en ligne)
- ↑ 16,0 et 16,1 Karl Sörelius et Anders Wanhainen, « Challenging Current Conservative Management of Uncomplicated Acute Type B Aortic Dissections », EJVES short reports, vol. 39, , p. 37–39 (ISSN 2405-6553, PMID 29988823, Central PMCID 6031758, DOI 10.1016/j.ejvssr.2018.05.010, lire en ligne)
- ↑ E. W. Larson et W. D. Edwards, « Risk factors for aortic dissection: a necropsy study of 161 cases », The American Journal of Cardiology, vol. 53, no 6, , p. 849–855 (ISSN 0002-9149, PMID 6702637, DOI 10.1016/0002-9149(84)90418-1, lire en ligne)
- ↑ W. C. Roberts, « Frequency of systemic hypertension in various cardiovascular diseases », The American Journal of Cardiology, vol. 60, no 9, , p. 1E–8E (ISSN 0002-9149, PMID 2959147, DOI 10.1016/0002-9149(87)90534-0, lire en ligne)
- ↑ Giulio Cesar Gequelim, Djanira Aparecida da Luz Veronez, Gustavo Lenci Marques et Camila Harumi Tabushi, « Thoracic aorta thickness and histological changes with aging: an experimental rat model », Journal of geriatric cardiology: JGC, vol. 16, no 7, , p. 580–584 (ISSN 1671-5411, PMID 31447898, Central PMCID 6689520, DOI 10.11909/j.issn.1671-5411.2019.07.001, lire en ligne)
- ↑ Loren F. Hiratzka, George L. Bakris, Joshua A. Beckman et Robert M. Bersin, « 2010 ACCF/AHA/AATS/ACR/ASA/SCA/SCAI/SIR/STS/SVM guidelines for the diagnosis and management of patients with thoracic aortic disease: executive summary. A report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines, American Association for Thoracic Surgery, American College of Radiology, American Stroke Association, Society of Cardiovascular Anesthesiologists, Society for Cardiovascular Angiography and Interventions, Society of Interventional Radiology, Society of Thoracic Surgeons, and Society for Vascular Medicine », Catheterization and Cardiovascular Interventions: Official Journal of the Society for Cardiac Angiography & Interventions, vol. 76, no 2, , E43–86 (ISSN 1522-726X, PMID 20687249, DOI 10.1002/ccd.22537, lire en ligne)
- ↑ Sabreen Mkalaluh, Marcin Szczechowicz, Bashar Dib et Alexander Weymann, « Open surgical thoracoabdominal aortic aneurysm repair: The Heidelberg experience », The Journal of Thoracic and Cardiovascular Surgery, vol. 156, no 6, , p. 2067–2073 (ISSN 1097-685X, PMID 30041925, DOI 10.1016/j.jtcvs.2018.05.081, lire en ligne)