ULaval:MED-1202/Embolie et hypertension pulmonaires
Embolie pulmonaire

La maladie thromboembolique veineuse est formée de deux entités :
- La thrombose veineuse (elle siège habituellement aux membres inférieurs)
- L’embolie pulmonaire (migration d’un caillot sanguin du site de la thrombose vers les artères pulmonaires)
Elle est la 3e cause de mortalité cardiovasculaire avec une incidence de 1 sur 1000 patients hospitalisés par année. La mortalité globale attribuable à l’embolie pulmonaire est de 3 à 12%. La vaste majorité des décès sont secondaires à un diagnostic non reconnu.
Il y a trois phénomènes qui expliquent la formation d’un caillot dans le réseau veineux (triade de Virchow)
- Stase sanguine: altération du flot sanguin secondaire à une obstruction veineuse soit par compression extrinsèque, soit par diminution du débit cardiaque, soit par immobilisation;
- Inflammation de la paroi veineuse;
- Hypercoagulabilité: état héréditaire ou acquis.
Dans environ 80% des cas d’embolie pulmonaire, on retrouve une thrombose veineuse aux membres inférieurs.
| Type | Facteur |
|---|---|
| Acquis | Chirurgie dans les 3 derniers mois |
| Traumatisme | |
| Cancer | |
Mobilité réduite
| |
| Obésité | |
Obstétrique
| |
Médicaments
| |
| Insuffisance cardiaque congestive | |
| Héréditaires | Thrombophilies |
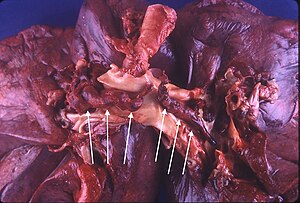
L’obstruction des artères pulmonaires par le caillot provoque une augmentation de la résistance pulmonaire par le biais de deux mécanismes :
- oblitération mécanique
- vasoconstriction humorale: elle est médiée par des substances vasoactives provenant du caillot et potentialisée par l’hypoxie.
Dans les embolies pulmonaires massives (> 50% du lit vasculaire) ou en présence d’une affection cardiaque ou pulmonaire sous-jacente, le ventricule droit est soumis à une surcharge importante conduisant au cœur pulmonaire aigu. La pression artérielle pulmonaire moyenne générée par le ventricule droit ne peut excéder 40 mmHg chez les patients sans pathologies cardio-pulmonaires.
Conséquences respiratoires
Lorsque le lit vasculaire s’obstrue, il y a une augmentation de l’espace mort puisque la ventilation est bonne, mais pas la perfusion. Il y a alors une augmentation du rapport ventilation/perfusion. L’hypocapnie prévalant dans les zones d’espace-mort alvéolaire favorise une pneumoconstriction et une broncho-constriction. Cela contribue à réduire la ventilation inefficace dans ces zones non fonctionnelles. Cela se traduit cliniquement par une atélectasie. Une augmentation du shunt physiologique dans les zones d’atélectasie est favorisée par la perte de surfactant au pourtour de l’embolie pulmonaire. Cela entraîne une hypoxémie dont la sévérité est proportionnelle à la sévérité de l’embolie.
Signes et symptômes
La sévérité des symptômes est habituellement proportionnelle à l’étendue de l’obstruction artérielle. L’auscultation peut être normale ou révéler des signes de consolidation pneumonique ou la présence d’un frottement pleural.
| Symptômes | |
|---|---|
| Signes |
Dans la majorité des cas, l’embolie pulmonaire évolue vers la résolution grâce au mécanisme de fibrinolyse naturelle. Cette résolution évolue pendant environ 6 semaines. Dans une minorité de cas, l’embolie pulmonaire peut conduire à la destruction d’une portion du parenchyme amenant un infarctus pulmonaire. L’embolie pulmonaire peut être mortelle, dans moins de 10% des cas. Le décès survient la plupart du temps très précocement, dans les 2 heures suivant l’embolie pulmonaire.
Les facteurs de mauvais pronostic sont :
- Dysfonction ventriculaire droite
- Augmentation des pro-BNP
- Thrombus dans le ventricule droit
- Troponine positive
Investigation de l’embolie pulmonaire
La démarche diagnostique doit se faire par étapes, en utilisant les examens les plus simples d’abord. L’estimation de la probabilité clinique est indispensable chez tous les patients suspectés d’une embolie pulmonaire. Pour ce faire, le Score de Wells est très utilisé en clinique.
| Critères | Points | Points (version simplifiée) |
Présent |
|---|---|---|---|
| Symptômes ou signes de thrombose veineuse profonde | 3 | 1 | |
| Autres diagnostics moins probables | 3 | 1 | |
| FC > 100/min | 1.5 | 1 | |
| Immobilisation (≥ 3 jours) ou chirurgie récente (< 4 semaines) | 1.5 | 1 | |
| Antécédents de thrombose veineuse profonde ou d'embolie pulmonaire | 1.5 | 1 | |
| Hémoptysies | 1 | 1 | |
| Cancer | 1 | 1 | |
| Probabilité | Faible | ||
| Probabilité (version simplifiée) | Peu probable | ||
- Version originale: faible (0-1), intermédiaire (2-6), Élevée (>6)[note 1]
- Version simplifiée: peu probable (0-1), plus probable (>1)[note 2]
Radiographie pulmonaire

Souvent dans la limite de la normale, mais permet d’éliminer d’autres pathologies. Lorsque la radiographie est anormale, on peut constater :
- Une opacité triangulaire à base pleurale suggestive d’un infarctus pulmonaire (Bosse de Hampton).
- Oligémie localisée associée à une artère pulmonaire dilatée
- Signes de pneumosconstriction avec élévation d’une coupole diaphragmatique
- Épanchement pleural – l’atélectasie crée un appel d’eau car il y a pression négative
Gaz artériel
Il sert à objectiver une hypoxémie avec une alcalose respiratoire (car hyperventilation; moins de CO2)
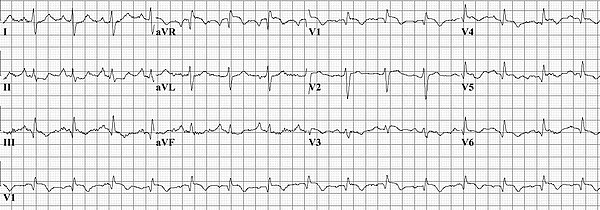
ECG
Il demeure normal la plupart du temps. Les signes d’un cœur pulmonaire sont :
- Tachycardie
- Ondes P pulmonaires hautes et pointues
- Déviation axiale droite
- Modification du complexe QRS – S1Q3T3
D-dimères
La détection de produits de dégradation du fibrinogène tels que les D-dimères peut aider au diagnostic. La principale faiblesse est la très mauvaise spécificité (bonne sensibilité > 95%). L’infection, le cancer, les maladies inflammatoires et le statut post-opératoire peuvent élever les D-dimères. Ce test doit donc être interprété à la lumière de la probabilité clinique.
Scintigraphie pulmonaire de perfusion et de ventilation

La scintigraphie pulmonaire de perfusion et de ventilation (aussi appelée scintigraphie V/Q) est l'examen le plus souvent utile au diagnostic d’embolie pulmonaire. Elle sert à démontrer les défauts de perfusion causés par l’embolie. Une scintigraphie pulmonaire normale élimine le diagnostic d’embolie.
On peut classer la scintigraphie en 4 catégories :
- Normale
- Probabilité faible (<20% de probabilité d’embolie): anomalies de ventilation et de perfusion sans anomalie radiologique correspondante, anomalies de perfusion plus petites que les anomalies radiologiques, anomalies de perfusion non segmentaires
- Probabilité intermédiaire (20-80% de probabilité d’embolie): défaut de ventilation et de perfusion en accord, un seul défaut de perfusion segmentaire, sans défaut de ventilation et sans anomalie radiologique
- Probabilité élevée (≥ 80% de probabilité d’embolie): ≥ 2 défauts segmentaires de perfusion avec ventilation normale et sans anomalie radiologique correspondante et défauts de perfusion beaucoup plus grands que les anomalies radiologiques.
Malheureusement, ~ 65% des patients chez qui on suspecte une embolie pulmonaire ont une probabilité intermédiaire ou faible à la scintigraphie, nécessitant une investigation supplémentaire.
Angiotomodensitométrie thoracique spiralée
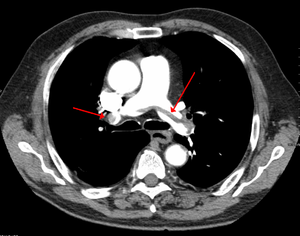
Donne des images qui révèlent la présence de caillots dans les troncs des artères pulmonaires proximales, lobaires ou segmentaires. Cet examen à lui seul ne peut éliminer la possibilité d’une embolie pulmonaire, étant donné que les caillots situés en périphérie sont difficilement objectivables.
Angiographie pulmonaire
Examen de référence pour confirmer le diagnostic d’embolie pulmonaire. Examen invasif qui recherche les défauts de remplissage et les occlusions artérielles. Cet examen est peu utilisé.
Échographie veineuse des membres inférieur – DOPPLER

La découverte d’une thrombophlébite proximale chez un patient chez qui on suspecte une embolie, permet de traiter le patient sans faire nécessairement de test diagnostique supplémentaire.
Algorithme décisionnel
Traitement
Dès qu’on soupçonne fortement une embolie pulmonaire, on doit entreprendre le traitement, même si le diagnostic n’est pas prouvé. La principale complication de l’anticoagulation est le risque de saignement. L’anticoagulation doit être d’une durée de 3 mois en présence de facteurs de risques transitoires. L’anticoagulation doit être prolongée à vie s’il y a thrombophilie ou récidives de maladies thromboemboliques. En présence d’une embolie pulmonaire massive avec instabilité hémodynamique, on peut envisager l’utilisation d’un agent thrombolytique. Cette médication accélère la lyse du caillot, mais avec une augmentation notable du risque d’hémorragie. Les bénéfices sur la réduction de la mortalité demeurent à être démontrés.
Héparine
C’est le traitement initial, elle prévient la récidive d’embolie pulmonaire. Cette molécule exerce rapidement son effet en diminuant la formation de caillots. On peut administrer l’héparine non-fractionnée par voie IV ou l’héparine de faible poids moléculaire par voie SC.
Anticoagulation
À long terme: Anticoagulant oral anti-vitamine K – Warfarine. Il est administré quotidiennement et on ajuste de manière à maintenir un taux d’INR entre 2-3.
Hypertension pulmonaire
Circulation pulmonaire

Le poumon est irrigué par une double circulation
- Circulation bronchique
- Dérive de la circulation systémique
- Fournit du sang artériel à la trachée et aux bronches
- Reçoit moins de 3% du débit cardiaque total
- Circulation pulmonaire
- Reçoit la totalité du débit cardiaque
- Son rôle principal est d’assurer les échanges gazeux alvéolo-capillaires
- Elle assure d’autres fonctions accessoires :
- Métabolique – synthèse de médiateurs
- Filtre circulatoire

La circulation pulmonaire est un système à basse pression et à faible résistance. La mesure des paramètres de la circulation pulmonaire s’effectue avec un cathétérisme cardiaque droit. Le cathéter Swan-Ganz est introduit par une veine et avancé jusqu’aux cavités cardiaques droites et aux artérioles pulmonaires. Voici les valeurs normales de pressions:
- Oreillette droite : 0 mmHg
- Ventricule droit : 15 mmHg
- Artères pulmonaires : 10 mmHg
- Pression capillaire bloquée : 8-10 mmHg
- Oreillette gauche : 5 mmHg
Régulation de la pression artérielle pulmonaire
La pression artérielle pulmonaire est régulée par plusieurs facteurs :
- Hypoxie: vasoconstricteur puissant au niveau des petites artères pulmonaires
- SNA
- La stimulation ⍺-sympathique provoque une vasoconstriction
- La stimulation β-sympathique provoque une vasodilatation
- Peu d’innervation parasympathique
- Hypercapnie: une vasoconstriction est observée soit par une action directe, soit par une acidose respiratoire secondaire.
- Variation de la pression alvéolaire: une augmentation de la pression alvéolaire par ventilation en pression positive est transmise aux capillaires pulmonaires et provoque une majoration de la pression artérielle pulmonaire.
- Pression de l’oreillette gauche: toute variation de la pression de l’oreillette gauche se répercute sur les compartiments artériels pulmonaires.
- Viscosité sanguine: l’augmentation de la viscosité sanguine augmente la résistance pulmonaire (Hématocrite > 55)
- Médiateurs vasoactifs
| Vasoconstricteurs | Vasodilatateurs |
|---|---|
Hypertension artérielle pulmonaire
L’hypertension artérielle pulmonaire (HTP) se définit par :
- Pression artérielle pulmonaire moyenne > 25 mmHg au repos
- Pression artérielle pulmonaire moyenne > 30 mmHg à l’effort
La circulation pulmonaire peut s’adapter à des changements importants grâce à sa distensibilité et son pouvoir de recrutement capillaire. Lorsque l’HTP apparaît, il y a déjà des dommages anatomiques et physiologiques importants. Les principales anomalies histologiques sont :
- Signes à la pathologie de l'hypertension pulmonaire
-
Lésion plexiforme
-
Fibrose intimale
-
Hypertrophie de la media et de l'intima
L’HTP est idiopathique dans 40% des cas et familiale dans 5% des cas. Dans le cas d’hypertension pulmonaire associée à une cardiopathie gauche, le cathétérisme cardiaque met en évidence une augmentation de la pression capillaire bloquée. L’hypertension artérielle pulmonaire post-embolique est liée à la persistance et à l’organisation fibreuse des caillots après une ou plusieurs embolies pulmonaires aiguës. L’HTP des affections respiratoires chroniques est secondaire à une augmentation de la résistance vasculaire pulmonaire principalement due à une hypoxie alvéolaire chronique. Elle n’a pas la gravité de l’HTP idiopathique.
Symptomatologie
Les symptômes cliniques d’HTP sont souvent non spécifiques :
- Dyspnée
- Intolérance à l’effort
- Douleur thoracique: angine secondaire à l’hypoperfusion de la paroi du ventricule droit (besoin en O2 augmenté et plus grosse contraction qui bloque la perfusion coronaire )
- Syncope
L’auscultation cardiaque met en évidence :
- Augmentation de la composante pulmonaire B2
- L’insuffisance cardiaque droite se manifeste par :
Investigation
L’échographie cardiaque est l’examen de choix face à une HTP suspectée. Elle permet d’obtenir une estimation de la pression artérielle pulmonaire systolique par la mesure de la vitesse du flux de l’insuffisance tricuspidienne. Le diagnostic d’HTP doit être confirmé par un cathétérisme cardiaque droit. En présence d’HTP, un test de vasoréactivité au NO est effectué lors du cathétérisme. Il permet d’identifier un sous-groupe de patients avec un pronostic plus favorable à long terme. Par la suite, l’investigation doit permettre d’exclure les HTP secondaires.
Traitement
L’utilisation des anticoagulants se justifie par le fait que les patients souffrants d’HTP ont un risque accru de thrombose intrapulmonaire et de thromboembolie. Cela s’explique par la stagnation du sang au niveau pulmonaire, des chambres cardiaques droites dilatées et une stase veineuse. L’anticoagulation orale (Walfarine) est indiquée dans l’HTP idiopathique, familiale, postembolique et associée aux connectivites.
L'oxygénothérapie peut être utilisée en présence d’hypoxémie. Les diurétiques sont utilisés en cas d’insuffisance cardiaque droite avec œdème périphérique. On suggère également une limitation des activités physiques. La grossesse est formellement contre-indiquée du fait du risque vital pour la mère et l’enfant.
HTP associée aux maladies respiratoires
Le traitement repose essentiellement sur l’oxygénothérapie étant donné que l’hypoxie alvéolaire chronique est le responsable des modifications structurales du lit vasculaire pulmonaire aboutissant à l’HTP. L’oxygène permet de lever la vasoconstriction pulmonaire hypoxique. Les traitements actuels ne permettent pas de guérir cette maladie grave.
Les patients atteints d'une HTP secondaire à une maladie thromboembolique chronique peuvent bénéficier d'une endartériectomie bilatérale des artères pulmonaires. Cette intervention permet de désobstruer le lit artériel pulmonaire.
Les vasodilatateurs purs comme les antagonistes calciques ne sont efficaces que chez les patients ayant une réponse aiguë au test de vasoréactivité. Les antagonistes des récepteurs de l’endothéline-1, la prostacycline intraveineuse « époprosténol » et les inhibiteurs des phosphodiestérases de type 5 ont des propriétés vasodilatatrices et un effet sur le remodelage vasculaire. L’époprosténol (prostacycline) représente le traitement de référence des formes sévères. Les antagonistes des récepteurs de l’endothéline-1 (bosentan) constituent un traitement oral de 1ère ligne chez les patients de classe fonctionnelle III.
Lorsque le traitement médical est insuffisant, la transplantation pulmonaire représente l’ultime recours.
Notes
Références
- ↑ P. S. Wells, D. R. Anderson, M. Rodger et I. Stiell, « Excluding pulmonary embolism at the bedside without diagnostic imaging: management of patients with suspected pulmonary embolism presenting to the emergency department by using a simple clinical model and d-dimer », Annals of Internal Medicine, vol. 135, no 2, , p. 98–107 (ISSN 0003-4819, PMID 11453709, lire en ligne)



