Cancer appendiculaire
| Maladie | |
| Caractéristiques | |
|---|---|
| Signes | Appendicite, Ascite, Masse abdominale, Péritonisme |
| Symptômes |
Appendicite, Anorexie , Syndrome carcinoïde, Fatigue , Douleur abdominale , Asymptomatique , Vomissement , Perte de poids , Température corporelle élevée |
| Diagnostic différentiel |
Appendicite, Kyste ovarien, Abcès appendiculaire, Lymphangiome kystique, Kyste mésentérique, Kyste rétropéritonéal, Cancer ovarien, Endométriome, Diverticule de Meckel, Maladie de Crohn |
| Informations | |
| Wikidata ID | Q4781026 |
|
| |
Les tumeurs malignes appendiculaires sont un groupe rare de tumeurs souvent trouvées accidentellement lors de l'ablation chirurgicale de l'appendice. Sur le plan histologique, cette tumeur maligne représente 0,5 à 1% de tous les échantillons de pathologie après appendicectomie.[1][2] Cliniquement, cette affection se présente le plus souvent comme une appendicite aiguë due à une obstruction de la lumière appendiculaire. Comme c'est le cas pour toutes les tumeurs malignes, une détection précoce est essentielle car le diagnostic tardif pourrait nuire au pronostic.[3]
Épidémiologie
Le cancer de l'appendice est observé dans 1% des prélèvements appendiculaires. Il y a davantage de tumeurs neuroendocrines chez les jeunes patients et davantage d'adénocarcinomes chez la population plus âgée[4] Une association accrue avec la néoplasie colique et la colite ulcéreuse chronique a été notée.[2] 20% des cas ont une tumeur colorectale synchrone. Il y a aussi une association avec les tumeurs rénale, ovarienne et mammaire. L'appendice est le deuxième site le plus fréquent pour les tumeurs neuroendocrines après le rectum selon la base de données SEER. Au moment du diagnostic, plus d'un tiers des tumeurs neuroendocriniennes sont métastatiques lors du diagnostic.[5][3]
Étiologies et pathologie
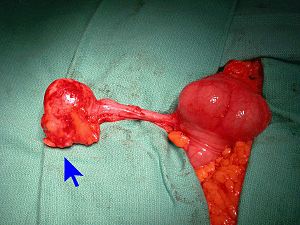
Pour comprendre l'origine tumorale, il faut comprendre les lignées cellulaires de l'appendice. La lignée épithéliale contient beaucoup de cellules à gobelet pour une production abondante exocrine de mucus. Un mucocèle est une collection de mucine épaissie accumulée par une obstruction. Celle-ci peut être causée par un processus tumoral ou non. Des tumeurs appendiculaires peuvent aussi sécréter de la mucine et causer un mucocèle. Il y a deux grandes classes de tumeurs appendiculaires, soit les tumeurs épithéliales et les tumeurs neuroendocrines. Comme l'appendice est principalement un tissu lymphoïde, des lymphomes appendiculaires peuvent survenir. L'étiologie est un lymphome de Burkitt avec un âge moyen de 18 ans et des lymphomes diffus à grandes cellules B chez le sujet âgé. [6][3] Finalement, les sarcomes sont également possibles.
Tumeurs épithéliales
Pour les adénocarcinomes, 90% des néoplasies sont mucineuses et 10% sont de type intestinal - soit le ratio inverse des néoplasies coliques. Le sous-type en bague à chaton offre le moins bon pronostic. Voici les différentes histologies des néoplasies épithéliales appendiculaires avec leur distribution.
| Type | % | Définition | Analogie colique |
| Simple mucocèle
Kyste de rétention |
20% | Δ dégénératifs épithéliaux 2aires à une obstruction (ex. : fécalithe) qui cause distension appendiculaire | |
| Hyperplasie muqueuse | 20% | Processus hyperplasique autonome | Polype hyperplasique |
| Cystadénome mucineux | 50% | Néoplasie bénigne avec pattern tuboglandulaire ou papillaire qui produit mucine ++ | Adénome villeux ou polype adénomateux |
| Cystadénocarcinome mucineux | 10% | Néoplasie maligne par invasion glandulaire et stromale | Tumeur colique mucineuse, tumeur villeuse maligne |

Les mécanismes qui entraînent des tumeurs malignes appendiculaires ne sont pas bien compris. Cependant, il a été postulé que les néoplasmes mucineux appendiculaires (AMN, un sous-ensemble majeur de tumeurs appendiculaires) suivent la même séquence adénome-carcinome que celle observée dans le cancer colorectal. Cette séquence commence par une mutation ponctuelle dans le proto-oncogène KRAS puis des mutations et / ou des délétions dans le gène TP53 sur Chr 17p. Ensuite, des mutations tronquées sur le gène APC sur 5q et le gène bêta-caténine contribuent toutes à son apparition. Une théorie alternative de l'instabilité des microsatellites (MSI) a été postulée comme résultant de mutations dans les gènes de réparation des mésappariements nucléotidiques, par exemple hMSH2, hMLH1, PMS1, PMS2 et GTBP.[7][8][9][3]
Tumeur neuroendocrine

18% des tumeurs neuroendocrines digestives touchent l'appendice. 75% sont situés au tiers distal, 95% ont moins de 2 cm, 10% sont symptomatiques. Les tumeurs sont rarement multicentriques (4,5%). Les tumeurs neuroendocrines ont une séquence cancéreuse différente. séquence à trouver et référencer[Référence nécessaire]
Physiopathologie
L'obstruction de la lumière appendiculaire par les cellules malignes
entraîne une inflammation de l'appendice, une stase veineuse et, finalement, une infection de l'appendice.[10] Dans les tumeurs mucineuses de l'appendice, il peut y avoir une dilatation kystique de
l'appendice due à l'obstruction de la lumière appendiculaire avec création d'un mucocèle.[11][12] Ces processus sont à la base de la présentation clinique la plus courante de cette maladie, l'appendicite aiguë.[3] Quant aux tumeurs neuroendocrines, elles sont souvent trouvées fortuitement dans le specimen d'une appendicite aiguë.
Présentation clinique
Dans plus de 50% des cas, il n'y a aucun symptôme, et cette malignité est détectée accidentellement. Cependant, la plupart des patients symptomatiques se présenteraient sous forme d'appendicite aiguë.[13][1] Les facteurs qui devraient augmenter la suspicion de néoplasie appendiculaire comprennent un âge supérieur à 50 ans avec des antécédents familiaux de cancer du côlon ou de maladie inflammatoire de l'intestin (MII), des caractéristiques évocatrices d'une appendicite chronique ou la présence d'une anémie inexpliquée [10] Le patient peut présenter des douleurs abdominales non spécifiques, des douleurs du quadrant inférieur droit, une perte de poids, une anorexie, de la fièvre, des vomissements, des caractéristiques d'obstruction intestinale par invagination et de la fatigue.[11] L'examen physique peut révéler une sensibilité abdominale du quadrant inférieur droit avec de la défense si le patient se présente en appendicite, une masse abdominale, la présence d'ascite ou les caractéristiques de la maladie métastatique.[3]
Facteurs de risque
Les mêmes facteurs de risque de l'adénocarcinome colique s'appliquent à ceux de l'appendice, excluant les tumeurs neuroendocrines.
Questionnaire
On doit questionner le patient tel une appendicite s'il se présente à l'urgence. Si le patient est vu en clinique, le patient doit être questionné sur son état général et sa digestion. Il est a noté que le mucocèle est souvent asymptomatique et découvert fortuitement sur l'imagerie.
Examen clinique
Le patient est examiné au niveau abdominal, incluant un toucher rectal. On recherche un tableau d'irritation péritonéale si le patient est en appendicite. Sinon, on recherche l'effet de masse au quadrant inférieur droit ou de l'ascite. La recherche d'adénopathies est également suggérée.
Examens paracliniques
Imagerie :
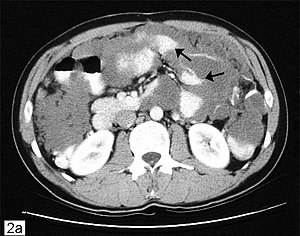
Les études d'imagerie constituent le pilier de l'évaluation initiale. Pour les mucocèles, les résultats échographiques comprennent des lésions allongées ou kystiques dans le quadrant inférieur droit (RLQ) avec des caractéristiques d'apparence interne en pelure d'oignon représentant une mucine lamellée, ce qui est une découverte pathognomonique.[11] Un défaut de la paroi appendiculaire avec fuite peut être le signe d'une rupture du mucocèle [11] Chez les patients présentant des caractéristiques d'appendicite aiguë, une tomodensitométrie ou une IRM révélant un appendice de plus de 15 mm avec des parois épaissies ou irrégulières est suspect pour une néoplasie.[14] Les radiographies simples de l'abdomen ont peu de valeur clinique et peuvent montrent rarement une calcification curviligne à la fosse iliaque droite.
Douteux : Autres résultats de tomodensitométrie suggérant que la PMP inclurait, mais sans s'y limiter, un écaillage de dépôts métastatiques. sur les surfaces séreuses et les cavités, et parfois, un rebord comme une calcification peut être noté.[15] Une biopsie percutanée à l'aiguille peut être essentielle pour confirmer la propagation métastatique mucineuse disséminée au péritoine.[16]
Analyses de laboratoire :
On dose l'antigène carcinoembryonnaire (CEA) lorsqu'il s'agit d'une tumeur épithéliale maligne comme on le ferait pour un cancer colorectal du reste du cadre colique.
Pour les tumeurs neuroendocrines du «foregut» - c'est-à-dire de l'appendice, du colon ou du rectum - le dosage de la chromogranine-A n'est pas représentatif de la charge néoplasique.
Colonoscopie :
Nous devons faire une colonoscopie en pré-opératoire lorsque le diagnostic est connu par l'imagerie. Si on découvre plutôt le diagnostic en per-opératoire, on doit compléter l'investigation par une colonoscopie 4 à 6 semaines post-opératoire. En effet, il peut y avoir une atteinte du bas fond cécal ou une lésion synchrone colique. La trouvaille classique du mucocèle appendiculaire est l'apparence en volcan avec écoulement de mucine possible.
Approche clinique
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Alors que les sections Questionnaire, Examen clinique et Examens paracliniques servent à énumérer, cette section sert à intégrer tous ces éléments pour discuter du raisonnement du clinicien. C'est en quelque sorte la manière dont les cliniciens réfléchissent lorsque confrontés à cette maladie : c'est la section par excellence pour l'enseignement. |
| Formats: | Texte, Liste à puces, Tableau |
| Balises sémantiques: | |
| Commentaires: |
|
| Exemple: | |
Diagnostic
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section traite de la manière dont on peut diagnostiquer une maladie en tenant compte de l'histoire, de l'examen clinique et des investigations. C'est dans cette section que se retrouveront les critères permettant d'infirmer ou de confirmer la présence de la maladie (lorsqu'ils existent). |
| Formats: | Texte, Liste à puces, Tableau |
| Balises sémantiques: | |
| Commentaires: |
|
| Exemple: | L'asystolie est un diagnostic électrocardiographique. L'absence d'activité électrique chez un patient inconscient sans pouls permet de confirmer le diagnostic, tout en s'assurant qu'il n'y a pas de cable débranché et que la calibration du moniteur est adéquate.
Selon le Fourth Universal Definition of Myocardial Infarction, l'infarctus aigu du myocarde est diagnostiqué lorsqu'il y a :
|
Diagnostic différentiel
Toute contribution serait appréciée.
| Description: | Cette section traite du diagnostic différentiel de la maladie, c'est-à-dire aux autres diagnostics à évoquer lorsque confronté à ce diagnostic. |
| Formats: | Liste à puces |
| Balises sémantiques: | Diagnostic différentiel |
| Commentaires: |
|
| Exemple: | Le diagnostic différentiel de l'appendicite comprend :
|
Une masse appendiculaire peut être confondue avec l'une des conditions suivantes. Ils comprennent l'appendicite aiguë, le lymphangiome kystique, le kyste mésentérique, le kyste rétropéritonéal, le kyste de l'ovaire, le cancer de l'ovaire et le diverticule de Meckel.[17][3].
Traitement
Toute contribution serait appréciée.
| Description: | Cette section décrit le traitement de la maladie. |
| Formats: | Liste à puces, Tableau, Texte |
| Balises sémantiques: | Traitement, Traitement pharmacologique |
| Commentaires: |
|
| Exemple: | |
La thérapie chirurgicale est le pilier de la thérapie des cancers de l'appendice; cependant, les cas avancés avec métastases à distance peuvent être chirurgicalement non résécables. L'intervention laparoscopique n'est pas recommandée car elle augmente le risque de rupture peropératoire et de propagation métastatique.[18] L'appendicectomie avec une large résection du mésoappendice afin d'exclure l'atteinte des ganglions lymphatiques peut être à la fois diagnostique et curative car la plupart des tumeurs appendiculaires sont diagnostiquées après l'évaluation histologique de l'échantillon appendiculaire .[19] D'autres modalités chirurgicales telles qu'une hémicolectomie droite sont indiquées en cas d'atteinte ganglionnaire, une grosse tumeur neuroendocrine avec des marges floues et une invasion méso-appendiculaire de plus de 3 mm [20] La chirurgie cytoréductive et la chimiothérapie intrapéritonéale chauffée sont particulièrement utiles dans les tumeurs mucineuses de l'appendice. Les tumeurs épithéliales de l'appendice non résécables chirurgicalement avec métastases à distance peuvent bénéficier d'une chimiothérapie adjuvante et de soins palliatifs à base de fluorouracile5.[3]
Suivi
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section traite du suivi de la maladie. |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: |
|
| Exemple: | |
Complications
Toute contribution serait appréciée.
| Description: | Cette section traite des complications possibles de la maladie. |
| Formats: | Liste à puces, Texte |
| Balises sémantiques: | Complication |
| Commentaires: |
|
| Exemple: | Les complications de l'infarctus du myocarde sont :
|
Pseudomyxoma peritonei (PMP) représente la croissance de cellules néoplasiques productrices de mucines dans la cavité péritonéale avec une ascite mucineuse résultante. La PMP peut être le stade de présentation pour une majorité de patients et est classée en fonction du grade comme adénomucinose péritonéale disséminée (DPAM) associée à LAMN et a moins de figures mitotiques et de cellules épithéliales simples et une adénocarcinomatose mucineuse péritonéale de haut grade (PMAC) généralement associée à adénocarcinome mucineux.[4][21][10].[3]
Des adhérences et une obstruction intestinale peuvent généralement survenir dans le cadre d'une maladie métastatique.[15] Métastases ovariennes et rétropéritonéales ainsi qu'hydroureteronephrosis, une complication rare peut survenir.[22][23][3]
Évolution
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section contient le pronostic et évolution naturelle de la maladie. Le pronostic est lié à la survie du patient atteint de la maladie. L'évolution naturelle est la manière dont évoluera la maladie du patient dans le temps. |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: | |
| Exemple: | La dissection aortique est associée une mortalité très élevée. Au moins 30% des patients décèdent après leur arrivée à l'urgence, et ce, même après une intervention chirurgicale. Pour ceux qui survivent à la chirurgie, la morbidité est également très élevée et la qualité de vie est mauvaise. La mortalité la plus élevée d'une dissection aortique aiguë est dans les 10 premiers jours. Les patients qui ont une dissection chronique ont tendance à avoir un meilleur pronostic, mais leur espérance de vie est raccourcie par rapport à la population générale.[1] Sans traitement, la mortalité est de 1 à 3% par heure au cours des 24 premières heures, 30% à une semaine, 80% à deux semaines et 90% à un an. |
Le pronostic dépend du type histologique, du stade avancé et du grade, de la propagation de la mucine au-delà du RLQ ainsi que de la présence de mucine cellulaire.[11] Les taux de survie à cinq ans varient de 27% à 93%. Les tumeurs à cellules en anneau ont le pire pronostic (27%) tandis que les tumeurs neuroendocriniennes sont les plus favorables (93%). [24] Le taux de survie à 10 ans pour l'adénocarcinome mucineux est inférieur à 10% .[25][3]
Prévention
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section traite des mesures préventives et du dépistage précoce de la maladie (lorsque pertinent). |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: | |
| Exemple: | La prévention primaire consiste à la prise en charge des facteurs de risque :
|
Les tumeurs appendiculaires présentent habituellement cliniquement des caractéristiques d'appendicite aiguë et sont souvent diagnostiquées après l'examen histologique d'un échantillon d'appendicectomie. Il est important de faire le suivi de l'examen histologique des échantillons d'appendicectomie pour s'assurer que les tumeurs de l'appendice ne sont pas manquées.
Références
- Cette page a été modifiée ou créée le 2020/09/21 à partir de Appendix Cancer (StatPearls / Appendix Cancer (2020/07/05)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/32310403 (livre).
- ↑ 1,0 et 1,1 https://www.ncbi.nlm.nih.gov/pubmed/12740466
- ↑ 2,0 et 2,1 https://www.ncbi.nlm.nih.gov/pubmed/28663356
- ↑ 3,00 3,01 3,02 3,03 3,04 3,05 3,06 3,07 3,08 3,09 et 3,10 https://www.ncbi.nlm.nih.gov/pubmed/32310403
- ↑ 4,0 et 4,1 https://www.ncbi.nlm.nih.gov/pubmed/26270447
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/25560182
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/3811021
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/8640546
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/7674315
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/10982779
- ↑ 10,0 10,1 et 10,2 Erreur de référence : Balise
<ref>incorrecte : aucun texte n’a été fourni pour les références nommées:7 - ↑ 11,0 11,1 11,2 11,3 et 11,4 https://www.ncbi.nlm.nih.gov/pubmed/23439060
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/16699309
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/17511043
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/17374868
- ↑ 15,0 et 15,1 https://www.ncbi.nlm.nih.gov/pubmed/1609724
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/18328658
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/16973770
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/9716778
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/10235354
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/21970481
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/31069398
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/28598731
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/18291037
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/12115365
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/19641451
