Cancer appendiculaire
| Classe de maladie | |||
 Apparence macroscopique d'un mucocèle appendiculaire | |||
| Caractéristiques | |||
|---|---|---|---|
| Signes | Appendicite, Ascite, Masse abdominale, Péritonisme | ||
| Symptômes |
Appendicite, Anorexie , Syndrome carcinoïde, Fatigue , Douleur abdominale , Asymptomatique , Vomissement , Perte de poids , Température corporelle élevée | ||
| Informations | |||
| Terme anglais | Appendicular neoplasm | ||
| Autres noms | Néoplasie appendiculaire | ||
| Wikidata ID | Q4781026 | ||
| SNOMED CT ID | 363411007 | ||
| Spécialités | Oncologie, Chirurgie générale, Gastro-entérologie | ||
| |||
Le cancer appendiculaire est un cancer de l'appendice. Ces cancers sont souvent trouvées accidentellement lors de l'ablation chirurgicale de l'appendice.[1]
Épidémiologie
Le cancer de l'appendice est observé dans 0,5-1% des prélèvements appendiculaires et a une incidence de 0,97 cas par 100 000 de population [2][3][4][5]. Il y a davantage de tumeurs neuroendocrines chez les jeunes patients et davantage d'adénocarcinomes chez la population plus âgée[6]. Une association accrue avec la néoplasie colique et la colite ulcéreuse chronique a été notée.[4] 20% des cas ont une tumeur colorectale synchrone. Il y a aussi une association avec les tumeurs rénale, ovarienne et mammaire. L'appendice est le deuxième site le plus fréquent pour les tumeurs neuroendocrines après le rectum selon la base de données SEER. Au moment du diagnostic, plus d'un tiers des tumeurs neuroendocriniennes sont métastatiques lors du diagnostic.[7][1]
Classification
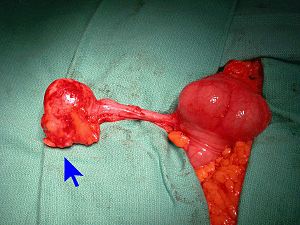

Les tumeurs appendiculaires sont divisées de la manière suivante[8][9][10][1] :
- les tumeurs non épithéliales :
- les tumeurs neuroendocrines[note 1]
- le GIST
- des lymphomes[note 2], dont le lymphome de Burkitt[note 3] et le lymphomes diffus à grandes cellules B[note 4]
- les sarcomes
- les tumeurs épithéliales [11][12]:
- les tumeurs épithéliales non invasives :
- les tumeurs épithéliales invasives
- les adénocarcinomes mucineux (le plus fréquent parmi les adénocarcinomes)
- les adénocarcinomes de type intestinal
- les adénocarcinomes à cellules en bague à chaton
- les tumeurs adénocarcinoïdes[note 8].
Physiopathologie
L'obstruction de la lumière appendiculaire par les cellules malignes entraîne une inflammation de l'appendice, une stase veineuse et, finalement, une infection de l'appendice.[13] Dans les tumeurs mucineuses de l'appendice, il peut y avoir une dilatation kystique de l'appendice due à l'obstruction de la lumière appendiculaire avec création d'un mucocèle.[14][15] Ces processus sont à la base de la présentation clinique la plus courante de cette maladie, l'appendicite aiguë.[1] Quant aux tumeurs neuroendocrines, elles sont souvent trouvées fortuitement dans le spécimen d'une appendicite aiguë.
Les mécanismes qui entraînent des tumeurs malignes appendiculaires ne sont pas bien compris. Cependant, il a été postulé que les néoplasmes mucineux appendiculaires (AMN, un sous-ensemble majeur de tumeurs appendiculaires) suivent la même séquence adénome-carcinome que celle observée dans le cancer colorectal. Cette séquence commence par une mutation ponctuelle dans le proto-oncogène KRAS puis des mutations et/ou des délétions dans le gène TP53 sur le Chr17p. Ensuite, des mutations tronquées sur le gène APC sur 5q et le gène bêta-caténine contribuent toutes à son apparition. Une théorie alternative de l'instabilité des microsatellites (MSI) a été postulée comme résultant de mutations dans les gènes de réparation des mésappariements nucléotidiques, par exemple hMSH2, hMLH1, PMS1, PMS2 et GTBP.[16][17][18][1]
Les adénocarcinomes mucineux ont des glandes invasives avec des atypies de haut-grade et de la mucine extra-cellulaire qui occupent plus de 50% de la lésion. Les lésions expriment les marqueurs p53, CD44 et CDX2, comme leur équivalent colique. La variante avec cellules en bagues à chaton est plus agressive puisque moins bien différenciée et a davantage de métastases lymphatiques. [13]
La lignée épithéliale contient beaucoup de cellules à gobelet pour une production abondante exocrine de mucus. Un mucocèle est une collection de mucine épaissie accumulée par une obstruction. Celle-ci peut être causée par un processus tumoral ou non. Des tumeurs appendiculaires peuvent aussi sécréter de la mucine et causer un mucocèle.
Présentation clinique
Facteurs de risque
Les mêmes facteurs de risque de l'adénocarcinome colique s'appliquent à ceux de l'appendice, excluant les tumeurs neuroendocrines. Les facteurs qui devraient augmenter la suspicion de néoplasie appendiculaire comprennent un âge supérieur à 50 ans avec des antécédents familiaux de cancer du côlon ou de maladie inflammatoire intestinale (MII), des caractéristiques évocatrices d'une appendicite chronique ou la présence d'une anémie inexpliquée.
Questionnaire
Dans plus de 50% des cas, il n'y a aucun symptôme, et cette malignité est détectée accidentellement. Cependant, la plupart des patients symptomatiques se présenteraient sous forme d'appendicite aiguë.[19][5] On doit questionner le patient tel une appendicite s'il se présente à l'urgence. Si le patient est vu en clinique, le patient doit être questionné sur son état général et sa digestion. Il est a noté que le mucocèle est souvent asymptomatique et découvert fortuitement sur l'imagerie.
Le patient peut présenter des douleurs abdominales non spécifiques, des douleurs du quadrant inférieur droit, une perte de poids, une anorexie, de la fièvre, des vomissements, des caractéristiques d'obstruction intestinale et de la fatigue.[14] Dans le cadre d'une tumeur neuroendocrine, un syndrome carcinoïde est également possible avec une charge métastastique au foie.
Examen clinique
À l'examen physique, on recherchera [1]:
- à l'examen abdominal :
- d'un tableau d'appendicite
- du péritonisme
- une masse abdominale au quadrant inférieur droit
- de l'ascite
- des adénopathies à l'examen des aires ganglionnaires.
Examens paracliniques
Imagerie
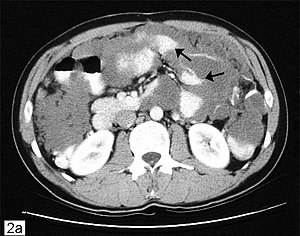
Les études d'imagerie constituent le pilier de l'évaluation initiale[20].
- Pour les mucocèles, les trouvailles à l'échographie abdominale comprennent des masses abdominales allongées ou masses abdominales allongées dans le quadrant inférieur droit avec des caractéristiques d'apparence interne en pelure d'oignon représentant une mucine lamellée, ce qui est une découverte pathognomonique. Un défaut de la paroi appendiculaire avec fuite peut être le signe d'une rupture du mucocèle. [14]
- Chez les patients présentant des caractéristiques d'appendicite aiguë, une TDM abdominopelvienne C+ ou une IRM abdominopelvienne révélant un appendice de plus de 15 mm avec des parois épaissies ou irrégulières est suspect pour une néoplasie.[21] Un nodule rehaussant dans la paroi est évocateur d'un adénocarcinome. S'il y a des bulles d'air dans le mucocèle, celui-ci est probablement surinfecté. Les dépôts mucineux d'un pseudomyxome peritonei peuvent être identifiés facilement à la tomodensitométrie.
- La radiographie abdominale a peu de valeur diagnostique et peut rarement démontrer une calcification curviligne à la fosse iliaque droite.
- La plupart des tumeurs neuroendocrines appendiculaires expriment les récepteurs à la somatostatine et donc une scintigraphie à la somatostatine peut identifier les foyers actifs.
- La tomographie par émission de positron peut être utilisé pour démontrer une maladie métastastique.
- La tomographie par émission de positron au (68Ga)-dotatate est encore plus spécifique et peut détecter jusqu'à 65% de lésions occultes non vues à la scintigraphie à la somatostatine.
Analyses de laboratoire
Tumeur épithéliale
On dose les marqueurs tumoraux suivants lors du diagnostic. Leur valeur prédictive de récidive, de rémission ou de progression n'ont pas été établi[22]. Ils sont néanmoins utilisé pour monitorer la réponse au traitement.
- On dose l'antigène carcinoembryonnaire (CEA) lorsqu'il s'agit d'une tumeur épithéliale maligne comme on le ferait pour un cancer colorectal du reste du cadre colique.[22]
- Un dosage normal du CA-125 lors du diagnostic est favorable et prédit la capacité à faire une cytoréduction complète dans le cadre d'une atteinte péritonéale.[23]
- Un dosage de base élevé du CA 19-9 est un facteur de mauvais pronostic indépendant de survie sans progression et peut être utilisé pour déterminer la récidive après une chirurgie de cytoréduction et chimiothérapie intra-péritonéale. [23][24]
Tumeurs neuroendocrines
Les tumeurs neuroendocrines ne sont pas souvent biochimiquement actives à moins d'avoir une charge métastatique significative particulièrement au niveau hépatique. On dose la chromogranine-A et les 5-HIAA urinaires sur 24h. Des valeurs élevées sont associées à un moins bon pronostic. Ces marqueurs ne sont toutefois pas utiles au diagnostic ou pour guider le plan de traitement.[22]
Colonoscopie
Nous devons faire une colonoscopie en pré-opératoire lorsque le diagnostic est connu par l'imagerie[22]. Si on découvre plutôt le diagnostic en per-opératoire, on doit compléter l'investigation par une colonoscopie 4 à 6 semaines post-opératoire. En effet, il peut y avoir une atteinte du bas fond cécal ou une lésion synchrone colique. La trouvaille classique du mucocèle appendiculaire est l'apparence en volcan avec écoulement de mucine possible. On trouve des adénomes synchrones dans 13% des coloscopies effectuées par les patients avec tumeurs épithéliales[25]. Inversement, on trouve moins de 4% d'adénome appendiculaire chez les patients avec cancer colorectal du reste du cadre colique[26]. Les tumeurs neuroendocrines appendiculaires sont rarement associées à d'autres tumeurs neuroendocrines synchrones, mais elles ont un taux élevé d'adénome ou d'adénocarcinome colorectal. [27]
Approche clinique
L'approche clinique dépend s'il s'agit d'un diagnostic fortuit à l'imagerie ou la pathologie finale d'une appendicectomie, ou plutôt si la néoplasie est diagnostiquée avant l'intervention chirurgicale. Idéalement, il faut débuter par un bilan complet pour document le plus adéquatement le stade de la maladie. Par la suite, si le patient n'est pas métastatique, on procèdera à l'intervention chirurgicale qui sera diagnostique et thérapeutique par le fait-même.
Les buts de l'intervention chirurgicale d'une néoplasie mucineuse sont les suivants :
- diminuer le risque de perforation de la mucocèle (avoir un seuil de conversion en laparotomie bas)
- évaluer le mésoappendice
- évaluer le reste de la cavité abdominale : éliminer collections mucineuses
- évaluer la possibilité d'une tumeur synchrone.
Il est à noter que cette approche est idéalement faite par des chirurgiens-oncologues. S'il s'agit d'une découverte fortuite lors d'une appendicectomie pour appendicite en urgence, les principes demeurent et on documente le plus possible pour en faire part au surspécialiste qui établira la conduite finale à la lumière de la pathologie définitive.
L'approche clinique pour une tumeur neuroendocrine est sensiblement la même, soit évaluer le mésoappendice pour son envahissement ou l'atteinte lymphatique, la charge ganglionnaire et faire le bilan d'extension pour la maladie métastatique.
Diagnostic différentiel
Une masse kystique appendiculaire peut être confondue avec l'une des conditions suivantes[28]
- l'appendicite ou l'abcès appendiculaire
- le lymphangiome kystique
- le kyste mésentérique
- le kyste rétropéritonéal
- le kyste ovarien
- le cancer ovarien
- le diverticule de Meckel
- une maladie de Crohn compliquée
- l'endométriome.
Une néoplasie neuroendocrine solide de l'appendice peut être confondue avec toute pathologie cécale (crohn ou cancer), toute pathologie appendiculaire (l'appendicite le plus fréquemment) ou d'autres néoplasies appendiculaires solides (lymphome, adénocarcinome de type intestinal, sarcome, métastases).
Le staging du cancer appendiculaire peut être consulté ici.
Traitement
Traitement chirurgical
La thérapie chirurgicale est le pilier de la thérapie des cancers de l'appendice. Cependant, les cas avancés avec métastases à distance ou une carcinomatose péritonéale peuvent être chirurgicalement non résécables. L'appendicectomie avec une large résection du mésoappendice afin d'exclure l'atteinte des ganglions lymphatiques peut être à la fois diagnostique et curative pour la plupart des tumeurs appendiculaires.[29]
| Type de tumeur | Traitement chirurgical proposé |
|---|---|
| Tumeur épithéliale de bas grade |
|
| Tumeur épithéliale de haut grade |
|
| Adénocarcinome |
|
| Adénocarcinoïde |
|
| Tumeurs neuroendocrines |
|
| Maladie métastatique |
|
Il n'est pas recommandé de procéder à une résection s'il y a apparence de carcinomatose d'emblée, car ceci ne change pas le pronostic. Une appendicectomie seule avec la chimiothérapie intra-péritonéale est adéquate[22]
Un algorithme de prise en charge pour les adénocarcinome mucineux est présenté ici.
Traitement adjuvant
Pour les tumeurs épithéliales, le traitement adjuvant par chimiothérapie à base de 5-FU est indiqué s'il y a atteinte ganglionnaire ou atteinte péritonéale. Le plan est défini en clinique des tumeurs avec une approche multi-disciplinaire. En effet, la chimiothérapie intra-péritonéale après éradication de toute maladie macroscopique double la survie contrairement à la chimiothérapie seule. [32]
Le traitement adjuvant dépend essentiellement du sous-type histologique et du stade de la maladie.
Suivi
Tumeur épithéliale de bas grade
Il n'y a pas de lignes directrices officielles, mais il est suggéré de faire un minimum de 2 ans de suivi car il y a un faible risque de développer un pseudomyxome péritonéi. Une TDM aux 6 mois pour 2 ans est donc suggéré.[22]
Tumeur épithéliale maligne
Une approche de suivi plus agressive est suggérée et se rapproche de celle utilisée pour le suivi des cancers colorectaux, soit une imagerie aux 4 à 6 mois pour 2 ans, puis aux années pour au moins un total de 5 ans. Les marqueurs sont également dosés. [22]
Tumeur neuroendocrine
Il n'y a aucune ligne directrice standardisée car les séries sont trop petites pour établir des recommandations claires. Il est suggéré de faire des suivis aux 6 à 12 mois, mais pour une durée allant jusqu'à 10 ans après une résection curative. Le tout est modulé selon le degré d'agressivité de la lésion initiale. On dose aussi les marqueurs tumoraux que l'on pourra corréler à une imagerie ciblée. [22]
Évolution
Pour les tumeurs épithéliales mucineuses, le pseudomyxome peritonei est l'évolution redoutée. Pseudomyxoma peritonei (PMP) représente la croissance de cellules néoplasiques productrices de mucines dans la cavité péritonéale. La PMP peut être le stade de présentation pour une majorité de patients et est classée en fonction du grade comme adénomucinose péritonéale disséminée (DPAM) associée à LAMN et a moins de figures mitotiques et de cellules épithéliales simples et une adénocarcinomatose mucineuse péritonéale de haut grade (PMAC) généralement associée à adénocarcinome mucineux.[6][33][1]
Pour les tumeurs neuroendocrines, la maladie métastatique peut évoluer et amener le décès du patient.
Prévention
Les tumeurs appendiculaires présentent habituellement cliniquement des caractéristiques d'appendicite aiguë et sont souvent diagnostiquées après l'examen histologique d'un échantillon d'appendicectomie. Il est important de faire le suivi de l'examen histologique des échantillons d'appendicectomie pour s'assurer que les tumeurs de l'appendice ne sont pas manquées.
Notes
- ↑ 18% des tumeurs neuroendocrines digestives touchent l'appendice. 75% sont situés au tiers distal, 95% ont moins de 2 cm, 10% sont symptomatiques. Les tumeurs sont rarement multicentriques (4,5%).
- ↑ Comme l'appendice est principalement un tissu lymphoïde, des lymphomes appendiculaires peuvent survenir.
- ↑ Âge moyen de 18 ans
- ↑ Chez le sujet âgé
- ↑ LAMNs pour low grade appendiceal mucinous neoplasm. Histologiquement, il s'agit d'un adénome bien différencié. Il peut y avoir de la mucine extraluminale associée. Anciennement, ces lésions étaient communément appelées mucocèle ou cystadénome mucineux.
- ↑ Peuvent être perforée, avoir de la fibrose pariétale, de la mucine qui dissèque la paroi ou de la mucine acellulaire dans les tissus mous péri-appendiculaires.
- ↑ HAMN pour high-grade appendicular mucinous neoplasm. Ils ont les mêmes caractéristiques mais avec des atypies marquées.
- ↑ C'est un mélange entre les tumeurs épithéliales et les tumeurs neuroendocrines. Il s'agit d'une tumeur des cellules à gobelet qui expriment de la chromogranine-A. Son pronostic est moins bon que les tumeurs non épithéliales et doit donc être pris en charge comme un adénocarcinome.
Références
- Cette page a été modifiée ou créée le 2020/09/21 à partir de Appendix Cancer (StatPearls / Appendix Cancer (2020/07/05)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/32310403 (livre).
- Cet article a été créé en partie ou en totalité le 2021-01-01 à partir de Chirurgie (application), créée par Dre Hélène Milot, Dr Olivier Mailloux et collaborateurs et partagé sous la licence CC-BY-SA 4.0 international
- ↑ 1,0 1,1 1,2 1,3 1,4 1,5 et 1,6 Azeberoje Osueni et Yuvraj S. Chowdhury, StatPearls, StatPearls Publishing, (PMID 32310403, lire en ligne)
- ↑ S. J. Connor, G. B. Hanna et F. A. Frizelle, « Appendiceal tumors », Diseases of the Colon & Rectum, vol. 41, no 1, , p. 75–80 (ISSN 0012-3706, DOI 10.1007/bf02236899, lire en ligne)
- ↑ S. J. Connor, G. B. Hanna et F. A. Frizelle, « Appendiceal tumors », Diseases of the Colon & Rectum, vol. 41, no 1, , p. 75–80 (ISSN 0012-3706, DOI 10.1007/bf02236899, lire en ligne)
- ↑ 4,0 et 4,1 Walid L. Shaib, Rita Assi, Ali Shamseddine et Olatunji B. Alese, « Appendiceal Mucinous Neoplasms: Diagnosis and Management », The Oncologist, vol. 22, no 9, , p. 1107–1116 (ISSN 1549-490X, PMID 28663356, Central PMCID 5599200, DOI 10.1634/theoncologist.2017-0081, lire en ligne)
- ↑ 5,0 et 5,1 Perry J. Pickhardt, Angela D. Levy, Charles A. Rohrmann et Amir I. Kende, « Primary neoplasms of the appendix: radiologic spectrum of disease with pathologic correlation », Radiographics: A Review Publication of the Radiological Society of North America, Inc, vol. 23, no 3, , p. 645–662 (ISSN 0271-5333, PMID 12740466, DOI 10.1148/rg.233025134, lire en ligne)
- ↑ 6,0 et 6,1 Walid L. Shaib, Michael Goodman, Zhengjia Chen et Sungjin Kim, « Incidence and Survival of Appendiceal Mucinous Neoplasms: A SEER Analysis », American Journal of Clinical Oncology, vol. 40, no 6, , p. 569–573 (ISSN 1537-453X, PMID 26270447, DOI 10.1097/COC.0000000000000210, lire en ligne)
- ↑ Schelomo Marmor, Pamela R. Portschy, Todd M. Tuttle et Beth A. Virnig, « The rise in appendiceal cancer incidence: 2000-2009 », Journal of Gastrointestinal Surgery: Official Journal of the Society for Surgery of the Alimentary Tract, vol. 19, no 4, , p. 743–750 (ISSN 1873-4626, PMID 25560182, DOI 10.1007/s11605-014-2726-7, lire en ligne)
- ↑ « Référence Tumeurs appendiculaires », sur oncologik.fr (consulté le 27 février 2023)
- ↑ (en) « Types of Appendiceal (Appendix) Cancer | Memorial Sloan Kettering Cancer Center », sur www.mskcc.org (consulté le 27 février 2023)
- ↑ R. J. Stewart et M. Mirakhur, « Primary malignant lymphoma of the appendix », The Ulster Medical Journal, vol. 55, no 2, , p. 187–189 (ISSN 0041-6193, PMID 3811021, Central PMCID 2448335, lire en ligne)
- ↑ Norman J Carr, Frederic Bibeau, Robert F Bradley et Peggy Dartigues, « The histopathological classification, diagnosis and differential diagnosis of mucinous appendiceal neoplasms, appendiceal adenocarcinomas and pseudomyxoma peritonei », Histopathology, vol. 71, no 6, , p. 847–858 (ISSN 0309-0167, DOI 10.1111/his.13324, lire en ligne)
- ↑ K. F. Fournier, R. Royal, L. A. Lambert et M. Taggart, « Mucinous appendiceal tumors of uncertain malignant potential (UMP): Prognostic factors and implications for treatment and follow-up. », Journal of Clinical Oncology, vol. 29, no 4_suppl, , p. 372–372 (ISSN 0732-183X et 1527-7755, DOI 10.1200/jco.2011.29.4_suppl.372, lire en ligne)
- ↑ 13,0 et 13,1 Shayna Brathwaite, Jonathan Rock, Martha M. Yearsley et Tanios Bekaii-Saab, « Mixed Adeno-neuroendocrine Carcinoma: An Aggressive Clinical Entity », Annals of Surgical Oncology, vol. 23, no 7, , p. 2281–2286 (ISSN 1068-9265 et 1534-4681, DOI 10.1245/s10434-016-5179-2, lire en ligne)
- ↑ 14,0 14,1 et 14,2 Sree Harsha Tirumani, Margaret Fraser-Hill, Rebecca Auer et Wael Shabana, « Mucinous neoplasms of the appendix: a current comprehensive clinicopathologic and imaging review », Cancer Imaging: The Official Publication of the International Cancer Imaging Society, vol. 13, , p. 14–25 (ISSN 1470-7330, PMID 23439060, Central PMCID 3582328, DOI 10.1102/1470-7330.2013.0003, lire en ligne)
- ↑ Robert F. Bradley, John H. Stewart, Gregory B. Russell et Edward A. Levine, « Pseudomyxoma peritonei of appendiceal origin: a clinicopathologic analysis of 101 patients uniformly treated at a single institution, with literature review », The American Journal of Surgical Pathology, vol. 30, no 5, , p. 551–559 (ISSN 0147-5185, PMID 16699309, DOI 10.1097/01.pas.0000202039.74837.7d, lire en ligne)
- ↑ M. Perucho, « Microsatellite instability: the mutator that mutates the other mutator », Nature Medicine, vol. 2, no 6, , p. 630–631 (ISSN 1078-8956, PMID 8640546, DOI 10.1038/nm0696-630, lire en ligne)
- ↑ G. Marra et C. R. Boland, « Hereditary nonpolyposis colorectal cancer: the syndrome, the genes, and historical perspectives », Journal of the National Cancer Institute, vol. 87, no 15, , p. 1114–1125 (ISSN 0027-8874, PMID 7674315, DOI 10.1093/jnci/87.15.1114, lire en ligne)
- ↑ D. C. Chung, « The genetic basis of colorectal cancer: insights into critical pathways of tumorigenesis », Gastroenterology, vol. 119, no 3, , p. 854–865 (ISSN 0016-5085, PMID 10982779, DOI 10.1053/gast.2000.16507, lire en ligne)
- ↑ Anupam Dixit, John H. P. Robertson, Satvinder S. Mudan et Charles Akle, « Appendiceal mucocoeles and pseudomyxoma peritonei », World Journal of Gastroenterology, vol. 13, no 16, , p. 2381–2384 (ISSN 1007-9327, PMID 17511043, Central PMCID 4147153, DOI 10.3748/wjg.v13.i16.2381, lire en ligne)
- ↑ Samira M. Sadowski, Vladimir Neychev, Corina Millo et Joanna Shih, « Prospective Study of 68Ga-DOTATATE Positron Emission Tomography/Computed Tomography for Detecting Gastro-Entero-Pancreatic Neuroendocrine Tumors and Unknown Primary Sites », Journal of Clinical Oncology, vol. 34, no 6, , p. 588–596 (ISSN 0732-183X et 1527-7755, DOI 10.1200/jco.2015.64.0987, lire en ligne)
- ↑ Thara Persaud, Niall Swan et William C. Torreggiani, « Giant mucinous cystadenoma of the appendix », Radiographics: A Review Publication of the Radiological Society of North America, Inc, vol. 27, no 2, , p. 553–557 (ISSN 1527-1323, PMID 17374868, DOI 10.1148/rg.272065134, lire en ligne)
- ↑ 22,0 22,1 22,2 22,3 22,4 22,5 22,6 22,7 et 22,8 Sean C. Glasgow, Wolfgang Gaertner, David Stewart et Jennifer Davids, « The American Society of Colon and Rectal Surgeons, Clinical Practice Guidelines for the Management of Appendiceal Neoplasms », Diseases of the Colon and Rectum, vol. 62, no 12, , p. 1425–1438 (ISSN 1530-0358, PMID 31725580, DOI 10.1097/DCR.0000000000001530, lire en ligne)
- ↑ 23,0 et 23,1 S. van Ruth, A. A. M. Hart, J. M. G. Bonfrer et V. J. Verwaal, « Prognostic value of baseline and serial carcinoembryonic antigen and carbohydrate antigen 19.9 measurements in patients with pseudomyxoma peritonei treated with cytoreduction and hyperthermic intraperitoneal chemotherapy », Annals of Surgical Oncology, vol. 9, no 10, , p. 961–967 (ISSN 1068-9265 et 1534-4681, DOI 10.1007/bf02574513, lire en ligne)
- ↑ F. Di Fabio, W. Aston, F. Mohamed et K. Chandrakumaran, « Elevated tumour markers are normalized in most patients with pseudomyxoma peritonei 7 days after complete tumour removal », Colorectal Disease, vol. 17, no 8, , p. 698–703 (ISSN 1462-8910, DOI 10.1111/codi.12924, lire en ligne)
- ↑ R.M. Smeenk, M.L.F. van Velthuysen, V.J. Verwaal et F.A.N. Zoetmulder, « Appendiceal neoplasms and pseudomyxoma peritonei: A population based study », European Journal of Surgical Oncology (EJSO), vol. 34, no 2, , p. 196–201 (ISSN 0748-7983, DOI 10.1016/j.ejso.2007.04.002, lire en ligne)
- ↑ Muhammad Najm Khan et Brendan J. Moran, « Four Percent of Patients Undergoing Colorectal Cancer Surgery may have Synchronous Appendiceal Neoplasia », Diseases of the Colon & Rectum, vol. 50, no 11, , p. 1856–1859 (ISSN 0012-3706, DOI 10.1007/s10350-007-9033-2, lire en ligne)
- ↑ Irvin M. Modlin, Kevin D. Lye et Mark Kidd, « A 5-decade analysis of 13,715 carcinoid tumors », Cancer, vol. 97, no 4, , p. 934–959 (ISSN 0008-543X et 1097-0142, DOI 10.1002/cncr.11105, lire en ligne)
- ↑ Opinion d'expert (Dre Hélène Milot) [3 octobre 2020]
- ↑ R. Miraliakbari et W. H. Chapman, « Laparoscopic treatment of an appendiceal mucocele », Journal of Laparoendoscopic & Advanced Surgical Techniques. Part A, vol. 9, no 2, , p. 159–163 (ISSN 1092-6429, PMID 10235354, DOI 10.1089/lap.1999.9.159, lire en ligne)
- ↑ D. J. Evers et V. J. Verwaal, « Indication for oophorectomy during cytoreduction for intraperitoneal metastatic spread of colorectal or appendiceal origin », British Journal of Surgery, vol. 98, no 2, , p. 287–292 (ISSN 0007-1323, DOI 10.1002/bjs.7303, lire en ligne)
- ↑ John T. Mullen et Diane M.F. Savarese, « Carcinoid tumors of the appendix: A population-based study », Journal of Surgical Oncology, vol. 104, no 1, , p. 41–44 (ISSN 0022-4790, DOI 10.1002/jso.21888, lire en ligne)
- ↑ Vic J. Verwaal, Serge van Ruth, Eelco de Bree et Gooike W. van Slooten, « Randomized Trial of Cytoreduction and Hyperthermic Intraperitoneal Chemotherapy Versus Systemic Chemotherapy and Palliative Surgery in Patients With Peritoneal Carcinomatosis of Colorectal Cancer », Journal of Clinical Oncology, vol. 21, no 20, , p. 3737–3743 (ISSN 0732-183X et 1527-7755, DOI 10.1200/jco.2003.04.187, lire en ligne)
- ↑ Gita Yashwantrao Karande, Wei Ming Chua, Raphael Shih Zhu Yiin et Kang Min Wong, « Spectrum of computed tomography manifestations of appendiceal neoplasms: acute appendicitis and beyond », Singapore Medical Journal, vol. 60, no 4, , p. 173–182 (ISSN 0037-5675, PMID 31069398, Central PMCID 6482419, DOI 10.11622/smedj.2019035, lire en ligne)
