Ulcère duodénal
| Maladie | |||
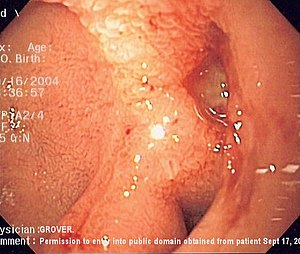 Ulcère duodénal en OGD | |||
| Caractéristiques | |||
|---|---|---|---|
| Signes | Sensibilité à la palpation, Distension abdominale , Signes vitaux normaux | ||
| Symptômes |
Méléna, Douleur épigastrique, Hématémèse, Douleur abdominale, Rectorragies | ||
| Diagnostic différentiel |
Gastrite, Colique biliaire, Syndrome coronarien aigu, Cholécystite aiguë, Pancréatite aiguë, Tumeur duodénale, Reflux gastro-œsophagien, Ulcère gastrique, Dyspepsie (symptôme) | ||
| Informations | |||
| Terme anglais | Duodenal ulcer | ||
| Wikidata ID | Q172941 | ||
| Spécialités | Chirurgie générale, Gastro-entérologie, Médecine d'urgence, Médecine familiale | ||
| |||
L'ulcère duodénal est une perte de la substance muqueuse au niveau du duodénum (le plus souvent au niveau du bulbe) secondaire à l'action corrosive des sécrétions gastriques. L'ulcération se produit à la suite de dommages à la muqueuse qui s'étendent au-delà de la couche superficielle et atteignent la muscularis mucosae.
Épidémiologie
Près de 5 à 10 % de la population développera un ulcère peptique au cours de sa vie[1][2]. L'ulcère duodénal est le plus fréquent et représente le 2/3 des ulcères peptiques[3]. L'incidence est de 1 à 2 %, mais la maladie est plus fréquente dans les zones où l'incidence de H. pylori est plus élevée[4][5]. Les ulcères duodénaux peuvent survenir dans n'importe quel groupe d'âge. Cependant, ils sont le plus souvent diagnostiqués chez les patients âgés de 20 à 45 ans et sont plus fréquents chez les hommes que chez les femmes.
Étiologies
Les deux principales causes d'ulcère duodénal sont des antécédents d'utilisation récurrente ou importante d'AINS ainsi qu'un diagnostic de helicobacter pylori[6]. D'autres causes d'ulcères duodénaux incluent le syndrome de Zollinger-Ellison et les antécédents de chimiothérapie[7].
Physiopathologie
Infection à H. pylori
H. pylori est retrouvé chez jusqu'à 90 % des cas d'ulcère duodénal. Le mécanisme par lequel H. pylori prédispose les individus n'est pas clair. On pense que la colonisation par H. pylori et l'inflammation persistante entraînent un affaiblissement de la couche superficielle de la muqueuse, ce qui la rend vulnérable à l'acide gastrique. Il est possible que H. pylori augmente la production d'acide par l'intermédiaire des mécanismes inflammatoires[8][7]. Les médiateurs inflammatoires libérés diminuent l'activité des cellules D sécrétant la somatostatine, ce qui entraîne une hyperactivité des cellules G sécrétrices de gastrine et stimule la production d'acide par les cellules pariétales.
AINS
Les prostaglandines jouent un rôle crucial dans le développement de la muqueuse protectrice de l'intestin grêle. Leur synthèse est catalysée par l'enzyme cyclooxygénase (COX), qui existe sous deux isoformes, COX-1 et COX-2. Les AINS agissent en inhibant la voie médiée par COX-1 et COX-2, et leur utilisation prolongée entraîne une diminution importante et persistante des prostaglandines conduisant à une susceptibilité aux lésions muqueuses[7].
Complications
L'hémorragie résulte de l'érosion d’un vaisseau sanguin de la muqueuse duodénale par un ulcère. L'ulcère peut aussi pénétrer la musculeuse, sans rencontrer un vaisseau sanguin, jusqu’à perforer la séreuse. Les vaisseaux principaux qui peuvent être rencontrés sont l'artère gastroduodénale et les artères pancréaticoduodénales supéro-antérieure et postérieure[9].
Présentation clinique
Facteurs de risque
Les facteurs de risque d'ulcère duodénal sont les suivants :
- l'infection à helicobacter pylori
- la prise d'acide acétylsalicylique ou d'AINS, particulièrement si les patients présentent les caractéristiques suivantes :
- une durée de traitement supérieure à 1 semaine
- une dose élevée
- le type d'AINS (risque plus élevé avec l'indométacine et le naproxène, par exemple)[10]
- la prise concomitante de corticostéroïdes, d'anticoagulants ou d'inhibiteurs sélectifs de la recapture de la sérotonine (ISRS)
- un âge supérieur à 60 ans
- le tabagisme
- l'alcool
- les antécédents familiaux d'ulcère peptique.
Questionnaire
Les patients peuvent présenter les symptômes suivants :
- une douleur abdominale épigastrique
- de l'hématémèse
- du méléna
- des rectorragies.
En cas de perforation, la douleur abdominale est subite, aiguë et sévère.
Examen clinique
À l'examen physique, on peut noter les signes suivants :
- les signes vitaux sont normaux, à moins d'une perforation[note 1]
- l'examen abdominal pour révéler :
- une sensibilité à la palpation épigastrique
- une distension abdominale
- il faut rechercher les signes de complication : l'abdomen de bois, un rebond positif, une diminution du péristaltisme (iléus).
Examens paracliniques
En général, les examens requis sont :
- une FSC : l'anémie ferriprive est fréquente, mais la thrombocytopénie est également importante à obtenir
- les ions et la créatininémie : important pour calculer les doses éventuelles des médicaments, pour l'administration de soluté (le cas échéant), pour dépister l'IRA ou l'IRC
- l'INR et le TCA (dépister les coagulopathies)
- un grouper-croiser (en cas de saignement important)
- un gaz veineux et des lactates (en cas de saignement important ou pour dépister un choc hémorragique).
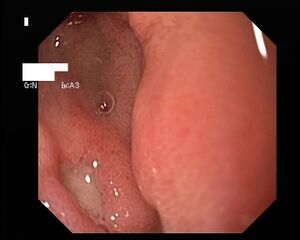
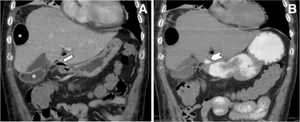
Imagerie
- L'OGD est l'examen de choix pour visualiser l'ulcère duodénal. La plupart sont situés dans la première partie du duodénum à moins de 3 cm du pylore[11]. L'OGD n'est pas requise lorsque la radiographie permet de détecter un ulcère non compliqué, mais est recommandée chez les patients présentant des symptômes réfractaires à la thérapie pour éliminer une autre cause d'ulcère. Contrairement aux ulcères gastriques, les ulcères duodénaux présentent rarement un risque néoplasique et la biopsie de routine n'est donc pas indiquée[12].
- La tomodensitométrie peut détecter les ulcères duodénaux perforés.
- Le repas baryté avec contraste est une option pour les patients présentant des contre-indications à l'OGD :
- le baryum est privilégié comme agent de contraste en électif
- on favorise l'hydrosoluble en urgence si on a un doute sur une perforation.
- À la radiographie de l'abdomen, en position debout, de l'air sous les coupoles est visible s'il y a perforation.
H. pylori
Une fois le diagnostic de l'ulcère gastro-duodénal posé, il est essentiel d'établir l'étiologie de la maladie pour orienter le traitement et prévenir les récidives[7]. La recherche de H. pylori est indiquée pour tous les patients. Les options de dépistage sont présentées dans le tableau suivant[7][13][14].
| Méthode | Indication | Caractéristiques |
|---|---|---|
| Test respiratoire à l'urée |
|
|
| Sérologie pour l'Helicobacter pylori (ELISA) |
|
|
| Biopsie duodénale et uréase rapide (CLO test) |
|
|
| Culture d'une biopsie duodénale |
|
|
| Biopsie duodénale sur gastroscopie (protocole de Sydney) |
|
|
Approche clinique
Le diagnostic d'ulcère duodénal ou gastrique doit être considéré chez les patients présentant des symptômes de dyspepsie ou de douleur abdominale haute qui rapportent également des antécédents d'utilisation d'AINS ou un diagnostic antérieur de Helicobacter pylori. Le tableau ci-dessous présente les principales différences entre l'ulcère gastrique et duodénal. Tout patient chez qui est diagnostiqué un ulcère gastro-duodénal doit subir un test de dépistage de H. pylori[7]. Chez les jeunes patients avec un ulcère loin du bulbe duodénal, il est indiqué de mesurer le taux de gastrine à jeun pour écarter la présence d'un gastrinome.
| Ulcère gastrique | Ulcère duodénal | |
|---|---|---|
| Présentation clinique |
|
|
| Mécanisme |
|
|
| Risque de néoplasie |
|
|
Diagnostic
Le diagnostic de l'ulcère duodénal peut être fait directement par la visualisation de l'ulcère en endoscopie supérieure.
Diagnostic différentiel
Le diagnostic différentiel de l'ulcère duodénal peut inclure[7][15] :
- un ulcère gastrique
- une gastrite
- une pancréatite aiguë
- un reflux gastro-œsophagien
- une cholécystite aiguë
- une colique biliaire
- un syndrome coronarien aigu
- de la dyspepsie
- une tumeur duodénale.
Traitement
Traitement médical
Les IPP sont à prescrire chez tous les patients : cela permet de soulager les symptômes et favoriser la guérison de l'ulcère. La durée du traitement est généralement de 4 à 8 semaines et varie fortement en fonction des symptômes, du niveau d'observance ainsi que du risque de récidive. En présence de complications, un traitement plus long sera nécessaire (8 à 12 semaines) ou jusqu'à ce que la résolution de l'ulcère soit confirmée par une nouvelle endoscopie. La durée du traitement dépend également du statut H. pylori. S'il est traité, l'ulcère guérira de lui-même par la suite et le traitement par IPP pourra être cessé après la résolution des symptômes.
Pour les patients anémiques, du fer PO sera prescrit jusqu'à la résolution de l'anémie. Typiquement, il s'agit d'un traitement de sulfate ferreurs 300 mg PO die X 3 mois.
D'autres interventions incluent de[7] :
- cesser le tabagisme, la consommation d'alcool et de caféine
- cesser ou réduire la prise d'AINS.
Éradication de Helicobacter pylori
L'éradication de H. pylori est associée à une amélioration des symptômes et à des taux plus faibles de récidive. Les thérapies disponibles permettent d'obtenir un taux d'éradication pouvant aller jusqu'à 90 %[16]. La première ligne de traitement est[17] :
- la quadruple thérapie concomitante sans bismuth (inhibiteur de la pompe à proton BID + clarithromycine 500 mg BID + métronidazole 500 mg BID + amoxicilline 1 g BID x 14 jours[note 2]) OU
- le bismuth en quadruple thérapie (IPP BID + métronidazole 500 mg QID + tétracycline 500 mg QID + bismuth QID x 14 jours).
Prise en charge des complications
L'OGD dans les 24 heures suivant l'admission réduit les besoins en transfusion sanguine et la durée de l'hospitalisation. Les patients hémodynamiquement stables avec un faible risque de complication peuvent obtenir leur congé après la procédure. Le traitement endoscopique est indiqué afin de prévenir la récurrence de saignement dans les cas suivants[18] :
- les caillots adhérents
- les vaisseaux visibles
- le saignement actif.
Malgré une prise en charge appropriée, une récidive du saignement peut survenir chez jusqu'à 10 % des patients[18]. Le traitement endoscopique peut alors être répété avant de passer au traitement chirurgical ou angiographique.
| Complication | Description de la prise en charge |
|---|---|
| Hémorragie | 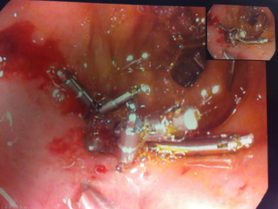
En cas d'échec de l'intervention endoscopique ou si le patient est hémodynamiquement instable malgré une réanimation adéquate, envisager[22] :
Si le patient est hémodynamiquement stable, envisager une procédure chirurgicale anti-reflux acide[22] :
|
| Perforation | 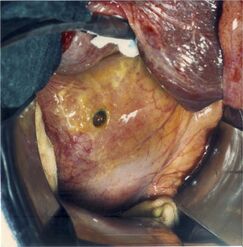
|
| Obstruction | En cas d'obstruction persistante malgré l'éradication de H. pylori, la dilatation par ballon endoscopique devrait être tentée[25]. Si le traitement endoscopique échoue, une gastrojéjunostomie chirurgicale peut être nécessaire. |
Suivi
Il est nécessaire de confirmer l'éradication 4 semaines après le traitement de H. pylori. Plus de 90 % des ulcères duodénaux guérissent après quatre semaines de traitement avec un IPP. Lorsqu'un ulcère duodénal répond aux IPP, au traitement d'éradication de H. pylori et à l'arrêt des AINS, une endoscopie de suivi n'est pas nécessaire. L'endoscopie de suivi est indiquée en cas de symptômes réfractaires pour éliminer une autre cause d'ulcère[26].
Complications
Les principales complications associées aux ulcères duodénaux sont les suivantes[27][7] :
- l'hémorragie digestive haute
- la perforation (2-10 %) et la péritonite
- l'obstruction gastrique distale secondaire à l'œdème ou à la fibrose.
Évolution
Le pronostic des ulcères duodénaux est variable en fonction de la gravité de la présentation initiale. Les ulcères duodénaux principalement causés par l'utilisation d'AINS peuvent être résolus par l'arrêt du médicament et le traitement des symptômes avec des taux de résolution élevés. Les personnes qui ont développé des ulcères à cause d'une infection à H. pylori nécessiteront un traitement de l'infection et les taux de résolution varieront en fonction de son éradication. Les patients qui présentent une ulcération ou une perforation sévère auront des taux de mortalité plus élevés et seront à risque de complications associées à une intervention chirurgicale. L’hémorragie digestive peut entraîner la mort dans 5 à 10 % des cas[7][28].
Prévention
Les mesures de prévention de l'ulcère duodénal sont les suivantes[7] :
- cessation tabagique
- réduire la consommation d'alcool
- éviter la prise d'AINS.
Notes
Références
- Cet article a été créé en partie ou en totalité le 2021/04/22 à partir de Chirurgie (application), créée par Dre Hélène Milot, Dr Olivier Mailloux et collaborateurs et partagé sous la licence CC-BY-SA 4.0 international
- Cette page a été modifiée ou créée le 2021/01/26 à partir de Duodenal Ulcer (StatPearls / Duodenal Ulcer (2020/04/29)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/32491322 (livre).
- ↑ Pertti Aro, Tom Storskrubb, Jukka Ronkainen et Elisabeth Bolling-Sternevald, « Peptic Ulcer Disease in a General Adult Population: The Kalixanda Study: A Random Population-based Study », American Journal of Epidemiology, vol. 163, no 11, , p. 1025–1034 (ISSN 0002-9262, DOI 10.1093/aje/kwj129, lire en ligne)
- ↑ Angel Lanas et Francis K L Chan, « Peptic ulcer disease », The Lancet, vol. 390, no 10094, , p. 613–624 (ISSN 0140-6736, DOI 10.1016/s0140-6736(16)32404-7, lire en ligne)
- ↑ D. R. Cave, « Transmission and epidemiology of Helicobacter pylori », The American Journal of Medicine, vol. 100, no 5A, , p. 12S–17S; discussion 17S–18S (ISSN 0002-9343, PMID 8644777, DOI 10.1016/s0002-9343(96)80224-5, lire en ligne)
- ↑ R. E. Pounder et D. Ng, « The prevalence of Helicobacter pylori infection in different countries », Alimentary Pharmacology & Therapeutics, vol. 9 Suppl 2, , p. 33–39 (ISSN 0269-2813, PMID 8547526, lire en ligne)
- ↑ Angel Lanas et Francis K L Chan, « Peptic ulcer disease », The Lancet, vol. 390, no 10094, , p. 613–624 (ISSN 0140-6736, DOI 10.1016/s0140-6736(16)32404-7, lire en ligne)
- ↑ B. J. Marshall et J. R. Warren, « Unidentified curved bacilli in the stomach of patients with gastritis and peptic ulceration », Lancet (London, England), vol. 1, no 8390, , p. 1311–1315 (ISSN 0140-6736, PMID 6145023, DOI 10.1016/s0140-6736(84)91816-6, lire en ligne)
- ↑ 7,00 7,01 7,02 7,03 7,04 7,05 7,06 7,07 7,08 7,09 et 7,10 Gisela A. Ocasio Quinones et Andrew Woolf, StatPearls, StatPearls Publishing, (PMID 32491322, lire en ligne)
- ↑ J. E. Crabtree, « Gastric mucosal inflammatory responses to Helicobacter pylori », Alimentary Pharmacology & Therapeutics, vol. 10 Suppl 1, , p. 29–37 (ISSN 0269-2813, PMID 8730257, DOI 10.1046/j.1365-2036.1996.22164003.x, lire en ligne)
- ↑ Shimpei Anami, Hiroki Minamiguchi, Naoaki Shibata et Takao Koyama, « Successful endovascular treatment of endoscopically unmanageable hemorrhage from a duodenal ulcer fed by a renal artery: A case report », World Journal of Clinical Cases, vol. 6, no 15, , p. 1012–1017 (ISSN 2307-8960, PMID 30568956, Central PMCID 6288507, DOI 10.12998/wjcc.v6.i15.1012, lire en ligne)
- ↑ Musa Drina, « Peptic ulcer disease and non-steroidal anti-inflammatory drugs », Australian Prescriber, vol. 40, no 3, , p. 91–93 (PMID 28798512, Central PMCID PMC5478398, DOI 10.18773/austprescr.2017.037, lire en ligne)
- ↑ (en) « Peptic ulcer differential diagnosis - wikidoc », sur www.wikidoc.org (consulté le 23 avril 2021)
- ↑ (en) Subhas Banerjee, Brooks D. Cash, Jason A. Dominitz et Todd H. Baron, « The role of endoscopy in the management of patients with peptic ulcer disease », Gastrointestinal Endoscopy, vol. 71, no 4, 2010-04-xx, p. 663–668 (DOI 10.1016/j.gie.2009.11.026, lire en ligne)
- ↑ (en) « Chirurgie », sur App Store (consulté le 24 avril 2021)
- ↑ Julia Fashner et Alfred C. Gitu, « Diagnosis and Treatment of Peptic Ulcer Disease and H. pylori Infection », American Family Physician, vol. 91, no 4, , p. 236–242 (ISSN 0002-838X et 1532-0650, lire en ligne)
- ↑ J. G. Meran, S. Wagner, J. Hotz et M. Manns, « [Differential diagnosis of peptic ulcer] », Wiener Medizinische Wochenschrift (1946), vol. 142, no 8-9, , p. 154–161 (ISSN 0043-5341, PMID 1509765, lire en ligne)
- ↑ William D. Chey, Grigorios I. Leontiadis, Colin W. Howden et Steven F. Moss, « ACG Clinical Guideline: Treatment of Helicobacter pylori Infection », The American Journal of Gastroenterology, vol. 112, no 2, , p. 212–239 (ISSN 1572-0241, PMID 28071659, DOI 10.1038/ajg.2016.563, lire en ligne)
- ↑ (en) Carlo A. Fallone, Naoki Chiba, Sander Veldhuyzen van Zanten et Lori Fischbach, « The Toronto Consensus for the Treatment of Helicobacter pylori Infection in Adults », Gastroenterology, vol. 151, no 1, , p. 51–69.e14 (ISSN 0016-5085 et 1528-0012, DOI 10.1053/j.gastro.2016.04.006, lire en ligne)
- ↑ 18,0 et 18,1 Hwai-Jeng Lin, Kun Wang, Chin-Lin Perng et Rudy Tan Chua, « Early or Delayed Endoscopy for Patients with Peptic Ulcer Bleeding », Journal of Clinical Gastroenterology, vol. 22, no 4, 1996-06-xx, p. 267–271 (ISSN 0192-0790, DOI 10.1097/00004836-199606000-00005, lire en ligne)
- ↑ J. Y. Lau, J. J. Sung, Y. H. Lam et A. C. Chan, « Endoscopic retreatment compared with surgery in patients with recurrent bleeding after initial endoscopic control of bleeding ulcers », The New England Journal of Medicine, vol. 340, no 10, , p. 751–756 (ISSN 0028-4793, PMID 10072409, DOI 10.1056/NEJM199903113401002, lire en ligne)
- ↑ (en) Loren Laine et Dennis M Jensen, « Management of Patients With Ulcer Bleeding », American Journal of Gastroenterology, vol. 107, no 3, 2012-03-xx, p. 345–360 (ISSN 0002-9270, DOI 10.1038/ajg.2011.480, lire en ligne)
- ↑ (en) Loren Laine et Dennis M Jensen, « Management of Patients With Ulcer Bleeding », American Journal of Gastroenterology, vol. 107, no 3, 2012-03-xx, p. 345–360 (ISSN 0002-9270, DOI 10.1038/ajg.2011.480, lire en ligne)
- ↑ 22,0 et 22,1 (en) « Chirurgie », sur App Store (consulté le 6 mai 2021)
- ↑ (en) Subhas Banerjee, Brooks D. Cash, Jason A. Dominitz et Todd H. Baron, « The role of endoscopy in the management of patients with peptic ulcer disease », Gastrointestinal Endoscopy, vol. 71, no 4, 2010-04-xx, p. 663–668 (DOI 10.1016/j.gie.2009.11.026, lire en ligne)
- ↑ (en) « Chirurgie », sur App Store (consulté le 6 mai 2021)
- ↑ Anila Kumar et Pavan Annamaraju, StatPearls, StatPearls Publishing, (PMID 32491758, lire en ligne)
- ↑ (en) Subhas Banerjee, Brooks D. Cash, Jason A. Dominitz et Todd H. Baron, « The role of endoscopy in the management of patients with peptic ulcer disease », Gastrointestinal Endoscopy, vol. 71, no 4, 2010-04-xx, p. 663–668 (DOI 10.1016/j.gie.2009.11.026, lire en ligne)
- ↑ Stephen W. Behrman, « Management of complicated peptic ulcer disease », Archives of Surgery (Chicago, Ill.: 1960), vol. 140, no 2, , p. 201–208 (ISSN 0004-0010, PMID 15724004, DOI 10.1001/archsurg.140.2.201, lire en ligne)
- ↑ Pierre Poitras et Marc Bilodeau, L'appareil digestif : des sciences fondamentales à la clinique, dl 2020 (ISBN 978-2-7606-4157-0 et 2-7606-4157-0, OCLC 1178667316, lire en ligne)
