ULaval:MED-1230/Maladies du nouveau-né
Le nouveau-né normal est né entre 37 et 42 semaines et pèse de 2.5 à 3.8 kg. Au-delà de ces valeurs, le nouveau-né est davantage vulnérable à toutes sortes de problématiques de santé.
Retard de croissance
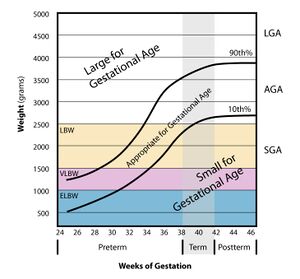
Aussi abrévié PAG ("petit pour âge gestationnel").
- < 10e rang percentile ou < 2 déviations standards
- < 2.5 kg[note 1]
Le Retard de croissance in utero (RCIU) correspond à un poids inférieur au 3e percentile.
Le retard de croissance touche 3 à 10% des nouveau-nés. C'est une incapacité à atteindre son plein potentiel de croissance par une atteinte génétique ou environnementale. Il faut distinguer le retard de croissance de la prématurité (< 37 semaines) car il est normal d’être petit dans ce cas. La courbe de croissance intra-utérine est mesurée selon trois paramètres:
- la taille
- le périmètre crânien
- la masse à la naissance
On retrouve deux types de retard de croissance :
Asymétrique
- Poids < taille < périmètre crânien (la taille et le périmètre crânien sont souvent préservés). Il est causé par un apport nutritionnel compromis in-utéro, voici les principales causes :
- Placentaires (décollement, anomalie morphologique, infarctus, infection)
- Maternelles (maladie chronique, hypoxémie, malnutrition, substances toxiques)
- Fœtales (grossesse multiple)
Le retard de croissance survient la plupart du temps plus tardivement (2e ou 3e trimestre)
Symétrique
Atteinte des 3 paramètres de croissance, dont le périmètre crânien, l’atteinte est donc proportionnelle (poids, taille et périmètre crânien). Le retard de croissance symétrique est plus inquiétant que l’asymétrique; diagnostic plus inquiétant.
Le retard de croissance survient la plupart du temps plus précocement que le type asymétrique.
Les principales causes sont :
- Anomalies chromosomiques
- Syndrome génétique
- Infection congénitale virale
- Exposition à des tératogènes
Le retard de croissance nous inquiète car il peut entraîner plusieurs complications :
- Asphyxie périnatale
- Hypothermie
- Hypoglycémie[note 2]
- Polycythémie (plus de GR)
- Intolérance digestive
- Entérocolite nécrosante
Le pronostic varie selon l’étiologie en cause, mais la mortalité est supérieure chez ces enfants. De plus, on sait qu’à long terme :
- Il peut y avoir une altération du potentiel de croissance ayant un impact sur la taille future.
- Il y a un risque dans le développement neurologique
- L’enfant sera plus à risque d’avoir un syndrome métabolique ultérieur (HTA et diabète)
Macrosomie
Souvent abrévié GAG ("gros pour l'âge gestationnel").
- > 90e rang percentile
- > 3.8 kg
Historiquement, la définition de Macrosomie était simplement enfant de plus de 4 kg sans tenir compte de l'âge gestationnel, et du fait qu'un nouveau né de 27 semaines n'aura pas 4 kg, mais peut avoir des complications liées à son poids au 99 percentile pour sa maturité. Couramment les deux termes GAG et macrosomie sont souvent intervertis.
Plusieurs complications peuvent survenir chez l’enfant macrosome :
- Augmentation de l’incidence des césariennes et des instrumentations
- Risque d’accouchement difficile
- Asphyxie
- Aspiration méconiale
- Risque de traumatisme obstétrical
- Hypoglycémie: lorsqu’un bébé est gros, c’est souvent parce qu’il a eu un apport important en insuline pendant la grossesse. Il est donc à risque élevé d’hypoglycémie à la naissance.[note 3]
Il faudra alors faire une surveillance accrue du nouveau-né :
- Examen complet (évauation du risque syndromique)
- Recherche de fracture de clavicule et d’atteinte du plexus brachial
- Surveillance systématique de la glycémie
Hypothermie
Les nouveau-nés qui sont particulièrement vulnérables à l’hypothermie sont :
- Petit poids de naissance; particulièrement si < 32 semaines
- Les nouveau-nés nécessitant une réanimation prolongée
- Les nouveau-nés qui sont très malades
La perte de chaleur peut se faire par conduction (contact avec des objets froids ou mouillés)
- On va préchauffer la balance et les cassettes de radiographies
- On va couvrir la balance avec une couverture chaude
- On doit toutefois utiliser avec prudence la chaleur radiante
La perte de chaleur peut se faire par convection (air froid et courant d’air)
- On va s’éloigner des courants d’air
- On va élever les côtés du lit
- On va fermer les portes
- On va augmenter la température ambiante
La perte de chaleur peut se faire par évaporation (après l’accouchement, le bain ou l’application de linges humides)
- On va sécher complètement le nouveau-né
- On va remplacer les linges mouillés
- On va utiliser prudemment la chaleur radiante
- On ne baignera pas un bébé qui est compromis
La perte de chaleur peut se faire par radiation (murs et vitres froides)
- On va utiliser un incubateur à double parois
- On va utiliser la sonde thermique de la table chauffante
- On va s’éloigner des murs extérieurs et des fenêtres
L’hypothermie est très néfaste pour les nouveau-nés.
- Entraîne une libération de noradrénaline
- Effet direct: vasoconstriction donc hypoxie et hypoxémie puis acidose lactique
- Effet direct noradrénergique: augmentation du taux métabolique et consommation O2 donc hypoxie puis acidose lactique
- Effet indirect noradrénergique: augmentation de l'utilisation des graisses brunes alors risque d'acidose lactique
- Une production importante d’acide lactique peut mener au décès.
Détresse respiratoire
À la naissance, plusieurs mécanismes de transition se mettent en branle :
- Résorption du liquide alvéolaire (mécanisme le plus fréquemment problématique)
- Ouverture et expansion alvéolaire
- Diminution des résistances pulmonaires vasculaires
- Fermeture du canal artériel
Il existe donc une multitude de causes à la détresse respiratoire. La détresse respiratoire est un symptôme fréquent et non-spécifique alors on doit toujours penser à éliminer une infection. Évidemment, la détresse respiratoire est une urgence.
| Origine | Cause |
|---|---|
| Pulmonaire |
|
| Infectieuse |
|
| Cardiaque |
|
| Neurologique |
|
| Génétique | Cause métabolique |
| Hématologique |
|
Tachypnée transitoire du nouveau-né

Condition de détresse respiratoire la plus fréquente, mais heureusement, elle est bénigne. Elle est causée par un défaut de résorption du liquide alvéolaire.
- Détresse respiratoire débute rapidement après la naissance (< 2 heures)
- Résolution se fait habituellement en 12 à 24 heures, peut aller jusqu’à 72 heures si la condition est sévère
Les facteurs de risque :
- Césarienne
- Accouchement rapide.
À la radiographie pulmonaire:
- Grands volumes pulmonaire
- Vascularisation proéminente
- Présence de liquide dans les scissures.
Ces nouveau-nés ont besoin d’un traitement de support (O2 habituellement < 40%)
Membranes hyalines

Cette condition est causée par un déficit en surfactant, une substance sécrété par les pneumocytes de type 2 et rendant les alvéoles moins difficiles à ouvrir. Sans ce surfactant, le nouveau-né est alors incapable de générer une pression inspiration suffisante pour ouvrir les alvéoles et il s’en suit une micro-atélectasie progressive.
La détresse respiratoire apparaît de façon progressive et le pic se situe à 24-48 heures.
Les facteurs de risque :
- Prématurité
- Mère diabétique
Radiographie pulmonaire :
- Petits volumes pulmonaires
- Un fin granité reflétant l’atélectasie alvéolaire
- Un bronchogramme aérien.
Traitement de support :
- Peep (positive end-expiratory pressure)
- Surfactant exogène
- Intubation
Anamnèse et examen si détresse respiratoire
Plusieurs informations sont utiles à l’anamnèse :
- Âge gestationnel, grossesse et accouchement
- Apgar et poids à la naissance
- Facteurs de risque infectieux
- Évolution de la détresse
- Lien avec l’alimentation?[note 4]
À l’examen clinique, on recherche :
- Tachypnée / Signes de détresse respiratoire ( FR > 60/min)
- Rechercher le tirage
- Battement des ailes du nez
- Sus-sternal (surtout signe d'une obstruction respirtoire)
- Sous-sternal
- Intercostal
- Sous-costal
- Plainte expiratoire (grunting) (audible avec/sans stéthoscope)
- Symétrie du murmure vésiculaire
- Rechercher le tirage
- Signes de fatigue (apnée et bradycardie)
- FR < 40/min
- Apnée
- Gasping (signe de mauvais augure)
Les investigations à faire sont :
- Radiographie pulmonaire
- Gaz sanguin (artériel ou capillaire)
- Hématocrite (FSC avec différentielle)
Traitement
- Selon la cause spécifique.
- Support ventilatoire doit être installé selon la sévérité
- Toujours considérer les antibiotiques si la cause est infectieuse.
Infections
Les facteurs de risque pour l'infection du nouveau-né sont multiples.
- Avant l’accouchement
- Dépistage maternel positif pour le streptocoque du groupe B
- Bactériurie maternelle au streptocoque du groupe B
- Infection maternelle
- Naissance antérieure d’un bébé avec le streptocoque du groupe B
- Mort-né antérieur à terme inexpliqué
- Pendant l’accouchement
- Travail prématuré
- Rupture prématuré des membranes
- Rupture des membranes depuis plus de 18 heures
- Température maternelle (≥ 38°C)
- Signes et symptômes de chorioamnionite
- Présence de liquide méconial
- Néonatal
- Besoin de réanimation ou de procédures invasives
- Prématurité (car peut être dû à une infection)
Les signes et symptômes cliniques de l’infection du nouveau-né sont non-spécifiques. Puisque le système immunitaire du nouveau-né est immature, l’infection peut amener une détérioration rapide et dévastatrice.
- Instabilité thermique
- Détresse respiratoire ou apnées
- Tachycardie ou choc
- Atteinte de l’état général
- Léthargie ou irritabilité
- Intolérance digestive
- Ictère
- Hépatosplénomégalie
- Pétéchies
- Cyanose
Lorsque l'instabilité thermique, la détresse respiratoire et la tachycardie sont présente, il y a un risque de détérioration rapide.
Les principaux agents infectieux retrouvés sont :
- Streptocoque du groupe B (le plus fréquent)
- Escherichia Coli[note 5]
- Listeria monocytogenes
- Haemophilus influenzae
- Virus, moins fréquent, mais il ne faut pas manquer l’herpès
Investigation
- Hémoculture
- Formule sanguine complète avec différentielle
- PCR si disponible
- Radiographie s'il y a symptômes respiratoires
- Ponction lombaire si la méningite fait partie du diagnostique différentiel.
Traitement
- Antibiothérapie IV : Ampicilline + gentamicine ou tobramycine (car certains germes résistants)
- Surveiller et traiter les complications de l’infection :
- Choc
- Hypoglycémie
- Thrombocytopénie
- Coagulopathie
- TOUJOURS évaluer la possibilité d’une méningite.
Hypoglycémie
Le glucose est le principal substrat énergétique cérébral. Puisqu’il y a une augmentation relative de la masse cérébrale chez le nouveau-né p/r au reste du corps, celui-ci a une consommation plus importante (6 mg / kg / min). L’hypoglycémie entraîne un risque de séquelles neurologiques à long terme.
L’hypoglycémie se définit comme[note 6] :
- En post-natal immédiat : < 2.2 - 2.6 mmol/L
- Maintient : < 2.8 - 3 mmol/L
Étiologies de l’hypoglycémie :
- Apport insuffisant
- Diminution des réserves en glycogène (prématuré, RCIU)
- Hyperinsulinisme
- Diabète gestationnel
- Macrosomie
- Beckwith
- Désordres endocriniens
- Polycythémie (les globules rouges utilisent uniquement le glucose)
- Consommation accrue d'énergie (états adrénergiques): infection, hypothermie, anoxie, choc
| Problème | Mécanisme |
|---|---|
| Retard de croissance intra-utérin ou PAG | ↓ Glycogène |
| Prématurité | |
| Macrosomie | Hyperinsulinisme |
| Diabète gestationnel | |
| Stress physiologique (ex: infection) | ↑ Utilisation du glucose |
Examen clinique
- État nutritionnel
- Signes de sepsis ou de choc
- Recherche d'un syndrome
- Anomalie endocrinienne ou métabolique
- Évaluation de l'état neurologique (c'est là que les principaux symptômes se manifesteront)
Il faut TOUJOURS contrôler la glycémie capillaire par une glycémie laboratoire. Cependant, il ne faut pas attendre la valeur du laboratoire avant d'initier un traitement.
Les symptômes d’hypoglycémie sont non-spécifiques :
- Tremblements et trémulations
- Agitation
- Instabilité thermique
- Hypothermie
- Apathie, léthargie et hypotonie
- Apnée et respirations irrégulières ou tachypnée
- Mauvaise succion ou refus de boire (difficulté à alimenter)
- Vomissement
- Cyanose
- Cri (pleurs) perçant ou faible
- Convulsion si sévère
Traitement
Pour prévenir l’hypoglycémie, il faut principalement éviter l’hypothermie et le jeûne
- Alimentation entérale rapide si possible (mettre au sein)
- Soluté précoce chez le prématuré
Le traitement thérapeutique consiste à :
- Si asymptomatique : alimentation entérale d’abord (augmenter les boires et compléter avec préparations lactées), s’il y a des conditions à risque, on utilise la voie parentérale d’emblée (soluté de dextrose 10%)
- Si symptomatique, soluté D10%, il faut faire attention à l'utilisation de bolus[note 7] et ne les utiliser que si le nouveau-né est symptomatique
Étroite surveillance de la glycémie
- aux 15 à 30 minutes, jusqu’à ce que 2 mesures consécutives soient > 2.6 mmol/L.
- Si la glycémie est très basse, on fait une FSC, mais on ne doit pas retarder le traitement.
Ictère
L’ictère est secondaire à la déposition de bilirubine dans les tissus.
- Présent chez 50 à 60% des nouveau-nés à terme.
- Présent chez la majorité des prématurés
- Le risque dépend de l'âge, de la courbe de croissance et des facteurs de risques
- Progression céphalo->caudale avec l'augmentation de la bilirubine
- Figure : 65-135 umol/L
- Corps : 255 umol/L
Métabolisme de la bilirubine

Dégradation de l’hème --> produit de la biliverdine --> produit de la bilirubine non-conjugué (la bilirubine non conjuguée est produite avant d’arriver au foie)
Origine de l'hème :
- 90% de la dégradation de l’hémoglobine des globules rouges
- 10% de la dégradation des autres protéines (ex : cytochromes et catalases)
Excrétion de la bilirubine
- Uptake hépatique
- Conjugaison
- Excrétion biliaire
La bilirubine arrive par voie sanguine a/n du foie où elle est conjuguée et ensuite relâchée dans les canaux biliaires vers le duodénum pour être excrétée dans les selles. La bilirubine est conjuguée à l’acide glucuronique par l’enzyme glucuronyl-transférase. Un cycle entéro-hépatique permet de récupérer une partie de la bilirubine qui aurait été éliminée dans les selles.
Ictère physiologique
Causé par l’accumulation de bilirubine indirecte[note 8]. L’ictère physiologique n’est pas sévère : < 250 mmol/L. L’augmentation maximale de la bilirubine indirecte doit être de +/- 85 mmol/L/jour. Il n’y a pas de pathologie sous-jacente et l'examen clinique est normal.
Physiopathologie
Caractéristiques qui peuvent causer un ictère physiologique, chez le nouveau-né :
- Augmentation de la production de bilirubine (destruction des globules rouges)
- Diminution de la conjugaison de la bilirubine par immaturité enzymatique (à 1 semaine, la valeur de la glucoronyl-transférase est de 1% la valeur adulte)
- Augmentation du cycle entéro-hépatique
- Intestin stérile chez le nouveau-né
- Présence de β-glucoronidase au niveau de la muqueuse intestinale et dans le lait maternel qui augmente la réabsorption de la bilirubine.
L’augmentation de la bilirubinémie peut entraîner des effets potentiellement graves :
- La bilirubine a un potentiel neurotoxique (si > 515 µmol/L)
- La bilirubine libre traverse la barrière hémato-encéphalique et cause des dommages cellulaires.
- Atteinte aigue et/ou chronique
À long terme, une hyperbilirubinémie modérée peut entrainer :
- Dysfonction neurologique mineure
- Anomalies du tonus à 1 an
Manifestations cliniques
L'ictère est secondaire à la déposition de bilirubine dans les tissus. Il touchera 50 à 60% des nouveau-nés à terme et la majorité des prématurés. La progression se fait en céphalo-caudal:
- Figure: 56-135 umol/L
- Corps complet: > 255 umol/L
L’ictère se présente après 24 heures de vie et il y a un pic après 2 à 4 jours.
- L’ictère est plus tardif chez le prématuré.
- Il se résout en 2 semaines.
Ictère pathologique
Si l’hyperbilirubinémie est directe, il s’agit toujours d’un processus pathologique. L’hyperbilirubinémie est pathologique si :
- Elle est associée à certaines conditions pathologiques
- Le nouveau-né est > 95e percentile de bilirubinémie pour l’âge (accentuation des mécanismes responsables de l’ictère physiologique)
L’ictère pathologique apparaît dans les premières 24 heures de vie et son augmentation est rapide.
Conditions pathologiques où il y a augmentation de la production de bilirubine :
- Ecchymoses, céphalhématome, polycythémie
- Hémolyse iso-immune (incompatibilité Rh, ABO)
- Hémolyse non-immune (anomalie de membrane, anomalie enzymatique, etc.)
- Infection
Conditions pathologiques où il y a diminution de la clairance de la bilirubine :
- Anomalies enzymatiques de conjugaison (maladie de Criggler-Najjar et syndrome de Gilbert)
- Maladie métabolique
- Hypothyroïdie
Voici les différentes conditions pathologiques où il y a augmentation du cycle entérohépatique :
- Déshydratation
- Échec de l’allaitement
- Diminution de la motilité intestinale
- Obstruction intestinale
Kernictère
Les risques associés à l'hyperbilirubinée sont principalement neurologiques. On nomme kernictère la déposition de bilirubine a/n cérébral. Les structures les plus atteintes sont:
- Noyaux gris centraux
- La substantia nigra
- L’hippocampe
- Noyaux des nerfs crâniens
Les taux de bilirubine doivent être élevés. Les autres facteurs de risque de kernictère sont :
- Grande vitesse de progression
- Grande proportion de bilirubine libre (moins d’albumine pour lier)
- Grande perméabilité de la barrière hémato-encéphalique.
- L'asphyxie, l'acidose, l'hypoxémie, le jeûne, les infections et l'hypoT augmentent la perméabilité de la barrière.
Manifestations cliniques
- Atteinte immédiate :
- Cri d’allure neurologique
- Léthargie
- Hypotonie
- Évolution vers la stupeur, l’hypertonie, l’irritabilité, l’opisthotonos (contracture importante), fièvre
- Coma, convulsion et décès
- Un risque auditif est également présent
À long terme, un kernictère modéré peut entraîner une atteinte chronique irréversible :
- Chorée athétose
- Retard moteur
- Dysfonction cognitive
- Surdité
- Anomalies des mouvements oculaires
- Dysplasie dentaire
Traitement de l’ictère

Pour prévenir l’hyperbilirubinémie :
- Améliorer la fréquence et la qualité de l’allaitement (permet un bon transit intestinal)
- BLM «bili light measurement» (lecture transcutanée de la bilirubine)
La photothérapie est le traitement de base de l’hyperbilirubinémie indirecte
- Traitement sécuritaire et efficace
- Permet l’isomérisation de structure de la bilirubine qui est liposoluble en lumirubine hydrosoluble excrétable dans l’urine.
- L'exposition au soleil n'est que très peu efficace en comparaison, l'efficacité dépend de:
- L'irradiance
- Type de lumière
- Distance entre source et bébé
- La quantité de surface exposé à la lumière
Les effets secondaires de la photothérapie sont :
- Sensibilité rétinienne (protection oculaire obligatoire)
- Augmentation des pertes insensibles (risque de déshydratation)
- Perturbation du contact mère-enfant
- Éruption cutanée possible
- Selles plus liquides
- Bronze baby syndrome (ne pas faire de photothérapie chez les nouveau-nés avec hyperbilirubinémie directe car ne fonctionnera pas et en plus teindra la peau du bébé).
On peut également faire des exsanguino-transfusion ou donner des immunoglobulines. Les immunoglobulines permettent de neutraliser les anticorps maternels présents dans le sang du bébé lors de l'isoimmunisation (incompatibilité Rh)
Facteurs de risque d’ictère
Les facteurs de risque d’ictère sévère sont :
- Bilirubine sérique total (BST) > 95e percentile
- Ictère dans les premiers 24 heures de vie
- Maladie hémolytique
- Céphalhématome
- Prématurité
- Fratrie ayant eu photothérapie
- Allaitement exclusif difficile
- Origine asiatique
Les facteurs de risque mineurs d’ictère sont :
- Bilirubine sérique total entre 75e et 95e percentile
- Ictère avant le congé d’hôpital
- Macrosome de mère diabétique
- Polycythémie
- Sexe masculin
- Âge maternel > 25 ans
- Prédisposition génétique
Prématurité

On parle de prématurité lorsque l'enfant est né en deçà de 37 semaines de gestation. La prématurité représente 4 à 10% des naissances. La limite de la viabilité s'est grandement abaissé durant les dernières décennies et on la situe aujourd'hui à +/- 23 semaines[note 9]. La naissance se fera en centre tertiaire si l’enfant a moins de 34 semaines. Selon le degré de prématurité, le pronostic ne sera pas le même.

Voici quelques définitions :
- Prématurité : 32 à 36 semaines
- Grande prématurité : 28 à 32 semaines
- Extrême prématurité : < 28 semaines
Chez les prématurés, on classe les poids selon :
- Petit poids de naissance (LBW) : 1.5 kg à 2.5 kg (7-8%)
- Très petit poids de naissance (VLBW) : 1 kg à 1.5 kg (2%)
- Extrême petit poids de naissance (ELBW) : < 1 kg (0.5%)
Chez un nouveau-né, tous les organes sont présents, mais ils sont en phase de finition. Plusieurs problèmes sont donc reliés à la prématurité :
- Thermorégulation: moins de graisse
- Infection: les anticorps de la mère sont uniquement transmis vers la fin de la grossesse
- Système respiratoire (déficit en surfactant)
- Membranes hyalines
- Apnées
- Hypoglycémie et hypocalcémie
- Problèmes digestifs
- Succion immature
- Tolérance limite
- Entérocolite
- Problèmes neurologiques (immaturité, risque d’hémorragie, séquelles à long terme possibles)
- C’est dans le dernier trimestre qu’il y a formation des synapses
- Le cerveau est donc moins développé et très fragile.
- Problèmes ophtalmologique (rétinopathie)
- Problèmes d’audition
Traitement
Les prématurés seront d'emblée placés dans un incubateur afin de les maintenir dans un milieu stable et de les protéger des infections. Le but des soins au prématuré est de supporter leur dépendance:
- Les nouveau-nés doivent être gavés jusqu’au développement de leur réflexe de succion (34 semaines)
- Avant 24-25 semaines, les nouveaux-nés ont besoin d’être intubés.
Notes
- ↑ Il est important de comprendre qu’un poids seul ne veut absolument rien dire, on a besoin de l’âge gestationnel.
- ↑ L'hypoglycémie n'est pas toujours immédiate en cas de PAG, mais après quelques heures, le temps que les apports maternels soient épuisés et que le défaut soit décompensé.
- ↑ L'hypoglycémie en cas de GAG est immédiate si elle est le résultat d'un surplus d'insuline qui va avec l'effort de la naissance provoquer rapidement la situation clinique.
- ↑ Pourrait indiquer une atrésie de l'oesophage.
- ↑ Certains E. coli sont même résistants à l'ampiciline.
- ↑ Controversé.
- ↑ Les bolus entraînent des swings au niveau de la glycémie et de l'insuline.
- ↑ L’accumulation de bilirubine directe est liée à une maladie.
- ↑ Viabilité ici ne veut pas dire absence de séquelles.
