ULaval:MED-1202/Pathologies pleurales
La plèvre est une membrane métaboliquement active. La composition et la quantité de liquide pleural sont très stables. L’apparition d’un épanchement pleural est le résultat d’un déséquilibre entre la formation et la réabsorption. Lors de l'épanchement pleural, une évaluation clinique associée à l’analyse du liquide pleural devrait suffire pour en déterminer l’étiologie. Comme pathologies fréquentes de la plèvre, l'on compte la pneumonie bactérienne qui se complique dans 40% des cas d’un épanchement pleural, le mésothéliome malin et le pneumothorax.
Physiologie pleurale
La plèvre est une membrane métaboliquement active. Elle est impliquée dans l’homéostasie de l’espace pleural et dans la réponse à l’inflammation. Il existe un espace réel de 20 µm entre la plèvre viscérale et pariétale où on retrouve le liquide pleural (0.3 ml/kg). Les cellules mésothéliales recouvrent les deux surfaces pleurales.Le liquide pleural origine des vaisseaux systémiques des membranes pleurales et a une faible teneur en protéine. L’absorption des liquides pleuraux se réalise essentiellement au niveau des lymphatiques de la plèvre pariétale. La régulation du liquide pleural dépend essentiellement de l’efficacité du drainage lymphatique.
Pathophysiologie de l’épanchement pleural

La composition et la quantité de liquide pleural sont très stables. L’apparition d’un épanchement pleural est le résultat d’un déséquilibre entre la formation et la réabsorption.
Augmentation de la formation de liquide
- Augmentation de la perméabilité
- Augmentation de la pression micro-vasculaire (pression veineuse)
- Diminution de la pression pleurale
- Diminution de la pression plasmatique oncotique
Diminution de la réabsorption
- Diminution de la contractilité lymphatique
- Inflammation
- Anomalies endocriniennes
- Infiltration des lymphatiques par le cancer
- Lésion secondaire à la radiothérapie
- Anomalies anatomiques
- Diminution de la fonction lymphatique
- Limitation des mouvements respiratoires (paralysie du diaphragme)
- Compression extrinsèque (fibrose pleurale)
- Blocage des stomata lymphatiques (cancer)
- Diminution de la pression intrapleurale
Présentation clinique

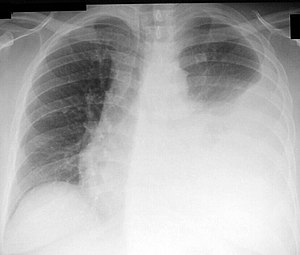
Dans 75% des cas, une évaluation clinique associée à l’analyse du liquide pleural devrait suffire pour déterminer l’étiologie de l’épanchement pleural. L’épanchement pleural peut être secondaire à des maladies locales de la plèvre ou du poumon ou à des maladies systémiques.
Les symptômes principaux à rechercher sont :
- Douleur thoracique pleurale ou constante
- Dyspnée: intensité proportionnelle à l’importance de l’épanchement pleural et à la condition sous-jacente
- Toux: Augmente lors des changements de position
- Signes d’atteinte de l’état général
L’examen physique peut montrer les anomalies suivantes :
- Abolition des vibrations vocales
- Matité franche
- Diminution ou abolition du murmure vésiculaire
- Diminution de l’amplitude respiratoire
La radiographie pulmonaire est l’examen initial à faire chez tous les patients lorsqu’on suspecte un épanchement pleural. La radiographie standard sera anormale en présence de 250 ml de liquide. Une tomodensitométrie thoracique sera effectuée afin de mieux visualiser la plèvre et le poumon. On peut noter des épaississements pleuraux, des nodularités ainsi que des loculations. L’échographie pleurale est utilisée afin de visualiser les loculations et effectuer une ponction pleurale sous guidance lorsqu’elle est impossible à l’aveugle.
Ponction pleurale

La ponction pleurale reste le premier geste à accomplir devant un épanchement pleural. L’analyse du liquide permet de fournir des informations utiles dans la démarche diagnostique. L’étape initiale de l’évaluation d’un épanchement consiste à déterminer s’il s’agit d’un exsudat ou d’un transsudat. Cette étape est primordiale afin de préciser quel est le diagnostic différentiel et le besoin d’investigation
Voici les critères de Light. Si 1 des 3 critères est présent, il s’agit d’un exsudat :
- Contenu en protéine du liquide pleural / Contenu en protéine du sérum >= 0.5
- LDH du liquide pleural / LDH du sérum >= 0.6
- LDH du liquide pleural > 2/3 de la limite supérieure de la valeur normale.
Si aucun des critères de Light n’est présent, il s’agit d’un transsudat. Un épanchement pleural exsudatif résulte d’une inflammation pulmonaire ou pleurale amenant une fuite protéique. Le drainage lymphatique peut également être diminué. L’exsudat peut également être secondaire à un mouvement de liquide de l’espace péritonéal.
Étiologies
Exsudats
Les exsudats sont causés par une fuite protéique.
- Infection (pneumonie, pleurésie tuberculeuse, infection virale, infection parasitaire)
- Inflammatoire (pleurésie amiantosique, embolie pulmonaire, sarcoïdose, syndrome de Dressler, radiothérapie)
- Néoplasie (cancer pulmonaire, cancer métastatique à la plèvre, mésothéliome, leucémies et lymphomes)
- Anomalies lymphatiques (chylothorax, lymphoedème, lympangiomyomatose)
- Maladies du collagène
- Augmentation de la pression intrapleurale
- Pathologie de la cavité abdominale
- Hypothyroïdie
- Médicaments
- Idiopathique
Transsudats
Les transsudats sont secondaires à un déséquilibre entre la pression oncotique et hydrostatique. Ils peuvent aussi résulter d’un mouvement de liquide en provenance de l’espace péritonéal. L’insuffisance cardiaque est une cause fréquente de transsudat, quoi qu'elle peut aussi causer des exsudats.
- Augmentation de la pression hydrostatique
- Diminution de la pression oncotique
- Autres
Caractérisation
Afin de mieux caractériser un exsudat, il y a d’autres paramètres à prendre en considération. La cytologie du liquide pleural ramène un diagnostic de cancer dans 60% des cas. Il s’agit le plus souvent d’un cancer du poumon, mais il peut aussi s’agit d’un cancer du sein, de l’ovaire et de l’estomac. En l’absence de diagnostic après une première ponction, il est utile de répéter une 2e ponction pleurale. Dans 20% des cas, on ne découvre pas l’étiologie de l’épanchement pleural malgré une investigation approfondie. Il est alors justifié de recourir à une évaluation par thoracoscopie. Pour les patients chez qui l’étiologie de l’épanchement pleural demeure indéterminée, il est important de les suivre régulièrement. Il s’agit souvent d’une néoplasie.
La thoracoscopie permet l’exploration complète de la cavité pleurale. Elle permet des gestes diagnostics (biopsie) et thérapeutiques. Elle est indiquée dans l’investigation de l’épanchement pleural idiopathique. L’avantage de la thoracoscopie est de pouvoir réaliser dans un même temps un talcage pleural afin de diminuer les récidives d’épanchement néoplasique.
Décompte cellulaire
- Globules blancs
- > 50 000 polynucléaires/mm3 : empyème
- > 10 000 polynucléaires/mm3 : processus aigu
- S’il y a prédominance lymphocytaire (70% et +)
- Pleurésie tuberculeuse
- Néoplasie maligne
- Éosinophiles: > 10% des cellules totales
- Globules rouges: > 100 000 GR/mm3
- Traumatisme
- Néoplasie
pH
Le pH normal est de 7.6. Si le pH < 7.3, on est possiblement en présence de:
- Infection du liquide pleural
- Pleurésie tuberculeuse
- Pleurésie rhumatoïde
- Cancer
Glucose
Si le glucose < 3.3 mmol/L, on est possiblement en présence de:
- Pleurésie rhumatoïde
- Pleurésie tuberculeuse
- Épanchement parapneumonique
- Empyème
- Néoplasie
Amylase
Si l'amylase pleurale est supérieure à la limite supérieure de la valeur sérique normale
Aspect macroscopique
- Purulent: Empyème
- Laiteux
- Chylothorax
- Pseudochylothorax
- Hémorragique
- Hémothorax traumatique
- Néoplasie
- Exposition à l’amiante
Cytologie

La cytologie du liquide pleural ramène un diagnostic de cancer dans 60%. Il s’agit le plus souvent d’un cancer du poumon, de métastases, mais il peut aussi s’agit d’une coinfection (pneumonie, pleurésie tuberculeuse, infection virale, infection parasitaire).
Pneumonie bactérienne

La pneumonie bactérienne se complique dans 40% des cas d’un épanchement pleural, dont 5-10% évolueront vers un empyème. Cela résulte d’une cascade inflammatoire où interviennent plusieurs cytokines de l’inflammation. Une ponction pleurale doit être effectuée lorsqu’il y a plus de 1 cm de liquide sur l'image radiologique faite en décubitus latéral.
Les épanchements parapneumoniques peuvent évoluer en trois phases :
- Exsudatif :
- Épanchement parapneumonique non compliqué
- Augmentation de la pression liquidienne interstitielle pulmonaire
- Liquide stérile
- Prédominance neutrophilique (> 90% des cellules du liquide)
- Fibropurulent
- Épanchement parapneumonique compliqué; empyème
- Invasion bactérienne dans l’espace pleural
- Réaction inflammatoire favorisant la déposition de fibrine
- Loculations (cloisonnement)
- Organisée: La plèvre pariétale et viscérale s’épaissit et il y a :
- Formation d’une coque fibreuse
- Diminution de l’expansion pulmonaire
On retrouve les mêmes bactéries que celles responsables de la pneumonie.
La persistance de fièvre et l’existence d’une douleur thoracique lors d’une pneumonie peuvent faire craindre une évolution vers un épanchement parapneumonique. Lorsque l’épanchement est infecté par des bactéries anaérobes, les symptômes s’installent de façon progressive.
L’analyse du liquide est l’élément principal afin de caractériser l’épanchement parapneumonique.
- L’invasion bactérienne de l’espace pleural produit une acidose qui se note par :
- pH < 7.2
- Glucose < 2.2
- La lyse des neutrophiles entraîne une augmentation des LDH
| Anatomie de l’espace pleural | Bactériologie | Biochimie | Pronostic | Drainage |
|---|---|---|---|---|
| A0 : épanchement pleural parapneumonique non compliqué (< 10 mm en débubitus latéral) | Bx : Inconnu
+ |
Cx : Inconnu
+ |
Très bon | Non |
| A1 : épanchement pleural parapneumonique non compliqué
(> 10 mm et < ½ hémithorax) |
B0 : Gram et culture –
+ |
Co : pH ≥ 7.2
Glucose ≥ 2.2 + |
Modéré | Non |
| A2 : épanchement pleural parapneumonique compliqué
EMPYÈME (≥ ½ hémithorax) Loculation ou épaississement de la plèvre pariétale |
OU
B1 : gram et culture + B2 : pus |
OU
C2 : pH < 7.2 Glucose < 2.2 |
Modéré
Mauvais |
Oui |
Traitement

Le traitement de l’épanchement pleural parapneumonique a trois objectifs :
- Permettre une évacuation complète du pus
- Traitement de l’infection
- Favoriser la réexpansion pulmonaire afin de prévenir les séquelles respiratoires
L’épanchement parapneumonique non compliqué (A0 et A1) se résout normalement avec les antibiotiques pour le traitement de la pneumonie. L’épanchement pleural compliqué (A2) nécessite la mise en place d’un drain thoracique afin d’effectuer un drainage complet de l’espace pleural.
Une thoracoscopie est effectuée pour libérer l’espace pleural des possibles loculations. Une décortication est nécessaire lorsqu’il y a échec au traitement ou présence d’une coque fibreuse. Une stérilisation de la cavité pleurale est obtenue avec une antibiothérapie de 4 à 6 semaines.
Mésothéliome malin


Le mésothéliome pleural malin est une tumeur agressive de l’adulte. L’exposition professionnelle aux fibres d’amiantes reste le facteur de risque principal. Parmi les métiers à risque l'on compte :
- Mines d’amiante
- Chantier naval
- Bâtiment
- Fabrication d’objets en amiante
Une exposition asbestosique est retrouvée dans 70% des cas. Le risque croit avec la durée d’exposition, mais une forte exposition sur quelques semaines peut être suffisante pour être cancérigène. Il existe un temps de latence d’environ 40 ans entre l’exposition et le développement du mésothéliome malin. La fibre d’amiante retrouvée au Québec est la chrysotile. Le tabac n’est pas un facteur de risque. Il existe une prédisposition familiale. 80% des patients sont des hommes, en raison de leur histoire professionnelle
Les patients se présentent avec dyspnée, douleur thoracique et des signes de l’état général. La dyspnée est multifactorielle :
- Accumulation de liquide pleural
- Épaississements pleuraux
- Restriction thoracique
On peut palper des masses à l’hémithorax témoignant d’une progression au niveau de la paroi thoracique. Le mésothéliome malin tend davantage à progresser localement qu’à se propager à distance.
Diagnostic
La radiographie pulmonaire démontre un épanchement pleural lorsqu’on est en début de maladie. L’évolution se fait par la suite avec une perte de volume du poumon qui se retrouve comprimé par la plèvre atteinte. Un exsudat lymphocytaire séro-sanguinolant est ce qu’on retrouve lors de la ponction pleurale. La thoracoscopie est la meilleure méthode pour l’obtention d’un diagnostic définitif.
Il existe 3 types histologiques de mésothéliome :
- Épithélial: meilleur pronostic
- Sarcomatoïde: évolution rapide et défavorable
- Mixte
Le pronostic est réservé : survie médiane de 12 mois. L’âge avancé, une maladie étendue et un mésothéliome de type sarcomatoïde sont des facteurs de mauvais pronostic.
-
Mésothéliome à la cytologie
-
Mésothéliome à la radiographie
-
Mésothéliome au TDM
-
mésothéliome au TDM
Traitement
Malheureusement, le traitement demeure largement à visée palliative.
Pneumothorax
Normalement, le poumon adhère à la paroi thoracique grâce à l’existence d’une pression négative entre les 2 feuillets de la plèvre. Lorsque cette pression est abolie par une infiltration d'air, on est en présence d'un pneumothorax. On dénombre différents types de pneumothorax :
- Primaire
- Survient sans évènement précipitant et en l’absence de maladie pulmonaire sous-jacente.
- : tabagisme, sexe masculin, antécédents familiaux de pneumothorax primaire
- Survient majoritairement dans la vingtaine
- Secondaire: pneumothorax arrivant sans évènement précipitant, mais en présence d’une malade pulmonaire sous-jacente (MPOC, fibrose kystique, infection pulmonaire, cancer pulmonaire)
- Traumatique
- Iatrogénique: pneumothorax survenant suite à certaines procédures diagnostiques
Un pneumothorax peut être sous tension ou non, le premier type étant plus sérieux, car il y a compression des structures du médiastin et du poumon contra-latéral.
-
Pneumothorax droit, notez la déviation du médiastin
-
Pneumothorax au TDM
-
Pneumothorax secondaire dû à une bulle d'emphysème (visible au sommet du poumon droit)
Présentation clinique
La présentation classique d'un pneumothorax est une douleur thoracique pleurétique d'apparition subite accompagnée d'une dyspnée. L'examen physique peut mettre en évidence une diminution des murmures vésiculaires et de l,amplitude thoracique. On peut également retrouver de l'emphysème sous-cutané
Les signes suivants se retrouvent dans un pneumothorax sous tension:
- Tachycardie
- Hypoxémie
- Hypotension
Traitement

La prise en charge du pneumothorax a pour objectif de retirer l’air de l’espace pleural et de prévenir la récidive. En présence d’un pneumothorax primaire, la prévention de la récidive devrait être proposée après le 2e épisode de pneumothorax. En présence d’un pneumothorax secondaire, la prévention de la récidive devrait être offerte dès le 1e. La thoracoscopie avec pleurodèse mécanique est l’option de choix pour prévenir efficacement la récidive d’un pneumothorax.







