Tumeur phyllode
| Maladie | |||
 Tumeur phyllode bénigne du sein. Une petite quantité de stroma mammaire normal (qui est plus éosinophile que la tumeur) se trouve dans le coin supérieur droit de l'image. | |||
| Caractéristiques | |||
|---|---|---|---|
| Signes | Masse mammaire, Écoulement mammaire , Masses mammaires fermes, Distension des veines superficielles, Rétraction du mamelon, Ulcération cutanée | ||
| Symptômes |
Masse mammaire (approche clinique), Masse non douloureuse, Évoluer rapidement, Masse qui dépasse de la peau, Étirer la peau, Ulcération cutanée | ||
| Diagnostic différentiel |
Sarcome, Maladie fibrokystique des seins, Tumeur stromale périductale, Carcinome métaplasique, Fibroadénome du sein | ||
| Informations | |||
| Terme anglais | Phyllodes tumor | ||
| Autres noms | cystosarcome phyllode | ||
| |||
Une tumeur phyllode est une tumeur rare du sein qui se développe dans le tissu conjonctif , appelé stroma ; elles sont donc des tumeurs non-épithéliales. Le stroma mammaire comprend le tissu et les ligaments qui entourent les canaux galactophores, les vaisseaux sanguins et les canaux lymphatiques du sein. [1] La tumeur phyllode présente un continuum morphologique allant de bénigne à maligne. Les tumeurs phyllodes présentent un stroma cellulaire myxoïde séparé par de longues fentes de tissu épithélial (comprimé). Ces longues fentes sont la principale caractéristique qui différencie ces tumeurs du fibroadénome du sein, plus courant. Avec un peu d'imagination, elles peuvent vaguement ressembler à des feuilles. D'ailleurs, le nom "phyllodes" vient du mot grec signifiant "en forme de feuille".
Épidémiologie
La tumeur phyllode du sein est une tumeur fibroépithéliale rarement rencontrée, qui représente 0,3 % à 1 % de toutes les tumeurs.[1][2] Les tumeurs phyllodes surviennent principalement chez les femmes d'âge moyen (âge moyen à la présentation, 40 à 50 ans), environ 15 à 20 ans plus tard que les fibroadénomes du sein.[3] Les tumeurs phyllodes surviennent principalement chez les femmes, bien que l'on ait signalé quelques cas chez les hommes.[4]
L'analyse des données du registre du Programme de surveillance, d'épidémiologie et de résultats finaux (SEER) de 2000 à 2004 a indiqué que 500 femmes sont diagnostiquées chaque année aux États-Unis avec des tumeurs phyllodes malignes.[5]
Étiologies
Les facteurs de risque génétiques des tumeurs phyllodes sont largement inconnus, mais la littérature décrit des tumeurs phyllodes chez des patients atteints du syndrome de Li-Fraumeni et chez un couple mère-fille.[6] Les rares cas de tumeurs phyllodes chez les hommes sont souvent associés à une gynécomastie, ce qui suggère un rôle pour le déséquilibre hormonal.[7] Les chercheurs ont postulé que l'induction stromale des tumeurs phyllodes peut se produire en raison des facteurs de croissance produits par l'épithélium mammaire. Les traumatismes, la grossesse, l'augmentation de l'activité œstrogénique et la lactation sont occasionnellement impliqués comme facteurs stimulant la croissance tumorale. La nature de ces facteurs n'est pas bien comprise, mais l'endothéline-1, un stimulateur de la croissance des fibroblastes mammaires, pourrait être un facteur contributif.[8]
Physiopathologie
Contrairement au carcinome mammaire, les tumeurs phyllodes prennent naissance à l'extérieur des lobules et des canaux, dans le tissu conjonctif du sein, appelé stroma, y compris les ligaments et le tissu graisseux entourant les lobules, les canaux, la lymphe et les vaisseaux sanguins du sein. Outre les cellules épithéliales des canaux et des lobules, les tumeurs phyllodes peuvent également contenir des cellules stromales.[9] Les tumeurs phyllodes se développent le plus souvent de novo, bien que des cas de progression d'un fibroadénome en tumeur phyllode aient été signalés.[10] Sur la base des caractéristiques histologiques, y compris l'atypie nucléaire, la cellularité stromale, l'activité mitotique, l'apparence de la marge tumorale et la prolifération stromale, l'Organisation mondiale de la santé (OMS) classe les tumeurs phyllodes bénignes, limites (borderline) et malignes.[1] Les tumeurs phyllodes ont une récurrence inhérente et/ou potentiel métastatique, qui varie en fonction du grade histologique.
Caractéristiques moléculaires
Des études récentes ont porté sur la définition d'une classification moléculaire des tumeurs phyllodes. Des études d'hybridation génomique comparative ont montré des déséquilibres chromosomiques récurrents, notamment +1q, -6q, -13q, -9p, -10p et +5p. Bien qu'actuellement aucune aberration chromosomique n'ait été trouvée comme étant spécifique aux tumeurs phyllodes, certains auteurs ont rapporté que les tumeurs phyllodes de bas grade et de haut grade (limite/malignes) se séparent en deux groupes génétiques basés sur les altérations génomiques, les tumeurs phyllodes de haut grade montrant constamment un gain 1q et une perte 13q et les tumeurs phyllodes de bas grade montrant peu ou pas d'altérations.[11] Les données préliminaires de l'hybridation génomique comparative (CGH) sur réseau démontrent une délétion interstitielle 9p21 impliquant le locus CDKN2A et une délétion 9p dans les tumeurs phyllodes malignes et certaines tumeurs phyllodes de bas grade.[12]
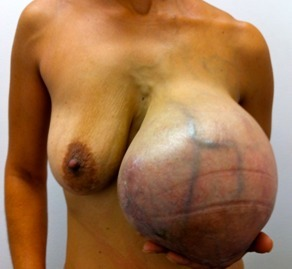
Présentation clinique
Facteurs de risque
Les experts ne savent pas ce qui cause les tumeurs phyllodes. Les facteurs de risques qui semblent contribuer sont:
- le sexe féminin
- le syndrome de Li-Fraumeni
- l'âge (dans la quarantaine)
- les traumatismes mammaires
- la grossesse.
Questionnaire
Au questionnaire:[1]
- une tumeur phyllode ressemble à une bosse dans le sein
- elle n'est généralement pas douloureuse
- les tumeurs phyllodes peuvent évoluer rapidement et atteindre une largeur de 3 centimètres, soit un peu plus d'un pouce, en quelques semaines ou quelques mois seulement
- elles se développent souvent rapidement, même si elles sont bénignes. Les patients peuvent décrire qu'elles dépassent de la peau.
- parfois, elles peuvent étirer la peau ou provoquer un ulcère sur le sein.

Examen clinique
À examen clinique des seins:[1]
- masses mammaires unilatérales, fermes et indolores qui étirent la peau sus-jacente avec une distension des veines superficielles
- la taille peut aller de 1 à 45 cm et peut occuper tout le sein
- écoulement mammaire sanglant causé par un infarctus spontané de la tumeur a déjà été décrit
- les ulcérations et la rétraction du mamelon sont rares.
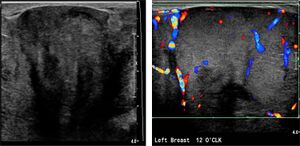
Examens paracliniques
Les examens paracliniques qui peuvent aider au diagnostics sont:
- la mammographie: Les résultats d'imagerie sur la mammographie sont typiquement une masse dense lobulée ronde avec des marges partiellement indistinctes ou circonscrites. Les calcifications au sein de la masse sont rares, mais elles peuvent être importantes.[13]
- l'échographie: À l'échographie, la tumeur phyllode se présente comme une masse hypoéchogène, partiellement indistincte ou partiellement circonscrite, avec un rehaussement postérieur fréquent. Une composante kystique est plus typique des tumeurs phyllodes malignes. Les tumeurs phyllodes présentent souvent une vascularisation accrue au Doppler.[14]
- l'IRM: L'IRM peut être utile pour évaluer l'invasion de la paroi thoracique dans le cas d'une tumeur phyllode maligne. Les caractéristiques présentes à l'IRM sont généralement un signal faible et hétérogène sur les images pondérées en T1, bien que des zones d'hémorragie hyperintense en T1 puissent être visibles. Les images pondérées en T2 montrent généralement une masse lobulée avec du liquide hyperintense dans des espaces en forme de fente et parfois une hyperintensité dans les tissus environnants.[15]
- la biopsie au trocart: Une biopsie à l'aiguille n'est pas utile. Une biopsie au trocart permettra de confirmer le diagnostic, mais il pourrait être difficile de distinguer une tumeur phyllode bénigne d'un fibroadénome.
- la biopsie excisionnelle: La plupart des gens ont besoin de cette procédure pour obtenir un diagnostic. Le chirurgien qui enlèvera toute la masse l'enverra en pathologie pour examiner les tissus. Cette biopsie peut montrer si la tumeur est bénigne, à la limite du cancer ou maligne. Si le chirurgien craint une tumeur phyllode plutôt qu'un fibroadénome (signes indirects à l'imagerie), il fera une excision avec une marge de sécurité pour éviter la récidive.
Histopathologie
Examen macroscopique
Les tumeurs phyllodes forment des masses bien circonscrites, fermes et saillantes. Lorsqu'elle est coupée, la surface est beige ou rose à grise et peut se présenter comme charnue et mucoïde. Le motif caractéristique en forme de verticille avec des fentes incurvées ressemblant à des bourgeons de feuilles est plus évident dans les grandes lésions, mais les lésions plus petites peuvent avoir un aspect homogène. Des hémorragies ou des nécroses peuvent être présentes dans les grandes lésions.[2]
Examen microscopique

Les tumeurs phyllodes présentent un schéma de croissance intra-canaliculaire amélioré avec des projections en forme de feuilles dans des luminescences allongées et dilatées de façon variable. La composante épithéliale est constituée de cellules épithéliales luminales et myoépithéliales étirées dans des fentes en arc de cercle surmontant des franges stromales.[2]
Classification
Plusieurs systèmes de classification ont été proposés, mais l'utilisation du système à trois niveaux, comprenant la tumeur phyllode bénigne, la tumeur phyllode limite et la tumeur phyllode maligne, est préférée car cette approche conduit à une plus grande certitude aux extrémités du spectre de ces lésions fibro-épithéliales.[2]
Tumeurs phyllodes bénignes
Cette variété représente 60 à 75 % de toutes les tumeurs phyllodes. Dans les tumeurs phyllodes bénignes, le stroma est généralement plus cellulaire que dans les fibroadénomes. Les noyaux stromaux à cellules fusiformes sont uniformes, et les mitoses sont rares, généralement moins de 5 par 10 champs de haute puissance. Les zones de cellularité stromale éparse, de hyalinisation ou de changements myxoïdes ne sont pas rares, reflétant l'hétérogénéité stromale. Les marges sont généralement bien délimitées et poussantes.[2]
Tumeurs phyllodes à la limite de la malignité
Ces tumeurs sont diagnostiquées lorsque la masse ne possède pas toutes les caractéristiques histologiques défavorables trouvées dans les tumeurs phyllodes malignes. Les tumeurs phyllodes à la limite de la malignité peuvent présenter des mitoses fréquentes (5 à 9 pour 10 champs de haute puissance), une cellularité stromale modérée, une bordure circonscrite ou focalement invasive, et des atypies stromales. La croissance excessive du stroma est souvent absente.[2]
Tumeurs phyllodes malignes
Les tumeurs phyllodes malignes présentent une combinaison de pléomorphisme nucléaire marqué des cellules stromales, une surcroissance stromale définie comme l'absence d'éléments épithéliaux dans un champ microscopique de faible puissance ne contenant que du stroma, une augmentation des mitoses (supérieure ou égale à 10 par 10 champs de haute puissance), une cellularité stromale accrue, généralement diffuse, et des bordures infiltrantes.[2]
| Critères | Bénigne | Limite | Maligne |
|---|---|---|---|
| Contour de la tumeur | Bien défini | Bien défini; peut être localement infiltrant | Infiltrant |
| Cellularité stromale | Faible cellularité | Cellularité moyenne | Cellularité marquée et diffuse |
| Atypies stromales | Aucune à peu | Peu à moyenne | Élevée |
| Activité mitotique | < 5 par champ | 5-9 par champ | > 10 par champ |
| Croissance stromale excessive | Absente | Absente à très focale | Présentes |
| Éléments hétérogéneuses à caractère maligne | Absents | Absents | Peut être présents |
Immunohistochimie
De multiples marqueurs immunohistochimiques ont fait l'objet de recherches dans le but d'améliorer la classification des tumeurs phyllodes et de prédire leur pronostic. Les études démontrent que p53, Ki67, CD117, EGFR, p16, et VEGF (étant le plus faible dans les tumeurs phyllodes bénignes et le plus élevé dans les tumeurs phyllodes malignes) sont associés aux grades histologiques des tumeurs phyllodes, mais aucun n'a été prouvé comme étant cliniquement utile.[17][18][19][20]
Parmi ces marqueurs, l'expression de p53 et l'indice Ki67 ont été rapportés dans certaines études comme étant significativement associés aux survies sans maladie et globale, mais d'autres études n'ont trouvé aucune association avec la récidive ou le comportement clinique.[21][22]
L'expression de PAX3 et de SIX1 par immunohistochimie et par analyse de l'expression génétique a récemment été identifiée dans les tumeurs phyllodes borderline et malignes et est corrélée à un mauvais pronostic clinique.[23]
Approche clinique
Les tumeurs phyllodes ont été définies pour la première fois en 1774 comme un type géant de fibroadénome. Elles se différencient des fibroadénomes sur le plan histologique par une cellularité accrue, et sur le plan clinique par la récurrence locale et la propagation métastatique. Cliniquement, elles se présentent comme une masse mammaire bénigne à croissance rapide. Chez certaines patientes, la lésion peut se manifester par une croissance soudaine et récente après avoir été présente pendant plusieurs années. Elles sont généralement situées dans le quadrant supérieur externe, et peuvent rarement être bilatérales. Le diagnostic préopératoire de ce phénomène rare est important pour décider de l'approche chirurgicale appropriée. Elles apparaissent comme des lésions hyperdenses, larges, rondes/lobulaires, bien circonscrites sur l'échographie, qui est la modalité d'imagerie initiale de choix[24].
Diagnostic
Les tumeurs sont généralement ressenties comme une bosse indolore dans le sein, mais certaines peuvent être douloureuses. Elles ont tendance à se développer rapidement et à étirer la peau. Parfois, elles sont d'abord visibles lors d'un examen d'imagerie (comme une échographie ou une mammographie), auquel cas il est souvent difficile de les distinguer des fibroadénomes. Le diagnostic peut souvent être établi par une biopsie au trocart, mais il est parfois nécessaire d'enlever la totalité de la tumeur (au cours d'une biopsie excisionnelle) pour être sûr qu'il s'agit bien d'une tumeur phyllode, et qu'elle est maligne ou non. Les éléments qui orientent vers une tumeur phyllode sont la présence d'une masse palpable à croissance rapide, une grande taille (> 3cm), une imagerie suggestive d'un fibroadénome, sauf pour la taille et/ou les antécédents de croissance.[25]
Diagnostic différentiel
Les diagnostics différentiels des tumeurs phyllodes comprennent:
- un fibroadénome du sein: le principal diagnostic différentiel pour la tumeur phyllode bénigne est le fibroadénome ayant un motif intracanaliculaire prononcé.[26]
- un sarcome: la tumeur maligne des phyllodes peut être confondue avec des sarcomes purs du sein[27]
- une tumeur stromale périductale: la tumeur stromale périductale est une entité qui se superpose histologiquement à la tumeur phyllode maligne, la principale différence étant l'absence de processus en forme de feuille. Elle est non circonscrite et consiste en une prolifération de cellules fusiformes localisée autour de tubules ouverts.[28]
- un carcinome métaplasique: le carcinome est également dans le diagnostic différentiel de la tumeur phyllode maligne, mais la démonstration immunohistochimique de la différenciation épithéliale permet de résoudre le problème.
- la maladie fibrokystique des seins.
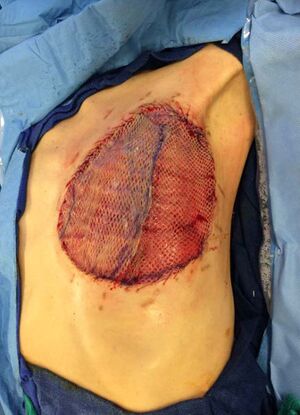
Traitement
Une excision complète locale avec des marges supérieures à 1 cm est souvent curative et réduit le risque de récidive locale.[29][30] Les tumeurs de grande taille nécessitent une mastectomie. Malgré l'incidence plus élevée de récidive locale secondaire à la chirurgie conservatrice du sein, les études n'ont montré aucune différence entre la chirurgie conservatrice du sein et la mastectomie en ce qui concerne la survie sans métastases ou la survie globale.
Différents types de chirurgie sont utilisés pour traiter les tumeurs phyllodes :
- la mastectomie partielle : le chirurgien enlève la tumeur, ainsi qu'au moins 1 centimètre de tissu autour. L'ablation de ce tissu supplémentaire permet de prévenir la réapparition de la tumeur. Après l'opération, un pathologiste examine les tissus au microscope. S'il n'est pas sûr que le chirurgien ait retiré toutes les cellules tumorales, la patiente peut avoir besoin d'une nouvelle intervention chirurgicale pour retirer une zone plus large de tissu mammaire sain.
- la quadrantectomie : si la tumeur est plus importante, le chirurgien enlève toute la partie du sein qui la contient.
- la mastectomie totale : le chirurgien retire l'ensemble du sein. La patiente peut subir une chirurgie de reconstruction mammaire en même temps ou après la mastectomie. En général, il n'est pas nécessaire de retirer les ganglions lymphatiques de l'aisselle près du sein, car les tumeurs phyllodes s'y propagent rarement.
Les options de traitement adjuvant comprennent principalement la radiothérapie, qui s'est montrée capable de réduire la récidive locale pour les tumeurs phyllodes malignes ou récidivantes. Les recherches n'ont pas montré d'avantage clinique à l'administration d'une chimiothérapie adjuvante.
Suivi
Les tumeurs phyllodes ne sont généralement pas cancéreuses, mais elles peuvent parfois revenir après le traitement. Habituellement, ces tumeurs reviennent dans l'année ou les deux années qui suivent l'opération. Les tumeurs cancéreuses peuvent revenir plus tôt.
Pour détecter la tumeur si elle revient, la patiente doit se soumettre à un suivi régulier. Un examen clinique des seins doit être programmé tous les 4 à 6 mois. Des examens d'imagerie de routine comme les mammographies, les échographies et les IRM sont également recommandés pour vérifier le retour de la tumeur dans le sein affecté.
Complications
Les complications[31]:
- récidive locale (21 %): Des récidives locales peuvent survenir dans toutes les tumeurs phyllodes, à un taux global de 21%, avec des intervalles de 10% à 17%, 14% à 25%, et 23% à 30% pour les tumeurs bénignes, à la limite de la malignité, et phyllodes, respectivement. Les récidives locales se développent généralement dans les 2 à 3 ans.
- métastases distantes: Les métastases à distance sont presque exclusivement une caractéristique des tumeurs phyllodes malignes. Les poumons (66 %), les os (28 %) et le cerveau (9 %) sont les sites de propagation les plus courants. Dans de rares cas, les métastases peuvent toucher le foie et le cœur.
Évolution
Le pronostic de la tumeur phyllode est bon, avec une survie à 10 ans de 87%. Le risque de récidive varie selon la taille de la tumeur et l'approche chirurgicale.
La plupart des tumeurs phyllodes se comportent de manière bénigne, avec des récidives locales dans une petite proportion de cas. Très rarement, la tumeur peut métastaser, le plus souvent dans les cas de tumeurs de grade malin.
Les tumeurs phyllodes malignes ont un mauvais pronostic.
Prévention
Les patientes peuvent être invitées à examiner régulièrement leurs seins et à consulter leur médecin si une anomalie est détectée.? Cela permettra de détecter les tumeurs à un stade plus précoce et ainsi éviter les complications malignes de la maladie.
Références
- Cette page a été modifiée ou créée le 2021/07/11 à partir de Phyllodes Tumor Of The Breast (StatPearls / Phyllodes Tumor Of The Breast (2020/11/10)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/31082182 (livre).
- Cet article a été créé en partie ou en totalité le 2021/07/10 à partir de Chirurgie (application), créée par Dre Hélène Milot, Dr Olivier Mailloux et collaborateurs et partagé sous la licence CC-BY-SA 4.0 international
- ↑ 1,0 1,1 1,2 1,3 et 1,4 Faten Limaiem et Sarang Kashyap, StatPearls, StatPearls Publishing, (PMID 31082182, lire en ligne)
- ↑ 2,0 2,1 2,2 2,3 2,4 2,5 et 2,6 Yanhong Zhang et Celina G. Kleer, « Phyllodes Tumor of the Breast: Histopathologic Features, Differential Diagnosis, and Molecular/Genetic Updates », Archives of Pathology & Laboratory Medicine, vol. 140, no 7, , p. 665–671 (ISSN 1543-2165, PMID 27362571, DOI 10.5858/arpa.2016-0042-RA, lire en ligne)
- ↑ Pengfei Jing, Bing Wei et Xiaoqin Yang, « Phyllodes tumor of the breast with nipple discharge: A case report », Medicine, vol. 97, no 52, , e13767 (ISSN 1536-5964, PMID 30593154, Central PMCID 6314703, DOI 10.1097/MD.0000000000013767, lire en ligne)
- ↑ Y. Ansah-Boateng et F. A. Tavassoli, « Fibroadenoma and cystosarcoma phyllodes of the male breast », Modern Pathology: An Official Journal of the United States and Canadian Academy of Pathology, Inc, vol. 5, no 2, , p. 114–116 (ISSN 0893-3952, PMID 1315437, lire en ligne)
- ↑ Taiwo Adesoye, Heather B. Neuman, Lee G. Wilke et Jessica R. Schumacher, « Current Trends in the Management of Phyllodes Tumors of the Breast », Annals of Surgical Oncology, vol. 23, no 10, , p. 3199–3205 (ISSN 1534-4681, PMID 27334214, Central PMCID 5021443, DOI 10.1245/s10434-016-5314-0, lire en ligne)
- ↑ Charles E. Foucar, Ashley Hardy, Kalliopi P. Siziopikou et Lilian Wang, « A mother and daughter with phyllodes tumors of the breast », Clinical Breast Cancer, vol. 12, no 5, , p. 373–377 (ISSN 1938-0666, PMID 22981939, DOI 10.1016/j.clbc.2012.07.011, lire en ligne)
- ↑ V. T. Nielsen et C. Andreasen, « Phyllodes tumour of the male breast », Histopathology, vol. 11, no 7, , p. 761–762 (ISSN 0309-0167, PMID 3040567, DOI 10.1111/j.1365-2559.1987.tb02690.x, lire en ligne)
- ↑ Shashi Prakash Mishra, Satyendra Kumar Tiwary, Manjaree Mishra et Ajay Kumar Khanna, « Phyllodes tumor of breast: a review article », ISRN surgery, vol. 2013, , p. 361469 (ISSN 2090-5785, PMID 23577269, Central PMCID 3615633, DOI 10.1155/2013/361469, lire en ligne)
- ↑ J. W. Mitus, P. Blecharz, J. Jakubowicz et M. Reinfuss, « Phyllodes tumors of the breast. The treatment results for 340 patients from a single cancer centre », Breast (Edinburgh, Scotland), vol. 43, , p. 85–90 (ISSN 1532-3080, PMID 30521986, DOI 10.1016/j.breast.2018.11.009, lire en ligne)
- ↑ Shahbaz Habib Faridi, Bushra Siddiqui, Syed Shamshad Ahmad et Mohammad Aslam, « Progression of Fibroadenoma to Malignant Phyllodes Tumour in a 14-Year Female », Journal of the College of Physicians and Surgeons--Pakistan: JCPSP, vol. 28, no 1, , p. 69–71 (ISSN 1681-7168, PMID 29290198, DOI 10.29271/jcpsp.2018.01.69, lire en ligne)
- ↑ Marick Laé, Anne Vincent-Salomon, Alexia Savignoni et Isabelle Huon, « Phyllodes tumors of the breast segregate in two groups according to genetic criteria », Modern Pathology: An Official Journal of the United States and Canadian Academy of Pathology, Inc, vol. 20, no 4, , p. 435–444 (ISSN 0893-3952, PMID 17334353, DOI 10.1038/modpathol.3800756, lire en ligne)
- ↑ A. M. Jones, R. Mitter, R. Springall et T. Graham, « A comprehensive genetic profile of phyllodes tumours of the breast detects important mutations, intra-tumoral genetic heterogeneity and new genetic changes on recurrence », The Journal of Pathology, vol. 214, no 5, , p. 533–544 (ISSN 0022-3417, PMID 18288784, DOI 10.1002/path.2320, lire en ligne)
- ↑ Hongna Tan, Shengjian Zhang, Haiquan Liu et Weijun Peng, « Imaging findings in phyllodes tumors of the breast », European Journal of Radiology, vol. 81, no 1, , e62–69 (ISSN 1872-7727, PMID 21353414, DOI 10.1016/j.ejrad.2011.01.085, lire en ligne)
- ↑ L. Liberman, E. Bonaccio, D. Hamele-Bena et A. F. Abramson, « Benign and malignant phyllodes tumors: mammographic and sonographic findings », Radiology, vol. 198, no 1, , p. 121–124 (ISSN 0033-8419, PMID 8539362, DOI 10.1148/radiology.198.1.8539362, lire en ligne)
- ↑ Jung Lim Yoo, Ok Hee Woo, Yoon Kyung Kim et Kyu Ran Cho, « Can MR Imaging contribute in characterizing well-circumscribed breast carcinomas? », Radiographics: A Review Publication of the Radiological Society of North America, Inc, vol. 30, no 6, , p. 1689–1702 (ISSN 1527-1323, PMID 21071383, DOI 10.1148/rg.306105511, lire en ligne)
- ↑ « Click on image to zoom », sur cdn.amegroups.cn (consulté le 11 août 2021)
- ↑ Yvonne Noronha, Anwar Raza, Brian Hutchins et Donald Chase, « CD34, CD117, and Ki-67 expression in phyllodes tumor of the breast: an immunohistochemical study of 33 cases », International Journal of Surgical Pathology, vol. 19, no 2, , p. 152–158 (ISSN 1940-2465, PMID 21087983, DOI 10.1177/1066896910382009, lire en ligne)
- ↑ Puay-Hoon Tan, Thiyagarajan Jayabaskar, George Yip et Yen Tan, « p53 and c-kit (CD117) protein expression as prognostic indicators in breast phyllodes tumors: a tissue microarray study », Modern Pathology: An Official Journal of the United States and Canadian Academy of Pathology, Inc, vol. 18, no 12, , p. 1527–1534 (ISSN 0893-3952, PMID 16258510, DOI 10.1038/modpathol.3800488, lire en ligne)
- ↑ Gary M. K. Tse, Philip C. W. Lui, Joaquim S. L. Vong et Kin-Mang Lau, « Increased epidermal growth factor receptor (EGFR) expression in malignant mammary phyllodes tumors », Breast Cancer Research and Treatment, vol. 114, no 3, , p. 441–448 (ISSN 1573-7217, PMID 18443904, DOI 10.1007/s10549-008-0030-5, lire en ligne)
- ↑ Rooshdiya Z. Karim, Sebastien K. Gerega, Y. H. Yang et Andrew Spillane, « p16 and pRb immunohistochemical expression increases with increasing tumour grade in mammary phyllodes tumours », Histopathology, vol. 56, no 7, , p. 868–875 (ISSN 1365-2559, PMID 20497245, DOI 10.1111/j.1365-2559.2010.03562.x, lire en ligne)
- ↑ Kan Yonemori, Tadashi Hasegawa, Chikako Shimizu et Taro Shibata, « Correlation of p53 and MIB-1 expression with both the systemic recurrence and survival in cases of phyllodes tumors of the breast », Pathology, Research and Practice, vol. 202, no 10, , p. 705–712 (ISSN 0344-0338, PMID 16889904, DOI 10.1016/j.prp.2006.05.006, lire en ligne)
- ↑ A. Niezabitowski, B. Lackowska, J. Rys et A. Kruczak, « Prognostic evaluation of proliferative activity and DNA content in the phyllodes tumor of the breast: immunohistochemical and flow cytometric study of 118 cases », Breast Cancer Research and Treatment, vol. 65, no 1, , p. 77–85 (ISSN 0167-6806, PMID 11245343, DOI 10.1023/a:1006457304526, lire en ligne)
- ↑ Wai Jin Tan, Aye Aye Thike, Boon Huat Bay et Puay Hoon Tan, « Immunohistochemical expression of homeoproteins Six1 and Pax3 in breast phyllodes tumours correlates with histological grade and clinical outcome », Histopathology, vol. 64, no 6, , p. 807–817 (ISSN 1365-2559, PMID 24438019, DOI 10.1111/his.12329, lire en ligne)
- ↑ Turan Acar, Ercüment Tarcan, Mehmet Hacıyanlı et Erdinç Kamer, « How to approach phyllodes tumors of the breast? », Turkish Journal of Surgery/Ulusal cerrahi dergisi, vol. 31, no 4, , p. 197–201 (ISSN 1300-0705, PMID 26668526, Central PMCID 4674039, DOI 10.5152/UCD.2015.2941, lire en ligne)
- ↑ (en) « Guidelines Detail », sur NCCN (consulté le 10 août 2021)
- ↑ Saba Yasir, Aziza Nassar, Rafael E. Jimenez et Sarah M. Jenkins, « Cellular fibroepithelial lesions of the breast: A long term follow up study », Annals of Diagnostic Pathology, vol. 35, , p. 85–91 (ISSN 1532-8198, PMID 30029048, DOI 10.1016/j.anndiagpath.2018.01.005, lire en ligne)
- ↑ Wataru Goto, Shinichiro Kashiwagi, Koji Takada et Yuka Asano, « [A Case of a Malignant Phyllodes Tumor That Was Difficult to Distinguish from Stromal Sarcoma] », Gan to Kagaku Ryoho. Cancer & Chemotherapy, vol. 45, no 13, , p. 2429–2431 (ISSN 0385-0684, PMID 30692487, lire en ligne)
- ↑ Ana M. Burga et Fattaneh A. Tavassoli, « Periductal stromal tumor: a rare lesion with low-grade sarcomatous behavior », The American Journal of Surgical Pathology, vol. 27, no 3, , p. 343–348 (ISSN 0147-5185, PMID 12604890, DOI 10.1097/00000478-200303000-00007, lire en ligne)
- ↑ Richard D. Pezner, Timothy E. Schultheiss et I. Benjamin Paz, « Malignant phyllodes tumor of the breast: local control rates with surgery alone », International Journal of Radiation Oncology, Biology, Physics, vol. 71, no 3, , p. 710–713 (ISSN 0360-3016, PMID 18234448, DOI 10.1016/j.ijrobp.2007.10.051, lire en ligne)
- ↑ (en) Ashley Simpson, Pamela Li et Jill Dietz, « Diagnosis and management of phyllodes tumors of the breast », Annals of Breast Surgery, vol. 5, no 0, (ISSN 2616-2776, DOI 10.21037/abs-20-99, lire en ligne)
- ↑ Puay Hoon Tan, Aye Aye Thike, Wai Jin Tan et Minn Minn Myint Thu, « Predicting clinical behaviour of breast phyllodes tumours: a nomogram based on histological criteria and surgical margins », Journal of Clinical Pathology, vol. 65, no 1, , p. 69–76 (ISSN 1472-4146, PMID 22049216, DOI 10.1136/jclinpath-2011-200368, lire en ligne)
