Retard de développement (approche clinique)
| Approche clinique | |
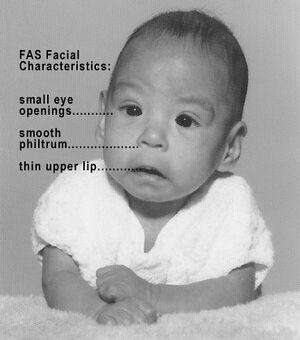 Syndrome d'alcoolisation foetal | |
| Caractéristiques | |
|---|---|
| Informations | |
| Terme anglais | Retard de développement |
|
| |
Retard de développement (21)
Le développement chez l'humain fait référence aux changements physiques, cognitifs et psychosociaux qui se produisent tout au long de la vie. De nombreuses sphères de développement progressent de manière séquentielle au fil du temps. Voici les principales sphères du développement : [1]
- Développement moteur - moteur fin et grossier
- Développement du langage (tout le spectre des compétences en communication, y compris les gestes et la parole)
- Développement cognitif/ jeu ( mémoire, apprentissage, résoudre des problèmes)
- Développement au niveau des habiletés sociales ( ex. interaction avec les enfants de son environnement)
- Développement des compétences adaptatives (Activités de la vie quotidienne (AVQ))
Lors d'un retard de développement, l'enfant peut présenter un retard dans une seule sphère de façon isolée, comme un retard de langage. Le retard de développement global , quant à lui, est généralement déterminé lorsque l'enfant présente une performance inférieure à deux écarts types sous la moyenne dans au moins deux sphères de développement, mentionnés plus haut [2]. Ce diagnostic est habituellement réservé pour les enfants âgés de moins de 5 ans . Par contre, beaucoup de ces enfants présenteront dans le futur une déficience intellectuelle (DI).
Noter que la déficience intellectuelle (DI) est une trouble neurodéveloppemental débutant avant l'âge de 18 ans. Elle se caractérise par des déficits développementaux importants tout au long de la vie, touchant principalement l'intelligence et le développement des compétences adaptatives, avec l'atteinte d'au moins un domaine adaptatif (conceptuel, social et pratique). Pour faire un diagnostic de DI, il faut présenter des limitations dans les deux cas suivants:
- Fonctions intellectuelles : atteinte de la résolution de problèmes, le raisonnement, le jugement, l'apprentissage scolaire et par l'expérience, la planification et l'abstraction. L'atteinte peut être confirmée par la clinique et des tests d'intelligences standardisés. Cela correspond généralement à un quotient intellectuel (QI) inférieur à deux écarts-types ou plus à la moyenne ( scores de QI habituellement <70)
- Fonctions adaptatives : limitations dans un ou plusieurs champs de fonctionnement de la vie quotidienne: communication, indépendance et participation sociale dans différents lieux comme l'école, le travail, la maison. Une assistance est souvent nécessaire au long cours pour un fonctionnement optimal dans les différents environnements quotidiens. [3][1]
Ces déficits se doivent de survenir DURANT la période de développement.
Épidémiologie
À l'échelle mondiale, en 2016, environ 52,9 millions d'enfants ont un retard de développement identifiable. Étant donné que 95% de la population réside dans des pays à revenu faible et intermédiaire , il existe un risque accru de retard et de troubles du développement. [4]
Voici quelques statistiques :
- Bien que la prévalence exacte du retard de développement soit inconnue, selon l'Organisation mondiale de la santé (OMS), 10% de la population de chaque pays a un problème au niveau du développement chez l'enfant que ce soit dans une ou plusieurs sphères.[5]
- Aux États-Unis, c'est environ 15% des enfants qui auraient au moins un problème au niveau du développement. [6]
- Le retard global de développement et la DI concerneraient jusqu'à 3% de la population en pédiatrie [1]
De même, la prévalence du retard dans le développement impliquant des domaines respectifs chez les enfants est: [6]
- Cognitif (1% à 1,5%)
- Troubles d'apprentissage (8%)
- Parole et langage (2% à 19%)
L' incidence de retard de développement serait légèrement plus accrue chez les hommes, probablement en raison de la variabilité génétique sur le chromosome X.[7][8] Ainsi, la prévalence de DI varie en fonction du sexe et de l'âge de la personne; il serait plus élevé chez l'homme et chez l'individu d'âge scolaire. De même, c'est environ 20 à 30 % plus d'hommes que de femmes qui sont diagnostiqués avec une DI.
Les autres facteurs de risque rapportés sont :
- L' âge maternel avancé
- La pauvreté
- Le faible niveau d'éducation chez la mère
- L'âge paternel avancé jouerait également un rôle dans le développement d'une DI légère à modérée. [2]
Étiologies
L'étiologie du retard de développement est souvent multifactorielle. Lorsqu'elle est connue, l'étiologie peut inclure des facteurs génétiques, environnementaux et / ou psychosociaux. Parmi les causes de DI connues, les anomalies génétiques sont les plus fréquentes. [2]
Causes génétiques: Les modèles de développement sont souvent familiaux, y compris la marche et la conversation tardives chez les parents. Néanmoins, ces retards de développement peuvent également représenter des risques de syndromes ou de troubles du développement. Il existe une variation considérable dans la génétique des troubles du développement, allant des variantes du nombre de copies (CNV), des insertions, des délétions et des duplications. Le facteur génétique connu le plus courant pour la DI est le syndrome du X fragile, un trouble de répétition des trinucléotides (CGG) ciblant le gène FMR1 (Fragile X Mental Retardation) situé sur le chromosome X. X Fragile semble également conférer un risque de TSA . Le retard de développement et les phénotypes physiques peuvent être associés à d'autres troubles dans lesquels il y a des chromosomes ou des morceaux de chromosomes supplémentaires, par exemple, le syndrome de Down (trisomie 21), le syndrome d'Edward (trisomie 18) et le syndrome de Patau (trisomie 13) [9][10][11]. Les autre troubles chromosomiques comprennent le syndrome de Coffin-Lowry, principalement chez l'homme, et le syndrome de Rett chez la femme.[7]
Causes environnementales : Un grand nombre de facteurs environnementaux peuvent entraîner des retards de développement. Ces facteurs peuvent affecter le développement à un ou plusieurs points du processus de développement. [12] Par exemple, les toxines, les infections (TORCH), les agents tératogènes( ex. Isotrétinoïne) et les carences nutritionnelles sont quelques causes environnementales de retard de développement. [2]
| Atteintes | Pathologies |
|---|---|
| Retard de développement global | Anténatales ou périnatales
Intrinsèques
Post-natales
Comorbidités parfois associés au retard de développement : |
| Retard du langage et de la parole | Troubles du langage
Troubles de la parole
|
| Retard de la motricité grossière | Atteinte myopathie :
Atteinte neuropathique :
Atteinte moelle épinière:
Autre :
|
Physiopathologie
À l'exception des syndromes spécifiques qui incluent un retard de développement, la grande majorité des retards de développement sont idiopathiques. Bien que la physiopathologie exacte sous-jacente soit inconnue, plusieurs mécanismes ont été proposés par des études épidémiologiques qui conduisent à une sorte de retard de développement et / ou de handicaps. Étant donné que certaines formes de retard de développement peuvent survenir dans les familles, on suppose que les gènes jouent un rôle important dans le retard de développement. [12]
Une multitude de gènes et de mécanismes de transmission génétique ont été proposés. Alors que pour certaines causes de retard de développement telles que le X fragile ou le syndrome de Down , des étiologies génétiques sont connues, pour la plupart des autres, ce n'est pas aussi clair. Même pour des troubles bien caractérisés comme le trouble du spectre autistique, il existe plus de 100 allèles à risque [12]
L'axe hypothalamo-hypophysaire (AHH) est responsable de la régulation normale de la réponse au stress. Les facteurs de stress psychosociaux pendant la grossesse, l'activation immunitaire maternelle et la modification de l'AHH peuvent affecter de manière significative le développement cérébral du fœtus, mais il n'y a pas de relations de cause à effet spécifiques pour la plupart des troubles. Boyce et ses collègues ont proposé le concept de sensibilité différentielle. Cela suggère que le risque d'anomalies du développement est accru par une variété de facteurs qui créent une vulnérabilité biologique aux facteurs de stress environnementaux, mais ne sont exprimés que lorsque les stress environnementaux se produisent. De plus, même les enfants vulnérables peuvent réussir si les conditions environnementales sont très favorables et incitent à la résilience. [14][15][12]
Approche clinique
Une anamnèse complète et un examen physique approfondi sont des éléments essentiels de l'examen de l'enfant présentant un retard de développement. Des informations supplémentaires peuvent également être recueillies par une interaction avec l'enfant via des jouets adaptés à son âge (par exemple, des voitures miniatures, des blocs, des crayons de couleur et du papier) et en regardant l'enfant se déplacer dans la clinique. De plus, les vidéos personnelles peuvent s'avérer utiles. [16][12]
Lors du questionnaire, il importe toujours de se demander :[13]
- Est-ce qu'il y a une lenteur, une stagnation ou une régression du développement ? La régression est toujours inquiétante.
- L'enfant a-t-il une stimulation adéquate dans son environnement[note 1] ?
- Est-ce qu'il présente une surdité ou une cécité ?
- Est-ce qu'il présente un retard de développement dans une seule sphère ou est-ce un retard global ?
Pour répondre à cette dernière question, Il importe de connaître avant tout chacune des étapes normales du développement psychomoteur (en fonction des différentes sphères) selon l'âge de l'enfant.
Voici un tableau qui décrit le développement psychomoteur normal en fonction de l'âge de 1 mois jusqu'à 5 ans :
| Âge | Moteur grossier | Moteur fin | Parole-Langage | Cognitif/jeu | Social/Émotionnel |
|---|---|---|---|---|---|
| 1 mois |
|
|
|
|
|
| 2 mois |
|
|
Pas de sourire à 3 mois est préoccupant. |
|
|
| 4 mois |
|
|
|
|
|
| 6 mois |
|
|
|
|
|
| 9 mois |
|
|
|
|
|
| 12 mois |
|
|
|
|
|
| 18 mois |
Un enfant qui ne marche pas à 18 mois est préoccupant. |
|
< 10 mots à 18 mois est préoccupant. |
|
|
| 2 ans |
|
|
|
|
|
| 3 ans |
|
|
|
|
|
| 4 ans |
|
|
|
|
|
| 5 ans |
|
|
|
|
|
Aussi, en résumé, voici certaines des étapes importantes à retenir pour faire le diagnostic de retard de développement:
| Étape de développement | Âge moyen pour l'acquisition | Acquisition tardive |
|---|---|---|
| Sourire lorsqu'entend la voix de ses parents | 1 mois | 6 semaines |
| Roucoulement | 6 semaines | 2 mois et 3 semaines |
| Suit du regard un objet (180 degrés) | 2 mois et 2 semaines | 3 mois et 3 semaines |
| Tourne du ventre au dos | 4 mois et 2 semaines | 6 mois |
| Babillage | 5 mois | 9 mois |
| Transfert un objet d'une main à l'autre | 6 mois | 8 mois |
| S'assied sans aide | 9 mois | 11 mois |
| Pince inférieure pour saisir objets | 8 mois et 2 semaines | 14 mois |
| Maman et papa non spécifique ( Mamama et papapa) | 9 mois et 2 semaines | 13 mois |
| Premiers pas ( sans aide ) | 12 mois et 2 semaines | 15 mois |
| Dit trois mots ( en excluant papa et maman) | 13 mois et 2 semaines | 18 mois et 1 semaine |
| Imitation des adultes | 15 mois | 18 mois |
| Désigne au moins 6 parties du corps | 15 mois | 18 mois |
| Se déshabille en partie sans aide | 18 mois | 24 mois |
| S'habille sans aide | 3 ans et 6 mois | 4 ans et 6 mois |
| Dessine un bonhomme avec au moins 3 parties | 3 ans et 9 mois | 4 ans et 9 mois |
L'acquisition tardive dans le tableau signifie que 90% des enfants ont habituellement acquis cette étape à cet âge. Vous pouvez aussi vous référer aux drapeaux rouges, listés plus bas pour cibler certains éléments pouvant faire suspecter un retard de développement. Il importe de connaitre les étapes de développement normal afin de cibler tout retard chez l'enfant pour agir de façon précoce. Débuter rapidement, par exemple, les services de réadaptation peut permettre de minimiser les impacts négatifs au long cours. Par contre, les étapes de développement peuvent varier grandement d'un enfant à l'autre; il n'y a pas lieu de s'inquiéter si l'enfant reste dans les limites de la normale.[1]
Lors des visites périodiques, le médecin se doit de faire une surveillance du développement par rapport aux différentes sphères. Les parents sont souvent les premiers à dénoter une problématique dans le développement de leur enfant. Il importe ainsi de donner une attention particulière aux inquiétudes de ces derniers. Ils connaissent leur enfant mieux que nous! De même, lors de l'évaluation de l'enfant prématuré, il est essentiel de prendre en compte l'âge corrigé de ce dernier jusqu'à 2 ans d'âge, afin de ne pas identifier, de façon erronée, un retard de développement. Notez que le développement psychomoteur peut être influencé par des facteurs reliés à l'enfant ( ex. hérédité) et des facteurs reliés à l'environnement ( niveau socio-économique, culture).[17][13]
Différents outils de dépistage sont offerts sous plusieurs formes( PedsDM, ASQ, M-chat_R/F) . Certains consistent à faire remplir un questionnaire seulement aux parents; d'autres visent à faire participer l'enfant et les parents. Ces tests ne sont, cependant, pas diagnostiques. En pratique, à moins que la fratrie, par exemple, ait un problème de développement important, les médecins font habituellement seulement une surveillance du développement lors des visites périodiques. Des outils de suivi, comme l’ABCdaire 0-5 ans( différents éléments disponibles : feuillets de suivi en fonction de l’âge, courbes de croissance de l’OMS et calculateur de l’IMC...) peuvent être utiles à ce moment. [20]
Questionnaire
- Questionner les antécédents obstétricaux:
- Âge de la mère durant la grossesse et son vécu au niveau psychosocial et affectif
- Prise de poids durant la grossesse ( rechercher une malnutrition maternelle ? malnutrition foetale?)
- Problèmes médicaux(ex. diabète, épilepsie, hypertension) ou chx chez la mère
- Trauma durant la grossesse
- Exposition à des toxines ( ex. radiations, vapeurs toxiques) ou consommation d'alcool, de rx ou de drogues durant la grossesse
- Sx infectieux (syndrome d'allure grippal, fièvre) ou contact avec personne malade pendant la grossesse
- Tests trisomie 21 fait ?, autres tests de dépistage ?
- Suivi de routine de la grossesse : nombre d'échographie, prise de poids de la maman, dépistage de l'aneuploïdie fœtale.
- Questionner le déroulement de l'accouchement :
- Travail prolongé?
- Présence de complications( souffrance foetale, présentation non optimale, césarienne, réanimation du bébé) ou instrumentation ( forceps, ventouse)
- Score Apgar à la naissance
- Mesure poids-taille-périmètre crânien à la naissance.
- Souffrance foetale : ph cordon, méconium
- Durée du séjour à l' hôpital
- Évaluer la période néonatale. Rechercher:
- Présence d'hypotonie
- Ictère important et prolongé
- Hypothyroïdie
- Infection, fièvre
- Détresse respiratoire importante
- Alimentation difficile
- Hémorragies intraventriculaires cérébrales
- Convulsions
- Détresse respiratoire, intubation, ventilation mécanique
- Résultats de dépistage du nouveau-né: Dépistage néonatal sanguin (Phénylcétonurie, Hypothyroïdie congénitale, Tyrosinémie de type 1, Déficit en acyl-CoA déshydrogénase des acides gras à chaîne moyenne (MCADD), syndromes drépanocytaires majeurs, fibrose kystique) et dépistage néonatal urinaire (maladie acides aminés et organiques)
- Antécédents médicaux détaillés en post-natale:
- Rechercher la présence d'otites à répétions nécessitant des tubes (peut causer problème d'audition chez l'enfant)
- Questionner la prise de RX ( en particulier ceux pouvant avoir un effet sur le comportement ou l'état d'éveil , ex. phénobarbital)
- Présence d' infections du SNC? (ex. méningite, encéphalite)
- Connu pour traumatisme crânien?
- Connu maladies chroniques engendrant beaucoup d'hospitalisations?
- L'enfant a-t-il déjà eu de l'épilepsie ou des convulsions afébriles?
- Questionner les éléments psycho-sociaux chez l'enfant:
- Vit-il dans une famille biparentale, monoparentale, reconstituée? Si parents séparés, quels sont les arrangements pour la garde de l'enfant? Est-il dans une famille d'accueil ou est-ce qu'il l'a déjà été ?
- Rechercher le niveau de stimulation de l'enfant : y-a-t-il beaucoup de jeu à la maison ? Quelles sont les capacités parentales ? Les parents passent-ils beaucoup de temps avec leur enfant? L'enfant va-t-il à l'école ou à la garderie ?
- Réseau de soutien des parents : ont-ils des amis? des ressources s'ils nécessitent de l'aide ?
- Langues parlées à la maison et dans les autres environnements de l'enfant
- Problématiques infra familiales ?
- Consommation de substances psycho-actives par les parents?
- Questionner plus précisément les éléments reliés au retard:
- Questionner par rapport au développement psychomoteur dans les différentes sphères de la conception à l'âge actuel de l'enfant ( voir tableau plus haut pour orientation en fonction de l'âge). Dans quelles sphères l'enfant semble-t-il présenter un retard ? Est-ce que c'est une régression ou l'enfant n'a jamais atteint cette étape?
- Comment l'enfant fonctionne-t-il à la maison, à l'école ou à la garderie ( ou autres environnements qu'il fréquente)?
- Autres symptômes associés ? Rechercher la présence de stéréotypies, convulsions, tr de comportement...
- À quel moment les parents ont commencé à avoir une inquiétude par rapport au développement?
Recueillez les antécédents familiaux détaillés: La construction d'un arbre généalogique est souvent utile. Une histoire familiale sur trois générations doit être effectuée, évaluant les troubles neurodéveloppementaux et génétiques, les mortinaissances, les décès néonatals et les fausses couches,
Aussi:
- Y-a-t-il cosanguinité ? région, origine (ex. 2 parents venant de Charlevoix)
- Origine ethnique ?
- Rechercher si présence de maladie génétique/héréditaire dans la famille
- Y-a-t-il eu aussi des retards de développement dans la famille ? Présence d'handicap intellectuel ?
- Tb neurologiques ( épilepsie ? Gilles de la Tourette? Dystrophie musculaire?)
- Problèmes d'audition (surdité) ou de vision importante ( myopie ou hypermétropie chez les parents lorsqu'ils étaient enfants)
- TSA dans la famille ?
- Présence de TDAH?
- Obtenir un historique de vaccination
- Obtenez une histoire nutritionnelle - (c.-à-d. Habitudes alimentaires).
- Collecter des données sur les performances sociales et scolaires à l'école: trouble d'apprentissage, décrochage scolaire chez les parents? Préciser niveau de scolarité des parents.
Questionnaire plus spécifique pour trouble de langage :
- Important d'essayer de dépister de la surdité qui pourrait expliquer un trouble de langage
- Questionner les antécédents culturels et linguistiques ( important pour l'évaluation)
Il est toujours nécessaire de rechercher une cause qui pourrait être réversible et pour laquelle on peut agir rapidement, comme par exemple : exposition à des substances toxiques ou une importante négligence.
| Trouvaille | Penser à ... | Précisions |
|---|---|---|
| Neurologiques | ||
| Faiblesse musculaire | Toute maladie du SN périphérique | Atteinte musculaire
Atteinte médullaire
Atteinte sensitivo-motrice ( avec atteinte sensitive, ex. paresthésies) Fabry Refsum Neuropathie à axones géants |
| Hypotonie grave et persistante sans faiblesse musculaire habituellement |
|
|
| Convulsions |
|
|
| Ataxie |
|
|
| Digestif | ||
| Constipation chronique | Syndrome de Williams | Syndrome de Williams: [note 23][36] |
| Hyperphagie | Syndrome de Prader-Willi | Syndrome de Prader-Willi :[note 11] [27] |
| Douleur abdominale et vomissements | Intoxication au plomb | Autres éléments suggestifs : Vit dans une maison ou garderie construite avant 1950, immigration récente, rénovations au domicile, certaines professions chez le parent ( ex. fonderie, soudure, réparation carrosserie).[37] |
| Musculo-squelettique | ||
| Anomalies de la démarche (SCP) associés à stéréotypie des mains | Syndrome de Rett | [note 19] |
| Autistiques | ||
|
Trouble du spectre de l'autisme |
Autres affections parfois associées : neurofibromatose, phénylcétonurie, syndrome d'Angelman, de Cohen, Cornelia de Lange, de Prader-Willi, de Rett, de Smith-Lemli-Opitz et Williams. L'intoxication au plomb peut provoquer aussi un TSA.[38][39] |
| Comportementaux | ||
|
TDAH (comorbidité associée à des étiologies liés au retard de développement): sclérose tubéreuse de Bourneville, SAF, syndrome X fragile | Il n'y a pas de cause unique au TDAH. Il pourrait y avoir une composante génétique et neurobiologique( différence système dopaminergique et noradrénergique, diminution activité frontale). Différents facteurs de risque:
Affections associées liés au retard de développement : [40]
|
| Rires ou sourires fréquents, apparence joyeuse et hyperexcitabilité | Syndrome d'Angelman | [note 17] |
| ORL | ||
| Perte langagière subite après développement N. | Syndrome de Landau-Kleffner | [note 21][35] |
Examen clinique
À l'examen physique, comme tout examen physique chez l'enfant, il importe d'observer l'enfant dans son environnement, et ce, dès le questionnaire, ce qui peut nous donner de bons indices par rapport à son niveau de développement[12]:
- Observer la communication: réaction à son nom , contact visuel...
- Tester la compréhension du langage. Faire des consignes simples( ex. montre-moi ton nez) puis plus complexes (ex. va chercher tel objet et ramène le sur la chaise ). Il est possible de poser d'autres questions aussi : ex. Quel âge as-tu? De quelle couleur est ton pantalon ?
- Faire parler l'enfant et évaluer l'expression du langage. Bonne structure de phrase? On peut demander de raconter une histoire, nommer des couleurs..
- Évaluer la capacité d'imitation de l'enfant. On peut lui demander de faire comme nous certains gestes.
- Rechercher les comportements particuliers: enfant très lent, agitation, stéréotypies ( ex.mains crispées)
- Réactions sociales avec parent et médecin . Quelle est sa réaction face à une personne inconnue ?
- Interaction lors des jeux s'il y a lieu; il peut être intéressant de jouer avec l'enfant. Faire dessiner l'enfant aussi ( ex. bonhomme simple via l'épreuve de Goodenough)
Voici un tableau résumant l'essentiel de l'examen physique à faire:
| Examen et trouvailles | Penser à... | Informations complémentaires |
|---|---|---|
| Évaluation des paramètres de croissance : taille , poids et périmètre crânien . L'enfant suit-il ses courbes de croissance? Y-a-t-il des signes de dysmorphisme ? | ||
| Microcéphalie |
|
|
| Macrocéphalie |
|
|
| Petite taille | Syndrome de Down | Syndrome de Down: Autres éléments à rechercher à l'E/P:
Autres informations sur le syndrome : [note 14] |
| Grande taille | Syndrome de Sotos | [note 15] |
| Obésité |
|
Laurence-Moon-Bield: [note 22]
Syndrome de Prader-Willi: [note 11] |
| Forme du crâne, fontanelle .. Présence de plagiocéphalie, dolichocéphalie, scaphocéphalie? | Plagiocéphalie : Craniosynostose | |
| Rechercher des stigmates d'anomalie génétique ou chromosomique | ||
| Visage | ||
| Traits grossiers | Maladie de surcharge | Description plus générale de la maladie : [note 13] |
| Narines antéversés |
|
Smith Lemli Opitz : [note 26] [43]
Cornelia de Lange : [note 25] |
| Faciès amimétique | Myotonie de Steinert | Description plus générale de la maladie : [note 6] |
| Microphtalmie, rétrécissement des fentes palpébrales, plis épicanthal, milieu du visage petit ou plat, philtrum sous-développé , lèvre supérieure fine + un petit menton | SAF | 2nd à l'exposition à l'alcool in utero. |
| Visage elfique
Quelques caractéristiques: étroitesse bitemporelle, front large, nez court associé à un long philtrum, lèvres charnues et bouche large |
Syndrome de Williams | Description plus générale du syndrome: [note 23] |
| Yeux | ||
| Colobome | Syndrome CHARGE | Syndrome CHARGE: [note 27] [45] |
| Bleu étoilé au niveau de l'iris | Syndrome de Williams | Description plus générale du syndrome: [note 23] |
| Nodules de Lisch | Neurofibromatose de type 1 | Hamartomes, situés au niveau de l'iris. 75% des enfants NF1 en auront et ces nodules débutent habituellement à l'enfance.
Description plus générale: [note 20] |
| Épicanthus | Syndrome de Down | [note 14] |
| Nez | ||
| Extrémité bulbeuse proéminente | Syndrome de DiGeorge | Syndrome de DiGeorge : [note 28] [46] |
| Bouche | ||
| Palais ogival |
|
Syndrome de Treacher Collins: [note 29] [47]
Syndrome de Down : Protusion de la langue en raison du palais ogival observé |
| Oreilles | ||
| Surdité | Syndrome de Treacher Collins | Anomalies de l'oreille externe sont courantes dans ce syndrome . Autres informations: [note 29] |
| Mains et pieds | ||
| Syndactylie | Syndrome Smith-Lemli-Opitz | Description plus générale du syndrome : [note 26] |
| Peau | ||
|
Sclérose tubéreuse de Bourneville | Description plus générale : [note 16]
|
|
Neruofibromatose de type 1 | Habituellement, les enfants atteints de NF1 auront plus ≥ 6 tâches café au lait. À noter qu'il peut être normal chez certains enfants non atteints de NF1 d'avoir 2-3 tâches café au lait.[34]
Autres manifestations à l'E/P:
Description plus générale : [note 20] |
| Pli palmaire altéré (par exemple, semblable à une «crosse de hockey» au pli palmaire supérieur) | SAF | Avec autres traits du visage spécifiques tel que décrit dans ce tableau. |
| Cheveux | ||
| Cheveux en torsades et court ( crépus) et hypo pigmenté | Maladie de Menkes | Description générale de la maladie : [note 12] |
| Examen abdominal- à la recherche d'une organomégalie | ||
| Hépatomégalie ou splénomégalie | Maladies de Surcharge | Différents sous-types de la maladie. Par contre, habituellement touche davantage les tissus réticulo-endothéliaux riches en lysosomes ( ex.rate), ce qui explique la splénomégalie [29]Autres éléments par rapport à ces maladies : [note 13] |
| Anomalies organes génitaux | ||
| Ambiguïté sexuelle | Syndrome Smith-Lemli-Opitz | Description plus générale du syndrome : [note 26] |
| Augmentation volume des testicules après puberté | Syndrome X fragile | Autres informations: [note 18] |
| Examen du rachis | ||
| Présence de dysmorphisme ? Rechercher touffe de poils, fossette... | Spina bifida | |
| Scoliose |
|
|
| Examen neurologique : réflexes, forces musculaires, sensibilités, réflexes archaïque , posture et démarche | ||
| Moro encore + à 6 mois, hyperréflexie, spasticité: difficulté à s'asseoir, jambes en ciseaux, dysmorphie | Atteinte centrale | Ex. Peut être le tableau d'une malformation cérébrale ( ex. schizencéphalie) |
| Hypotonie importante, absence de réflexes, petite masse musculaire, petits pleurs, Gower+ | Atteinte périphérique | Ex. Dystrophie musculaire de Duchenne[note 4] |
Retard de motricité :
|
|
Neuropathies sensitivo-motrices :
Charcot-Marie Tooth : [note 8] Déjerine-Sottas: [note 9] |
|
|
Myopathie ex. :
Werdning-Hoffman : [note 7] |
| Examen général, incluant un examen bucco-oral | ||
| Rechercher présence d'ecchymoses à des localisations moins fréquentes. Est-ce que les blessures sont en regard d'une proéminence osseuse ?
Avec patron reconnaissable : forme d'objet, d'une main ou ligature? À l'examen bucco-oral : rechercher présence de blessures au frein de la lèvre supérieure ou langue |
Penser à maltraitance si :
|
Endroits moins classiques pour retrouver des ecchymoses :
La maltraitance peut se présenter sous forme de fractures ou de trauma crânien également. |
Durant l'entrevue, également, toujours observerez les interactions parentales : présence de dépression ? stress?
Drapeaux rouges
Voici quelques drapeaux rouges; aussi, la régression ne s’explique jamais et doit toujours être investiguée.
| Âge | Signaux d’alarmes |
|---|---|
| 6 semaines | Pas de contact visuel |
| 2 mois |
|
| 6 mois | Persistance du réflexe de Moro |
| 8 mois |
|
| 12 mois |
|
| 18 mois |
|
| 2 ans |
|
| À tout âge | Une régression est toujours inquiétante |
Examens paracliniques
En général, l'investigation permet le plus possible de déterminer l'étiologie du retard et faire du counseling génétique s'il y a lieu.
- Test audiologique ( audiogramme ) important à faire dans tous les cas de retard de développement
- Un examen ophtalmologique dans tous les cas aussi:
- Évaluer la vision, en particulier si les parents ont des problèmes de vison
- Évaluer la rétine. Rechercher des signes évocateurs de certaines maladies: cherry red spots chez les sphingolipidoses ( maladie de surcharge), rétinite pigmentaire dans les maladies mitochondriales, choriorétinite en toxoplasmose congénitale.
| Examen | Quand ce test est justifié | Résultats | Penser à... |
|---|---|---|---|
| TSH[note 31][1] | Petite taille, intolérance au froid, problèmes d'alimentation, faciès gonflé, macroglossie, grandes fontanelles, peau sèche, jaunisse prolongée ( sx d'hypothyroïdie ) | TSH augmenté
T4 diminué |
Hypothyroïdie congénitale |
| Hybridation génomique comparative ( CGH)- Recommandé en première intention, sauf si suspicion d'un trouble spécifique à l'E/P | Le meilleur test diagnostic utilisé seul
Retard global de développement et persistant Suspicion d'anomalie génétique au questionnaire et à l'E/P Notes : La sensibilité du caryotype correspond à moins de la moitié de celle du CGH Possibilité d'ajouter certaines examens plus spéciaux comme des sondes spécifiques et l'hybridation in situ en fluorescence( FISH). |
Délétion chromosomique dans la région 22q11 ( FiSH peut être utilisé) | Syndrome de DiGeorge |
| Délétion chromosomique 15q11-13
Chromosome paternel |
Syndrome de Prader-Willi | ||
| Délétion chromosomique 15q11-13
Chromosome maternel |
Syndrome d'Angelman | ||
| Suppression en 7q.11.23. Détecté FISH avec des sondes spécifiques du gène de l'élastine | Syndrome de Williams | ||
| Caryotype sur bande G | Si signes évocateurs d'un syndrome de Down ou autre aneuploïdie, comme celle associée aux chromosomes sexuels, dans le cas du Klinefelter | 47, XXY | Syndrome du Klinefelter |
| 47XX ou 47XY |
| ||
| Test d'ADN du gène de l’X fragile (FMR1). | Devrait être fait en première ligne chez les garçons et les filles ayant un retard de développement ou HI, car souvent symptomatologie non spécifique chez nourrissons et jeunes enfants
D'autres sources le recommande si présence de caractéristiques classiques ou hommes avec retard de développement ET antécédents familiaux de DI. |
Identification de mutation d'expansion anormale d'une répétition triplet CGG du gène FMR1 | Syndrome X fragile |
| Recherche mutation pathogène TSC1 ou TSC2 dans l'ADN des tissus normaux | Si suspicion de sclérose tubéreuse de Bourneville et impossible de faire diagnostic clinique | Mutation pathogènes des protéines TSC1 ou TSC2 +( ex. non-sens ou faux sens) | Sclérose tubéreuse de Bourneville |
| Analyse moléculaire du gène MECP2 | Lors de la symptomatologie classique (Développement normal puis perte de parole et stéréotypies de mains) ou trouble de développement modéré à grave | Identification de mutations du gène MECP2 | Syndrome de Rett |
| Hémogramme avec dosage de la plombémie | Si suspicion d'intoxication au plomb ( douleur abdominale, vo, fatigue ) | Plombémie augmentée ( degrés variables ) | Intoxication au plomb |
Recherche de virus et sérologies:
|
Il pourrait être approprié de dépister les maladies congénitales en présence de problèmes neurologiques, microcéphalie ou perte de l'audition ou vision.
Consultation en infectiologie pédiatrique probable |
IgG positives avec IgM et / ou IgA positives.
Parasite T. gondii + par PCR liquide biologique |
Suggestif d' infection à Toxoplasma gondii congénitale ( Notes : si IgG diminue au cours des 6 premiers mois de la vie de l'enfant, cela suggère des IgG maternel)
Détection parasite via PCR confirme dx de toxoplasmose congénitale |
| CMV+ dans la culture ou PCR | Infection congénitale à CMV. Il est important que la culture ou la recherche de PCR soit fait avant 3 semaines de vie, car sinon possibilité de contamination post-natale. | ||
| Culture virus rubéole + ou IgM spécifique + | Rubéole congénitale( Y penser aussi si rubéole + durant la grossesse) | ||
| Si test tréponémiques + ( détecte anticorps contre le T. pallidum) | Syphilis congénitale | ||
| IgM + herpès simplex | Infection congénitale virus herpès. Par contre, rare que les IgM sont +,car le nourrisson a souvent une immunodéficience face aux virus. À penser si infection de la mère durant la grossesse et symptomatologie classique chez l'enfant (ex. microcéphalie, conjonctivite, choriorétinite.. ) | ||
| Sérologie : ADN viral + ou ARN viral plasmatique + | Infection VIH. Note: si en haut de 18 mois, possibilité de faire la recherche d'anticorps anti-VIH via sérologie ELISA( avant 18 mois, ce serait non fiable, car les anticorps pourraient être transmis de la mère) | ||
| Créatinine-kinase | Faiblesse qui apparaît vers l'âge de 2 à 3 ans. Les enfants ont habituellement de la difficulté à courir, monter les escaliers et se relever du sol | Maximal à l'âge de 2 ans :
En général 10 à 20 fois la limite supérieure de la normale et peut être plus élevée[21] |
Dystrophie musculaire de Duchenne |
| Électromyogramme
Biopsie musculaire |
Changements myopathiques, généralement constitués de petits potentiels polyphasiques. Mais rarement utilisé pour le dx
Biopsie musculaire et analyse de dystrophine étaient avant importants, mais plus essentiel maintenant pour le dx | ||
| Gaz sanguins, dosage acide lactique et pyruvique plasmatiques, ammoninémie, amino-acidémie ou amino-acidurie, acidurie organique, dosage enzymatique dans les leucocytes ou fibroblastes, recherche mucopolysaccharides dans l'urine | Si tableau clinique évocateur d'erreurs innées du métabolisme ou de surcharge :
|
Hyperlactacidémie |
|
| Ammoninémie |
| ||
| Doser fer et vitamine b12 | Le faire en particulier si à la HMA, présence de pica ou restrictions au niveau alimentaire | Hb en bas de 120g/L | Anémie |
| Examen | Quand ce test est justifié | Résultats | Penser à... |
|---|---|---|---|
| IRM ou TDM
mais IRM plus précis |
|
Malformations cérébrales | Lissencéphalie,pachygyrie |
| Hétérotopie de la substance grise | (Cause rare d'épilepsie ) | ||
| Calcifications | • Sclérose tubéreuse de Bourneville
• Infection congénitale : calcifications cérébrales diffuses dans le cas de la toxoplasmose, calcifications cérébrales périventriculaires dans le cas du CMV | ||
| Électroencéphalographie (EEG) |
|
Activité épileptique à l'EEG | Épilepsie probable |
| Étude radiologique de déglutition | Trouble de déglutition associé au retard de développement | Anomalies au test de déglutition | Trouble de déglutition + |
Note : Lorsque qu'aucun diagnostic d'étiologie après l'E/P et l'HMA, la société canadienne de pédiatrie recommande de dépister le X fragile et de faire une bilan de base métabolique :
- Au niveau sanguin: Hémogramme, Glucose, Gaz sanguins, Urée, créatinine, Électrolytes (pour calculer le trou anionique, ALT, AST, TSH, Créatine kinase, Ammoniaque, Lactate, Acides aminés, Profil d’acylcarnitine, carnitine (libre et totale), Homocystéine, Cuivre, céruloplasmine, Biotinidase, Ferritine, vitamine B12 en présence de restrictions alimentaires ou de pica, Dosage du plomb en présence de facteurs de risque d’une exposition
- Au niveau urinaire : Acides organiques, Métabolites de la créatine, Purines, pyrimidines, Glycosaminoglycanes[1]
Pour certains syndromes, le diagnostic clinique parfois suffit. En voici deux exemples :
| Critères diagnostiques | Diagnostic |
|---|---|
|
Au moins 2 critères parmi les suivants :
|
Souvent, toutes les manifestations peuvent apparaître plus tard au cours de l'enfance, ce qui rend le diagnostic clinique plus difficile. Une analyse génétique pour confirmer est alors nécessaire, en recherchant des mutations au niveau du gène NF1 sur le chromosome 17. |
Critères majeurs:
Critères mineurs :
Un diagnostic certain : Deux critères majeurs ou un critère majeur et de deux mineurs. Diagnostic possible : Un critère mineur et un majeur. |
|
Traitement
La prise en charge du retard de développement dépendra de son étiologie. Lors d'une régression chez un enfant, il importe de référer rapidement ce dernier pour évaluation en pédiatrie spécialisée.
Les buts principaux sont: [13][52]
- Favoriser le plein potentiel de l'enfant et atténuer les plus possible les conséquences de l'handicap s'il y a lieu
- Renforcer et optimiser le fonctionnement au quotidien chez l'enfant ( ex. à la maison, à l'école, dans la communauté). Évaluer les problématiques à ce niveau et les impacts sur la famille.
La gestion du retard de développement lors de problèmes graves et complexes se fait rarement à un seul individu; une intervention pluridisciplinaire, pour s'adapter à chaque enfant, est habituellement de mise. Ainsi, cette équipe comprend parfois des fournisseurs de soins primaires ainsi que des surspécialistes pédiatriques tels que des neurologues ou des pédopsychiatres. En outre, les compétences d'autres disciplines peuvent être nécessaires, par exemple, la psychologie, la génétique, l'orthophonie, l'ergothérapie, la physiothérapie, les nutritionnistes, etc. En bref, les stratégies de traitement sont généralement multi-modales.[12] Les interventions associées doivent également commencer tôt et être soutenue afin de minimiser le plus possible le retard de développement; le médecin de famille se doit ainsi d'adresser rapidement le patient.
Les éléments essentiels sont :
- Assurer une communication efficace avec l'enfant: claire et concrète.
- Soutien avec les familles : Leur donner des pistes pour pouvoir accompagner adéquatement leur enfant. De plus, les services de soutien peuvent les aider à faire face à l'anxiété, à la dépression et à l'impuissance vécue. Il peut être intéressant aussi pour eux d'être en contact avec d'autres parents dont l'enfant a un retard de développement. Un travailleur social peut ainsi cibler des organismes de soutien en ce sens. Des services de répit existe également dans les ressources communautaires ( par exemple, à Québec, la maison Laura Lémerveil).
- S'assurer d'une surveillance du développement de l'enfant avec retard de développement; plusieurs intervenants peuvent être impliqués en ce sens (pédiatres, neurologues)
- Adapter l'environnement de l'enfant pour qu'il soit fonctionnel et sécuritaire pour lui.
Interventions possibles
- Si un manque de stimulation serait la cause la plus probable du retard de développement ( que ce soit au niveau du langage ou au niveau de d'autres sphères) : favoriser la fréquentation par l'enfant d'une structure éducative ( garderie, crèche, prématernelle) ou encore lui faire faire des ateliers de stimulation. Il peut avoir finalement un accompagnement individuel à la garderie pour inciter à la stimulation, par exemple.
- Chez les enfants ayant un retard moteur, langagier ou cognitif, il est important d'avoir accès à un service de réadaptation :
- Ergothérapie : Peut être intéressant si troubles praxiques, par exemple. Aussi, par exemple dans le cas d'un TSA, peut faire une thérapie de désensibilisation afin d'assurer une meilleure adaptation au niveau des activités quotidienne.
- Physiothérapeute : Favoriser la mobilité entre autres
- Orthophonie : Si retard de langage, faire la référence rapidement.[53]
- Retard simple du langage: se corrige avant l'âge de 6 ans normalement.
- Trouble primaire du langage : suivi habituellement tout le long de la scolarisation avec orthophonie et orthopédagogue
- Trouble de la parole: Si lié à une fente palatine, nécessite une équipe spécialisée. L'enfant devrait être référé précocement en orthophonie, env. vers l'âge de 2 ans.
- Si période associé à un bégaiement chez l' enfant de moins de 4 ans, rassurer les parents; possible que ce soit normal à cet âge. Si le trouble de fluidité continue pendant plus de 6 mois ou après 4 ans - référer en orthophonie.
- Si présence de mutisme sélectif - référer en psychologie pour soutien.
- Diététique : Si malnutrition associé à des troubles métaboliques ou endocriniens ou si désir d'évaluer l'état nutritionnel de l'enfant.
- Éléments reliés aux éléments fonctionnels au quotidien. Par exemple, pour favoriser un meilleur apprentissage, adapter l'environnement scolaire ( classe avec moins d'enfants, accompagnement dans une classe régulière, s'asseoir près du professeur, avoir plus de temps pour faire certains travaux... )
Éléments traitables
Éléments possiblement traitables pouvant améliorer le pronostic :[13][53]
Maladie de Menkes : Les symptômes sont reliés à une carence en cuivre. Le traitement consiste en l'administration parentérale d'un complexe cuivre-histidine.
Malnutrition : Référer en diététique, tel que spécifié plus haut.
Intoxication au plomb : Prise en charge en fonction de la plombémie et si le patient est symptomatique ou non. Par exemple, si pt asymptomatique et plombémie <5 mcg / dL : dépistage anémie ferriprive, trouver les causes potentielles d'explosion au plomb. La chélation n'est pas recommandée pour les plombémie <45 mcg / dL (2,17 micromol / L).
HTIC 2nd à l'hydrocéphalie : Ventriculostomie endoscopique du 3e ventricule ( dérivation ventriculo-péritonéale ). Autres éléments à ajouter :
- Tête surélevée de 20 à 30 degrés.
- Éviter hypoxie /hypercapnie
- Traitement de la fièvre s'il y a lieu
- Pressions artérielles dans les limites supérieures. Utilisation liquides isotoniques PRN.
- Sédation, analgésie PRN.
Si décompensation malgré les éléments ci-dessus : possibilité d'ajouter d'autres éléments ex. Mannitol 20%.
Si évidence de surdité de conduction qui pourrait expliquer un retard de langage : Myringotomie avec tubes transtympaniques de ventilation
Si évidence de surdité neuro sensorielle : Prothèse auditive ou pose d' implant cochléaire
Si présence d' infections congénitales[51]:
- Infection à CMV : Traitement du nouveau-né symptomatique avec Ganciclovir IV x 6 semaines ou Valganciclovir po x 3 à 6 mois ( mais controversé). La voie po serait tout aussi efficace.
- Rubéole: aucun tx spécifique
- Syphilis congénitale : Péneciline G IV x 10-14 jours si diagnostic sûr. Si dx seulement probable: Pénéciline benzathine IM x 1 dose.
- Toxoplasmose : Pyriméthamine et Sulfadiazine avec supplément d'acide folinique ( risque de toxicité médullaire) x 2 à 6 mois. Corticothérapie po si choriorétinite ou hyperprotéinorachie.
- Herpès : chez le nouveau-né, acyclovir IV.
Parfois, il est trop tard pour certaine affection si non diagnostiqué avant apparition du retard de développement:
- Phénylcétonurie ( Donner une diète réduite en phénylalanine, association avec retard mental si non traité )
- Hypothyroïdie congénitale ( peut donner un crétinisme congénital si non traité )
C'est pourquoi, maintenant, au Québec, nous avons accès au programme de dépistage néonatal . Dépistage néonatal sanguin: phénylcétonurie, hypothyroïdie congénitale, tyrosinémie de type 1, Déficit en acyl-CoA déshydrogénase des acides gras à chaîne moyenne (MCADD), syndromes drépanocytaires majeurs et fibrose kystique.
Si problèmes associés à certaines maladies responsables du retard de développement, les traiter selon l'évaluation :
- Épilepsie : Si première crise- le traitement doit être envisagé en fonction du type de crise, de l'EEG et éléments neurologiques. Habituellement, on commence à traiter à la 2ième crise. Différentes médications disponibles pour traiter l'épilepsie, en voici quelques exemples :
- Acide Valproïque. Indication: Enfant de plus de 1 an avec épilepsie généralisée ( absence, crise tonico-cloniques, crises mycoloniques)
- Carbamazépine. Indication : crise focale
- Clobazam. Indication: Épilepsie généralisée et focale
- Clonazépam Indication : absences, crises atoniques , crises mycloniques
- Éthosuximide. Indication : Petit mal-absence
- TDAH :
- Intervention psychosociale: S'adapte à l'enfant. Propose par exemple un programme d'aide pour les habiletés sociales ou un traitement au niveau du comportement. Possibilité aussi de faire une thérapie familiale pour donner des outils aux parents et aux frères et soeurs.
- Tx pharmaco : classe des stimulants le plus souvent utilisée (médicaments avec méthylphénidate ou dextroamphetamine)
- Dépression : Plus fréquente dans le syndrome de Down( nécessite souvent un suivi important) :
- Psychothérapie
- Si nécessaire , psychothérapie : fluxotéine en première ligne chez l'enfant et l'adolescent. En 2ième ligne : sertraline, esciptalopram ou citalopram.
Suivi
Le membre principal de l'équipe, souvent le fournisseur de soins primaires ( médecin de famille), se doit d'établir un partenariat thérapeutique avec l'équipe de soins pédiatriques. Il doit également éduquer et fournir aux parents les informations nécessaires sur le retard de développement. Par contre, il est important de prendre le temps de bien évaluer l'enfant lors des suivis ( comment ce dernier évolue? Y-a-t-il une progression dans l'acquisition de certaines compétences ou non?) avant de fournir des informations qui pourraient, si données trop hâtivement, être fausses. Après des mois d'évaluation, avec des interventions, bien souvent, multimodales, un diagnostic, un pronostic et les complications associées pourront être fournis à la famille si c'est le cas . Le soutien psychosocial et l'orientation parentale vers des organismes communautaires de soutien au besoin ( tel que décrit plus haut) sont des éléments essentiels aux soins. De même, les informations doivent être fournies à un niveau compatible avec la capacité des parents à comprendre, car cela améliorera l'acceptation et le respect des plans de soins. [7] [12] En général, ainsi, le médecin de famille se doit de maintenir la communication afin de soutenir la famille du patient tout au long du suivi de leur enfant. Dans les maladies plus complexes expliquant le retard de développement ( ex. syndromes ou maladies génétiques), l'évolution peut être variable, s'accompagnant de pic et creux; l'accompagnement de la famille est alors de mise dans tout ce processus. Notons que les retards de développement n'impliquent pas toujours des diagnostics graves. En effet, par exemple, le retard simple de développement laisse habituellement peu de conséquences et disparait avant l'entrée à l'école. [13]
Lorsque le diagnostic est posé, des suivis plus spécifiques s'imposent. Voici quelques exemples :
- En ce qui concerne le patient atteint de trisomie 21, il est important de faire des suivis par rapport aux diverses manifestations associées : maladie coealiaque (dépistage symptomatique) et hypothyroïdie (dépistage annuel).
- Il importe aussi de suivre les complications de certaines maladies chromosomiques et/ou syndromes ( ex. épilepsie, TDAH, troubles de l'humeur ) et faire une prise en charge PRN.
- Dans le cas de suivi pour un TSA, le praticien doit détecter la présence de comorbidités associés ( trouble du sommeil, compulsions, automutilation, agressivité, anxiété, TOC, TDAH, syndrome de Gilles de la Tourette). Une référence en pédopsychiatrie peut être nécessaire [54]. Un soutien psychosocial peut être aussi requis par la famille entourant l'enfant atteint de TSA.
Complications
Les complications vont dépendre de l'étiologie associée au trouble de développement[13] :
- Si troubles alimentaires : retard pondéral, carences nutritionnelles, obésité
- spasticité
- contractures
- scoliose
- ostéoporose
- sialhorrhée
- dysphagie
- RGO
- constipation
- pneumonie d'aspiration
- Conditions associées : TDAH, anxiété/ dépression , trouble du comportement, TSA.
- maltraitance
- isolement social
- toxicomanie
- analphabétisme
- précarité
Notes
- ↑ Dans les milieux plus défavorisés, on encourage fortement la maternelle 4 ans.
- ↑ on commence à être inquiet si l’enfant ne marche pas à 18 mois).
- ↑ Un enfant de moins 2 ans n'a pas vraiment de préférence pour un côté ou un autre. Si l'on est capable de dire tôt si l'enfant est droitier ou gaucher, un AVC est peut-être à soupçonner.
- ↑ 4,0 4,1 et 4,2 Maladie récessive liée au chromosome X. La faiblesse apparaît vers l'âge de 2 à 3 ans. Les enfants ont habituellement de la difficulté à courir, monter les escaliers et se relever du sol
- ↑ 5,0 et 5,1 Plusieurs sous-types ( 23 sont autosomiques récessives et 8 autosomiques dominantes). Apparition d'une faiblesse proximale progressive symétrique avec ou sans atteinte au niveau du visage.
- ↑ 6,0 6,1 et 6,2 La présentation peut varier selon la forme congénitale ou infantile. Transmission autosomique dominante. Peut engendrer problématique de langage en raison de la faiblesse musculaire au niveau du palais et de la langue. Dans la forme infantile, des troubles du rythme ou de la conduction cardiaque ( bloc auriculo-ventriculaire ou un bloc de branche incomplet) peuvent survenir chez l'adolescent
- ↑ 7,0 et 7,1 Dégénérescence des cellules de la corne ventrale de la moelle épinière et des noyaux moteurs dans le tronc cérébral inférieur. L'enfant devient symptomatique vers l'âge de 6 mois. Présence également d'hyporéflexie, fasciculations au niveau de la langue et difficultés pour têter + avaler. Faiblesse des muscles respiratoires qui engendre une insuffisance respiratoire progressive qui peut être à l'origine du décès
- ↑ 8,0 et 8,1 Rassemble un groupe de polyneuropathies périphériques. Implique mutations de certains gènes responsables de la formation de la myéline, des jonctions lacunaires et des axones. Il existe 7 types plus généraux ( CMT1 À CMT7). Symptomatologie générale : début de faiblesse musculaire distale et pied tombant avec atrophie musculaire distale associée. Les enfants présentent également des pieds creux et des orteils marteaux. Les symptômes sensoriels sont présents mais - importants que l'atteinte musculaire.
- ↑ 9,0 et 9,1 Classé dans le CMT3. Neuropathie démyélinisante importante débutant dans la petite enfance avec un déficit moteur qui est progressif. Atteinte sensitive associée et aréflexie ostéotendineuse.
- ↑ La plupart des enfants nés avec hypothyroïdie congénitale présenteront peu ou pas de symptômes . Autres signes et symptômes associés : Vitesse de croissance décélérée, intolérance au froid, difficulté d'alimentation, macroglossie, fontanelles importantes, peau sèche, jaunisse prolongée
- ↑ 11,0 11,1 et 11,2 Syndrome qui est dû à une anomalie du chromosome 15 paternel (15q11-q13). Hypotonie présente dès la naissance, associé à une mauvaise alimentation et retard de croissance. Puis, patient présente augmentation de l'appétit ( hyperphagie) et de l'obésité chez l'enfant et l'adulte. Une légère DI est présente dans 2/3 des cas.
- ↑ 12,0 et 12,1 Maladie génétique congénitale lié à l'X . Défaut d'une protéine de transport permettant l'absorption du cuivre dans l'intestin (gène ATP7A). Retard de développement qui apparait au cours de la petite enfance et associés à des sx neurologiques et de l'épilepsie. Également associé à un ictère prolongé, une hypothermie, une hypoglycémie en période néonatale.
- ↑ 13,0 13,1 et 13,2 Dans les maladies de surcharge, il y a des anomalies au niveau des enzymes lysosomales, ce qui entraine une accumulation de métabolites non dégradés. En fonction des métabolites non dégradés, il y a différents sous-types : mucopolysaccharidoses, sphingolipidoses et mucolipidoses.
- ↑ 14,0 14,1 et 14,2 Présence d'un chromosome 21 surnéméraire, de façon sporadique ( chromosome 47XX ou 47XY). Hypotonie présente chez le nouveau-né. Autres symptômes associés : DI légère à modérée, petite taille, malformations cardiaques congénitales( canal atrioventriculaire la plus fréquente), malformations digestives ( ex. atrésie duodénale ou de l'oesopage), malformations musculosquelettiques( instabilité atlanto-axiale ).
- ↑ 15,0 et 15,1 Syndrome 2nd à des mutations et des délétions du gène NSD1 (localisé sur le chromosome 5q35). Autres éléments associés : Souvent associé à un âge osseux avancé. Complications néonatales possibles comme l'hypotonie. Éléments à rechercher à l'E/P : Visage avec éléments particuliers : ex. menton pointu, front large et bombé, hypertélorisme et cheveux fins. Présence de grande taille et macrocéphalie également.
- ↑ 16,0 et 16,1 Maladie génétique autosomique dominante. Causée par une mutation du gène TSC1 sur le chromosome 9 ou du gène TSC2 sur le chromosome 16. L’épilepsie est la manifestation la plus associée à la STB. Atteint environ 60-90%des patients . Autres manifestations associées : Possibilité de tubers (malformation cérébrale qui pourrait être responsable de l'épilepsie) et nodules sous-épendymaires/ tumeurs sous-épendymaires à cellules géantes( bloque le foramen de Moro) Angiomyolipome (AML), kystes rénaux, carcinome rénal Hamartrome rétinien. Habituellement, si lésion bénigne rare d'avoir atteinte de la vision. Rhabdomyomes cardiaques: découvert lors de l'échographie lors du suivi de grossesse. Lymphangioléiomyomatose, mais survient habituellement chez les femmes adultes.
- ↑ 17,0 17,1 et 17,2 Secondaire à une délétion interstitielle entre 15q11 et 15q13 sur le chromosome 15 maternel. Environ 80% des enfants atteints du Syndrome d'Angelman auront de l'épilepsie à l'âge de 2 ans. Peut se présenter sous forme de convulsions, mais tous les types de crise ont été rapportées dans ce syndrome. Autres éléments caractéristiques : Déficience intellectuelle sévère Comportement hypermotorique Fascination pour l'eau Comportements avec la bouche et difficulté d'attention
- ↑ 18,0 18,1 et 18,2 Trouble lié à une anomalie du gène FMR1 sur le chromosome X. Cause héréditaire la plus fréquente de DI. Environ 10 à 20% des garçons atteints du syndrome développent de l'épilepsie. L'âge moyen d'apparition est environ de 2 ans.
- ↑ 19,0 et 19,1 Syndrome 2nd à une mutation du gène methyl CpG binding protein 2 (MECP2). Survient la plupart du temps chez les filles; rare chez les garçons. Autres manifestations associées : Irrégularités respiratoires avec épisodes d'apnée et d'hyperventilation, Anomalies cardiaques ( ex. intervalle QT prolongé) Scoliose Séquence classique : Développement normal ad 6 à 18 mois et perte de parole, stéréotypie des mains et anomalies de la démarche
- ↑ 20,0 20,1 et 20,2 Affecte le gène NF1 qui est situé sur le chromosome 17. Maladie autosomale dominante, mais dans 20 à 50% des cas, la maladie est engendrée par une mutation de novo. Notez que, dans les faits, peu de patients atteints de neurofibromatose auront de l'épilepsie ( 7%) Autres manifestations : Gliome des voies optiques : astrocytomes pilocytaires de grade 1. Débute entre l'âge de 3 à 7 ans. Peuvent être associés, lorsque symptomatique aux sx suivants : céphalées, proptose, limitation mouvement des yeux. Tumeur cérébrale: peu fréquent Hypersignaux T2 de la substance blanche Maladie vasculaire cérébrale: possibilité par ex. de Moyamoya
- ↑ 21,0 et 21,1 L'étiologie exacte de ce syndrome n'est pas connue. Des mutations dans le gène GRIN2A (16p13.2) pourraient être impliqués. Correspond à une encéphalopathie épileptique autosomale dominante. Les manifestations épileptiques arrivent chez le 2/3 des patients. Aussi, développement normal jusqu'à 3 à 6 ans puis perte langagière de type agnosie verbale auditive. Âge d'apparition + tardif qu'un autiste, ce qui permet de les différencier.
- ↑ 22,0 et 22,1 Maladie autosomale récessive. Ce syndrome serait 2nd à des mutations sur les gènes BBS5 ou MKKS. Syndrome associé à ataxie à la marche qui peut se développer en paraplégie spastique à l'âge adulte. Associé aussi à la rétinite pigmentaire pouvant engendrer de la cécité.
- ↑ 23,0 23,1 et 23,2 Syndrome secondaire à une microdélétion chromosomique située dans la région q11.23 d'un des chromosomes 7. La constipation est un problème courant et peut être associé à des complications de diverticulose, de prolapsus rectal, d'hémorroïdes et, de façon plus rare, de perforation intestinale. Autres manifestations : Hypercalcémie qui peut entrainer une néphrocalcinose Malformations cardiaques : ex. Sténose aortique supravalvaire HTA qui se développe chez environ 50 % des patients ayant un syndrome de Williams. La sténose des artères rénales peuvent engendrer une HTA réno-vasculaire.
- ↑ Syndrome de délétion 5p. Autres manifestations associées : visage rond, hypertélorisme, cri aigu de miaulement à la naissance.
- ↑ 25,0 et 25,1 Associée surtout à un synophrys ( confluence des deux sourcils à la base du nez) La mutation de trois gènes seraient impliqués : NIPBL, SMC1A,SMC3. Engendre un retard de croissance et un DI sévère. Autres manifestations associées à l'E/P: lèvre supérieure mince, doigts parfois manquants, syndactylie des 2e et 3e orteils.
- ↑ 26,0 26,1 26,2 et 26,3 Syndrome secondaire à un déficit autosomal récessif liés à mutations du gène DHCR7 (11q13.4), nécessaire à la synthèse du cholestérol. Engendre : DI, retard de croissance, hypospadias, microcéphalie et polysyndactylie.
- ↑ : Peut être sporadique ou ou se transmettre selon un mode autosomique dominant. Le colobome est présent dans 75 à 90% des cas. Autres anomalies associées à l'E/P: Anomalies cardiaques Atrésie des choanes Retard de croissance et développement Anomalies génitales : hypogonadisme Malformation oreille
- ↑ Secondaire à Microdélétions 22q11.2. Triade classique : anomalies cardiaques, hypocalcémie et hypoplasie thymique. Possible aplasie entrainant une HypoPTH et déficit lymphocytes T. Peut engendrer des troubles du langage ou de la parole et retard de développement. Autres éléments à rechercher à l'E/P : oreilles basses implantées, rétrognathisme( mâchoire vers l'arrière), hypertélorisme, entre autres
- ↑ 29,0 et 29,1 Syndrome secondaire à la mutation de certains gènes (mutations du gène TCOF1 (5q32-q33.1) ou des gènes POLR1C (6p21.1) et POLR1D (13q12.20) . Autres éléments à rechercher à l'E/P en plus du palais ogival : micrognathisme, yeux avec une inclinaison antimongoloïde (yeux tombants ) et pommettes plates.
- ↑ S'il y a présence de signes spécifiques au questionnaire ou à l'E/P, faire les tests précis pour éliminer cette anomalie génétique ou la confirmer.
- ↑ Au Québec, présence du dépistage néonatal sanguin. Selon l'Association Américaine de Neurologie, si dépistage néonatal négatif, il ne serait pas nécessaire de refaire le test. Par contre, refaire le test peut permettre de ne pas manquer les cas acquis et les origines hypothalamiques et pituitaire
Références
- Cette page a été modifiée ou créée le 2020/12/24 à partir de Developmental Delay (StatPearls / Developmental Delay (2020/09/19)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/32965902 (livre).
- ↑ 1,00 1,01 1,02 1,03 1,04 1,05 1,06 1,07 1,08 1,09 et 1,10 « L’évaluation de l’enfant ayant un retard global du développement ou un handicap intellectuel », sur Société canadienne de pédiatrie (consulté le 3 avril 2021)
- ↑ 2,00 2,01 2,02 2,03 2,04 2,05 2,06 2,07 2,08 2,09 et 2,10 (en) « Intellectual disability in children: Evaluation for a cause », sur Up to date (consulté le 3 avril 2021)
- ↑ 3,0 et 3,1 (en) « Intellectual disability in children: Definition, diagnosis, and assessment of needs », sur Up to date (consulté le 3 avril 2021)
- ↑ Erica Salomone, Laura Pacione, Stephanie Shire et Felicity L. Brown, « Development of the WHO Caregiver Skills Training Program for Developmental Disorders or Delays », Frontiers in Psychiatry, vol. 10, , p. 769 (ISSN 1664-0640, PMID 31780960, Central PMCID 6859468, DOI 10.3389/fpsyt.2019.00769, lire en ligne)
- ↑ Lílian de Fátima Dornelas, Neuza Maria de Castro Duarte et Lívia de Castro Magalhães, « [Neuropsychomotor developmental delay: conceptual map, term definitions, uses and limitations] », Revista Paulista De Pediatria: Orgao Oficial Da Sociedade De Pediatria De Sao Paulo, vol. 33, no 1, 2015-01-xx, p. 88–103 (ISSN 1984-0462, PMID 25662016, Central PMCID 4436961, DOI 10.1016/j.rpped.2014.04.009, lire en ligne)
- ↑ 6,0 et 6,1 Kirsten Vitrikas, Dillon Savard et Merima Bucaj, « Developmental Delay: When and How to Screen », American Family Physician, vol. 96, no 1, , p. 36–43 (ISSN 1532-0650, PMID 28671370, lire en ligne)
- ↑ 7,0 7,1 et 7,2 Pradeep Vasudevan et Mohnish Suri, « A clinical approach to developmental delay and intellectual disability », Clinical Medicine (London, England), vol. 17, no 6, , p. 558–561 (ISSN 1473-4893, PMID 29196358, Central PMCID 6297696, DOI 10.7861/clinmedicine.17-6-558, lire en ligne)
- ↑ Kirsten Ann Donald, Catherine J. Wedderburn, Whitney Barnett et Raymond T. Nhapi, « Risk and protective factors for child development: An observational South African birth cohort », PLoS medicine, vol. 16, no 9, , e1002920 (ISSN 1549-1676, PMID 31560687, Central PMCID 6764658, DOI 10.1371/journal.pmed.1002920, lire en ligne)
- ↑ Rachel D. Burnside, Romela Pasion, Fady M. Mikhail et Andrew J. Carroll, « Microdeletion/microduplication of proximal 15q11.2 between BP1 and BP2: a susceptibility region for neurological dysfunction including developmental and language delay », Human Genetics, vol. 130, no 4, , p. 517–528 (ISSN 1432-1203, PMID 21359847, Central PMCID 6814187, DOI 10.1007/s00439-011-0970-4, lire en ligne)
- ↑ Diana Miclea, Loredana Peca, Zina Cuzmici et Ioan Victor Pop, « Genetic testing in patients with global developmental delay / intellectual disabilities. A review », Clujul Medical (1957), vol. 88, no 3, , p. 288–292 (ISSN 1222-2119, PMID 26609258, Central PMCID 4632884, DOI 10.15386/cjmed-461, lire en ligne)
- ↑ Randi J. Hagerman, Elizabeth Berry-Kravis, Walter E. Kaufmann et Michele Y. Ono, « Advances in the treatment of fragile X syndrome », Pediatrics, vol. 123, no 1, , p. 378–390 (ISSN 1098-4275, PMID 19117905, Central PMCID 2888470, DOI 10.1542/peds.2008-0317, lire en ligne)
- ↑ 12,0 12,1 12,2 12,3 12,4 12,5 12,6 et 12,7 Israr Khan et Bennett L. Leventhal, StatPearls, StatPearls Publishing, (PMID 32965902, lire en ligne)
- ↑ 13,00 13,01 13,02 13,03 13,04 13,05 13,06 13,07 13,08 13,09 13,10 13,11 et 13,12 Jean Turgeon, Dictionnaire de pédiatrie Weber 3e édition, Montréal, Chenelière édition, , 1366 p. (ISBN 978-2-7650-4746-9), p.998-1005
- ↑ Jun Udagawa et Kodai Hino, « Impact of Maternal Stress in Pregnancy on Brain Function of the Offspring », Nihon Eiseigaku Zasshi. Japanese Journal of Hygiene, vol. 71, no 3, , p. 188–194 (ISSN 1882-6482, PMID 27725421, DOI 10.1265/jjh.71.188, lire en ligne)
- ↑ Bruce J. Ellis et W. Thomas Boyce, « Differential susceptibility to the environment: toward an understanding of sensitivity to developmental experiences and context », Development and Psychopathology, vol. 23, no 1, , p. 1–5 (ISSN 1469-2198, PMID 21262035, DOI 10.1017/S095457941000060X, lire en ligne)
- ↑ Martin Bellman, Orlaith Byrne et Robert Sege, « Developmental assessment of children », BMJ (Clinical research ed.), vol. 346, , e8687 (ISSN 1756-1833, PMID 23321410, DOI 10.1136/bmj.e8687, lire en ligne)
- ↑ 17,0 et 17,1 Jean Turgeon, Dictionnaire de pédiatrie Weber, Montréal, Chenelière éducation, , 1366 p. (ISBN 978-2-7650-4746-9), p. 29-35
- ↑ (en) « Developmental-behavioral surveillance and screening in primary care »,
- ↑ Jean Turgeon, Dictionnaire de pédiatrie Weber, Montréal, Chenelière éducation, , 1366 p. (ISBN 978-2-7650-4746-9), p. 29-35
- ↑ « Outils ABCdaire », sur CHU Ste-Justine (consulté le 3 avril 2021)
- ↑ 21,0 et 21,1 (en) « Duchenne and Becker muscular dystrophy: Clinical features and diagnosis », sur Up to date (consulté le 3 avril 2021)
- ↑ « Dystrophie musculaire de Duchenne et de Becker », sur Merck Manuel (consulté le 3 avril 2021)
- ↑ « Dystrophie musculaire des ceintures », sur Merck Manuel,
- ↑ (en) « Myotonic dystrophy: Etiology, clinical features, and diagnosis », sur Up to date (consulté le 3 avril 2021)
- ↑ « Amyotrophies musculaires spinales (SMAs) », sur Merck Manuel (consulté le 4 avril 2021)
- ↑ 26,0 et 26,1 (en) « Charcot-Marie-Tooth disease: Genetics, clinical features, and diagnosis » (consulté le 3 avril 2021)
- ↑ 27,0 et 27,1 (en) « Clinical features, diagnosis, and treatment of Prader-Willi syndrome » (consulté le 3 avril 2021)
- ↑ (en) « Overview of dietary trace elements » (consulté le 4 avril 2021)
- ↑ 29,0 et 29,1 (en) « Revue générale des maladies de surcharge lysosomale » (consulté le 4 avril 2021)
- ↑ 30,0 et 30,1 « Syndrome de Down (trisomie 21) », sur Merck Manuel (consulté le 4 avril 2021)
- ↑ 31,0 31,1 31,2 et 31,3 « Sclérose tubéreuse de Bourneville », sur CHU de Ste Justine (consulté le 3 avril 2021)
- ↑ 32,0 et 32,1 (en) « Microdeletion syndromes (chromosomes 12 to 22) », sur Up to date (consulté le 3 avril 2021)
- ↑ 33,0 33,1 et 33,2 (en) « Fragile X syndrome: Clinical features and diagnosis in children and adolescents », sur Up to date (consulté le 4 avril 2021)
- ↑ 34,0 34,1 et 34,2 « Neurofibromatose », sur CHU Ste-Justine (consulté le 3 avril 2021)
- ↑ 35,0 et 35,1 (en) « Epilepsy syndromes in children », sur Up to date (consulté le 3 avril 2021)
- ↑ (en) « Williams syndrome », sur Up to date (consulté le 3 avril 2021)
- ↑ (en) « Intellectual disability in children: Definition, diagnosis, and assessment of needs », sur Up to date (consulté le 3 avril 2021)
- ↑ (en) « Troubles du spectre autistique », sur Merck Manuel (consulté le 4 avril 2021)
- ↑ Jean Turgeon, Dictionnaire de pédiatrie Weber 3e édition, Montréal, Chenelière éducation, 1366 p. (ISBN 978-2-7650-4746-9), p.1183-1187
- ↑ (en) « Attention deficit hyperactivity disorder in children and adolescents: Epidemiology and pathogenesis », sur Up to date (consulté le 4 avril 2021)
- ↑ « Syndrome d'alcoolisme fœtal », sur Merck Manuel (consulté le 3 avril 2021)
- ↑ 42,0 et 42,1 (en) « Microcephaly in infants and children: Etiology and evaluation » (consulté le 4 avril 2021)
- ↑ 43,0 et 43,1 (en) « Laboratory issues related to maternal serum screening for Down syndrome », sur Up to date (consulté le 4 avril 2021)
- ↑ (en) « Macrocephaly in infants and children: Etiology and evaluation », sur Up to date,
- ↑ (en) « Assessment of the newborn infant », sur Up to date (consulté le 4 avril 2021)
- ↑ (en) « Syndrome de DiGeorge » (consulté le 4 avril 2021)
- ↑ (en) « Syndromes with craniofacial abnormalities », sur Up to date (consulté le 4 avril 2021)
- ↑ (en) « Sclérose tubéreuse de Bourneville (tuberous sclerosis complex) », sur Merck Manuel (consulté le 3 avril 2021)
- ↑ Jean Turgeon, Dictionnaire de pédiatrie Weber 3e édition, Montréal, Chenelière éducation, , 1366 p., p.590-600
- ↑ Jean Turgeon, Dictionnaire de pédiatrie Weber 3e édition, Montréal, Chenelière éducation, , 1366 p., p. 1075
- ↑ 51,0 51,1 et 51,2 Jean Turgeon, Dictionnaire de pédiatrie Weber, Montréal, Édition Chenelière, , 1366 p., p. 730-734
- ↑ (en) « Intellectual disability in children: Management, outcomes, and prevention », sur Up to date (consulté le 3 avril 2021)
- ↑ 53,0 et 53,1 Jean Turgeon, Dictionnaire de pédiatrie Weber 3e édition, Montréal, Chenelière éducation, , 1366 p., p.1165-1170
- ↑ Jean Turgeon, Dictionnaire de pédiatrie Weber 3e édition, Montréal, Chenelière éducation, 1366 p., p.1183-1187
