Rétinite pigmentaire
| Maladie | |
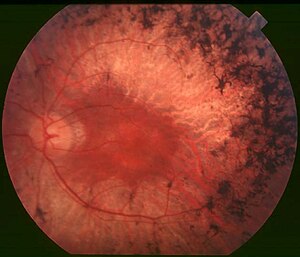 Fond d'oeil d'une rétinite pigmentaire - Stade léger | |
| Caractéristiques | |
|---|---|
| Signes | Spicule osseux, Rétrécissement vasculaire, Pâleur anormale du disque optique |
| Symptômes |
Nyctalopie, Photopsie, Adaptation rapide de la lumière, Rétrécissement des champs visuels, Vision en tunnel |
| Diagnostic différentiel |
Rétinite punctata albescens, Dystrophie des cônes / bâtonnets, Infections choriorétiniennes |
| Informations | |
| Terme anglais | Retinitis Pigmentosa |
| Spécialité | Ophtalmologie |
|
| |
La rétinite pigmentaire en tant qu'entité clinique a été initialement décrite en 1853, mais le nom n'a été associé à la maladie qu'en 1857.[1] Considéré par la plupart comme un terme impropre, le terme rétinite persiste aujourd'hui, même si l'inflammation n'a qu'un petit rôle dans la progression naturelle de la maladie. La rétinite pigmentaire (RP) n'est pas une entité unique, mais plutôt un groupe de troubles qui entraînent une perte progressive de la vision.
Également connue sous le nom de dystrophie rétinienne héréditaire, elle affecte 1 personne sur 4000 aux États-Unis et environ une personne sur 5000 dans le monde, faisant de la RP la maladie héréditaire la plus courante de la rétine. Il est généralement bilatéral, mais il a été signalé une atteinte oculaire unilatérale de la RP. Bien qu'elle puisse présenter et évoluer avec une variété de manifestations cliniques, le premier symptôme de la RP est généralement la nyctalopie, ou perte de vision nocturne, qui est suivie d'un rétrécissement progressif des champs visuels. Au fil du temps, selon la gravité et le taux de progression de la maladie, une vision tunnel ou une perte de vision complète peut en résulter.
Au fur et à mesure que la maladie progresse, d'autres caractéristiques peuvent également se développer, notamment la perte d'une discrimination précise des couleurs et, éventuellement, une perte d'acuité visuelle. La plupart des patients conserveront une certaine perception de la lumière même avec une RP à un stade avancé, car la macula continue de fonctionner. L'effet tardif le plus troublant de la RP est peut-être le développement de la photopsie (éclairs perçus de lumière), probablement due à une privation sensorielle. Cela peut même évoluer au point d'hallucinations visuelles.
La maladie peut impliquer une perte de vision seule, et dans ce cas est appelée RP "non syndromique". La majorité des cas de RP, environ 70% à 80%, entrent dans la catégorie non syndromique. Lorsque la RP survient en conjonction avec une maladie systémique, elle est appelée RP «syndromique». La forme la plus courante de RP syndromique est le syndrome d'Usher, qui implique une perte auditive neurosensorielle associée à une perte de vision [2].[3]
Épidémiologie
La rétinite pigmentaire non syndromique a une prévalence mondiale d'environ un sur 5000, et les porteurs sont au nombre d'environ un sur 1000.
Les hommes sont affectés un peu plus souvent que les femmes en raison de la forme liée à l'X qui s'exprime plus fréquemment chez les hommes.
La RP syndromique est beaucoup moins courante, les estimations du syndrome d'Usher variant de 1,8 à 6,2 cas pour 100 000 personnes. L'âge moyen d'apparition des symptômes dépend du type génétique. La forme autosomique récessive développera des symptômes au début de l'adolescence, mais les personnes atteintes de RP autosomique dominante n'auront probablement pas de symptômes avant la vingtaine.
Plus des trois quarts des personnes atteintes de RP seront symptomatiques et présentes pour une évaluation clinique et un diagnostic de la maladie à l'âge de 30 ans.[3]
Étiologies
Les mutations génétiques responsables de la rétinite pigmentaire produisent un dysfonctionnement biochimique affectant spécifiquement les photorécepteurs des bâtonnets dans la rétine. Les défauts peuvent être associés à de multiples voies de blessures, y compris l'apoptose, les dommages légers, le dysfonctionnement du transport ciliaire et le stress du réticulum endoplasmique. Le résultat commun de toutes les voies possibles est la mort des photorécepteurs à tige.[4]
Étant donné que les bâtonnets sont responsables de la vision par faible luminosité, la perte toujours croissante de ces cellules produit la cécité nocturne caractéristique associée à la RP et une diminution progressive de la vision périphérique. Finalement, la destruction d'un grand nombre de bâtonnets a un effet délétère sur l'épithélium pigmentaire rétinien (EPR) et commence également à affecter les photorécepteurs à cône. Lorsque les cônes commencent à succomber à l'environnement toxique créé par la mort progressive des cellules de la rétine, une dyschromatopsie ou une perturbation de la perception des couleurs peut se développer.
Plus de 100 loci génétiques sur 50 gènes différents se sont révélés être à l'origine de multiples modes de transmission et d'expression de la rétinite pigmentaire. Environ 20% des cas de RP sont autosomiques récessifs, avec 10% à 20% autosomiques dominants et 10% liés à l'X récessif. Les autres cas sont qualifiés de sporadiques, et aucun antécédent familial ou base moléculaire connue n'est trouvé.[3]
Physiopathologie
Comme mentionné précédemment, il existe de multiples mécanismes génétiquement dirigés pour la progression de la rétinite pigmentaire. L'apoptose est essentiellement une programmation physiologique de la mort cellulaire, qui peut être déclenchée par une mutation génétique. L'apoptose peut également être induite par la communication de cellule à cellule entre les photorécepteurs eux-mêmes.[5] Par conséquent, la mort des bâtonnets peut également se propager aux récepteurs du cône. L'exposition à la lumière peut exacerber les mécanismes phototoxiques. Il s'agit notamment des mutations du métabolisme du rétinol et de l'accélération de la consommation d'oxygène dans l'environnement, ce qui peut améliorer la dégénérescence des photorécepteurs, à la fois en bâtonnet et en cône. [6] La fonction ciliaire est importante pour le transport des nutriments et autres substances dans la rétine. Certaines mutations génétiques, dont celle du syndrome d'Usher, peuvent altérer cette fonction et entraîner une vulnérabilité cellulaire.[7] Le stress dans le réticulum endoplasmique peut provoquer la libération de radicaux libres, avec une stimulation ultérieure de l'hypoperfusion de la rétine et des lésions des cellules endothéliales vasculaires.[8]
Trois signes cliniques typiques de la rétinite pigmentaire sont la présence d'une pigmentation du spicule osseux, un rétrécissement vasculaire et une pâleur du nerf optique. Les dépôts de pigment de mélanine, du nom de leur forme d'étoile spiculaire osseuse caractéristique, sont dus aux cellules épithéliales du pigment rétinien qui se détachent et migrent vers des emplacements périvasculaires de la rétine. La cause exacte de cette migration n'est pas entièrement comprise, pas plus que le rétrécissement des vaisseaux rétiniens, bien qu'une suggestion soit que cela résulte d'une diminution de la demande métabolique due à la mort d'un grand nombre de photorécepteurs. Le changement d'apparence du disque optique est probablement dû à la formation de cellules gliales qui recouvrent le disque et augmentent la réflectivité, produisant une "pâleur cireuse" [1].[3]
Présentation clinique
Questionnaire
La présentation typique de la RP implique des plaintes de troubles visuels commençant tôt dans la vie. Habituellement, cela inclut un sentiment relativement vague d'être incapable de bien voir avec des situations de faible luminosité, ou celles nécessitant une adaptation rapide de la lumière aux environnements sombres. Certaines personnes notent des difficultés à conduire la nuit, car les phares venant en sens inverse et d'autres sources de lumière vive dans l'environnement rendent difficile pour eux de se réadapter à l'obscurité par la suite. Le rétrécissement des champs visuels n'est pas évident au départ mais deviendra apparent au fil du temps.
Un pedigree génétique pour la famille du patient sera essentiel pour déterminer le type de modèle de transmission et aider au pronostic. Un historique complet et un examen des systèmes sont nécessaires pour identifier d'autres systèmes affectés en plus de la déficience visuelle pour identifier les variantes syndromiques de RP. De plus, un examen de l’exposition possible à des maladies infectieuses ou à des toxines qui pourraient produire une «imitation» de la maladie devrait être entrepris.
Examen physique
Les découvertes physiques comprennent la «triade classique» observée lors d'un examen fundoscopique de la pigmentation du spicule osseux, du rétrécissement vasculaire et de la pâleur anormale du disque optique. Ceux-ci peuvent ne pas être évidents au début de la maladie, et le degré auquel des anomalies sont observées varie en fonction de la gravité de la maladie.
D'autres signes physiques associés peuvent inclure des cataractes sous-capsulaires et un œdème maculaire.
Alors que l'examen externe de l'œil est généralement normal, les patients RP présentent un risque plus élevé de kératocône par rapport à la population générale. Pourtant, le développement du kératocône est assez rare.[9] Les erreurs de réfraction se produisent également plus fréquemment chez les patients RP que dans la population générale.[1][3]
Examens paracliniques
Une évaluation ophtalmologique complète pour toute personne suspectée de RP est nécessaire, y compris un examen fundoscopique expert et l'évaluation de la fonction rétinienne.
Ces tests établiront une ligne de base et aideront à déterminer le taux de progression et à formuler un pronostic pour la maladie. L'évaluation du champ visuel avec périmétrie cinétique est considérée comme le moyen le plus efficace d'évaluer la perte de vision périphérique.
Une évaluation de la vision des couleurs sera nécessaire pour déterminer la présence et la progression de la dyschromatopsie, indiquant le degré d'implication des photorécepteurs des cônes. L'évaluation électrophysiologique de l'ensemble de la rétine est également utile, car des anomalies électrorétinographiques peuvent être détectées précocement, même avant la nyctalopie et les anomalies fundoscopiques.[1]
L'imagerie rétinienne a fait des progrès significatifs. Dans le passé, l'angiographie à la fluorescéine était la méthode prédominante utilisée, mais les nouvelles modalités non invasives ont rendu les études plus faciles à réaliser et plus sensibles à la détection des anomalies. L'ophtalmoscopie laser à balayage à optique adaptative (AOSLO) permet une évaluation à haute résolution de la rétine pour détecter les dommages aux photorécepteurs au début de la maladie. Ce processus est susceptible d'être utile pour surveiller la progression de la maladie ainsi que pour évaluer l'efficacité de l'efficacité du traitement.[1]
Aucun test de laboratoire spécifique n'est indiqué, sauf en cas de suspicion d'autres processus pathologiques contribuant à une perte de vision, tels que la syphilis ou la rétinopathie à cytomégalovirus (CMV), ou à moins qu'un test génétique de confirmation ne soit indiqué.[3]
Diagnostic différentiel
Le diagnostic différentiel de la perte de vision progressive est complexe.
La rétinite pigmentaire est un diagnostic clinique qui peut être confirmé par la présence d'une atteinte oculaire bilatérale avec troubles de la vision nocturne et perte progressive de la vision périphérique. Les résultats physiques à l'examen fundoscopique révèlent une pigmentation du spicule osseux, avec un rétrécissement vasculaire et une pâleur du disque optique. Il convient également de noter qu'il existe des variantes de RP avec des différences significatives dans les résultats physiques.
- La rétinite punctata albescens (RPA) se présente fréquemment comme une cécité nocturne pendant l'enfance. Lors d'un examen fundoscopique direct, les résultats incluent une pâleur discale moins saillante (ou même absente), un rétrécissement vasculaire moins prononcé et les spicules osseux sont rares ou absents. Au lieu de cela, il y a de petites taches blanches couvrant la majorité du fond d'œil dans RPA. La connaissance de ces variantes est nécessaire pour éviter d'exclure RP et ses sous-classes du différentiel.[10]
- D'autres maladies peuvent imiter les premiers résultats et une évaluation minutieuse doit être entreprise pour poser le bon diagnostic. Une imitation possible est la dystrophie des cônes / bâtonnets. Cette rétinopathie progressive peut être différenciée de la RP par l'apparition d'une dyschromatopsie avant la nyctalopie, car les photorécepteurs du cône sont affectés plutôt que les bâtonnets. Une autre considération pour la nyctalopie dans l'enfance est la cécité nocturne stationnaire congénitale (CSNB). L'altération de la vision en basse lumière est présente à la naissance et contrairement à la RP, elle est généralement non progressive. [11][12]
- Les infections choriorétiniennes, telles que la syphilis, le CMV ou même la maladie de Lyme peuvent produire des symptômes évocateurs de RP. Une histoire minutieuse aidera généralement à identifier ces possibilités, et des tests de laboratoire pour confirmation seront indiqués.
La perte de vision peut être le résultat de plusieurs autres maladies, dont la sarcoïdose et le lupus érythémateux disséminé. L'atteinte systémique en plus de la perte de vision devrait inciter à une évaluation approfondie de ces processus inflammatoires et d'autres. Une carence en vitamine A et un traumatisme doivent également être pris en compte.[3]
Traitement
Il n'existe aucun traitement standard pour les patients atteints de rétinite pigmentaire.
Le traitement le plus largement recommandé depuis de nombreuses années a été la supplémentation en vitamine A, dont certaines études ont montré qu'elle ralentissait le taux de détérioration de la rétine.[13]
- Cependant, une récente revue Cochrane n'a trouvé aucun avantage significatif pour la vitamine A pour la RP.[14] Lorsque des patients individuels sont supplémentés en vitamine A à forte dose, les tests de la fonction hépatique doivent être surveillés.
Ces dernières années, les causes génétiques de la RP ont été mieux comprises et de nouveaux traitements sont en cours de développement pour lutter contre la maladie. Les investigations spécifiques au gène ou à la mutation indiquent la possibilité que la thérapie d'augmentation génétique soit conçue pour restaurer l'expression génique normale dans les photorécepteurs. D'autres recherches impliquent une thérapie de remplacement cellulaire, qui implique la transplantation de cellules progénitrices rétiniennes (ou cellules souches non oculaires) dans l'œil, pour repeupler la rétine avec des photorécepteurs fonctionnels.
Il existe de nombreux types d'implants rétiniens électroniques qui se sont révélés très prometteurs pour restaurer une vision partielle chez les patients atteints d'une maladie en phase terminale. Une sorte de technologie qui a été intéressante utilise les informations auditives pour se substituer à l'entrée sensorielle visuelle.[15] Bien que ces voies soient très prometteuses pour la restauration et la préservation de la vision, il existe des problèmes complexes pour la gestion de la réadaptation de ces patients, ainsi que des défis spécifiques au dispositif, tels que la longévité fonctionnelle.[1][3]
Pronostic
Le pronostic des patients atteints de rétinite pigmentaire dépend de l'âge d'apparition et du mode de transmission.
Des symptômes d'apparition précoce et une perte de vision sévère et une cécité nocturne sont attendus avec la forme autosomique récessive de la RP.
L'expression autosomique dominante est la moins sévère et associée à l'apparition plus progressive des symptômes plus tard dans la vie adulte.
La perte de vision la plus grave survient avec la RP récessive liée à l'X.
La vision en tunnel est attendue vers la fin de toutes les formes de RP, et presque tous les patients RP seront légalement aveugles à un moment donné de la progression de leur maladie. La perte totale de vision est heureusement rare, car la fonction maculaire permet généralement une perception de la lumière, même après perte d'acuité.[3]
Références
- ↑ 1,0 1,1 1,2 1,3 1,4 et 1,5 Sanne K. Verbakel, Ramon A. C. van Huet, Camiel J. F. Boon et Anneke I. den Hollander, « Non-syndromic retinitis pigmentosa », Progress in Retinal and Eye Research, vol. 66, , p. 157–186 (ISSN 1873-1635, PMID 29597005, DOI 10.1016/j.preteyeres.2018.03.005, lire en ligne)
- ↑ Uwe Wolfrum et Kerstin Nagel-Wolfrum, « [The Usher Syndrome, a Human Ciliopathy] », Klinische Monatsblatter Fur Augenheilkunde, vol. 235, no 3, , p. 273–280 (ISSN 1439-3999, PMID 29534264, DOI 10.1055/a-0573-9431, lire en ligne)
- ↑ 3,0 3,1 3,2 3,3 3,4 3,5 3,6 3,7 et 3,8 Teri B. O'Neal et Euil E. Luther, StatPearls, StatPearls Publishing, (PMID 30137803, lire en ligne)
- ↑ Yi Jing Yang, Jun Peng, Deng Ying et Qing Hua Peng, « A Brief Review on the Pathological Role of Decreased Blood Flow Affected in Retinitis Pigmentosa », Journal of Ophthalmology, vol. 2018, , p. 3249064 (ISSN 2090-004X, PMID 29682340, Central PMCID 5845519, DOI 10.1155/2018/3249064, lire en ligne)
- ↑ Heping Xu, Mei Chen et John V. Forrester, « Para-inflammation in the aging retina », Progress in Retinal and Eye Research, vol. 28, no 5, , p. 348–368 (ISSN 1873-1635, PMID 19560552, DOI 10.1016/j.preteyeres.2009.06.001, lire en ligne)
- ↑ Artur V. Cideciyan, Samuel G. Jacobson, Tomas S. Aleman et Danian Gu, « In vivo dynamics of retinal injury and repair in the rhodopsin mutant dog model of human retinitis pigmentosa », Proceedings of the National Academy of Sciences of the United States of America, vol. 102, no 14, , p. 5233–5238 (ISSN 0027-8424, PMID 15784735, DOI 10.1073/pnas.0408892102, lire en ligne)
- ↑ Jose L. Badano, Norimasa Mitsuma, Phil L. Beales et Nicholas Katsanis, « The ciliopathies: an emerging class of human genetic disorders », Annual Review of Genomics and Human Genetics, vol. 7, , p. 125–148 (ISSN 1527-8204, PMID 16722803, DOI 10.1146/annurev.genom.7.080505.115610, lire en ligne)
- ↑ Max Andresen H, Tomás Regueira H et Federico Leighton, « [Oxidative stress in critically ill patients] », Revista Medica De Chile, vol. 134, no 5, , p. 649–656 (ISSN 0034-9887, PMID 16802059, DOI 10.4067/s0034-98872006000500015, lire en ligne)
- ↑ Kelly Shintani, Diana L. Shechtman et Andrew S. Gurwood, « Review and update: current treatment trends for patients with retinitis pigmentosa », Optometry (St. Louis, Mo.), vol. 80, no 7, , p. 384–401 (ISSN 1558-1527, PMID 19545852, DOI 10.1016/j.optm.2008.01.026, lire en ligne)
- ↑ Elodie Dessalces, Béatrice Bocquet, Jérôme Bourien et Xavier Zanlonghi, « Early-onset foveal involvement in retinitis punctata albescens with mutations in RLBP1 », JAMA ophthalmology, vol. 131, no 10, , p. 1314–1323 (ISSN 2168-6173, PMID 23929416, DOI 10.1001/jamaophthalmol.2013.4476, lire en ligne)
- ↑ Kentaro Kurata, Katsuhiro Hosono et Yoshihiro Hotta, « Long-Term Clinical Course in a Patient with Complete Congenital Stationary Night Blindness », Case Reports in Ophthalmology, vol. 8, no 1, , p. 237–244 (ISSN 1663-2699, PMID 28512427, Central PMCID 5422747, DOI 10.1159/000462961, lire en ligne)
- ↑ Christina Zeitz, Christoph Friedburg, Markus N. Preising et Birgit Lorenz, « [Overview of Congenital Stationary Night Blindness with Predominantly Normal Fundus Appearance] », Klinische Monatsblatter Fur Augenheilkunde, vol. 235, no 3, , p. 281–289 (ISSN 1439-3999, PMID 29390235, DOI 10.1055/s-0043-123072, lire en ligne)
- ↑ Kelly Shintani, Diana L. Shechtman et Andrew S. Gurwood, « Review and update: current treatment trends for patients with retinitis pigmentosa », Optometry (St. Louis, Mo.), vol. 80, no 7, , p. 384–401 (ISSN 1558-1527, PMID 19545852, DOI 10.1016/j.optm.2008.01.026, lire en ligne)
- ↑ Sobharani Rayapudi, Stephen G. Schwartz, Xue Wang et Pamela Chavis, « Vitamin A and fish oils for retinitis pigmentosa », The Cochrane Database of Systematic Reviews, no 12, , CD008428 (ISSN 1469-493X, PMID 24357340, Central PMCID 4259575, DOI 10.1002/14651858.CD008428.pub2, lire en ligne)
- ↑ Jamie Ward et Peter Meijer, « Visual experiences in the blind induced by an auditory sensory substitution device », Consciousness and Cognition, vol. 19, no 1, , p. 492–500 (ISSN 1090-2376, PMID 19955003, DOI 10.1016/j.concog.2009.10.006, lire en ligne)
