Pneumonie chez l'enfant et le nourrisson
| Classe de maladie | |||
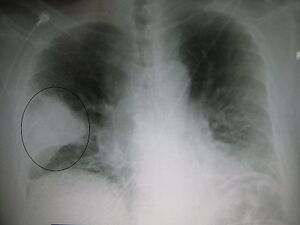 Radiographie de face d'un patient ayant une pneumonie du lobe moyen droit | |||
| Caractéristiques | |||
|---|---|---|---|
| Signes | Agitation, Apnée, Bronchophonie , Tirage , Tachypnée , Battement des ailes du nez, Râles, Crépitements, Matité, Altération de l'état de conscience , ... [+] | ||
| Symptômes |
Douleurs abdominales, Incapacité à tolérer les aliments, Douleurs pleurétiques, Douleurs cervicales, Toux | ||
| Étiologies |
Staphylococcus aureus, Cytomégalovirus, Haemophilus influenzae, Chlamydia trachomatis, Coqueluche, Streptocoque du groupe B, Mycoplasma pneumoniae, E. coli, Mycobacterium tuberculosis, Adénovirus, ... [+] | ||
| Informations | |||
| Terme anglais | Pneumonie pédiatrique | ||
| |||
La pneumonie se réfère à toute inflammation de la plèvre viscérale, du tissu conjonctif, des voies respiratoires, des alvéoles et des structures vasculaires entourant les poumons[1], associée à une consolidation de l'espace alvéolaire. Elle est causé par un pathogène microbien, en général bactérien, mais peut être causée par un organisme viral ou fongique également.
Épidémiologie
À l'échelle mondiale, la pneumonie est l'une des principales causes de morbidité et de mortalité chez les enfants de moins de cinq ans.[2] Bien que la majorité des décès attribuables à la pneumonie chez les enfants surviennent principalement dans les pays en voie de développement, le fardeau de la maladie est considérable dans les pays développés, considérant les coûts associés aux soins de santé liés à la pneumonie. [3][4] On estime à 120 millions le nombre de cas de pneumonie par an dans le monde entraînant jusqu'à 1,3 millions de décès.[5] Les jeunes enfants de moins de deux ans dans le monde en développement représentent près de 80 % des décès pédiatriques consécutifs à la pneumonie. [6] Le pronostic de la pneumonie est meilleur dans le monde développé, avec un nombre moindre de décès mais le fardeau de la maladie est extrême. Ceci s'explique par environ 2,5 millions de cas par an. Environ le tiers à la moitié de ces cas conduisent à des hospitalisations.[7][4] Bien que les pneumonies virales et bactériennes se produisent tout au long de l'année, elles sont plus fréquentes pendant les mois d'hiver. L'introduction du vaccin antipneumococcique a considérablement réduit le risque de pneumonie [4], d'autant plus que la vaccination antipneumococcique réduit également le risque de pneumonie virale[1].
Maladies
Les étiologies de pneumonies sont nombreuses, il est noté que les agents responsables varient
| Pneumonie | Description |
|---|---|
| Pneumonie communautaire |
|
| Pneumonie d'inhalation | Lorsqu'un terrain propice à l'aspiration existe, la pneumonie peut être due à une colonisation par une flore buccale anaérobie[1]:
Les facteurs de risque d'inhalation comprennent des antécédents de convulsions, d'anesthésie ou d'un épisode de baisse du niveau de conscience, de maladie neurologique, de dysphagie, de reflux gastro-œsophagien, d'utilisation d'une sonde nasogastrique ou encore d'aspiration d'un corps étranger. |
| Pneumonie nosocomiale | Survient souvent dans les unités de soins intensifs où la ventilation mécanique, les cathéters à demeure et l'administration d'antibiotiques à large spectre sont courants. À noter qu'il est admis d’exclure les infections maternofœtales survenant dans les 48 premières heures de vie. [16] |
| Population spéciale |
|
Étiologies
Les étiologies de pneumonies sont nombreuses. Il est à noter que les agents responsables varient selon l'âge et le milieu dans lequel l'infection a été contractée. Les virus sont les pathogènes les plus fréquemment rencontrés au cours des deux premières années de vie (virus respiratoire syncytial, influenza, métapneumovirus humain, virus para influenza, adénovirus, coronavirus). [21]
| Bactérie | Bactérie atypique | Virus | |
|---|---|---|---|
| Nouveau-né |
| ||
| 1 à 3 mois |
|
| |
| 3 mois à 5 ans |
|
| |
| > 5 ans |
|
|
|
Physiopathologie
La pneumonie est une invasion des voies respiratoires inférieures, sous le larynx, par des agents pathogènes qui pénètrent le corps par inhalation, par aspiration, par invasion de l'épithélium respiratoire ou par propagation hématogène.[23] Elle survient lorsqu'il y a altération des défenses immunitaires. Cependant, il existe des barrières à l'infection qui comprennent des structures anatomiques (poils nasaux, les cornets, l'épiglotte, cils), et une immunité humorale et cellulaire.[23] Une fois ces barrières franchies, l'infection, transmise soit par propagation de gouttelettes (principalement infection virale), soit par colonisation du nasopharynx (principalement infection bactérienne), entraîne une inflammation et des blessures ou la mort de l'épithélium et des alvéoles environnants. Ceci s'accompagne finalement d'une migration des cellules inflammatoires vers le site de l'infection, provoquant un processus exsudatif qui à son tour altère l'oxygénation,[24] puis les espaces aériens des voies respiratoires se remplissent de globules blancs. Cette évolution diminue la compliance pulmonaire, bloquant les voies respiratoires et entraînant ainsi un piégeage aérien et une altération de la ventilation-perfusion. Dans le cas d'une infection sévère, une nécrose épithéliale bronchique, bronchiolaire et parenchymateuse est observée[1].
Il est important de souligner que même si plusieurs organismes peuvent causer une pneumonie, dans la majorité des cas, le microbe n'est pas identifié, et l'étiologie virale est la plus fréquente. [4]
Cinq modèles de pneumonie existent, notamment[1]:
- Pneumonie lobaire : implique un seul lobe (ébauche habituelle du S. pneumoniae) et comporte quatre stades :
- 1. La première étape survient dans les 24 heures et se caractérise par un œdème alvéolaire et une congestion vasculaire. Des bactéries et des neutrophiles sont présents.[4]
- 2. À la deuxième étape, l'hépatisation rouge, le lobe prend une consistance semblable à celle du foie. Ce stade est caractérisé par la présence de neutrophiles, de globules rouges et de cellules épithéliales desquamées. Les dépôts de fibrine dans les alvéoles sont fréquents.[4]
- 3. Le troisième stade, l'hépatisation grise, survient 2 à 3 jours plus tard et le poumon apparaît brun foncé. Il y a une accumulation d'hémosidérine et une hémolyse des globules rouges. [4]
- 4. La quatrième étape est l'étape de résolution, où les infiltrats cellulosiques sont résorbés et l'architecture pulmonaire est restaurée. Un processus de guérison qui n'est pas optimal pourrait entraîner l'apparition d'épanchements parapneumoniques et d'adhérences pleurales.[4]
- Bronchopneumonie : atteinte primaire des voies respiratoires et du tissu interstitiel environnant, souvent observée dans les pneumonies à Streptococcus pyogenes et Staphylococcus aureus).
- Pneumonie nécrosante : retrouvée dans la pneumonie d'inhalation (PI); la physiopathologie de la PI dépend de la nature du liquide inhalé. Retrouvée aussi dans les causes infectieuses telles que S.pneumoniae, S. pyogenes et S. aureus.
- Granulome caséeux (pneumonie tuberculeuse ou caséeuse)
- Pneumonie interstitielle et péribronchiolaire avec infiltration secondaire du parenchyme (lorsqu'une pneumonie virale sévère est compliquée d'une pneumonie bactérienne).
En ce qui concerne le schéma pathologique dans la pneumonie, on peut dire qu'il est subdivisé en deux : la pneumonie interstitielle ou l'atteinte parenchymateuse[1].
Présentation clinique
La présentation clinique de la pneumonie infantile varie selon l'agent pathogène responsable et le lieu de l'infection (communautaire vs nosocomiale).
Facteurs de risque
En général, de nombreux facteurs de risque peuvent non seulement contribuer à l'apparition d'une pneumonie, mais ils peuvent également aggraver l'état du patient. Parmi ceux-ci on retrouve[1]:
- la dysplasie bronchopulmonaire
- la fibrose kystique
- l'asthme
- la drépanocytose
- les troubles neuromusculaires, en particulier ceux associés à une conscience dépressive
- certains troubles gastro-intestinaux (par exemple, un reflux gastro-œsophagien, une fistule trachéo-œsophagienne)
- le trouble d'immunodéficience congénitale
- le trouble d'immunodéficience acquise
- la fumée du tabac (fumée secondaire pour les enfants en bas âge, tabagisme chez l'adolescent)
- l'absence de vaccination antipneumococcique.
Les facteurs de risque de la pneumonie d'inhalation[25]:
- un retard à la vidange gastrique
- un traumatisme
- un spasme du pylore
- un iléus
- des médicaments ralentisseurs du transit (morphiniques, sédatifs)
- une hypersécrétion gastrique
- une douleur
- un reflux gastro-œsophagien
- une hernie hiatale
- un surplus de poids: obésité
- une neuropathie diabétique avec dysautonomie
- des facteurs laryngés
- une intubation endotrachéale en pré-hospitalier
- une anesthésie générale
- une chirurgie urgente
- un traumatisme crânien
- une atteinte neuromusculaire
- une sclérose en plaque
- une guillain-Barré
- une paralysie des nerfs crâniens
- une dystrophie musculaire
Les facteurs de risque de résistance du Streptococcus pneumoniae :
- la fréquentation de la garderie
- l'âge : enfants âgés de < 2 ans
- une hospitalisation récente
- une traitement antibiotique récent (< 30 jours)
Questionnaire
Dans de nombreux cas, les plaintes associées à la pneumonie ne sont pas spécifiques et comprennent les symptômes suivants : [26]
- la toux
- la fièvre
- la tachypnée
- les difficultés respiratoires.
En effet, il n'existe aucun signe pathognomonique de pneumonie et les signes cliniques diffèrent selon l'âge de l'enfant[27] .
Par exemple, les nouveau-nés et les nourrissons peuvent ne présenter qu'une simple fièvre et une augmentation des leucocytes[28]. Ils peuvent également présenter les symptômes qui suivent plutôt qu'une toux :
- une incapacité à tolérer les aliments
- des grognements
- une apnée
- une agitation.
Chez l'enfant plus âgé ou l'adolescent, il est commun d'avoir :[28]
- des douleurs pleurétiques
- des douleurs abdominales : peut aussi représenter un signe classique de pneumonie [21]
- des douleurs cervicales (douleur référée).
Cependant, la combinaison de symptômes, y compris la fièvre, la tachypnée, les crépitements focaux et la diminution des bruits respiratoires, augmente la sensibilité pour détecter une pneumonie sur les radiographies pulmonaires.[27]
La pneumonie est un diagnostic clinique qui doit prendre en compte les antécédents de la maladie actuelle, les résultats de l'examen physique et les résultats des tests complémentaires ainsi que des examens d'imagerie. [4]
Les antécédents importants à obtenir comprennent :[29][4]
- la durée des symptômes
- les expositions
- les voyages
- les contacts avec des personnes malades
- l'état de santé de base de l'enfant, les maladies chroniques, les symptômes récurrents
- les antécédents de vaccination
- la santé maternelle ou les complications à la naissance chez les nouveau-nés.
| Paramètre | Signification |
|---|---|
| Âge | Peut orienter vers une étiologie virale (âge préscolaire) ou bactérienne (enfants plus âgés). |
| Durée des symptômes | Une toux chronique de plus de 4 semaines oriente vers une autre étiologie. |
| État nutritionnel | Un nourisson qui refuse de manger ou de boire. |
| Vaccination | La vaccination n'élimine pas une infection pulmonaire. |
| Prise d'antibiotiques | Peut changer l'administration de certaines molécules. Augmente la résistance. |
| Exposition à la tuberculose | Peut orienter vers une origine tuberculeuse dans certaines populations (nouveaux immigrants, population autochtone, voyage en pays endémique). |
| Contact avec des sujets malades
*Penser au SRAS-COV2 (COVID19) |
Chercher un contact récent, notamment en garderie, lors d'un séjour aux urgences ou d'un voyage outre-mer. |
| Antécédents personnels | Chercher les signes d'une autre pathologie ou de facteurs de risque : trouble neuromusculaire, obésité. |
| Récurrence des épisodes[28] | Peut orienter vers une aspiration, une anomalie anatomique congénitale, une fibrose kystique, une immunodéficience, de l'asthme, un corps étranger oublié. |
Examen clinique
Comme cité ci-haut, les symptômes de pneumonie peuvent être non spécifiques, surtout chez les nourrissons et les enfants plus jeunes. D’ordinaire, les enfants souffrent de fièvre et de tachypnée.
L'examen physique doit inclure l'observation des signes de détresse respiratoire, y compris [26]:
- la tachypnée
- les battement des ailes du nez
- le tirage sus-sternal, sous costal
- la respiration paradoxale
- l'hypoxie à l'air ambiant : la cyanose ne sera évidente qu’en cas d’hypoxémie très marquée. Une saturation en oxygène normale n’exclut pas la pneumonie, surtout au début de l’évolution de la maladie[30].
L'examen pulmonaire avec l'auscultation des crépitants ou des ronchi dans tous les champs pulmonaires avec le stéthoscope de taille appropriée peut également aider au diagnostic.
| Examen | Signification |
|---|---|
| Aspect général | |
| Rechercher une cyanose et une altération de l'état de conscience qui sont des signes de gravité. Une altération de l'état mental est un signe d'hypoxie. | |
| Signes vitaux | |
| Fièvre | Peut être le seul signe de pneumonie, la pyrexie est non spécifique à la pneumonie. |
| Tachypnée | Sa définition change selon l'âge du patient[31][note 1]:
|
| Hypoxémie | Prédictive de pneumonie |
| Signes de détresse respiratoire | |
| Tirage | |
| Battement des ailes du nez | |
| Geignement | Signe de gravité |
| Usage des muscles accessoires | Signe de gravité |
| examen pulmonaire | |
| Toux | Non spécifique |
| Auscultation | Les crépitements (râles, crépitations), diminution des bruits respiratoires, bruits respiratoires bronchiques, égophonie et bronchophonie sont évocateurs de pneumonie. |
| Frémissement | Penser à une consolidation du parenchyme |
| Matité | Penser à une consolidation du parenchyme ou épanchement pleural |
Il est primordial d'évaluer la gravité de l'état du patient afin de déterminer la nécessité de bilans paracliniques (sanguins ou radiologiques) ainsi que pour guider la thérapeutique. Pour ce, plusieurs paramètres sont pris en compte, notamment[28]:
- une température supérieure à 38,5 °C
- une fréquence respiratoire supérieure à 70/minute et supérieure à 50/minute pour les enfants plus âgés
- des rétractions sus-sternales, intercostales et sous-costales chez l'enfant de moins d'un an
- des difficultés respiratoires sévères
- des geignements
- des battement des ailes du nez
- une apnée
- une dyspnée importante
- une cyanose
- une altération de l'état de conscience
- une saturation en oxygène inférieure à 90 %
- une refus d'alimentation
- une tachycardie
- un temps de recoloration capillaire supérieur ou égal à deux secondes.
Pour préciser les possibilités dans la pneumopathie d'inhalation, il est nécessaire de mettre l'accent sur le fait que plusieurs tableaux existent allant de l’inhalation asymptomatique aux signes majeurs de défaillance respiratoire avec syndrome de détresse respiratoire aiguë (SDRA). Dans les formes symptomatiques, deux situations cliniques sont possibles :
- soit l’inhalation est manifeste : détresse respiratoire au décours de vomissements et/ou constatation de liquide gastrique dans l’oropharynx
- soit elle peut simplement être suspectée devant l'existence de facteurs de risque (cités ci-haut) comme la toux, la dyspnée, le wheezing. L’auscultation trouvera des râles sibilants et/ou des râles crépitants. Au cours des inhalations acides, la fièvre est souvent peu élevée initialement. Lors des inhalations périopératoires, la symptomatologie est qualifiée de majeure dans 30 % des cas[25].
Examens paracliniques
Les analyses de laboratoire chez les enfants soupçonnés d'avoir une pneumonie devrait idéalement commencer par des tests non invasifs et rapides au chevet du patient, y compris :
- Des tests sur écouvillon nasopharyngé pour la grippe, le virus respiratoire syncytial et le métapneumovirus humain lorsque disponibles et appropriés, afin de minimiser l'utilisation d'examens d'imagerie et de traitement antibiotique qui sont inutiles chez les enfants atteints de grippe ou de bronchiolite.
Les enfants qui présentent une maladie grave et qui semblent toxiques doivent subir les tests suivant :
- une formule sanguine complète
- une évaluation des électrolytes
- une évaluation des fonction rénale et hépatique
- des hémocultures[32].
Ces tests ne sont généralement pas nécessaires chez les enfants qui présentent une maladie bénigne. Les marqueurs inflammatoires n'aident pas à faire la distinction entre la pneumonie virale et bactérienne dans la population pédiatrique[32][33]. Cependant, ces tests peuvent être obtenus pour orienter la progression de la maladie et servir d'indicateurs pronostiques. Chez les enfants qui ont séjourné dans des régions où la tuberculose est endémique ou qui ont des antécédents d'exposition et qui présentent des signes et symptômes suspects de pneumonie, on doit obtenir :
- des échantillons de crachats
- des aspirations gastriques pour culture.
La coloration et la culture des expectorations ne sont pas utiles car les échantillons sont souvent contaminés par la flore buccale. Les hémocultures peuvent être effectuées mais sont souvent négatives. Aujourd'hui, la sérologie est utilisée pour déterminer la présence d'espèces de mycoplasmes, de légionelles et de chlamydia. La PCR est de plus en plus disponible dans la plupart des hôpitaux, mais le délai pour obtenir les résultats est tout de même de 24 à 48 heures.[4] Les patients ayant un contact infectieux faisant penser à la COVID-19, nécessitent également un diagnostic par PCR.
Il n'y a pas de directives claires pour l'utilisation systématique de la radiographie pulmonaire dans la population pédiatrique[32]. Bien que la radiographie pulmonaire puisse être utile dans le diagnostic et la confirmation de la pneumonie, [34] elle comporte des risques[note 2].
L'imagerie doit être limitée :
- aux enfants qui semblent toxiques
- à une maladie récurrente ou prolongée malgré le traitement
- aux nourrissons âgés de 0 à 3 mois présentant de la fièvre
- à une suspicion d'aspiration de corps étranger ou d'une malformation pulmonaire congénitale
- aux enfants de moins de 5 ans présentant de la fièvre, une leucocytose et aucune source d'infection identifiable[34]
- à une aggravation aiguë des infections des voies respiratoires supérieures ou pour écarter une masse sous-jacente chez les enfants [35][36][4].
Certaines caractéristiques radiographiques sont plutôt associées à certains pathogènes, mais ceci n'est pas pathognomonique. Ce tableau résume les grandes étiologies et leurs aspects radiologiques[28]:
| Etiologie | Aspect radiologique |
|---|---|
| Bactérienne ( S. Pneumoniae ) |
|
| Bactérienne atypique
(Mycoplasma pneumoniae) |
|
| Viral | Infiltrats interstitiels |
| Tuberculose (Mycobactérium Tuberculosis) | Adénopathie médiastinale ou hilaire. |
| Par inhalation |
|
Approche clinique
Au total, il faut penser à la pneumonie chez les enfants présentant une fièvre, une toux, des signes de détresse respiratoire. Le diagnostic pouvant être posé cliniquement, l'usage des bilans paracliniques est codifié (voir section bilans paracliniques).
Une fois le diagnostic posé, la prochaine étape est d'évaluer la nécessité d'une hospitalisation. Pour ce faire, plusieurs critères entrent en jeu, notamment: l'âge, la présence de tares, les maladies sous-jacente, etc. En général, l'hospitalisation est justifiée pour les enfants de moins de 3 mois. Sinon, il faut guetter les signes suivant afin de décider de l'hospitalisation de l'enfant[37]:
- une hypoxémie [SpO2 ] < 90 % à l'air ambiant
- une déshydratation ou une incapacité à boire ou à manger
- une détresse respiratoire modérée à sévère : fréquence respiratoire > 70 respirations/minute pour les nourrissons de moins de 12 mois et > 50 pour les enfants plus âgés
- une apparence toxique
- des conditions sous-jacentes pouvant prédisposer à une évolution plus grave de la pneumonie
- des complications (voir section complications)
- une suspicion ou confirmation que la PAC est due à un agent pathogène à virulence accrue, comme Staphylococcus aureus ou Streptococcus du groupe A (SGA)
- un échec du traitement ambulatoire (aggravation ou absence de réponse en 48 à 72 heures)[37]
- une douleur abdominale peut aussi représenter un signe classique de pneumonie[38].
Diagnostic différentiel
Le diagnostic différentiel de pneumonie peut se faire devant les différents tableaux cliniques et symptômes[4][28], ces diagnostic sont faciles à distinguer lors de l'anamnèse ou examen physique:
- une sténose aortique
- un syndrome d'aspiration (inhalation)
- l'asthme
- une atélectasie
- un défaut septal AV complet
- une bactériémie
- un traumatisme à la naissance
- un corps étranger
- une bronchiolite
- une insuffisance cardiaque
- une acidose métabolique
Traitement
Le traitement doit cibler l'agent pathogène suspecté d'être en cause, selon les informations recueillies à partir des antécédents et de l'examen physique. Une prise en charge symptomatique et de soutien est essentielle et comprend un supplément d'oxygène pour l'hypoxie, des antipyrétiques pour la fièvre et des liquides pour la déshydratation. Ceci est particulièrement important dans les cas de pneumopathie non infectieuse et de pneumonie virale pour lesquelles les antibiotiques ne sont pas indiqués. [26][39] Les antitussifs ne sont pas recommandés.[4]
Les nouveau-nés et les nourrissons de moins de 90 jours doivent être hospitalisés pour traitement, de même que les enfants immunodéprimés ou atteints d'autres maladies chroniques sous-jacentes comme la drépanocytose ou la fibrose kystique.[26] Les enfants n'ayant pas accès aux soins en raison de facteurs sociaux, ayant échoué au traitement ambulatoire ou ayant une tuberculose présumée doivent également être hospitalisé.[40][4]
En cas de suspicion de pneumonie bactérienne, traiter empiriquement avec des antibiotiques, en gardant à l'esprit les antécédents significatifs et les agents pathogènes bactériens communs à des groupes d'âge spécifiques.
Critères d'hospitalisation
La plupart des enfants atteints d’une pneumonie peuvent être soignés dans un cadre ambulatoire. Il n’y a pas de critères d’hospitalisation propre à la population d’âge pédiatrique. En général, l’hospitalisation est indiquée si l'enfant : [41][21][4]
- Est âgé de moins de 3 à 6 mois : le seuil d’hospitalisation devrait être plus faible pour les nourrissons de moins de six mois qui peuvent requérir davantage de soins de soutien et de surveillance et chez qui il peut être difficile de constater une détérioration clinique subtile.
- A une incapacité a s’alimenter.
- Ne peut tolérer un traitement par voie orale.
- Souffre de vomissements.
- Présente un état général altéré : enfant toxique ou léthargique.
- Est en déshydratation.
- Présente une détresse respiratoire (par exemple, geignement expiratoire, battement des ailes du nez, apnée, hypoxémie).
- A besoin d'oxygène.
- A une maladie cardiaque ou pulmonaire sous-jacente.
- A une immunodéficience.
- A une pneumonie compliquée (épanchement, empyème, abcès, etc.).
- Est dans un contexte épidémiologique de pathogène virulent ou multirésistant.
- Ne répond pas à une antibiothérapie orale : en cas de fièvre qui persiste plus de 48 à 72 heures après le début du traitement ou de détérioration clinique, réévaluer le patient et répéter la radiographie pour rechercher les complications qui demanderaient une hospitalisation [21].
- Est dans un contexte familiale où la faible participation parentale ne permet pas d’assurer l’adhésion au traitement.
Traitement ciblé
- Chez l’enfant en bon état général ayant une présentation clinique et un examen d'imagerie (le cas échéant) suggérant une infection virale : [21]
- Offrir un traitement de soutien.
- Il n'y a aucune indication justifiant la prise d’antibiotique.
- Il faut envisager de prescrire des antiviraux si une influenza est présumée ou démontrée et que l’enfant présente des facteurs de risque de maladie grave ou a besoin d’être hospitalisé, notamment si les symptômes ont fait leur apparition depuis moins de 48 heures[42].
- Si pneumonie bactérienne présumée ou pathogènes spéciaux, la prise en charge dépend de l'âge et du pathogène suspecté.
| Population d'âge ciblée | Traitement | Précision |
|---|---|---|
| Nouveau né | ||
| Ampicilline + aminoside
ou |
| |
| 1-3 mois | ||
| S. pneumoniae | Cefuroxime OU ampicilline | Si pneumonie atypique chez nourrisson de 1-3 mois, ajouter une couverture supplémentaire avec l'érythromycine ou la clarythromycine [26][43][4]. |
| 3 mois-5 ans | ||
| Amoxicilline (si modéré) OU ampicilline OU
cefuroxime |
||
| > 5 ans | ||
| Erythromycine OU clarithromycine (première intention) | Alternative : ampicillin OU cefuroxime | |
| Population spéciale | ||
| drépanocytose | Céfotaxime | Surtout quand l'état est grave. |
| Fibrose kystique | Pipéracilline | |
| VIH + | Sulfaméthoxazole/triméthoprime et prednisone
Si infection au cytomégalovirus : le ganciclovir et la gammaglobuline sont les agents préférés. |
|
| Agents pathogènes spéciaux | ||
| Varicelle | Acyclovir | |
| VRS | Ribavirine si patient à haut risque | |
| Staphylococcus aerus méthiciline-résistant | Clindamycine
Vancomycine[4] |
|
| Pneumonie d'inhalation[37] |
| |
Prise en charge de la pneumonie sévère
| Pneumonie qui necessite les soins intensifs[44][37] |
|---|
| Un seul de ces critères est nécessaire : |
| Patient a besoin d'une assistance ventilatoire qui n'est disponible qu'aux soins intensifs : ventilation mécanique, ventilation à pression positive non invasive, incapacité à maintenir SpO 2 > 92 %. |
| Signes d'insuffisance respiratoire imminente (léthargie, augmentation du travail respiratoire, épuisement avec ou sans hypercapnie) |
| Apnée récurrente ou respirations lentes et irrégulières |
| Compromis cardiovasculaire avec tachycardie progressive et/ou hypotension ne répondant pas au remplissage |
| Minimum deux de ces critères : |
| Fréquence respiratoire > 70 respirations/minute pour les nourrissons de < 12 mois et > 50 respirations/min pour les plus âgés |
| Apnée |
| Augmentation du travail respiratoire (rétractions, dyspnée, évasement nasal, grognements) |
| Pression partielle d'oxygène dans le sang artériel (PaO 2 ) : rapport FiO 2 < 250 |
| Infiltrats multilobaires |
| État mental altéré |
| Hypotension |
| Épanchement pleural |
| État comorbide (drépanocytose, déficit immunitaire, immunosuppression) |
| Acidose métabolique inexpliquée |
| Score d'alerte précoce pédiatrique > 6 |
| Pneumonie compliquée[37][45] |
| Épanchement parapneumonique/empyème : ceux qui sont simples doivent être traités par drainage et antibiotiques. Les épanchements compliqués sont traités par fibrinolyse et drainage par sonde thoracique, ou drainage chirurgical[46]. |
| Pneumonie nécrosante: traitement antibiotique prolongé. La décision de prolonger le traitement est basée sur la réponse clinique, mais en général un total de 4 ou 2 semaines après l'apyrexie. Une prudence est de mise face aux procédures d'intervention (pose d'un cathéter de drainage percutané) puisqu'elles augmentent le risque de complications. |
| Abcès pulmonaire: antibiothérapie prolongée. Si le patient est réfractaire au traitement antibiotique, une aspiration ou un drainage percutané est de mise (si l'état ne s'améliore pas ou s'aggrave après 72 heures d'antibiotiques). |
| Pneumatocèle: souvent la résolution est spontanée. Il est probable qu'une décompensation en pneumothorax survienne. |
Au Canada, la pneumonie non compliquée est traitée pendant sept à dix jours (cinq jours si on prescrit de l’azithromycine). Si elle se complique d'un empyème ou la formation d’un abcès, le traitement sera plus long. Il est possible de changer la voie d'administration du traitement, par exemple, passer à la voie orale lorsque l'état clinique du patient s'est amélioré.
Si on détecte un virus dans le prélèvement nasopharyngé ou si la radiographie pulmonaire est plutôt évocatrice d'une étiologie virale, le traitement consistera à dispenser des soins de soutien (oxygène et réhydratation, au besoin), sans prescrire d’antibiotiques.
| Patients instables | |
|---|---|
| En cas d'insuffisance respiratoire aigue : |
|
| En cas d'hypotension artérielle : | |
| En cas d'agitation ou d'altération de la conscience : |
|
Suivi
La surveillance paraclinique se fait en cas de pneumonie nécessitant l'hospitalisation et elle comprend[47]:
- une formule sanguine complète (FSC) au minimum toutes les 24 heures
- une évaluation de l'hémostase toutes les 24 heures (n'est pas indispensable si absence de choc ou signe de défaillance multiviscérale)
- une analyse des gaz du sang au moins toutes les 8heures
- un dosage de la protéine C réactive (CRP)
- des prélèvements respiratoires de contrôle : attendre un minimum de 48 heure après le début du traitement
- une radiographie thoracique au moins tous les jours : chez les patients ayant une pneumonie grave, à la recherche de complications
- une échographie cardiaque : dans les formes les plus graves pour apprécier le remplissage des cavités droites et la présence d'une hypertension artérielle pulmonaire
- une échographie thoracique : permet de rechercher un épanchement pleural
- une tomodensitométrie (TDM) thoracique : peu d'indications en aigue, permet le diagnostic des complications
Complications
Il est important d'avoir un indice élevé de suspicion de complications, en particulier chez les patients venant pour une réévaluation. Pour les patients de retour à domicile avec une prise en charge symptomatique ou de soutien pour une pneumonie virale suspectée, envisager une infection bactérienne secondaire ou d'autres diagnostics lors de la réévaluation. [48] Les enfants atteints d'infections bactériennes non compliquées qui ne répondent pas au traitement dans les 72 heures doivent être évalués pour les complications, y compris[4][28]:
- un épanchement pleural (pleurésie)
- un abcès pulmonaire
- une pneumonie nécrosante
- un pneumatocèle
- un empyème
- un pneumothorax [49].
Les autres complications systémiques de la pneumonie comprennent :
- la septicémie[4]
- la déshydratation
- l'arthrite
- la méningite
- le syndrome hémolytique et urémique [4]
- l'hyponatrémie (chez les enfants sous CPAP)
Ces complications sont des indications majeures à l'hospitalisation.
Évolution
Pour la plupart des enfants, le pronostic est bon. Une amélioration clinique apparait en général dans les 48 heures en cas de pneumonie bactérienne. La pneumonie virale a tendance à disparaître sans traitement et le temps de guérison est généralement plus court. Si l'état du patient ne s'améliore pas dans les délais prévus, il est recommandé de répéter la radiographie pulmonaire dans le but de chercher d'éventuelles complications.
Les enfants atteints de tuberculose courent un risque élevé de progression de la maladie si celle-ci n'est pas traitée. Les enfants immunodéprimés ont le pire pronostic. Chaque année, environ 3 millions d'enfants meurent de pneumonie et la majorité de ces enfants souffrent également d'autres comorbidités comme une cardiopathie congénitale, une immunosuppression ou une maladie pulmonaire chronique. En ce qui a trait à la radiographie, les signes de résolution de la pneumonie peuvent prendre jusqu'à six semaines pour être démontrés; il n'est cependant pas recommandé de la refaire si l'état du patient s'améliore.
Notes
Références
- Cette page a été modifiée ou créée le 2020/11/29 à partir de Pediatric Pneumonia (StatPearls / Pediatric Pneumonia (2020/11/21)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/30725625 (livre).
- ↑ 1,00 1,01 1,02 1,03 1,04 1,05 1,06 1,07 1,08 1,09 1,10 et 1,11 « Pneumonie chez les enfants: épidémiologie, pathogenèse et étiologie », sur uptodate, (consulté le 30 novembre 2020)
- ↑ Geeta Rao Gupta, « Tackling pneumonia and diarrhoea: the deadliest diseases for the world's poorest children », Lancet (London, England), vol. 379, no 9832, , p. 2123–2124 (ISSN 1474-547X, PMID 22682449, DOI 10.1016/S0140-6736(12)60907-6, lire en ligne)
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/23826497
- ↑ 4,00 4,01 4,02 4,03 4,04 4,05 4,06 4,07 4,08 4,09 4,10 4,11 4,12 4,13 4,14 4,15 4,16 4,17 4,18 4,19 4,20 4,21 et 4,22 Chiemelie Ebeledike et Thaer Ahmad, StatPearls, StatPearls Publishing, (PMID 30725625, lire en ligne)
- ↑ Igor Rudan, Katherine L. O'Brien, Harish Nair et Li Liu, « Epidemiology and etiology of childhood pneumonia in 2010: estimates of incidence, severe morbidity, mortality, underlying risk factors and causative pathogens for 192 countries », Journal of Global Health, vol. 3, no 1, , p. 010401 (ISSN 2047-2978, PMID 23826505, Central PMCID 3700032, DOI 10.7189/jogh.03.010401, lire en ligne)
- ↑ M. Garenne, C. Ronsmans et H. Campbell, « The magnitude of mortality from acute respiratory infections in children under 5 years in developing countries », World Health Statistics Quarterly. Rapport Trimestriel De Statistiques Sanitaires Mondiales, vol. 45, no 2-3, , p. 180–191 (ISSN 0379-8070, PMID 1462653, lire en ligne)
- ↑ Stephen R. C. Howie et David R. Murdoch, « Global childhood pneumonia: the good news, the bad news, and the way ahead », The Lancet. Global Health, vol. 7, no 1, , e4–e5 (ISSN 2214-109X, PMID 30497987, DOI 10.1016/S2214-109X(18)30446-7, lire en ligne)
- ↑ Fizzah Arif, « Updated Recommendations Of Rcog On Prevention Of Early Onset Neonatal Group B Streptococcus Infection », Journal of Ayub Medical College, Abbottabad: JAMC, vol. 30, no 3, , p. 490 (ISSN 1819-2718, PMID 30465394, lire en ligne)
- ↑ Julie C. Chen, Sue Jenkins-Marsh, Vicki Flenady et Susan Ireland, « Early-onset group B streptococcal disease in a risk factor-based prevention setting: A 15-year population-based study », The Australian & New Zealand Journal of Obstetrics & Gynaecology, vol. 59, no 3, , p. 422–429 (ISSN 1479-828X, PMID 30203834, DOI 10.1111/ajo.12891, lire en ligne)
- ↑ Amal A. Al Hazzani, Reham A. B. Bawazeer et Afaf I. Shehata, « Epidemiological characterization of serotype group B Streptococci neonatal infections associated with interleukin-6 level as a sensitive parameter for the early diagnosis », Saudi Journal of Biological Sciences, vol. 25, no 7, , p. 1356–1364 (ISSN 1319-562X, PMID 30505181, Central PMCID 6252016, DOI 10.1016/j.sjbs.2015.10.015, lire en ligne)
- ↑ GBD 2016 Lower Respiratory Infections Collaborators, « Estimates of the global, regional, and national morbidity, mortality, and aetiologies of lower respiratory infections in 195 countries, 1990-2016: a systematic analysis for the Global Burden of Disease Study 2016 », The Lancet. Infectious Diseases, vol. 18, no 11, , p. 1191–1210 (ISSN 1474-4457, PMID 30243584, Central PMCID 6202443, DOI 10.1016/S1473-3099(18)30310-4, lire en ligne)
- ↑ S. B. Omer, A. Sutanto, H. Sarwo et M. Linehan, « Climatic, temporal, and geographic characteristics of respiratory syncytial virus disease in a tropical island population », Epidemiology and Infection, vol. 136, no 10, , p. 1319–1327 (ISSN 0950-2688, PMID 18177515, Central PMCID 2870725, DOI 10.1017/S0950268807000015, lire en ligne)
- ↑ Bradford D. Gessner, Agustinus Sutanto, Mary Linehan et I. Gusti Gede Djelantik, « Incidences of vaccine-preventable Haemophilus influenzae type b pneumonia and meningitis in Indonesian children: hamlet-randomised vaccine-probe trial », Lancet (London, England), vol. 365, no 9453, 2005 jan 1-7, p. 43–52 (ISSN 1474-547X, PMID 15643700, DOI 10.1016/s0140-6736(04)17664-2, lire en ligne)
- ↑ F. T. Cutts, S. M. A. Zaman, G. Enwere et S. Jaffar, « Efficacy of nine-valent pneumococcal conjugate vaccine against pneumonia and invasive pneumococcal disease in The Gambia: randomised, double-blind, placebo-controlled trial », Lancet (London, England), vol. 365, no 9465, 2005 mar 26-apr 1, p. 1139–1146 (ISSN 1474-547X, PMID 15794968, DOI 10.1016/S0140-6736(05)71876-6, lire en ligne)
- ↑ « Infection coquelucheuse chez les nourrissons et les enfants: caractéristiques cliniques et diagnostic », sur uptodate, (consulté le 30 novembre 2020)
- ↑ « Épidémiologie des infections nosocomiales en néonatalogie », sur uptodate, (consulté le 30 novembre 2020)
- ↑ S. Stagno, D. M. Brasfield, M. B. Brown et G. H. Cassell, « Infant pneumonitis associated with cytomegalovirus, Chlamydia, Pneumocystis, and Ureaplasma: a prospective study », Pediatrics, vol. 68, no 3, , p. 322–329 (ISSN 0031-4005, PMID 6269042, lire en ligne)
- ↑ « Coronavirus disease 2019 (COVID-19): Clinical manifestations and diagnosis in children », sur uptodate, (consulté le 30 novembre 2020)
- ↑ Kseniya Dryahina, Kristýna Sovová, Alexandr Nemec et Patrik Španěl, « Differentiation of pulmonary bacterial pathogens in cystic fibrosis by volatile metabolites emitted by their in vitro cultures: Pseudomonas aeruginosa, Staphylococcus aureus, Stenotrophomonas maltophilia and the Burkholderia cepacia complex », Journal of Breath Research, vol. 10, no 3, 08 10, 2016, p. 037102 (ISSN 1752-7163, PMID 27506232, DOI 10.1088/1752-7155/10/3/037102, lire en ligne)
- ↑ Arturo J. Martí-Carvajal et Lucieni O. Conterno, « Antibiotics for treating community-acquired pneumonia in people with sickle cell disease », The Cochrane Database of Systematic Reviews, vol. 11, 11 14, 2016, CD005598 (ISSN 1469-493X, PMID 27841444, Central PMCID 6530651, DOI 10.1002/14651858.CD005598.pub4, lire en ligne)
- ↑ 21,0 21,1 21,2 21,3 21,4 et 21,5 « PNEUMONIE ACQUISE EN COMMUNAUTÉ CHEZ L’ENFANT DE 3 MOIS ET PLUS », sur INESSS, (consulté le 12 août 2023)
- ↑ (en) Tina Binesh Marvasti; Sydney McQueen, toronto notes, Toronto, Ontario, Toronto Notes for Medical Students, , 1390 p.
- ↑ 23,0 et 23,1 José A. Bengoechea et Joana Sa Pessoa, « Klebsiella pneumoniae infection biology: living to counteract host defences », FEMS microbiology reviews, vol. 43, no 2, 03 01, 2019, p. 123–144 (ISSN 1574-6976, PMID 30452654, Central PMCID 6435446, DOI 10.1093/femsre/fuy043, lire en ligne)
- ↑ Heather J. Zar, « Bacterial and viral pneumonia: New insights from the Drakenstein Child Health Study », Paediatric Respiratory Reviews, vol. 24, , p. 8–10 (ISSN 1526-0550, PMID 28687247, DOI 10.1016/j.prrv.2017.06.009, lire en ligne)
- ↑ 25,0 et 25,1 (en) D. Chatellier, S. Chauvet et R. Robert, « Pneumopathies d’inhalation », Réanimation, vol. 18, no 4, , p. 328–333 (DOI 10.1016/j.reaurg.2009.03.008, lire en ligne)
- ↑ 26,0 26,1 26,2 26,3 26,4 et 26,5 T. Jadavji, B. Law, M. H. Lebel et W. A. Kennedy, « A practical guide for the diagnosis and treatment of pediatric pneumonia », CMAJ: Canadian Medical Association journal = journal de l'Association medicale canadienne, vol. 156, no 5, , S703–711 (ISSN 0820-3946, PMID 9068582, Central PMCID 1232848, lire en ligne)
- ↑ 27,0 et 27,1 Mark I. Neuman, Michael C. Monuteaux, Kevin J. Scully et Richard G. Bachur, « Prediction of pneumonia in a pediatric emergency department », Pediatrics, vol. 128, no 2, , p. 246–253 (ISSN 1098-4275, PMID 21746723, DOI 10.1542/peds.2010-3367, lire en ligne)
- ↑ 28,0 28,1 28,2 28,3 28,4 28,5 28,6 et 28,7 « Pneumonie communautaire chez les enfants: caractéristiques cliniques et diagnostic », sur uptodate, (consulté le 1er décembre 2020)
- ↑ M. Don, « Risk factors of paediatric community-acquired pneumonia », The European Respiratory Journal, vol. 37, no 3, , p. 724–725; author reply 725 (ISSN 1399-3003, PMID 21357931, DOI 10.1183/09031936.00164010, lire en ligne)
- ↑ « La pneumonie chez les enfants et adolescents canadiens en santé : des points de pratique pour la prise en charge », sur ncbi, (consulté le 1er décembre 2020)
- ↑ (en) « Copyright », Pediatric Pulmonology, , iv (DOI 10.1016/B978-0-323-01909-5.50002-5, lire en ligne)
- ↑ 32,0 32,1 et 32,2 Kenneth McIntosh, « Community-acquired pneumonia in children », The New England Journal of Medicine, vol. 346, no 6, , p. 429–437 (ISSN 1533-4406, PMID 11832532, DOI 10.1056/NEJMra011994, lire en ligne)
- ↑ H. Nohynek, E. Valkeila, M. Leinonen et J. Eskola, « Erythrocyte sedimentation rate, white blood cell count and serum C-reactive protein in assessing etiologic diagnosis of acute lower respiratory infections in children », The Pediatric Infectious Disease Journal, vol. 14, no 6, , p. 484–490 (ISSN 0891-3668, PMID 7667052, DOI 10.1097/00006454-199506000-00004, lire en ligne)
- ↑ 34,0 et 34,1 R. I. Markowitz et E. Ruchelli, « Pneumonia in infants and children: radiological-pathological correlation », Seminars in Roentgenology, vol. 33, no 2, , p. 151–162 (ISSN 0037-198X, PMID 9583110, DOI 10.1016/s0037-198x(98)80019-9, lire en ligne)
- ↑ Yong-Woo Kim et Lane F. Donnelly, « Round pneumonia: imaging findings in a large series of children », Pediatric Radiology, vol. 37, no 12, , p. 1235–1240 (ISSN 0301-0449, PMID 17952428, DOI 10.1007/s00247-007-0654-3, lire en ligne)
- ↑ M. K. McLennan, « Radiology rounds. Round pneumonia », Canadian Family Physician Medecin De Famille Canadien, vol. 44, , p. 751, 757–759 (ISSN 0008-350X, PMID 9585845, Central PMCID 2277819, lire en ligne)
- ↑ 37,0 37,1 37,2 37,3 et 37,4 « Pneumonie chez l'enfant: traitement hospitalier », sur uptodate, (consulté le 1er décembre 2020)
- ↑ « PNEUMONIE ACQUISE EN COMMUNAUTÉ CHEZ L’ENFANT DE 3 MOIS ET PLUS », sur inesss, (consulté le 30 décembre)
- ↑ C. B. Hall, K. R. Powell, K. C. Schnabel et C. L. Gala, « Risk of secondary bacterial infection in infants hospitalized with respiratory syncytial viral infection », The Journal of Pediatrics, vol. 113, no 2, , p. 266–271 (ISSN 0022-3476, PMID 3397789, lire en ligne)
- ↑ Seema Jain, Derek J. Williams, Sandra R. Arnold et Krow Ampofo, « Community-acquired pneumonia requiring hospitalization among U.S. children », The New England Journal of Medicine, vol. 372, no 9, , p. 835–845 (ISSN 1533-4406, PMID 25714161, Central PMCID 4697461, DOI 10.1056/NEJMoa1405870, lire en ligne)
- ↑ Société canadienne de pédiatrie, « La pneumonie non compliquée chez les enfants et les adolescents canadiens en santé : points de pratique sur la prise en charge | Société canadienne de pédiatrie », sur www.cps.ca (consulté le 30 décembre 2020)
- ↑ « Pediatric pneumonia », sur ncbi, (consulté le 1er décembre 2020)
- ↑ 43,0 et 43,1 Maria Gabriella Matera, Paola Rogliani, Josuel Ora et Mario Cazzola, « Current pharmacotherapeutic options for pediatric lower respiratory tract infections with a focus on antimicrobial agents », Expert Opinion on Pharmacotherapy, vol. 19, no 18, , p. 2043–2053 (ISSN 1744-7666, PMID 30359143, DOI 10.1080/14656566.2018.1534957, lire en ligne)
- ↑ (en) John S. Bradley, Carrie L. Byington, Samir S. Shah et Brian Alverson, « The Management of Community-Acquired Pneumonia in Infants and Children Older Than 3 Months of Age: Clinical Practice Guidelines by the Pediatric Infectious Diseases Society and the Infectious Diseases Society of America », Clinical Infectious Diseases, vol. 53, no 7, , e25–e76 (ISSN 1537-6591 et 1058-4838, PMID 21880587, Central PMCID PMC7107838, DOI 10.1093/cid/cir531, lire en ligne)
- ↑ (en) Tina Q. Tan, Dan K. Seilheimer et Sheldon L. Kaplan, « Pediatric lung abscess: clinical management and outcome », The Pediatric Infectious Disease Journal, vol. 14, no 1, , p. 51–55 (ISSN 0891-3668, DOI 10.1097/00006454-199501000-00011, lire en ligne)
- ↑ « Prise en charge et pronostic de l'épanchement parapneumonique et de l'empyème chez l'enfant », sur uptodate, (consulté le 23 décembre 2020)
- ↑ 47,0 et 47,1 Yves Gillet, Valérie Lamarre, Daniel Floret, Urgence et soins intensifs pédiatriques, CHU st justine, , Pneumonie communautaire grave
- ↑ E. R. Wald, « Recurrent and nonresolving pneumonia in children », Seminars in Respiratory Infections, vol. 8, no 1, , p. 46–58 (ISSN 0882-0546, PMID 8372275, lire en ligne)
- ↑ B. J. Freij, H. Kusmiesz, J. D. Nelson et G. H. McCracken, « Parapneumonic effusions and empyema in hospitalized children: a retrospective review of 227 cases », Pediatric Infectious Disease, vol. 3, no 6, , p. 578–591 (ISSN 0277-9730, PMID 6514596, DOI 10.1097/00006454-198411000-00021, lire en ligne)
