Oedème local (approche clinique)
| Approche clinique | |
 Cellulite de la jambe droite | |
| Caractéristiques | |
|---|---|
| Examens paracliniques | Hémocultures, Profil de coagulation, Échographie Doppler, Dosage des D-dimères, Échographie de la veine proximale de la jambe, Mesure de la pression intracompartimentale, Imagerie, Détection d'antigène par PCR, Frottis de sang périphérique, Échographie scrotale |
| Drapeaux rouges |
Symptômes B, Crépitants, Dyspnée (symptôme), Nécrose, Syncope (symptôme), Douleur pleurétique (symptôme), Hypotension artérielle (signe clinique), Douleur importante, Desaturation |
| Informations | |
| Spécialités | Chirurgie vasculaire, infectiologie, dermatologie, rhumatologie |
|
| |
Oedème local (29-2)
L'oedème local se caractérise par une accumulation régionale de liquide dans l'espace interstitiel. [1][2]
Épidémiologie
La cause la plus fréquente d'œdème périphérique chez les patients de plus de 50 ans est l'insuffisance veineuse et est liée au vieillissement. [2]
Étiologies
Les causes de l'œdème local peuvent être divisées en fonction du mécanisme sous-jacent comme ci-dessous. [2][3]
- Augmentation de la pression hydrostatique capillaire
- Augmentation de la perméabilité capillaire
- Obstruction lymphatique (lymphoedème)
- Autres
Physiopathologie
Les compartiments de fluide dans le corps humain sont divisés entre les espaces intracellulaire et extracellulaire. L'espace extracellulaire constitue environ un tiers de l'eau corporelle totale, qui est ensuite divisée en volume plasmatique intravasculaire (25%) et en espace interstitiel extravasculaire (75%). L'équilibre des fluides entre ces compartiments est maintenu par les pressions hydrostatiques et oncotiques décrites par la loi de Starling qui stipule : [1][2][4]
Filtration = Kf x (Pc – Pfi – Oc + Ofi), où
- Kf représente le coefficient de filtration capillaire
- Pc représente la pression hydrostatique capillaire
- Pfi représente la pression hydrostatique au niveau du fluide interstitiel
- Oc représente la pression oncotique capillaire
- Ofi représente la pression oncotique au niveau du fluide interstitiel
Les deux autres facteurs qui jouent un rôle important dans l'équilibre des fluides sont la perméabilité de la paroi vasculaire et le système lymphatique qui recueille le fluide et les protéines filtrées de l'espace interstitiel et qui les renvoie vers le système vasculaire. Toute perturbation de cette homéostasie qui se traduit par une filtration nette hors de l'espace vasculaire ou une altération du retour de liquide par les lymphatiques conduit à une accumulation de liquide dans l'espace interstitiel que l'on appelle œdème. [1][2]
| Conditions | Mécanisme causal |
|---|---|
| Thrombose veineuse profonde[5] | La compression mécanique d'une veine profonde, généralement de la jambe, par un caillot de sang entraîne une augmentation de la pression veineuse. |
| Syndrome du compartiment [6] | L'augmentation de liquide dans un compartiment à volume fixe (ex : saignement) hausse la pression tissulaire et veineuse. Lorsque la pression interstitielle dépasse la pression de perfusion capillaire, un collapsus capillaire peut se produire, ce qui entraîne une diminution du flux sanguin, une anoxie et éventuellement une ischémie des tissus mous. La réponse musculaire à ceci est de libérer des substances augmentant la perméabilité vasculaire et le fluide dans le compartiment. Au fur et à mesure que les cellules commencent à se lyser, leur activité osmotique peut également attirer l'eau du compartiment vasculaire. |
| Insuffisance veineuse chronique [7] | L'insuffisance veineuse chronique est due soit à un reflux soit à une obstruction du flux sanguin veineux. Elle peut se développer à partir de l'incompétence valvulaire prolongée des veines superficielles, des veines profondes ou des veines perforantes qui les relient. Dans tous les cas, il en résulte une hypertension veineuse des membres inférieurs et cette pression hydrostatique veineuse constamment élevée peut entraîner un œdème des membres inférieurs. |
| Brûlure [8] | Les grandes brûlures (> 20% de la surface corporelle) provoquent une réponse systémique de la libération de médiateurs inflammatoires et vasoactifs, ce qui entraîne une perte de liquide localement au niveau du site de brûlure. |
| Cellulite [9] | La cellulite est caractérisée par un œdème résultant de la réponse des cytokines et des neutrophiles des bactéries pénétrant dans l'épiderme. |
| Fasciite nécrosante [10] | La fasciite nécrosante est une infection agressive de la peau et des tissus mous qui provoque la nécrose du fascia musculaire et des tissus sous-cutanés. Cette infection se déplace généralement le long du plan fascial, qui a un mauvais apport sanguin, laissant les tissus sus-jacents initialement non affectés, retardant potentiellement le diagnostic et l'intervention chirurgicale. Le processus infectieux peut se propager rapidement, provoquant une infection du fascia, des plans péri-fasciaux et provoquer une infection secondaire de la peau, des tissus mous et des muscles sus-jacents et sous-jacents.
L'infection transite rapidement par le fascia musculaire. Après plusieurs jours, la peau sus-jacente, qui ne semble pas affectée au départ, passera à une teinte érythémateuse, rouge-violet à bleu-gris. La texture de la peau deviendra indurée, gonflée, brillante et chaude au toucher. À ce stade, la peau est extrêmement sensible à la palpation et peut également être douloureuse hors de proportion avec les symptômes. La dégradation cutanée débutera dans 3 à 5 jours et s'accompagnera de bulles et de gangrène cutanée. La douleur est réduite dans la zone touchée en raison de petits vaisseaux thrombosés et de la destruction des nerfs superficiels dans les tissus sous-cutanés. Les stades avancés de l'infection sont caractérisés par des symptômes systémiques tels que fièvre, tachycardie et septicémie. |
| Filariose [11] | Les humains sont le principal réservoir de cette maladie parasitaire et les moustiques en sont le vecteur. Le moustique dépose des larves dans la circulation sanguine. Ils s'installent dans les ganglions lymphatiques et se transforment en vers adultes. Avec la prolifération des vers adultes, les lymphatiques deviennent occlus, ce qui perturbe le drainage lymphatique. |
| Lymphadénectomie [12] | Bien que la dissection des ganglions lymphatiques soit une partie importante de l'évaluation et du traitement du cancer, comme pour toute autre intervention chirurgicale, des complications peuvent survenir. Les complications dépendent du site et de l'étendue de la dissection. Les complications courantes comprennent la douleur, l'engourdissement et les infections des plaies chirurgicales. Les patients peuvent également développer un lymphœdème, qui est un gonflement et un œdème des bras ou des membres inférieurs, qui survient en raison de l'accumulation de lymphe dans le tissu interstitiel, provoquant une sensation de lourdeur et d'enflure dans la zone touchée. |
| Oedème idiopathique [2] | L'œdème idiopathique est mal compris et affecte principalement les femmes préménopausées. Les principales caractéristiques sont des épisodes périodiques d'œdème dans les mains, les jambes et des ballonnements abdominaux qui ne sont pas clairement liés au cycle menstruel. Par définition, c'est un diagnostic d'exclusion. Il est le plus courant dans les troisième et quatrième décennies de la vie. Les perturbations psychologiques et émotionnelles peuvent aggraver cette condition. |
| Lipoedème [2] | Dans le lipœdème, qui est une accumulation pathologique de tissu adipeux dans les extrémités, les pieds sont généralement épargnés. |
Approche clinique
L'histoire et le physique sont très importants en raison d'un large éventail de diagnostics différentiels dans l'œdème périphérique. [2] Pour les signes et symptômes à rechercher pour éliminer les causes d'oedème généralisé, voir Oedème généralisé (situation clinique).
Facteurs de risque
| Condition | Facteurs de risque à rechercher |
|---|---|
| Thrombose veineuse profonde [5] |
|
| Syndrome des loges [6] |
|
| Insuffisance veineuse chronique [7] |
|
| Cellulite [13][14] |
|
| Filariose [15] |
|
Questionnaire
L'identification du patient est importante pour identifier des causes possibles :
- Antécédents médicaux
- Antécédents chirurgicaux (ex : lymphadénectomie)
- Médicaments (ex : prise d'oestrogènes exogènes pour la thrombose veineuse profonde)
- Habitudes de vie (ex : sédentarité pour l'insuffisance veineuse chronique)
Il faut questionner les caractéristiques de l'oedème : [2][16]
- Moment de l'oedème : insidieux ou chronique
- Un gonflement aigu du membre dans les 72 heures est plus fréquent dans les cas de thrombose veineuse profonde, de cellulite, de blessure aiguë suite à un traumatisme ou d'initiation récente de nouveaux médicaments comme les inhibiteurs calciques.
- Association aux changements de position
- L'œdème dépendant est plus fréquent dans l'insuffisance veineuse qui s'améliore généralement avec l'élévation et s'aggrave avec la position du membre en bas du coeur.
- Localisation
- Membres inférieurs : unilatéral ou bilatéral
- Un œdème unilatéral suggère une atteinte locale comme une thrombose veineuse profonde, une cellulite ou une obstruction lymphatique due à une tumeur et à une radiothérapie.
- Membres inférieurs : unilatéral ou bilatéral
- Évaluation des maladies systémiques
Les symptômes associés doivent aussi être questionnés selon les étiologies considérées dans le diagnostic différentiel.
Examen clinique
Les signes vitaux peuvent aider à différencier les causes : [2]
- température : la fièvre peut être observée avec une infection (ex : cellulite)
- tension artérielle : l'hypotension et l'hypertension peuvent indiquer une cause d'oedème généralisée
Le reste de l'examen physique se concentre sur les divers éléments pouvant orienter vers un diagnostic précis :
- L'œdème doit être évalué pour détecter s'il prend le godet, s'il y a présence d'une sensibilité et si la peau présente des changements. Consulter le tableau dans la prochaine section.
- Dans les premiers stades du lymphœdème, l'oedème à godet se produit en raison d'un afflux de liquide riche en protéines dans l'interstitium avant la fibrose du tissu sous-cutané
- La sensibilité est fréquente dans la cellulite et la thrombose veineuse profonde tandis que la fasciite nécrosante est très souffrante
- La thrombose veineuse profonde aiguë et la cellulite peuvent augmenter la température de la peau sur la zone touchée en raison de l'activation de facteurs cellulaires et humoraux.
- L'insuffisance veineuse chronique est souvent associée à dermatite de stase due au dépôt d'hémosidérine. Dans les stades ultérieurs, les patients peuvent développer des ulcères veineux qui peuvent évoluer vers des érosions profondes et suintantes.
| Condition | Oedème à godet | Sensibilité / Douleur | Changements cutanés | Éléments additionnels | Image |
|---|---|---|---|---|---|
| Thrombose veineuse profonde | Oui | Oui | Érythème et chaleur | L'oedème peut atteindre le mollet et/ou tout le membre inférieur | 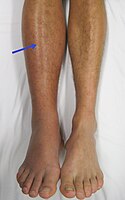
|
| Syndrome des loges | Non | Présentation classique de la douleur :
|
Signes de traumatismes (érythème, décoloration, coupures cutanées, etc.) | Le patient peut avoir une sensation réduite, en particulier à une discrimination en deux points. Il est possible d'observer une sensation de vibration diminuée.
Les mouvements régulés par les muscles affectés peuvent être limités. Il faut rechercher les pouls dorsaux du pied et du tibia postérieur. |

|
| Insuffisance veineuse chronique | Oui | Parfois | Stade avancé de la maladie: lésion cutanée blanchie sévère, atrophie cutanée, hyperpigmentation, capillaires veineux dilatés et formation d'ulcères recouvrant le plus souvent la malléole médiale | Il faut rechercher tout ulcère, pouls distal et neuropathie. Le test de Trendelenburg peut aider à différencier la TVP causée par les valves veineuses superficielles par rapport au système profond.
Si le membre est érythémateux, contrairement à la cellulite, le membre va blanchir si on l'élève au dessus du coeur. |
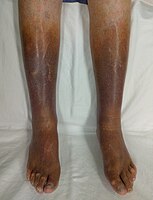
|
| Cellulite | Oui | Oui (à la palpation) | Zone mal délimitée avec érythème et chaleur au toucher
Possibilité d'un abcès cutané, de vésicules, de bulles ou de "peau d'orange" |
Le patient peut présenter une lymphadénopathie.
Elle affecte le plus souvent les membres inférieurs. C'est rarement bilatéral. Si des extrémités sont touchées, il faut examiner la sensation et les pouls pour surveiller de près le syndrome des loges. Contrairement à l'insuffisance veineuse, le membre ne va pas blanchir si on l'élève au dessus du coeur. |

|
| Fasciite nécrosante | Non | Oui (douleur atroce hors de proportion) |
|
Les stades avancés de l'infection sont caractérisés par des symptômes systémiques tels que fièvre, tachycardie et septicémie.
Il faut rechercher la présence de dysesthésie ou paresthésie. L'anesthésie peut également être présente dans certaines zones en raison d'une lésion des fibres nerveuses. |
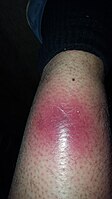
|
| Filariose | Oui / Non | Possible | bosses dans les tissus sous-cutanés | 
|
Drapeaux rouges
- douleur importante
- crépitants
- nécrose
- dyspnée, desaturation, douleur pleurale, syncope, hypotension
- symptômes B
Investigation
Les investigations à privilégier dépendent des conditions considérées dans le diagnostic différentiel :
- Les premiers efforts de bilan devraient se concentrer sur l'exclusion des principales causes d'oedème généralisé, notamment l'insuffisance cardiaque, l'insuffisance hépatique et l'insuffisance rénale. [2]
- Pour plus de détails, voir Oedème généralisé (situation clinique).
- L'échographie Doppler est la modalité de choix si la suspicion de thrombose veineuse profonde est élevée. Il peut également être utilisé pour confirmer le diagnostic d'insuffisance veineuse chronique. [2]
- Les autres investigations utiles pour une thrombose veineuse profonde sont : [5]
- Dosage des D-dimères (très sensibles mais pas très spécifiques)
- Profil de coagulation
- Échographie de la veine proximale de la jambe
- Pour le diagnostic du syndrome des loges, la mesure de la pression intracompartimentale reste le gold standard. La mesure est généralement effectuée à l'aide d'un manomètre à aiguille. [6]
- Selon les directives de pratique de l'Infectious Disease Society of America, lorsque la cellulite est suspectée, il est recommandé de ne pas recourir à l'imagerie de la zone infectée, sauf pour les patients atteints de neutropénie fébrile. Il faut envisager des hémocultures uniquement chez les patients immunodéprimés, ayant subi une blessure par immersion ou une morsure d'animal. Des hémocultures sont également nécessaires lorsqu'un patient présente des signes d'infection systémique. [18][19]
- Pour le filariose, la détection d'antigène par PCR est la méthode de diagnostic préférée car elle détecte également les infections latentes. Par ailleurs, deux échantillons de frottis de sang périphérique épais et minces peuvent être prélevés soit sur une ponction veineuse, soit sur un doigt/talon. Ceux-ci sont de préférence pris après 20 h, compte tenu de la périodicité nocturne des microfilaires, et colorés avec une coloration Giemsa ou H&E. L'échographie scrotale peut révéler des mouvements de vers adultes chez des hommes par ailleurs asymptomatiques. [20][21]
Prise en charge
Le traitement doit être guidé par une affection sous-jacente qui prédispose à la formation d'un œdème.[22]
- Dans tous les cas, de maintenir le membre oedématié élevé fait diminuer l'oedème
- La cellulite est traitée avec des antibiotiques
- Chez les patients atteints de thrombose veineuse profonde, un traitement anticoagulant soit avec de l'héparine de bas poids moléculaire ou des anticoagulants plus récents comme le rivaroxaban ou l'apixaban est utilisé. Des bas compressifs doivent être utilisés pour prévenir le syndrome post-thrombotique. [23]
- Chez les patients souffrant d'insuffisance veineuse chronique, les thérapies mécaniques, y compris l'élévation des jambes et les bas de contention, sont efficaces. Le traitement par bas compressifs est contre-indiqué dans les maladies artérielles périphériques car il peut compromettre davantage l'apport sanguin. [2]
- Dans le lymphœdème, le traitement implique une physiothérapie décongestive complexe composée d'un massage lymphatique manuel et de bandages multicouches. La thérapie d'entretien comprend des bas compressifs et des dispositifs de compression pneumatiques. [24]
- Chez les patients pour lesquels les médicaments sont l'agent offensant, ils doivent être arrêtés si possible et passer à une classe différente.[2]
Complications
Voici une liste non exhaustive des complications qui doivent être pries en compte :
- insuffisance veineuse chronique
- septicémie
- cellulite (pour les lymphoedèmes)
- suintement
Références
- Cette page a été modifiée ou créée le 2020/11/11 à partir de Peripheral Edema (StatPearls / Peripheral Edema (2020/07/04)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/32119339 (livre).
- ↑ 1,0 1,1 et 1,2 R. C. Little et J. M. Ginsburg, « The physiologic basis for clinical edema », Archives of Internal Medicine, vol. 144, no 8, , p. 1661–1664 (ISSN 0003-9926, PMID 6466021, DOI 10.1001/archinte.144.8.1661, lire en ligne)
- ↑ 2,00 2,01 2,02 2,03 2,04 2,05 2,06 2,07 2,08 2,09 2,10 2,11 2,12 et 2,13 Amandeep Goyal, Austin S. Cusick et Pankaj Bansal, StatPearls, StatPearls Publishing, (PMID 32119339, lire en ligne)
- ↑ Kathryn P. Trayes, James S. Studdiford, Sarah Pickle et Amber S. Tully, « Edema: diagnosis and management », American Family Physician, vol. 88, no 2, , p. 102–110 (ISSN 1532-0650, PMID 23939641, lire en ligne)
- ↑ Daniella Lent-Schochet et Ishwarlal Jialal, StatPearls, StatPearls Publishing, (PMID 30725750, lire en ligne)
- ↑ 5,0 5,1 et 5,2 Sheikh M. Waheed, Pujitha Kudaravalli et David T. Hotwagner, StatPearls, StatPearls Publishing, (PMID 29939530, lire en ligne)
- ↑ 6,0 6,1 6,2 et 6,3 John Kiel et Kimberly Kaiser, StatPearls, StatPearls Publishing, (PMID 30085512, lire en ligne)
- ↑ 7,0 7,1 et 7,2 Shivik K. Patel et Scott M. Surowiec, StatPearls, StatPearls Publishing, (PMID 28613694, lire en ligne)
- ↑ Timothy J. Schaefer et Shruti C. Tannan, StatPearls, StatPearls Publishing, (PMID 28613524, lire en ligne)
- ↑ 9,0 et 9,1 Brandon D. Brown et Kristen L. Hood Watson, StatPearls, StatPearls Publishing, (PMID 31747177, lire en ligne)
- ↑ Heather A. Wallace et Thomas B. Perera, StatPearls, StatPearls Publishing, (PMID 28613507, lire en ligne)
- ↑ 11,0 et 11,1 Thomas E. Newman et Andrew L. Juergens, StatPearls, StatPearls Publishing, (PMID 32310472, lire en ligne)
- ↑ Francesk Mulita et Shiva Kumar R. Mukkamalla, StatPearls, StatPearls Publishing, (PMID 33232067, lire en ligne)
- ↑ (en) M. Quirke, F. Ayoub, A. McCabe et F. Boland, « Risk factors for nonpurulent leg cellulitis: a systematic review and meta-analysis », British Journal of Dermatology, vol. 177, no 2, , p. 382–394 (DOI 10.1111/bjd.15186, lire en ligne)
- ↑ (en) Keith S Kaye, Lindsay A Petty, Andrew F Shorr et Marya D Zilberberg, « Current Epidemiology, Etiology, and Burden of Acute Skin Infections in the United States », Clinical Infectious Diseases, vol. 68, no Supplement_3, , S193–S199 (ISSN 1058-4838 et 1537-6591, PMID 30957165, Central PMCID PMC6452002, DOI 10.1093/cid/ciz002, lire en ligne)
- ↑ (en) Gayle B. Lourens et Denise K. Ferrell, « Lymphatic Filariasis », Nursing Clinics of North America, vol. 54, no 2, , p. 181–192 (DOI 10.1016/j.cnur.2019.02.007, lire en ligne)
- ↑ Maulik G. Shah, Shaun Cho, J. Edwin Atwood et Paul A. Heidenreich, « Peripheral edema due to heart disease: diagnosis and outcome », Clinical Cardiology, vol. 29, no 1, , p. 31–35 (ISSN 0160-9289, PMID 16477775, Central PMCID 6654652, DOI 10.1002/clc.4960290108, lire en ligne)
- ↑ Heather A. Wallace et Thomas B. Perera, StatPearls, StatPearls Publishing, (PMID 28613507, lire en ligne)
- ↑ (en) Dennis L. Stevens, Alan L. Bisno, Henry F. Chambers et E. Patchen Dellinger, « Practice Guidelines for the Diagnosis and Management of Skin and Soft Tissue Infections: 2014 Update by the Infectious Diseases Society of America », Clinical Infectious Diseases, vol. 59, no 2, , e10–e52 (ISSN 1058-4838 et 1537-6591, DOI 10.1093/cid/ciu296, lire en ligne)
- ↑ (en) Madeleine W. Cunningham, « Pathogenesis of Group A Streptococcal Infections », Clinical Microbiology Reviews, vol. 13, no 3, , p. 470–511 (ISSN 1098-6618 et 0893-8512, PMID 10885988, Central PMCID PMC88944, DOI 10.1128/CMR.13.3.470, lire en ligne)
- ↑ (en) Anish Chandy, Alok Singh Thakur, Mukesh Pratap Singh et Ashish Manigauha, « A review of neglected tropical diseases: filariasis », Asian Pacific Journal of Tropical Medicine, vol. 4, no 7, , p. 581–586 (DOI 10.1016/S1995-7645(11)60150-8, lire en ligne)
- ↑ Sabine Mand, Yeboah Marfo-Debrekyei, Matthias Dittrich et Kerstin Fischer, « [No title found] », Filaria Journal, vol. 2, no 1, , p. 3 (PMID 12636874, Central PMCID PMC151680, DOI 10.1186/1475-2883-2-3, lire en ligne)
- ↑ Shaun Cho et J. Edwin Atwood, « Peripheral edema », The American Journal of Medicine, vol. 113, no 7, , p. 580–586 (ISSN 0002-9343, PMID 12459405, DOI 10.1016/s0002-9343(02)01322-0, lire en ligne)
- ↑ Susan R. Kahn, Jean-Philippe Galanaud, Suresh Vedantham et Jeffrey S. Ginsberg, « Guidance for the prevention and treatment of the post-thrombotic syndrome », Journal of Thrombosis and Thrombolysis, vol. 41, no 1, , p. 144–153 (ISSN 1573-742X, PMID 26780743, Central PMCID 4715836, DOI 10.1007/s11239-015-1312-5, lire en ligne)
- ↑ Bryan C. Sleigh et Biagio Manna, StatPearls, StatPearls Publishing, (PMID 30725924, lire en ligne)

