Obstruction de l'intestin grêle
| Maladie | |||
 Radiographie abdominale démontrant une occlusion intestinale avec de multiples niveaux hydro-aériques | |||
| Caractéristiques | |||
|---|---|---|---|
| Signes | Sepsis, Hypovolémie, Masse abdominale, Péritonisme, Cicatrice, Hernie abdominale, Rigidité, Sensibilité diffuse ou focale, Ressaut, Masse rectale, ... [+] | ||
| Symptômes |
Nausées, Ballonnements, Absence de gaz, Douleur abdominale, Vomissement , Absence de selle | ||
| Diagnostic différentiel |
Maladies inflammatoires intestinales, Syndrome de pseudo-occlusion intestinale, Pullulation bactérienne, Iléus, Pancréatite aiguë, Ischémie mésentérique aiguë, Gastro-entérite virale, Constipation (signe clinique), Entérite bactérienne, Colite bactérienne | ||
| Informations | |||
| Terme anglais | Small bowel obstruction | ||
| Autres noms | Occlusion intestinale, Subocclusion, Pseudo-obstruction, Occlusion du grêle | ||
| Wikidata ID | Q16244733 | ||
| Spécialités | Chirurgie générale, Gastro-entérologie, Médecine d'urgence | ||
| |||
L'occlusion de l'intestin grêle est une urgence chirurgicale courante en raison d'un blocage mécanique de l'intestin. Les obstructions de l'intestin grêle peuvent être partielles ou complètes et peuvent être non étranglées ou étranglées. [1][2][3][4]
Épidémiologie
Plus de 300 000 laparotomies seraient pratiquées chaque année aux États-Unis pour une occlusion de l'intestin grêle. L'intestin grêle comprend 80% des obstructions intestinales. Il y a une incidence similaire chez les hommes et les femmes. Il y a une incidence plus élevée avec l'âge et le nombre d'interventions intra-abdominales. [5][4]
Les obstructions de l'intestin grêle représentent 15% des consultations pour douleur abdominale. 30% des cas ont besoin de chirurgie et 7 à 42% sont étranglées. [6]
Étiologies
Dans l'ordre, les trois causes les plus fréquentes sont [6]:
- les adhérences intestinales
- les néoplasies abdominales
- les hernies incarcérées.
Dans la population pédiatrique, les causes courantes comprennent l'atrésie intestinale, la sténose du pylore et l'invagination[4].
| Localisation de l'obstruction | Étiologies |
|---|---|
| Extraluminales | |
| Intramurales |
|
| Intraluminales |
Physiopathologie
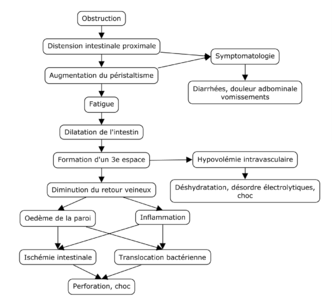
L'obstruction de l'intestin grêle entraîne une distension intestinale proximale et une décompression intestinale distale. Au début, le péristaltisme peut augmenter, entraînant des selles fréquentes et des diarrhées. Des vomissements peuvent survenir en raison de la distension proximale de l'intestin. À la suite de l'augmentation du péristaltisme, l'intestin se fatigue et se dilate. Une collection de fluide intraluminal, appelée 3e espace, se forme souvent dans l'intestin et dans sa paroi (oedème pariétal). Cela cause de la déshydratation, de l'hypovolémie et des désordres électrolytiques. Il est même possible de tomber en choc à cause de la formation du 3e espace. La ventilation peut aussi être compromise à cause de l'augmentation de la pression intra-abdominale. [7]
Avec l'augmentation de la pression intraluminale, le retour veineux de l'intestin diminue. Cela entraîne un œdème et une inflammation de la paroi intestinale. La paroi intestinale épaissie et inflammée présente un risque d'ischémie et de translocation bactérienne par perte de l'intégrité des jonctions cellulaires. La translocation bactérienne peut provoquer une péritonite et une bactériémie, le plus souvent dues à Escherichia coli. La translocation bactérienne amplifie l'inflammation. Au fur et à mesure que l'intestin augmente sa pression, le flux artériel sera coupé, entraînant une ischémie intestinale et éventuellement une perforation, une péritonite, un choc septique et la mort si elle n'est pas traitée.[8][4][6][7]
Présentation clinique
Facteurs de risque
Les principaux facteurs de risque d'obstruction de l'intestin grêle sont[6] :
- des antécédents de chirurgie abdominale :
- la laparotomie (63% forment des adhérences, 11-20% d'hernie incisionnelle)
- la laparoscopie (< 2% d'hernie incisionnelle, moins d'adhérences, mais présentes quand même[9])
- une chirurgie pelvienne (urologie, gynécologique, colorectale)
- les maladies inflammatoires intestinales
- avoir une néoplasie
- une hernie abdominale.
Questionnaire
Au questionnaire, les symptômes suivants sont suggestifs d'une obstruction de l'intestin grêle[6] :
- une douleur abdominale aiguë :
- initialement crampiforme et intermittente
- si la douleur abdominale devient constante, cela suggère de l'ischémie et du péritonisme
- la vitesse d'apparition de la douleur nous oriente vers une cause probable :
- une douleur à début abrupt pointe vers une hernie, un volvulus ou des adhérences
- une douleur à début lentement progressif pointe davantage vers une néoplasie ou une maladie inflammatoire
- les nausées et les vomissements sont des symptômes précoces, particulièrement si l'obstruction est haute (si les vomissements sont fécaloïdes, c'est un indice de pullulation bactérienne)
- les ballonnements peuvent être présents, particulièrement si l'obstruction est basse
- l'absence de gaz et l'absence de selle sont pathognomoniques (toutefois, le passage de selle n'exclue pas une occlusion complète : le site distal à l'occlusion doit se vider avant qu'il n'y ait plus de gaz et de selle).
Examen clinique
À l'examen physique, les signes suivants sont à rechercher[4][6][10][7] :
- les signes vitaux seront généralement normaux, mais on doit rechercher des signes de sepsis et d'hypovolémie
- à l'examen de l'abdomen
- rechercher la présence de cicatrices abdominales, d'hernie abdominale ou de masse abdominale
- à l'auscultation, on recherche des bruits intestinaux anormaux
- au début, les bruits intestinaux sont généralement augmentés et aigus (métalliques)
- les bruits intestinaux sont diminués (voire absents) si l'obstruction est avancée
- les mouvements de péristaltisme peuvent être visibles au début de l'obstruction
- la distension abdominale
- une sensibilité diffuse ou focale
- des signes de péritonisme (ressaut, défense abdominale involontaire, rigidité)
- au toucher rectal, on recherche une masse rectale et une impaction fécale.
Examens paracliniques
Des examens paracliniques sont nécessaires pour l'évaluation et la gestion de l'occlusion de l'intestin. Toutefois, outre confirmer le diagnostic et les complications franches, on recherche l’ischémie avant qu’elle ne se complique : on ne doit pas se fier uniquement aux examens paracliniques pour identifier le patient ayant besoin d'intervention chirurgicale. On doit interpréter les bilans avec diligence.
Bilan sanguin
Les analyses suivantes sont sensibles, mais peu spécifiques à l'occlusion [6]:
- la formule sanguine complète pour rechercher une leucocytose ainsi que pour se préparer à la chirurgie (hémoglobine et plaquette)
- les électrolytes, la créatininémie et l'urée pour évaluer l'état d'hydratation
- s'il y a déshydratation, une hyponatrémie, une augmentation de l'urée et de la créatininémie sont possibles
- l'hypokaliémie est fréquente dans les contextes de vomissements
- le gaz veineux et les lactates sériques pour rechercher des désordres acidobasiques
- l'acidose métabolique et l'hyperlactatémie peuvent être présents en cas de choc hypovolémique/septique ou en cas d'ischémie intestinale
- l'alcalose métabolique peut être présent en cas de déshydratation
- l'INR et le TCA en prévision de la chirurgie (peut être altéré si dénutrition).
Imageries
| Examen radiologique | Explications |
|---|---|
| Tomodensitométrie abdominale avec contraste[Se: 93 %][Sp: 100 %] |
|
| Radiographie abdominale[Se: 50 %][Sp: 75 %] |
|
| Échographie abdominale |
|
| Entéroclyse - transit du grêle standard |
|
| IRM abdominale |
|
| Entéro-IRM |
|
-
Radiographie simple en position debout d'une obstruction de l'intestin grêle
-
Niveaux aériens vus à la tomodensitométrie dans un cas d'occlusion de l'intestin grêle
-
Obstruction de l'intestin grêle à l'échographie
Approche clinique
Tout d'abord, face à un tableau qui laisse soupçonner une occlusion de l'intestin grêle, il est important de s'assurer que c'est bien une obstruction mécanique, et non fonctionnelle, comme ce serait le cas avec un iléus paralytique par exemple. Une augmentation du péristaltisme et des bruits intestinaux est un indice d'obstruction mécanique.
Ensuite, il faut différencier les occlusions du grêle et celles du côlon. Pour ce faire, on peut utiliser la radiographie simple de l'abdomen, qui montrera la présence d'air et de distension dans le côlon si c'est une obstruction du côlon.
L'occlusion peut être partielle ou complète, c'est-à-dire si la lumière intestinale est totalement obstruée ou non. L'absence totale de selles et de gaz oriente vers une occlusion complète. L'occlusion peut aussi être simple ou compliquée, s'il y a un compromis vasculaire et une menace d'ischémie de l'intestin. Les occlusions causées par une hernie étranglée ou par une anse borgne (closed-loop) sont des exemples d'occlusions compliquées. Plusieurs indices de l'étiologie peuvent être recherchés au questionnaire et à l'examen physique, notamment les antécédents de chirurgie abdominale, la présence d'hernie ou de symptômes suggestifs d'un cancer. Des examens d'imagerie nous permettent de confirmer la présence de l'occlusion intestinale et peuvent aussi préciser l'étiologie. L'examen de choix est la tomodensitométrie axiale, quand elle est possible, après avoir effectué une radiographie 3 incidences qui servira d'examen de référence pendant l'épisode de soin. Il est possible d'omettre la tomodensitométrie si le patient ne présente pas de signe de souffrance intestinale (température, leucocytose et/ou péritonisme) et que le patient a déjà eu une intervention chirurgicale. Le diagnostic le plus probable est alors l'occlusion sur adhérences.
Des études de laboratoire de routine doivent également être faits pour évaluer l'ischémie intestinale, l'inflammation, le degré de déshydratation et pour écarter les diagnostics concomitants. Ceux-ci peuvent inclure une formule sanguine complète, l'acide lactique, l'analyse d'urine et un bilan de coagulation. Il faut se rappeler toutefois que les analyses de laboratoire ne sont pertubées que lorsque la situation est avancée et on ne doit pas se fier uniquement à ce critère pour suspecter la souffrance intestinale. En effet, en utilisant uniquement les éléments cliniques, nous avons jusqu'à 50% d'erreur, et en combinant les éléments paracliniques tels que l'imagerie et les analyses sanguines, notre validité diagnostique augmente à 70-96%[16][7][8][17].
Le choix du traitement dépend de l'état clinique du patient. S'il y présence d'un abdomen aigu, aucun antécédent chirurgical, si une hernie est visualisée ou si les examens paracliniques pointent vers une occlusion compliquée, le traitement est chirurgical d'emblée. S'il n'y a pas d'abdomen aigu, le traitement conservateur peut être essayer pour environ 48h, selon le jugement clinique et l'évolution du patient. S'il échoue, il faudrait procéder au traitement chirurgical, qui consiste à lever la cause de l'obstruction et réséquer les parties non-viables d'intestin au besoin.[6]
Diagnostic
L'occlusion intestinale est suspectée cliniquement, mais confirmée par les examens paracliniques, qui nous permettent également de trouver l'étiologie et déterminer la sévérité de la situation.
Diagnostic différentiel
Le diagnostic différentiel de l'occlusion du grêle comprend :[4][18][19]
- la gastro-entérite virale
- l'entérite bactérienne
- la colite bactérienne
- l'iléus
- l'ischémie mésentérique
- la pancréatite aiguë
- le syndrome de pseudo-occlusion intestinale
- la pullulation bactérienne
- la maladie inflammatoire intestinale
- la constipation.
Traitement
Il y a une grande variabilité de pratique dans le traitement de l'occlusion intestinale[20] et il y a peu d'études de qualité sur le sujet.
Traitement conservateur
Le traitement conservateur (non chirurgical) peut être tenté sécuritairement dans les situations suivantes[6] :
- les étiologies suspectées sont les adhérences ou le post-opératoire précoce
- il n'y a pas d'indication chirurgicale (ex. signe d'ischémie), de signe clinique ou radiologique d'occlusion compliquée
- les situations médicales suivantes :
- la néoplasie intra-abdominale (carcinomatose)
- l'entérite radique en aigu (rarement efficace en chronique)
- la maladie de Crohn en aigu (rarement efficace en chronique, il faut alors se tourner vers un traitement chirurgical).
Le traitement initial de l'occlusion du grêle consiste en :
- la consultation en chirurgie générale sans délai
- garder le patient NPO
- l'analgésie PRN
- insérer un tube nasogastrique (décompression gastrique)[note 7]
- l'hydratation intraveineuse :
- elle permet de remplacer les pertes causées par les vomissements, la formation du 3e espace et le jeûne
- s'il y a beaucoup de vomissements ou si le drainage via le TNG est abondant, du KCl peut être ajouté au soluté de base
- elle permet de limiter le catabolisme via l'ajout de dextrose dans le soluté (soluté + KCl + dextrose)
- les antibiotiques :
- une sonde urinaire PRN pour monitorer les excrétats
- le test au contraste hydrosoluble (gastrografin) peut être tenté[14], car il est sécuritaire (pas d'augmentation de mortalité ou morbidité) et qu'il y a un faible risque d’ischémie lors du protocole (3-6%).
| Explications | |
|---|---|
| Pourquoi ? |
|
| Quand ? | Le moment d'administration du test au gastrografin est variable :
|
| Protocole |
Il est important de déclamper le TNG en cours de test si le patient est nauséeux, car il y a un risque d'aspiration si l'estomac se distend trop.
|
| Avantages |
|
| Utilité diagnostique |
|
| Évolution attendue |
|
Cette prise en charge conservatrice est souvent suffisante les occlusions partielles ou non compliquées de l'intestin grêle.
L'évolution attendue avec le traitement conservateur est une amélioration en 48h (85-95%) :
- 75% des occlusions partielles et 41-73% des occlusions complètes se résolvent
- 3-6% des occlusions vont s'étrangler.
Voici certains signes qui indiquent un échec au traitement conservateur :
- l'absence de reprise du transit en 5 jours (la mortalité et les complications augmentent après 3 jours de traitement conservateur[25])
- l'augmentation de la douleur ou de la distension abdominale
- de la fièvre de novo
- l'augmentation des globules blancs.
Si ce n'est pas un tableau clair d'échec, il est possible de répéter la TDM. Le clampage du TNG pendant 4h est aussi une option possible : si le résidu est < 100 cc et qu'il n'y a pas de nausées si de vomissements, on peut alors cesser le TNG.
Traitement chirurgical
Un traitement chirurgical est indiqué pour une occlusion de l'intestin grêle dans les cas suivants[6]:
- une obstruction compliquée (ischémie, anse borgne, hernie incarcérée)
- l'échec au traitement conservateur
- une occlusion sans antécédents chirurgicaux (un traitement conservateur pourrait être tenté dans certaines situations, voir ci-bas).
Le traitement chirurgical se fait :
- précocement s'il y a des signes de souffrance
- à la suite de l'échec à un traitement conservateur de 48h.
Le traitement chirurgical s'accompagne aussi d'une antibioprophylaxie pour prévenir les complications infectieuses de la chirurgie. L'approche chirurgicale peut se faire par laparotomie ou par laparoscopie.
| Approche chirurgicale choisie | Explications |
|---|---|
| Laparoscopie |
|
| Laparotomie | Voir la vidéo suivante [1] qui démontre l'utilisation de la fluorescéine pour évaluer la viabilité de l'intestin grêle.
|
Situations particulières
| Situation | Prise en charge particulière |
|---|---|
| Abdomen vierge |
|
| Carcinomatose |
|
| Pédiatrie |
|
| Occlusion post-opératoire précoce |
|
| Occlusion maligne |
|
Suivi
Après la résolution hospitalière de l'occlusion, il n'y a pas de suivi particulier, sauf si la cause est une maladie chronique (ex. entérite radique, maladie inflammatoire intestinale) ou s'il s'agit d'un cancer.
Le patient doit revenir s'il y a une récidive des symptômes, car les occlusions intestinales peuvent être récurrentes.
Complications
Les complications qui peuvent survenir à la suite d'une occlusion de l'intestin grêle sont[4]:
- la nécrose intestinale
- la perforation intestinale
- l'hypovolémie et le choc hypovolémique (formation d'un troisième espace)
- des dysélectrolytémies (hyponatrémie, hypernatrémie, hypokaliémie)
- l'acidose métabolique (par perte de bics dans les diarrhées et par vomissement des H+)
- le sepsis et le choc septique (par translocation bactérienne)
- la péritonite
- une bactériémie
- la perforation intestinale
- l'abcès intra-abdominal.
Évolution
L'évolution de la maladie dépend de la cause de l'obstruction intestinale. Lors d'un traitement chirurgical de l'occlusion, il y a un risque de faire de nouvelles adhérences, qui pourraient causer une autre occlusion par la suite.
Prévention
La prévention de l'occlusion de l'intestin grêle repose sur la prévention des étiologies sous-jacentes :
- la prévention de tout cancer abdominal
- la prévention de toute condition chirurgicale abdominale pour limiter le risque d'adhérence post-chirurgical
- la prévention des hernies inguinales (éviter de lever des charges lourdes)
- la prévention des rechutes des maladies inflammatoires intestinales.
Autrement, il est difficile de prévenir les occlusions intestinales elles-mêmes.
Notes
- ↑ Principalement après les chirurgies gastro-intestinales ou gynécologiques.
- ↑ le liquide accumulé dans la lumière intestinale sert de contraste aqueux ; par ailleurs, du contraste hydrosoluble peut être administré mais le patient est souvent porteur d'un tube nasogastrique
- ↑ Whirlpool sign, torsion des vaisseaux mésentériques.
- ↑ Gas dans les parois du grêle engendré par la nécrose
- ↑ Peut aussi être présent dans l'iléus
- ↑ Aussi présente si inflammation intestinale
- ↑ Il n'y a aucun avantage à positionner le TNG plus loin que l'estomac.
- ↑ Si les antibiotiques sont donnés, ils doivent couvrir la flore intestine, les bactéries Gram négatifs et les anaérobes
- ↑ Ce qu'on appelle «dérouler le grêle dans son entièreté»
- ↑ Secondaires à une ancienne infection abdominale ou d'origine congénitale.
Références
- Cet article a été créé en partie ou en totalité le 2020/10/16 à partir de Chirurgie (application), créée par Dre Hélène Milot, Dr Olivier Mailloux et collaborateurs et partagé sous la licence CC-BY-SA 4.0 international
- Cette page a été modifiée ou créée le 2020/10/12 à partir de Small Bowel Obstruction (StatPearls / Small Bowel Obstruction (2020/04/21)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/28846346 (livre).
- ↑ 1,0 et 1,1 Allison F. Linden, Manish T. Raiji, Jonathan E. Kohler et Erica M. Carlisle, « Evaluation of a water-soluble contrast protocol for nonoperative management of pediatric adhesive small bowel obstruction », Journal of Pediatric Surgery, vol. 54, no 1, , p. 184–188 (ISSN 1531-5037, PMID 30414689, DOI 10.1016/j.jpedsurg.2018.10.002, lire en ligne)
- ↑ John D. Gilbert et Roger W. Byard, « Obturator hernia and the elderly », Forensic Science, Medicine, and Pathology, vol. 15, no 3, , p. 491–493 (ISSN 1556-2891, PMID 30397870, DOI 10.1007/s12024-018-0046-z, lire en ligne)
- ↑ Katie Love Bower, Daniel I. Lollar, Sharon L. Williams et Farrell C. Adkins, « Small Bowel Obstruction », The Surgical Clinics of North America, vol. 98, no 5, , p. 945–971 (ISSN 1558-3171, PMID 30243455, DOI 10.1016/j.suc.2018.05.007, lire en ligne)
- ↑ 4,0 4,1 4,2 4,3 4,4 4,5 4,6 et 4,7 Michael A. Schick, Sarang Kashyap et Marcelle Meseeha, StatPearls, StatPearls Publishing, (PMID 28846346, lire en ligne)
- ↑ Matthew K. Edwards, Christopher S. Kuppler, Chasen A. Croft et Hannah M. Eason-Bates, « Adhesive Closed-loop Small Bowel Obstruction », Clinical Practice and Cases in Emergency Medicine, vol. 2, no 1, , p. 31–34 (ISSN 2474-252X, PMID 29849259, Central PMCID 5965135, DOI 10.5811/cpcem.2017.10.35927, lire en ligne)
- ↑ 6,00 6,01 6,02 6,03 6,04 6,05 6,06 6,07 6,08 6,09 6,10 6,11 6,12 6,13 6,14 6,15 et 6,16 « Application Chirurgie » (consulté le 16 octobre 2020)
- ↑ 7,0 7,1 7,2 et 7,3 (en) Courtney M. Touwnsend, R. Daniel Beauchamps, B. Mark Evers, Kenneth L. Mattox, Sabiston Textbook of Surgery, Philadelphie, Elsevier, (ISBN 978-0-323-40162-3), p. 1247
- ↑ 8,0 et 8,1 Brit Long, Jennifer Robertson et Alex Koyfman, « Emergency Medicine Evaluation and Management of Small Bowel Obstruction: Evidence-Based Recommendations », The Journal of Emergency Medicine, vol. 56, no 2, , p. 166–176 (ISSN 0736-4679, PMID 30527563, DOI 10.1016/j.jemermed.2018.10.024, lire en ligne)
- ↑ (en) T. Yamada, K. Okabayashi, H. Hasegawa et M. Tsuruta, « Meta-analysis of the risk of small bowel obstruction following open or laparoscopic colorectal surgery: Small bowel obstruction after colorectal surgery », British Journal of Surgery, vol. 103, no 5, , p. 493–503 (DOI 10.1002/bjs.10105, lire en ligne)
- ↑ Ramy Behman, Avery B. Nathens, Nicole Look Hong et Petros Pechlivanoglou, « Evolving Management Strategies in Patients with Adhesive Small Bowel Obstruction: a Population-Based Analysis », Journal of Gastrointestinal Surgery: Official Journal of the Society for Surgery of the Alimentary Tract, vol. 22, no 12, , p. 2133–2141 (ISSN 1873-4626, PMID 30051307, DOI 10.1007/s11605-018-3881-z, lire en ligne)
- ↑ Stefania Tamburrini, Marina Lugarà, Francesco Iaselli et Pietro Paolo Saturnino, « Diagnostic Accuracy of Ultrasound in the Diagnosis of Small Bowel Obstruction », Diagnostics (Basel, Switzerland), vol. 9, no 3, (ISSN 2075-4418, PMID 31390727, Central PMCID 6787646, DOI 10.3390/diagnostics9030088, lire en ligne)
- ↑ Maryam Al Ali, Sarah Jabbour et Salma Alrajaby, « ACUTE ABDOMEN systemic sonographic approach to acute abdomen in emergency department: a case series », The Ultrasound Journal, vol. 11, no 1, , p. 22 (ISSN 2524-8987, PMID 31544223, Central PMCID 6755127, DOI 10.1186/s13089-019-0136-5, lire en ligne)
- ↑ Ekin Ozturk, Marianne van Iersel, Martijn Mwj Stommel et Yvonne Schoon, « Small bowel obstruction in the elderly: a plea for comprehensive acute geriatric care », World journal of emergency surgery: WJES, vol. 13, , p. 48 (ISSN 1749-7922, PMID 30377439, Central PMCID 6196030, DOI 10.1186/s13017-018-0208-z, lire en ligne)
- ↑ 14,0 et 14,1 Adrian A. Maung, Dirk C. Johnson, Greta L. Piper et Ronald R. Barbosa, « Evaluation and management of small-bowel obstruction », Journal of Trauma and Acute Care Surgery, vol. 73, , S362–S369 (ISSN 2163-0755, DOI 10.1097/ta.0b013e31827019de, lire en ligne)
- ↑ 15,0 et 15,1 (en) Ellen X. Sun, Core Radiology, Cambridge University Press (ISBN 9781108966450)
- ↑ Lyndsey E. Wessels, Richard Y. Calvo, Casey E. Dunne et Jason M. Bowie, « Outcomes in adhesive small bowel obstruction from a large statewide database: What to expect after nonoperative management », The Journal of Trauma and Acute Care Surgery, vol. 86, no 4, , p. 651–657 (ISSN 2163-0763, PMID 30907786, DOI 10.1097/TA.0000000000002196, lire en ligne)
- ↑ Martin D. Zielinski, Patrick W. Eiken, Michael P. Bannon et Stephanie F. Heller, « Small Bowel Obstruction—Who Needs an Operation? A Multivariate Prediction Model », World Journal of Surgery, vol. 34, no 5, , p. 910–919 (ISSN 0364-2313 et 1432-2323, DOI 10.1007/s00268-010-0479-3, lire en ligne)
- ↑ Adrian K. McGrath, Fatimah Suliman, Noel Thin et Ashish Rohatgi, « Adult intussusception associated with mesenteric Meckel's diverticulum and antimesenteric ileal polyp », BMJ case reports, vol. 12, no 9, (ISSN 1757-790X, PMID 31537591, Central PMCID 6754700, DOI 10.1136/bcr-2019-230612, lire en ligne)
- ↑ Ioana Baiu et Mary T. Hawn, « Small Bowel Obstruction », JAMA, vol. 319, no 20, 05 22, 2018, p. 2146 (ISSN 1538-3598, PMID 29800183, DOI 10.1001/jama.2018.5834, lire en ligne)
- ↑ Herbert Freund, Reoperative Abdominal Surgery, Jaypee Brothers Medical Publishers (P) Ltd., (ISBN 978-1-907816-55-0, lire en ligne), p. 193–193
- ↑ Jose J. Diaz, Faran Bokhari, Nathan T. Mowery et Jose A. Acosta, « Guidelines for Management of Small Bowel Obstruction », The Journal of Trauma: Injury, Infection, and Critical Care, vol. 64, no 6, , p. 1651–1664 (ISSN 0022-5282, DOI 10.1097/ta.0b013e31816f709e, lire en ligne)
- ↑ Marco Ceresoli, Federico Coccolini, Fausto Catena et Giulia Montori, « Water-soluble contrast agent in adhesive small bowel obstruction: a systematic review and meta-analysis of diagnostic and therapeutic value », The American Journal of Surgery, vol. 211, no 6, , p. 1114–1125 (ISSN 0002-9610, DOI 10.1016/j.amjsurg.2015.06.012, lire en ligne)
- ↑ 23,0 et 23,1 Marco Ceresoli, Federico Coccolini, Fausto Catena et Giulia Montori, « Water-soluble contrast agent in adhesive small bowel obstruction: a systematic review and meta-analysis of diagnostic and therapeutic value », The American Journal of Surgery, vol. 211, no 6, , p. 1114–1125 (ISSN 0002-9610, DOI 10.1016/j.amjsurg.2015.06.012, lire en ligne)
- ↑ (en) B. C. Branco, G. Barmparas, B. Schnüriger et K. Inaba, « Systematic review and meta-analysis of the diagnostic and therapeutic role of water-soluble contrast agent in adhesive small bowel obstruction », British Journal of Surgery, vol. 97, no 4, , p. 470–478 (DOI 10.1002/bjs.7019, lire en ligne)
- ↑ Dean Schraufnagel, Sean Rajaee et Frederick Heaton Millham, « How many sunsets? Timing of surgery in adhesive small bowel obstruction », Journal of Trauma and Acute Care Surgery, vol. 74, no 1, , p. 181–189 (ISSN 2163-0755, DOI 10.1097/ta.0b013e31827891a1, lire en ligne)
- ↑ Muhammad S. Sajid, Amir H. Khawaja, Parv Sains et Krishna K. Singh, « A systematic review comparing laparoscopic vs open adhesiolysis in patients with adhesional small bowel obstruction », The American Journal of Surgery, vol. 212, no 1, , p. 138–150 (ISSN 0002-9610, DOI 10.1016/j.amjsurg.2016.01.030, lire en ligne)
- ↑ Tom Wiggins, Sheraz R. Markar et Adrian Harris, « Laparoscopic adhesiolysis for acute small bowel obstruction: systematic review and pooled analysis », Surgical Endoscopy, vol. 29, no 12, , p. 3432–3442 (ISSN 0930-2794 et 1432-2218, DOI 10.1007/s00464-015-4114-0, lire en ligne)
- ↑ Donal B. O’Connor et Desmond C. Winter, « The role of laparoscopy in the management of acute small-bowel obstruction: a review of over 2,000 cases », Surgical Endoscopy, vol. 26, no 1, , p. 12–17 (ISSN 0930-2794 et 1432-2218, DOI 10.1007/s00464-011-1885-9, lire en ligne)
- ↑ Christian Beardsley, Ruelan Furtado, Charles Mosse et Sivakumar Gananadha, « Small bowel obstruction in the virgin abdomen: the need for a mandatory laparotomy explored », The American Journal of Surgery, vol. 208, no 2, , p. 243–248 (ISSN 0002-9610, DOI 10.1016/j.amjsurg.2013.09.034, lire en ligne)
- ↑ Yvonne Ying-Ru Ng, James Chi-Yong Ngu et Andrew Siang-Yih Wong, « Small bowel obstruction in the virgin abdomen: time to challenge surgical dogma with evidence », ANZ Journal of Surgery, vol. 88, no 1-2, , p. 91–94 (ISSN 1445-1433, DOI 10.1111/ans.13714, lire en ligne)
- ↑ Yasuyuki Fukami, Yuji Kaneoka, Atsuyuki Maeda et Yuichi Takayama, « Clinical Effect of Water-Soluble Contrast Agents for Small Bowel Obstruction in the Virgin Abdomen », World Journal of Surgery, vol. 42, no 1, , p. 88–92 (ISSN 0364-2313 et 1432-2323, DOI 10.1007/s00268-017-4174-5, lire en ligne)
- ↑ Sarah E Cousins, Emma Tempest et David J Feuer, « Surgery for the resolution of symptoms in malignant bowel obstruction in advanced gynaecological and gastrointestinal cancer », Cochrane Database of Systematic Reviews, (ISSN 1465-1858, DOI 10.1002/14651858.cd002764.pub2, lire en ligne)
- ↑ Johannes Bükki, « Re: Recommendations for Bowel Obstruction With Peritoneal Carcinomatosis by Laval et al. », Journal of Pain and Symptom Management, vol. 48, no 5, , e5–e6 (ISSN 0885-3924, DOI 10.1016/j.jpainsymman.2014.07.006, lire en ligne)
- ↑ 34,0 34,1 et 34,2 Henry John Murray Ferguson, Claire Irene Ferguson, John Speakman et Tariq Ismail, « Management of intestinal obstruction in advanced malignancy », Annals of Medicine and Surgery, vol. 4, no 3, , p. 264–270 (ISSN 2049-0801, DOI 10.1016/j.amsu.2015.07.018, lire en ligne)
- ↑ Xingang Peng, Peige Wang, Shikuan Li et Guangyong Zhang, « Randomized clinical trial comparing octreotide and scopolamine butylbromide in symptom control of patients with inoperable bowel obstruction due to advanced ovarian cancer », World Journal of Surgical Oncology, vol. 13, no 1, (ISSN 1477-7819, DOI 10.1186/s12957-015-0455-3, lire en ligne)
- ↑ George P. Obita, Elaine G. Boland, David C. Currow et Miriam J. Johnson, « Somatostatin Analogues Compared With Placebo and Other Pharmacologic Agents in the Management of Symptoms of Inoperable Malignant Bowel Obstruction: A Systematic Review », Journal of Pain and Symptom Management, vol. 52, no 6, , p. 901–919.e1 (ISSN 0885-3924, DOI 10.1016/j.jpainsymman.2016.05.032, lire en ligne)
- ↑ Sharif H. Ellozy, Michael T. Harris, Joel J. Bauer et Stephen R. Gorfine, « Early Postoperative Small-Bowel Obstruction », Diseases of the Colon & Rectum, vol. 45, no 9, , p. 1214–1217 (ISSN 0012-3706, DOI 10.1007/s10350-004-6395-6, lire en ligne)
- ↑ 38,0 et 38,1 S. B. S. Sajja et M. Schein, « Early postoperative small bowel obstruction », British Journal of Surgery, vol. 91, no 6, , p. 683–691 (ISSN 0007-1323 et 1365-2168, DOI 10.1002/bjs.4589, lire en ligne)
- ↑ Naeem Goussous, Kevin M. Kemp, Michael P. Bannon et Michael L. Kendrick, « Early postoperative small bowel obstruction: open vs laparoscopic », The American Journal of Surgery, vol. 209, no 2, , p. 385–390 (ISSN 0002-9610, DOI 10.1016/j.amjsurg.2014.07.012, lire en ligne)



