Maladie vasculaire athérosclérotique
| Classe de maladie | |||
 Athérosclérose de l'aorte (maladie artérielle périphérique aorto-iliaque) | |||
| Caractéristiques | |||
|---|---|---|---|
| Signes | Aucun signe clinique | ||
| Symptômes |
Asymptomatique | ||
| Étiologies |
Athérosclérose | ||
| Informations | |||
| SNOMED CT ID | 400047006 | ||
| Spécialités | Chirurgie vasculaire, gastro-entérologie, chirurgie générale, néphrologie | ||
| |||
La maladie vasculaire athérosclérotique (MVAS) est causée par une sténose du réseau artériel qui entraîne un déséquilibre entre la demande est l'apport sanguin dans diverts organes.
Classification
La MVAS est une grande catégorie composée des maladies suivantes:
- la maladie artérielle périphérique infra-iliaque (MAP)
- la maladie artérielle périphérique aorto-iliaque
- les anévrismes autres que aortiques (lorsque causés par l'athérosclérose)
- la maladie artérielle périphérique des membres supérieurs
- l'ischémie mésentérique chronique
- la sténose des artères rénales
- la sténose de l'artère sous-clavière.
La MCAS, la maladie cérébébrovasculaire (AVC ischémique, sténose des carotides, démence vasculaire, insuffisance vertébro-basillaire) et la neuropathie optique ischémique antérieure ont la même physiopathologie mais ne sont pas inclues dans la MVAS.
Étiologies
L'étiologie de la MVAS est l'athérosclérose.[1]
Physiopathologie
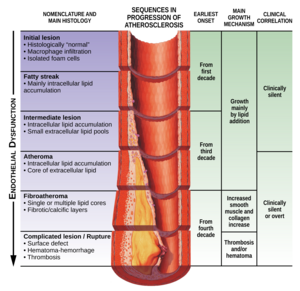
La physiopathologie de l'athérosclérose implique des interactions complexes entre le cholestérol et les cellules vasculaires dont les détails dépassent le cadre de cet article. La plaque d'athérosclérose s'accumule lentement à l'intérieur des artères. L'athérosclérose entraîne le rétrécissement des vaisseaux sanguins, et donc des limitations du flux sanguin. La limitation spécifique du flux sanguin dépend de l'étendue du rétrécissement des vaisseaux sanguins. Pour les personnes atteintes d'athérosclérose des vaisseaux, mais qui ne subissent pas de claudication, cela est dû aux artères qui compensent l'accumulation de plaque en se dilatant pour préserver le flux à travers le vaisseau. Pour ceux qui souffrent de claudication intermittente ou d'ischémie, le débit sanguin est encore suffisant pour alimenter les organes au repos avec suffisamment de sang car l'étendue de la sténose n'est pas significative. Pendant la marche ou la digestion, les organes ont besoin de plus de flux sanguin et, à leur tour, les vaisseaux essaieront de se dilater pour fournir suffisamment de sang. Cependant, pour les personnes atteintes de MVAS, l'artère ne peut plus se dilater et l'inadéquation entre l'offre et la demande du sang déclenche les symptômes . La diminution des demandes énergétiques du muscle (en ralentissant ou en s'arrêtant) permet à l'apport sanguin de «rattraper» et les symptômes ischémiques disparaissent. Au fur et à mesure que la sténose se poursuit, même parfois en pleine occlusion, cela entraîne une douleur au repos a cause d'une mauvaise perfusion des nerfs. [2][3]
Au fur et à mesure que le rétrécissement progresse ou obstrue complètement l'artère, le flux sanguin se déplace vers des artères plus petites parallèles à l'artère malade et forme ainsi une circulation collatérale. Bien que ce flux collatéral préserve la perfusion distale, le réseau de vaisseaux plus petits n'achemine jamais autant de flux sanguin que l'artère principale. [2][3]
Présentation clinique
Facteurs de risque
Les facteurs de risque se divisent en deux catégories ; modifiable et non modifiable[4][5][6][7] :
- modifiables
- le tabagisme[RR: 3-4] (facteur de risque modifiable le plus important)
- le diabète sucré (relation claire avec les niveaux d'A1c)
- l'HTA
- les dyslipidémies
- non-modifiables
Questionnaire
La MVAS sera souvent asymptomatique, cependant ses différentes formes pourront donner :
- de la claudication intermittente des membres inférieurs pour la MAP infra-iliaque
- des difficultés érectiles et de la claudication des fesses pour la MAP aorto-iliaque
- des syncopes lorsque le membre supérieur est levé en l'air pour la sténose de la sous-clavière (syndrome du vol de la sous-clavière)
- des douleurs abdominales post-prandiales pour l'ischémie mésentérique chronique
- une douleur abdominale pour l'AAA
- une TA difficile à contrôler et réfractaire au traitement pour la sténose des artères rénales.
Examen clinique
À l'examen clinique:
- iI est possible qu'il n'y ait pas de signes cliniques
- aux signes vitaux, une TA élevée et difficile à contrôler pourrait évoquer une sténose des artères rénales
- à l'examen vasculaire périphérique, rechercher une diminution des pouls, des souffles et un refill capillaire augmenté aux membres inférieurs dans la MAP infra et aorto-iliaque
- à l'examen des membres inférieurs et l'examen vasculaire périphérique[4], rechercher de la froideur, des plaies, un érythème, une perte de pilosité, un test de Buerguer positif[note 1]
- à l'examen cardiovasculaire rechercher des souffles ou des signes d'insuffisance cardiaque (la MCAS étant très co-morbide)
- à l'examen abdominal rechercher d'un souffle abdominal, évocateur d'une MAP aorto-iliaque, d'une sténose des artères rénales ou d'une ischémie mésentérique chronique; une masse pulsatile pourrait indiquer un AAA.
Traitement
Le traitement de la MVAS passera par :
- le contrôle des facteurs de risques, dont l'arrêt tabagique et la dyslipidémie
- des antiplaquettaires
- parfois des interventions chirurgicales pour corriger les sténoses.
Pour les détails sur le traitement, vous référer aux pages des maladies spécifiques.
Notes
- ↑ Attention, les cellulites sont fréquentes chez les patients atteint de MAP et pourraient causer un test de Buerger négatif.
Références
- ↑ « Canadian Society for Vascular Surgery - Maladie vasculaire périphérique (MVP) », sur canadianvascular.ca (consulté le 22 novembre 2022)
- ↑ 2,0 et 2,1 Michael R. Zemaitis, Julia M. Boll et Mark A. Dreyer, StatPearls, StatPearls Publishing, (PMID 28613496, lire en ligne)
- ↑ 3,0 et 3,1 Naomi M. Hamburg et Mark A. Creager, « Pathophysiology of Intermittent Claudication in Peripheral Artery Disease », Circulation Journal: Official Journal of the Japanese Circulation Society, vol. 81, no 3, , p. 281–289 (ISSN 1347-4820, PMID 28123169, DOI 10.1253/circj.CJ-16-1286, lire en ligne)
- ↑ 4,0 et 4,1 (en) L. Norgren, W. R. Hiatt, J. A. Dormandy et M. R. Nehler, « Inter-Society Consensus for the Management of Peripheral Arterial Disease (TASC II) », Journal of Vascular Surgery, série TASC II, vol. 45, no 1, Supplement, , S5–S67 (ISSN 0741-5214, DOI 10.1016/j.jvs.2006.12.037, lire en ligne)
- ↑ Iftikhar J. Kullo, Kent R. Bailey, Sharon L. R. Kardia et Thomas H. Mosley, « Ethnic differences in peripheral arterial disease in the NHLBI Genetic Epidemiology Network of Arteriopathy (GENOA) study », Vascular Medicine (London, England), vol. 8, no 4, , p. 237–242 (ISSN 1358-863X, PMID 15125483, DOI 10.1191/1358863x03vm511oa, lire en ligne)
- ↑ W. T. Meijer, D. E. Grobbee, M. G. Hunink et A. Hofman, « Determinants of peripheral arterial disease in the elderly: the Rotterdam study », Archives of Internal Medicine, vol. 160, no 19, , p. 2934–2938 (ISSN 0003-9926, PMID 11041900, DOI 10.1001/archinte.160.19.2934, lire en ligne)
- ↑ Smriti Murali Krishna, Joseph V. Moxon et Jonathan Golledge, « A Review of the Pathophysiology and Potential Biomarkers for Peripheral Artery Disease », International Journal of Molecular Sciences, vol. 16, no 5, , p. 11294–11322 (ISSN 1422-0067, PMID 25993296, Central PMCID 4463701, DOI 10.3390/ijms160511294, lire en ligne)
