Inhibiteurs de DPP-4
| Classe de médicament | |
 | |
| Caractéristiques | |
|---|---|
| Classes | Hypoglycémiants oraux |
| Voies d'administration |
PO |
| Informations | |
| Terme anglais | inhibiteurs de la DPP-4, inhibiteur de la dipeptidyl peptidase-4 |
| Autres noms | gliptines |
| Wikidata ID | Q419770 |
| SNOMED CT ID | 703351007 |
| Spécialité | Endocrinologie |
|
| |
Les inhibiteurs de la dipeptidyl peptidase 4 (' Inhibiteurs de DPP-4 ' ou gliptines) sont une classe de hypoglycémiants oraux qui bloquent la enzyme dipeptidyl peptidase-4 (DPP-4). Ils peuvent être utilisés pour traiter diabète sucré de type 2.
Le premier agent de la classe - sitagliptine - a été approuvé par FDA en 2006.[1]
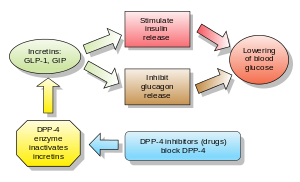
Glucagon augmente les niveaux de glucose sanguin, et les inhibiteurs de DPP-4 réduisent les niveaux de glucagon et de glucose sanguin. Le mécanisme des inhibiteurs de la DPP-4 est d'augmenter les niveaux incrétine (GLP-1 et GIP), [2][3][4] qui inhibent la libération de glucagon, ce qui à son tour augmente la sécrétion d'insuline, diminue la vidange gastrique et diminue les taux de glycémie.
Une méta-analyse de 2018 n'a trouvé aucun effet favorable des inhibiteurs de la DPP-4 sur la mortalité toutes causes confondues, la mortalité cardiovasculaire, infarctus du myocarde ou accident vasculaire cérébral chez les patients atteints de diabète de type 2. [5]
Généralement utilisé comme traitement de deuxième ou troisième ligne pour le diabète sucré de type 2. Ils peuvent être utilisés en monothérapie ou en thérapie combinée.
Indications
Contre-indications
Effets indésirables
- Dans les études contrôlées de la sitagliptine (en monothérapie et en association), l'incidence globale des effets indésirables / arrêt similaire au placebo
- Les effets indésirables les plus fréquemment rapportés comprennent la rhinopharyngite, l'URI, l'AH
- La surveillance post-commercialisation a révélé une association avec la sitagliptine et le développement d'une pancréatite aiguë
- Variables confondantes telles que le diabète, l'hypercholestérolémie, l'hypertriglycéridémie, l'obésité
- Également des rapports post-commercialisation de réactions allergiques graves (y compris des réactions anaphylactiques, angioedème, SJS)
- Des études sur d'autres médicaments de cette classe signalent en outre une lymphopénie, une toux, un œdème périphérique, une transaminite et une hypertension.
- Les autres effets indésirables signalés chez les patients prenant cette classe de médicaments comprennent des douleurs articulaires
Des effets indésirables, dont une rhinopharyngite, des maux de tête, des nausées, une hypersensibilité et des réactions cutanées, ont été observés dans les études cliniques.
Insuffisance cardiaque (association possible)
Les inhibiteurs de Dipeptidyl-Peptidase IV sont peut être[6][7][8][9][10][11][12] ou peut être pas[13][14][15][16] associés à l'insufisance cardiaque.
Cancer du pancréas (association possible)
Une étude de 2013 sur l'inhibiteur de la DPP-4, la sitagliptine, a révélé "des changements inquiétants dans les pancréas des rats qui pourraient conduire à un cancer du pancréas" .[17] Un deuxième article des mêmes auteurs a rapporté une augmentation des lésions précancéreuses dans les pancréas des donneurs d'organes qui avait pris des inhibiteurs du GLP-1. [18] En réponse à ces rapports, la FDA des États-Unis et l'Agence européenne des médicaments ont chacune entrepris des examens indépendants de toutes les données cliniques et précliniques relatives à l'association possible des inhibiteurs de la DPP-4 avec le cancer du pancréas. Dans une lettre conjointe adressée au New England Journal of Medicines, les agences ont déclaré que "les deux agences conviennent que les affirmations concernant une association causale entre les médicaments à base d'incrétine et la pancréatite ou le cancer du pancréas, telles qu'exprimées récemment dans la littérature scientifique et dans les médias, sont incompatibles avec les données actuelles. La FDA et l'EMA ne sont pas encore parvenues à une conclusion finale concernant une telle relation causale. Bien que la totalité des données qui ont été examinées rassurent, la pancréatite continuera d'être considérée comme un risque associé à ces médicaments jusqu'à ce que plus de données soient disponibles; les deux agences continuent d'enquêter sur ce signal de sécurité.[19]
Des poursuites ont été déposées dans lesquelles des plantiffs qui ont développé un cancer du pancréas affirment que les inhibiteurs ou les incrétines du DPP-IV ont un rôle causal dans le développement de leurs cancers.[20][21]
Pharmacologie clinique
Mode d'action
- Inhibe DPP-4, une enzyme exprimée à la surface de la plupart des types de cellules
- DPP-4 désactive d'autres peptides bioactifs, y compris les incrétines comme le glucagon-like peptide-1 (GLP-1).
- Le GLP-1 est sécrété en réponse aux nutriments, stimulant la libération d'insuline glucose-dépendante des cellules bêta pancréatiques, qui à son tour diminue le taux de sucre dans le sang.
- Réduit également la vidange gastrique et inhibe la libération postprandiale de glucagon
Inhibiteurs DPP-4 approuvés par la FDA
| Marque | Ingrédients actifs) |
|---|---|
| Januvia | sitagliptine |
| Janumet | sitagliptine, metformine |
| Janumet XR | sitagliptine, metformine ER |
| Onglyza | saxagliptine |
| Kombiglyze XR | saxagliptine, metformine ER |
| Tradjenta | linagliptine |
| Glyxambi | linagliptine, empagliflozine |
| Jentadueto | linagiptine, metformine |
| Nesina | alogliptine |
| Kazano | alogliptine, metformine |
| Oseni | alogliptine, pioglitazone |
Références
- Cette page a été modifiée ou créée le 2020/03/30 à partir de DPP-4 inhibitors (229353), écrite par les contributeurs de WikEM et partagée sous la licence CC-BY-SA 4.0. Le contenu original est disponible à https://wikem.org/wiki/DPP-4_inhibitors.
- ↑ Modèle:Cite press release
- ↑ C McIntosh, H Demuth, J Pospisilik et R Pederson, « Dipeptidyl peptidase IV inhibitors: How do they work as new antidiabetic agents? », Regulatory Peptides, vol. 128, no 2, , p. 159–65 (PMID 15780435, DOI 10.1016/j.regpep.2004.06.001)
- ↑ Margaret T Behme, John Dupré et Thomas J McDonald, « Glucagon-like peptide 1 improved glycemic control in type 1 diabetes », BMC Endocrine Disorders, vol. 3, no 1, , p. 3 (PMID 12697069, Central PMCID 154101, DOI 10.1186/1472-6823-3-3)
- ↑ J. Dupre, M. T. Behme, I. M. Hramiak, P. McFarlane, M. P. Williamson, P. Zabel et T. J. McDonald, « Glucagon-like peptide I reduces postprandial glycemic excursions in IDDM », Diabetes, vol. 44, no 6, , p. 626–30 (PMID 7789625, DOI 10.2337/diabetes.44.6.626)
- ↑ Sean L. Zheng, Alistair J. Roddick, Rochan Aghar-Jaffar, Matthew J. Shun-Shin, Darrel Francis, Nick Oliver et Karim Meeran, « Association Between Use of Sodium-Glucose Cotransporter 2 Inhibitors, Glucagon-like Peptide 1 Agonists, and Dipeptidyl Peptidase 4 Inhibitors With All-Cause Mortality in Patients With Type 2 Diabetes », JAMA, vol. 319, no 15, , p. 1580–1591 (PMID 29677303, Central PMCID 5933330, DOI 10.1001/jama.2018.3024)
- ↑ Li L, Li S, Deng K, Liu J, Vandvik PO, Zhao P et al., « Dipeptidyl peptidase-4 inhibitors and risk of heart failure in type 2 diabetes: systematic review and meta-analysis of randomised and observational studies. », BMJ, vol. 352, , i610 (PMID 26888822, DOI 10.1136/bmj.i610, lire en ligne)
- ↑ Scirica BM, Braunwald E, Raz I, Cavender MA, Morrow DA, Jarolim P et al., « Heart failure, saxagliptin, and diabetes mellitus: observations from the SAVOR-TIMI 53 randomized trial. », Circulation, vol. 130, no 18, , p. 1579-88 (PMID 25189213, DOI 10.1161/CIRCULATIONAHA.114.010389, lire en ligne) Review in: Ann Intern Med. 2015 Apr 21;162(8):JC11
- ↑ Udell JA, Cavender MA, Bhatt DL, Chatterjee S, Farkouh ME, Scirica BM (2015) Glucose-lowering drugs or strategies and cardiovascular outcomes in patients with or at risk for type 2 diabetes: a meta-analysis of randomised controlled trials. Lancet Diabetes Endocrinol 3 (5):356-66. DOI:10.1016/S2213-8587(15)00044-3 PMID: 25791290
- ↑ Clifton P, « Do dipeptidyl peptidase IV (DPP-IV) inhibitors cause heart failure? », Clin Ther, vol. 36, no 12, , p. 2072-9 (PMID 25453730, DOI 10.1016/j.clinthera.2014.10.009, lire en ligne)
- ↑ Weir DL, McAlister FA, Senthilselvan A, Minhas-Sandhu JK, Eurich DT, « Sitagliptin use in patients with diabetes and heart failure: a population-based retrospective cohort study. », JACC Heart Fail, vol. 2, no 6, , p. 573-82 (PMID 24998080, DOI 10.1016/j.jchf.2014.04.005, lire en ligne)
- ↑ Monami M, Dicembrini I, Mannucci E, « Dipeptidyl peptidase-4 inhibitors and heart failure: a meta-analysis of randomized clinical trials. », Nutr Metab Cardiovasc Dis, vol. 24, no 7, , p. 689-97 (PMID 24793580, DOI 10.1016/j.numecd.2014.01.017, lire en ligne)
- ↑ Scirica BM, Bhatt DL, Braunwald E, Steg PG, Davidson J, Hirshberg B et al., « Saxagliptin and cardiovascular outcomes in patients with type 2 diabetes mellitus. », N Engl J Med, vol. 369, no 14, , p. 1317-26 (PMID 23992601, DOI 10.1056/NEJMoa1307684, lire en ligne) Review in: Ann Intern Med. 2014 Jan 21;160(2):JC8-9
- ↑ Sengwee Toh, Christian Hampp, Marsha E. Reichman et David J. Graham, « Risk for Hospitalized Heart Failure Among New Users of Saxagliptin, Sitagliptin, and Other Antihyperglycemic Drugs: A Retrospective Cohort Study », Annals of Internal Medicine, vol. 164, no 11, , p. 705–714 (ISSN 1539-3704, PMID 27110660, Central PMCID 5178978, DOI 10.7326/M15-2568, lire en ligne)
- ↑ Kristian B. Filion, Laurent Azoulay, Robert W. Platt et Matthew Dahl, « A Multicenter Observational Study of Incretin-based Drugs and Heart Failure », The New England Journal of Medicine, vol. 374, no 12, , p. 1145–1154 (ISSN 1533-4406, PMID 27007958, DOI 10.1056/NEJMoa1506115, lire en ligne)
- ↑ Faiez Zannad, Christopher P. Cannon, William C. Cushman et George L. Bakris, « Heart failure and mortality outcomes in patients with type 2 diabetes taking alogliptin versus placebo in EXAMINE: a multicentre, randomised, double-blind trial », Lancet (London, England), vol. 385, no 9982, , p. 2067–2076 (ISSN 1474-547X, PMID 25765696, DOI 10.1016/S0140-6736(14)62225-X, lire en ligne)
- ↑ D. T. Eurich, D. L. Weir, S. H. Simpson et A. Senthilselvan, « Risk of new-onset heart failure in patients using sitagliptin: a population-based cohort study », Diabetic Medicine: A Journal of the British Diabetic Association, vol. 33, no 5, , p. 621–630 (ISSN 1464-5491, PMID 26206341, DOI 10.1111/dme.12867, lire en ligne)
- ↑ Matveyenko AV, Dry S, Cox HI, et al., « Beneficial endocrine but adverse exocrine effects of sitagliptin in the human islet amyloid polypeptide transgenic rat model of type 2 diabetes: interactions with metformin », Diabetes, vol. 58, no 7, , p. 1604–15 (PMID 19403868, Central PMCID 2699878, DOI 10.2337/db09-0058)
- ↑ Butler AE, Campbell-Thompson M, Gurlo T, Dawson DW, Atkinson M, Butler PC, « Marked expansion of exocrine and endocrine pancreas with incretin therapy in humans with increased exocrine pancreas dysplasia and the potential for glucagon-producing neuroendocrine tumors », Diabetes, vol. 62, no 7, , p. 2595–604 (PMID 23524641, DOI 10.2337/db12-1686)
- ↑ « Pancreatic Safety of Incretin-Based Drugs — FDA and EMA Assessment — NEJM »
- ↑ « Latest Januvia Lawsuits Alleging Pancreatic Cancer Help: Resource4thePeople Reports Cases Continue To Be Filed in Federal Multidistrict Litigation », DG, DigitalJournal.com, (consulté le 14 octobre 2013)
- ↑ « IN RE: INCRETIN MIMETICS PRODUCTS LIABILITY LITIGATION », USJP, United States Judicial Panel on Multidistric Litigation, (consulté le 26 août 2013)
