Endocardite
| Classe de maladie | |||
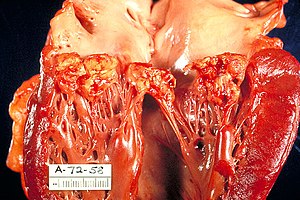 Endocardite à Haemophilus parainfluenzae sur un coeur atteint | |||
| Caractéristiques | |||
|---|---|---|---|
| Signes | Tâches de Roth, Splénomégalie, Confusion, Adénopathies, Pétéchies, Hépatomégalie, Ataxie , Signes méningés, Crépitants, Souffle cardiaque, ... [+] | ||
| Symptômes |
Frissons, Anorexie , Myalgies, Nausées, Céphalée , Diaphorèse nocturne, Fatigue , Arthralgie , Vomissement , Température corporelle élevée | ||
| Étiologies |
Lupus érythémateux disséminé, Syndrome des anticorps antiphospholipides, Pseudomonas aeruginosa, Streptococcus viridans, Granulomatose avec polyangéite, Staphyloccocus aureus, Streptococcus bêta-hémolytique du groupe A, Pneumocoques, Bactéries à Gram négatif, Enterococcus sp., ... [+] | ||
| Informations | |||
| Terme anglais | Endocarditis | ||
| Wikidata ID | Q82504 | ||
| SNOMED CT ID | 56819008 | ||
| Spécialités | Cardiologie, Médecine interne, Médecine familiale, Médecine d'urgence | ||
| |||
L'endocardite est une inflammation de l'endocarde, la membrane tapissant les chambres cardiaques et les valves.
Il existe deux types d'endocardite:
- Aiguë: Elle est une maladie fébrile qui endommage rapidement les structures cardiaques et se propage par dissémination hématologique. En absence de traitement, elle peut rapidement engendrer des complications en l'espace de quelques semaines.
- Subaiguë: Elle a un processus de maladie plus lent et peut être présente pendant des semaines à des mois avec une progression progressive, sauf si elle est compliquée par un événement embolique majeur ou une structure rompue.
Classification
L'endocardite infectieuse inclut:[1]
- l'endocardite bactérienne aiguë et subaiguë
- l'endocardite fongique
- l'endocardite virale (entité controversée)[2].
Il existe d'autres formes moins fréquentes d'endocardite :
- l'endocardite marantique (associée aux néoplasies productrices de mucine)[3]
- les lésions de Libman-Sacks (associé au lupus érythémateux disséminé par dépôts complexes immuns circulants)
- des formes associées aux atteintes auto-immunes.
Épidémiologie
L'endocardite infectieuse est une complication fréquente de la cardiopathie congénitale ou de la cardiopathie rhumatismale. Il est important de mentionner, cependant, que l'endocardite infectieuse peut aussi se présenter chez les individus sans malformations cardiaques. Dans les pays développés, la cardiopathie congénitale est le facteur prédisposant le plus important. Chez près de 30% des patients présentant une endocardite infectieuse, un facteur prédisposant est connu et identifié. Si des antécédents d'intervention dentaire sont connus, l'intervalle de temps entre l'apparition des symptômes et l'intervention varie de 1 à 6 mois. Les risques d'endocardite suivant une chirurgie cardiaque de routine sont faibles sauf s'il y a installation de matériel prothétique ; cela peut alors devenir un facteur prédisposant. Dans les pays développés, l'incidence de l'endocardite varie de 2,6 à 7 cas pour 100 000 habitants par an. L'âge médian des patients atteints d'endocardite est de 58 ans. [4][1]1-6% des endocardites sont d'origine fongique.[5] Environ 2.5% des endocardites sont d'origine non-infectieuse. Cette catégorie regroupe des endocardites marantiques, ou paranéoplasiques, des endocardites associées au lupus érythémateux disséminé ou associées au syndrome des anticorps antiphospholipides.[6]
Étiologies
Les germes les plus fréquemment incriminés dans une endocardite aiguë:
- staphyloccocus aureus (Staphylocoque doré): principale bactérie retrouvée dans la population adulte et pédiatrique
- streptococcus bêta-hémolytique du groupe A
- pneumocoques
- bactéries à Gram négatif
- Les bactéries pseudomonas aeruginosa et serratia marescens sont fréquemment observés chez les utilisateurs de drogues injectables.
Les germes les plus fréquemment incriminés dans une endocardite sub-aiguë :
- streptococcus viridans (dont Streptococcus bovis): particulièrement observé lors d'intervention dentaire.
Les germes plus rarement incriminés dans une endocardite sub-aiguë :
- streptococcus bêta-hémolytique du groupe A
- enterococcus sp.
- staphylococcus à coagulase négative (Staphylococcus saprophyticus, Staphylococcus epidermidis): particulièrement rencontré chez les patients avec cathéter central veineux à demeure[7][8][9][10][11]
- bactéries à Gram négatif à croissance fastidieuse (historiquement le groupe HACEK)
- fungi (ex, Candida sp, Aspergillus sp[12]): davantage présent chez les porteurs de valves prothétiques, les utilisateurs de drogues intraveineuses et les patients avec cardiostimulateur[5]
Étiologies de l'endocardite non-infectieuse ou marantique [3]
- lupus érythémateux disséminé
- Néoplasie productrice de mucine (ex, adénocarcinome du poumon, néoplasme du pancréas, du côlon)[13]
- syndrome des anticorps antiphospholipides
- granulomatose avec polyangéite
Physiopathologie
L'endocardite bactérienne peut être causée par une lésion endothéliale qui occasionne une infection directe par des organismes virulents ou par le développement d'un thrombus plaquettaire-fibrine non infecté qui devient un nid pour une bactériémie transitoire, sauf dans le cas de S. aureus, qui peut infecter l'endothélium intact. Ces organismes pénètrent dans la circulation sanguine de la peau, des surfaces muqueuses ou des sites précédemment infectés et adhèrent au thrombus non bactérien en raison de dommages valvulaires ou d'un flux sanguin turbulent. En l'absence de défenses de l'hôte, les bactéries sont autorisées à proliférer en formant de petites colonies et à se répandre dans la circulation sanguine. L'infection du côté gauche est beaucoup plus courante que l'infection du côté droit, sauf pour les utilisateurs de drogues intraveineuses. [14][4]
Dans le cas de l'endocardite non-infectieuse, telle que dans l'endocardite associée au lupus érythémateux disséminé, des complexes immuns peuvent donner naissance à des végétations friables constituées de plaquettes et fibrine, qui s'accolent au niveau de la valvule (lésion de Libman-Sacks). Il en va de même pour le syndrome des anticorps antiphospholipides. [15]
Les endocardites marastiques sont associées à un phénomène d'hypercoagulabilité causé par les cellules cancéreuses et à la réponse inflammatoire de l'hôte.[16]
Présentation clinique
Facteurs de risque
Voici les principaux facteurs de risques :[1][17]
- utilisateur de drogues intraveineuses
- valvulopathies : antécédent d'atteinte valvulaire cardiaque (rhumatisme articulaire aiguë), remplacement valvulaire
- immunosuppression : diabète, corticostéroïdes
- Âge avancé
- Implantation ou intervention sur un stimulateur cardiaque.
- cardiopathies congénitales
- cathéter veineux central
- soins dentaires.
Questionnaire
Le tableau clinique d'une endocardite aiguë est souvent insidieux:
- Les symptômes constitutionnels prédominent souvent avec de la fièvre et frissons.
- Certains décriront également de la fatigue, de la perte d'appétit et même de la diaphorèse nocturne.
- La chronologie des symptômes est souvent d'au moins quelques semaines.
- La clinique peut aussi inclure une constellation de symptômes non-spécifiques dont:
- myalgies
- arthralgies
- céphalées
- nausées avec ou sans vomissements.
Certains patients ne présenteront que des symptômes secondaires aux complications de l'endocardite. Voici quelques exemples :
- Insuffisance cardiaque droite : congestion veineuse périphérique, foie congestif
- Insuffisance cardiaque gauche : intolérance à l'effort, dyspnée, surcharge pulmonaire (toux, OTP, DPN)
- Atteintes auto-immunes : arthrite
- Atteintes emboliques : anévrisme mycotique (symptômes neurologiques)
Dans une grande proportion des cas, les patients présentent ou ont présenté un foyer infectieux récent. Il est important de chercher une porte d'entrée aux germes pathologiques. Plusieurs germes sont associées à une origine particulière (i.e. flore buccale, flore cutanée, foyer intestinal).
Examen clinique
À l'examen clinique[1] :
- Aux signes vitaux: fièvre
- À l'examen neurologique : des signes d'embolie ou d'abcès du SNC, dont des signes de méningisme, d'augmentation de la pression intracrânienne (ataxie, confusion), une altération du sensorium et des signes neurologiques focaux.
- À l'examen ophtalmologique : tâches de Roth
- À l'examen de la bouche : pétéchies buccales, mauvaise hygiène buccale (évoque un point d'entrée)
- À l'examen cardiaque : nouveau souffle cardiaque ou un changement dans la tonalité et intensité d'un souffle cardiaque, signes d'insuffisance cardiaque:
- Insuffisance cardiaque droite : OMI, foie congestif, augmentation de la TVC
- Insuffisance cardiaque gauche : surcharge pulmonaire (wheezing, crépitants)
- À l'examen abdominal : hépatomégalie et/ou splénomégalie.
- adénopathies
- À l'examen cutané : nodules d'Osler, pétéchies, lésions de Janeway et hémorragies en flammèche sous-unguéales. Ces signes se développent généralement tardivement au cours de la maladie.
Examens paracliniques
| Examens paracliniques | Commentaires |
|---|---|
| Hémocultures |
|
| Échocardiographie |
|
| Échographie trans-oesophagienne |
|
| PET-Scan cardiaque |
|
| ECG |
|
Approche clinique
L'approche clinique peut varier selon l'étiologie de l'endocardite[1].
Endocardite valvulaire native
- Elle implique principalement la valve mitrale suivie de la valve aortique.
- Elle est associée à une cardiopathie congénitale ou à une problématique causant une tension d'écoulement élevée.
- Elle est associée à un prolapsus valvulaire dans environ 20% des cas.
- Elle est associée à une maladie cardiaque dégénérative comme une valve aortique bicuspide, un syndrome de Marfan ou la syphilis.
Endocardite valvulaire prothétique
- L'endocardite valvulaire prothétique précoce est causée par Staphylococcus aureus et Staphylococcus epidermidis, incluant le SARM.
- Les streptocoques provoquent généralement une endocardite valvulaire prothétique tardive.
Endocardite infectieuse provoquée par des drogues injectables
- Le patient présente un nouveau souffle et/ou une douleur thoracique de type pleurétique.
- S. aureus est la cause la plus courante, mais les infections à SARM sont en augmentation.
- Atteinte classiquement du coeur droit, plus précisément de la valve tricuspidienne.
- Les bactéries à Gram négatif sont rarement impliquées.
Diagnostic
Les critères Duke permettent de diagnostiquer l'endocardite infectieuse advenant une incertitude clinique. Or, ceux-ci ne sont pas systématiquement utilisés en pratique. Les pierres d'assise du diagnostic demeurent la clinique, les hémocultures et l'imagerie cardiaque. Pour les formes non-infectieuses, elles se caractérisent par une imagerie cardiaque positive en présence d'hémocultures négatives.
| Critère | Type | Présent |
|---|---|---|
| Hémocultures positives pour les organismes typiques de l’endocardite infectieuse (S. viridans ou S. bovis, organismes HACEK[note 1], S. aureus sans autres sites primaires, entérocoques), issues de deux hémocultures séparées ou deux cultures positives provenant d’échantillons prélevés à > 12 heures d’intervalle, ou trois, ou une majorité de quatre hémocultures séparées (les premier et dernier échantillons étant prélevés à une heure d’intervalle) | Majeur | |
| Échocardiogramme avec masse intracardiaque oscillante sur la valve ou les structures de support, au niveau des flux de régurgitation, ou sur un matériel implanté en l’absence d’autres explications d’ordre anatomique, ou abcès, ou nouvelle déhiscence partielle de la valve prothétique ou nouvelle régurgitation valvulaire | Majeur | |
| Hémoculture positive unique pour Coxiella burnetii ou titre d’anticorps antiphase 1 IgG >1:800 | Majeur | |
| Prédisposition à une maladie cardiaque ou consommation de drogue par injection | Mineur | |
| Température > 38 °C | Mineur | |
| Phénomènes vasculaires : embolie artérielle, infarctus pulmonaire, anévrismes mycotiques, hémorragie intracrânienne, hémorragie de la conjonctive, placard érythémateux de Janeway | Mineur | |
| Phénomènes immunologiques : glomérulonéphrite, nœuds d’Osler, taches de Roth, facteur rhumatoïde | Mineur | |
| Preuve microbiologique : l’hémoculture est positive mais ne répond à aucun critère majeur mentionné ci-dessus ou preuve sérologique d’une infection active avec un organisme présentant les signes d’une endocardite (à l’exception du staphylocoque négatif quant à la coagulase et autres contaminants communs) | Mineur | |
| Résultat | Négatif | |
- Diagnostic : 2 Critères majeurs et 0 Critères mineurs
- Diagnostic : 1 Critères majeurs et 3 Critères mineurs
- Diagnostic : 0 Critères majeurs et 5 Critères mineurs
Traitement
Une consultation en infectiologie est toujours suggérée.[18]
Traitement médical
Endocardite infectieuse
En cas de situation urgente où l'attente des hémocultures est impossible à cause d'une instabilité hémodynamique, une antibiothérapie empirique doit être débutée. Lorsqu'un diagnostic définitif d'endocardite infectieuse est posé, l'antibiothérapie doit commencer le plus tôt possible après l'obtention des hémocultures. [26][27][1]
| Types d'endocardites | Traitement |
|---|---|
| Endocardite communautaire sur valve native ou prothétique (>12 mois post-chirurgical) | Gentamicine: 3 mg/kg/j IV en 1 injection
+ Ampiciline: 200 mg/kg/j IV en 6 injections + Cloxacilline: 150 mg/kg/j IV en 4–6 injections Si allergie à la pénicilline: Vancomycine + Gentamicine |
| Endocardite nosocomiale ou sur valve prothétique (<12 mois post-chirurgical) | Vancomycine: 30–60 mg/kg/j, perfusion IV continue (après dose de charge de 30 mg/kg)
+ Gentamicine: 3 mg/kg/j I, en 1 injection + Rifampicine: 900 mg (< 70 kg) ou 1200 mg (> 70 kg), IV ou PO en 1 ou 2 doses (uniquement pour valves prothétiques) |
La durée d'antibiothérapie est généralement de 2 à 6 semaines (à compter du jour où les cultures sont négatives[18]), dépendamment de l'organisme en cause.
Depuis l'étude POET (Partial Oral Treatment of Endocarditis) publié en 2019, la voie d'administration per os est désormais acceptée après une période initiale de 10 jours d'antibiothérapie IV et en absence de complications et de signes de sévérité chez les patients.[1]
| Organismes | Traitement |
|---|---|
| Streptocoques (viridans ou bovis[note 2]) résistants à la pénicilline | Valve native: Pénicilline G 24 millions UI/j durant 4 semaines + gentamicine 3 mg/kg/j (en 1 dose) durant 2 semaines OU ceftriaxone 2 g/j durant 4 semaines
Valve prothétique: Pénicilline G 24 millions UI/j + gentamicine 3 mg/kg/j (en 1 dose) durant 6 semaines OU ceftriaxone 2g/j + gentamicine 3 mg/kg/j (en 1 dose) durant 6 semaines |
| Streptocoques (viridans ou bovis[note 2]) sensibles à la pénicilline | Valve native: Pénicilline G 12-18 millions UI/j OU ceftriaxone 2 g/j durant 4 semaines
Valve prothétique: Pénicilline G 24 millions UI/j durant 4 semaines + gentamicine 3 mg/kg/j (en 1 dose) durant 2 semaines OU ceftriaxone 2 g/j durant 6 semaines ± gentamicine 3 mg/kg/j (en 1 dose) durant 2 semaines |
| Entérocoques | Valve native ou prothétique:
Ampicilline 2 g iv aux 4 h + gentamicine 1 mg/kg aux 8 h durant 4-6 semaines OU pénicilline G 18-30 millions UI/j + gentamicine 1 mg/kg aux 8 h durant 4-6 semaines |
| Staphylocoque | Valve native: Cloxacilline 2 g iv aux 4 h durant 6 semaines
Valve prothétique: cloxacilline 2 g IV aux 4 h + rifampicine 300 mg iv/po aux 8 h durant ≥ 6 semaines + gentamicine 3 mg/kg/j (en 2-3 doses) durant 2 semaines |
| HACEK[note 3] | Valve native ou prothétique:
Ceftriaxone 2 g/j OU ampicilline 12 g/j + gentamicine 1mg/kg aux 8 h durant 4 semaines (6 semaines si valve prothétique) Envisager ciprofloxacine 4-500 mg iv/po bid comme alternative si allergie grave aux bêtalactamines. |
Endocardite fongique
Pour les endocardites fongiques, une intervention chirurgicale est souvent recommandée en combinaison avec un traitement médical. Le traitement médical seul a été associé à une hausse d'emboli, de morbidité et de mortalité. Le traitement médical en cas d'endocardite à Candida est généralement le fluconazole (10–20 mg/kg pour 14 jours)[30]. Chez les patients sévèrement immunodéprimés qui ont subi une chirurgie cardiaque, la recommandation est l'amphotéricine B (0,7–1 mg/kg/jour pour 14 jours). Le rôle de l'anticoagulation est controversé, car les études montrent de moins bons résultats chez ces patients. [1]
Formes non-infectieuses
La prise en charge des formes non-infectieuses consistent principalement au traitement de la cause sous-jacente et/ou intervention chirurgicale. Un anticoagulant, soit l'héparine (IV ou à faible poids moléculaire), est habituellement efficace pour traiter l'endocardite non-infectieuse.[31]
Traitement chirurgical
Un traitement chirurgical peut être envisagé dans les situations suivantes [1] :
- Endocardite fongique sauf pour H. capsulatum.
- Septicémie persistante malgré une antibiothérapie.
- Embolies récurrentes.
- Atteintes structurelles cardiaques: en cas d'atteinte sévère de la valve aortique, de la valve mitrale ou de la valve prothétique avec une insuffisance cardiaque intraitable.
- Atteintes du tissu de conduction cardiaque.
Suivi
Hospitalier
Répéter les hémocultures à toutes les 24-48 heures jusqu'à leur négativation.[18]
En externe
Un suivi en externe est nécessaire afin de s'assurer de la compliance à l'antibiothérapie et d'ajuster la médication selon les effets secondaires. Dans certains cas particuliers, une échographie cardiaque sera nécessaire pour suivre des atteintes structurelles. D'autres imageries médicales peuvent également être nécessaires selon l'évolution clinique.
Complications
Plusieurs complications sont possibles [1][32] :
- Cardiaques :
- Extra-cardiaques :
Évolution
La mortalité intra-hospitalière de l'endocardite infectieuse est de 15 à 25 %, la mortalité à 6 mois de 30 % et la mortalité à 5 ans de 40 % environ. L'âge est un facteur pronostic important. La mortalité à un an chez les patients > 80 ans est à 37.3% et les patients < 65 ans à 13%. Les co-morbidités, tels que le diabète, l'insuffisance cardiaque ou l'insuffisance rénale dialysée, aggravent le pronostic. Il existe un risque de rechute (de l’ordre de 3 %) ou de récidive ultérieure (de l'ordre de 11 %).[33]
Pour les endocardites non-infectieuses, le pronostic est plutôt mauvais, en raison de la pathologie sous-jacente à la lésion cardiaque.[34]
Les endocardites fongiques sont associées à un plus haut taux de morbidité et mortalité intra-hospitalière. Elles augmentent le risque potentiel d'insuffisance cardiaque et de durée prolongée d'antibiotiques.[35]
Prévention
Grâce à la recommandation d'un traitement prophylactique, il y a eu une réduction significative de l'incidence de l'endocardite infectieuse chez les patients qui ont recours à des procédures. L'AHA a modifié les indications de prophylaxie et elles ont été réduites uniquement aux procédures dentaires (et non les procédures génito-urinaires et gastro-intestinales). [36][37][1]
Selon l'AHA, il y a plusieurs indications de prophylaxie avant une procédure pour prévenir les endocardites, dont [1]:
- Porteur de valve cardiaque prothétique ou matériel prothétique utilisé pour la réparation de la valve cardiaque.
- Patient avec antécédent d'endocardite infectieuse dans le passé.
- Greffé cardiaque avec valvulopathie
- Malformations cardiaques congénitales
- Cardiopathie cyanogène non réparé (incluant les enfants avec shunts et canaux).
- Cardiopathie complètement réparé avec du matériel prosthétique : 6 premiers mois post-procédure.
- Malformation réparée avec des défauts résiduels, telles que des fuites au niveau ou au pourtour du matériel ou d'un appareil prosthétiques.
L'antibioprophylaxie recommandée est :
- Amoxicilline 2g per os 1h avant la procédure OU ampicilline 2g IM/IV 30 minutes avant la procédure
- 2ème ligne (i.e. allergie à la pénicilline) : Céphalexine 2g per os ou clindamycine 600 mg per os 1h avant la procédure OU céfazolin 1g IV/IM 30 minutes avant la procédure.
Dans le cas d'endocardite non-infectieuse, aucune prophylaxie avant les procédures n'est recommandée.[38]
Finalement, pour les endocardites fongiques, si aucune chirurgie cardiaque n'a été faite suite à l'endocardite, le fluconazole au long cours, 400-800 mg/j, est recommandé. Si c'est une endocardite fongique sur prothèse, un traitement suspensif par fluconazole est recommandé à vie (prévention des rechutes).[39]
Notes
- ↑ Les organismes du groupe HACEK sont: Haemophilus spp., Actinobacillus actinomycetemcomitans, Cardiobacterium hominis, Eikenella et Kingella kingae. Ils sont normalement présents dans le microbiome humain, spécialement au niveau de la flore oro-pharyngée.
- ↑ 2,0 et 2,1 Aussi appelés strep oraux,
- ↑ Haemophilus, Aggregatibacter, Cardiobacterium hominis, Eikenella corrodens et Kingella.
Références
- Cette page a été modifiée ou créée le 2020/07/12 à partir de Endocarditis (StatPearls / Endocarditis (2020/07/12)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/29763019 (livre).
- ↑ 1,00 1,01 1,02 1,03 1,04 1,05 1,06 1,07 1,08 1,09 1,10 1,11 et 1,12 Aditi Gupta et Magda D. Mendez, StatPearls, StatPearls Publishing, (PMID 29763019, lire en ligne)
- ↑ William Wang, Ruhi Patel, James Huxley Beavis et Amer Harky, « Viral endomyocarditis: a mystery or a missed diagnosis? », Future Virology, vol. 16, no 10, , p. 641–644 (ISSN 1746-0794, DOI 10.2217/fvl-2021-0183, lire en ligne)
- ↑ 3,0 et 3,1 « Endocardite non infectieuse - Troubles cardiovasculaires », sur Édition professionnelle du Manuel MSD (consulté le 17 septembre 2022)
- ↑ 4,0 et 4,1 Viliane Vilcant et Ofek Hai, StatPearls, StatPearls Publishing, (PMID 29262218, lire en ligne)
- ↑ 5,0 et 5,1 (en) Sahil S Mamtani, Nawar Muneer Aljanabi, Robins P Gupta Rauniyar et Ashu Acharya, « Candida Endocarditis: A Review of the Pathogenesis, Morphology, Risk Factors, and Management of an Emerging and Serious Condition », Cureus, (ISSN 2168-8184, DOI 10.7759/cureus.6695, lire en ligne)
- ↑ A. Le Bot, P. Jégo, E. Donal et E. Flécher, « Les endocardites non infectieuses », La Revue de Médecine Interne, vol. 39, no 10, , p. 782–791 (ISSN 0248-8663, DOI 10.1016/j.revmed.2018.03.020, lire en ligne)
- ↑ 7,0 et 7,1 Alicia Galar, Ana A. Weil, David M. Dudzinski et Patricia Muñoz, « Methicillin-Resistant Staphylococcus aureus Prosthetic Valve Endocarditis: Pathophysiology, Epidemiology, Clinical Presentation, Diagnosis, and Management », Clinical Microbiology Reviews, vol. 32, no 2, 03 20, 2019 (ISSN 1098-6618, PMID 30760474, Central PMCID 6431130, DOI 10.1128/CMR.00041-18, lire en ligne)
- ↑ Malak Elbatarny, Anees Bahji, Gianluigi Bisleri et Andrew Hamilton, « Management of endocarditis among persons who inject drugs: A narrative review of surgical and psychiatric approaches and controversies », General Hospital Psychiatry, vol. 57, , p. 44–49 (ISSN 1873-7714, PMID 30908961, DOI 10.1016/j.genhosppsych.2019.01.008, lire en ligne)
- ↑ Abdalla Elagha et Ahmed Mohsen, « Cardiac MRI clinches diagnosis of Libman-Sacks endocarditis », Lancet (London, England), vol. 393, no 10182, , e39 (ISSN 1474-547X, PMID 31034381, DOI 10.1016/S0140-6736(19)30770-6, lire en ligne)
- ↑ Tatiana Bekker, Anusha Govind et Devin M. Weber, « A Case of Polymicrobial, Gram-Negative Pulmonic Valve Endocarditis », Case Reports in Infectious Diseases, vol. 2019, , p. 6439390 (ISSN 2090-6625, PMID 31032128, Central PMCID 6458857, DOI 10.1155/2019/6439390, lire en ligne)
- ↑ Michael McCann, Michael Gorman et Barry McKeown, « No Fever, No Murmur, No Problem? A Concealed Case of Infective Endocarditis », The Journal of Emergency Medicine, vol. 57, no 2, , e45–e48 (ISSN 0736-4679, PMID 31029399, DOI 10.1016/j.jemermed.2019.03.002, lire en ligne)
- ↑ « Les endocardites fongiques: mise au point » (consulté le 17 septembre 2022)
- ↑ A. Le Bot, P. Jégo, E. Donal et E. Flécher, « Les endocardites non infectieuses », La Revue de Médecine Interne, vol. 39, no 10, , p. 782–791 (ISSN 0248-8663, DOI 10.1016/j.revmed.2018.03.020, lire en ligne)
- ↑ Y. Jia, F. Fang et H. Wang, « [The clinical and pathological features of patients with infective endocarditis diagnosed at autopsy] », Zhonghua Nei Ke Za Zhi, vol. 56, no 10, , p. 725–728 (ISSN 0578-1426, PMID 29036951, DOI 10.3760/cma.j.issn.0578-1426.2017.10.003, lire en ligne)
- ↑ « Endocardite non infectieuse - Troubles cardiovasculaires », sur Édition professionnelle du Manuel MSD (consulté le 11 septembre 2022)
- ↑ A. Le Bot, P. Jégo, E. Donal et E. Flécher, « Les endocardites non infectieuses », La Revue de Médecine Interne, vol. 39, no 10, , p. 782–791 (ISSN 0248-8663, DOI 10.1016/j.revmed.2018.03.020, lire en ligne)
- ↑ Yuka Kiyota, Alessandro Della Corte, Vanessa Montiero Vieira et Karam Habchi, « Risk and outcomes of aortic valve endocarditis among patients with bicuspid and tricuspid aortic valves », Open Heart, vol. 4, no 1, , e000545 (ISSN 2053-3624, PMID 28674620, Central PMCID 5471870, DOI 10.1136/openhrt-2016-000545, lire en ligne)
- ↑ 18,0 18,1 18,2 18,3 18,4 18,5 et 18,6 « Infective Endocarditis in Adults: Diagnosis, Antimicrobial Therapy, and Management of Complications » (consulté le 17 octobre 2022)
- ↑ Pedro Antonio Martínez, Martín Guerrero, José Écil Santos et María Santos Hernández, « [Pediatric clinical experience in infectious endocarditis due to Candida spp] », Revista Chilena De Infectologia: Organo Oficial De La Sociedad Chilena De Infectologia, vol. 35, no 5, , p. 553–559 (ISSN 0717-6341, PMID 30725003, DOI 10.4067/s0716-10182018000500553, lire en ligne)
- ↑ Jevon Samaroo-Campbell, Arsalan Hashmi, Rajat Thawani et Manfred Moskovits, « Isolated Pulmonic Valve Endocarditis », The American Journal of Case Reports, vol. 20, , p. 151–153 (ISSN 1941-5923, PMID 30713335, Central PMCID 6369649, DOI 10.12659/AJCR.913041, lire en ligne)
- ↑ « Endocardite non infectieuse - Troubles cardiovasculaires », sur Édition professionnelle du Manuel MSD (consulté le 11 septembre 2022)
- ↑ Durack DT, Lukes AS, Bright DK. New criteria for diagnosis of infective endocarditis: utilization of specific echocardiographic findings. Duke Endocarditis Service. American Journal of Medicine. 96(3):200-9, 1994. PMID: 8154507
- ↑ Lukes AS, Bright DK, Durack DT. Diagnosis of infective endocarditis. Infect Dis Clin North Am. 1993 Mar;7(1):1-8. Review. PMID: 8463647
- ↑ Fournier PE, Casalta JP, Habib G, et al. Modification of the diagnostic criteria proposed by the Duke Endocarditis Service to permit improved diagnosis of Q fever endocarditis. Am J Med. 1996; 100:629. PMID: 8678083
- ↑ Li JS, Sexton DJ, Mick N, et al. Proposed modifications to the Duke criteria for the diagnosis of infective endocarditis. Clin Infect Dis. 2000; 30:633. PMID: 10770721
- ↑ Paula Anguita, Manuel Anguita, Juan C. Castillo et Paula Gámez, « Are Dentists in Our Environment Correctly Following the Recommended Guidelines for Prophylaxis of Infective Endocarditis? », Revista Espanola De Cardiologia (English Ed.), vol. 72, no 1, , p. 86–88 (ISSN 1885-5857, PMID 30585156, DOI 10.1016/j.rec.2018.04.029, lire en ligne)
- ↑ Karsten Keller, Lukas Hobohm, Thomas Munzel et Mir A. Ostad, « Incidence of infective endocarditis before and after the guideline modification regarding a more restrictive use of prophylactic antibiotics therapy in the USA and Europe », Minerva Cardioangiologica, vol. 67, no 3, , p. 200–206 (ISSN 1827-1618, PMID 30724268, DOI 10.23736/S0026-4725.19.04870-9, lire en ligne)
- ↑ « Endocardite », sur lanthiermed.com (consulté le 28 octobre 2022)
- ↑ « Infective Endocarditis in Adults: Diagnosis, Antimicrobial Therapy, and Management of Complications » (consulté le 17 octobre 2022)
- ↑ (en) Sahil S Mamtani, Nawar Muneer Aljanabi, Robins P Gupta Rauniyar et Ashu Acharya, « Candida Endocarditis: A Review of the Pathogenesis, Morphology, Risk Factors, and Management of an Emerging and Serious Condition », Cureus, (ISSN 2168-8184, DOI 10.7759/cureus.6695, lire en ligne)
- ↑ « Endocardite non infectieuse - Troubles cardiovasculaires », sur Édition professionnelle du Manuel MSD (consulté le 11 septembre 2022)
- ↑ Christine Selton-Suty, François Goehringer, Clément Venner et Carine Thivilier, « Complications et pronostic de l’endocardite infectieuse », La Presse Médicale, vol. 48, no 5, , p. 532–538 (ISSN 0755-4982, DOI 10.1016/j.lpm.2019.04.002, lire en ligne)
- ↑ Christine Selton-Suty, François Goehringer, Clément Venner et Carine Thivilier, « Complications et pronostic de l’endocardite infectieuse », La Presse Médicale, vol. 48, no 5, , p. 532–538 (ISSN 0755-4982, DOI 10.1016/j.lpm.2019.04.002, lire en ligne)
- ↑ « Endocardite non infectieuse - Troubles cardiovasculaires », sur Édition professionnelle du Manuel MSD (consulté le 11 septembre 2022)
- ↑ (en) Sahil S Mamtani, Nawar Muneer Aljanabi, Robins P Gupta Rauniyar et Ashu Acharya, « Candida Endocarditis: A Review of the Pathogenesis, Morphology, Risk Factors, and Management of an Emerging and Serious Condition », Cureus, (ISSN 2168-8184, DOI 10.7759/cureus.6695, lire en ligne)
- ↑ Pallav Garg, Dennis T. Ko, Krista M. Bray Jenkyn et Lihua Li, « Infective Endocarditis Hospitalizations and Antibiotic Prophylaxis Rates Before and After the 2007 American Heart Association Guideline Revision », Circulation, vol. 140, no 3, 07 16, 2019, p. 170–180 (ISSN 1524-4539, PMID 31023074, DOI 10.1161/CIRCULATIONAHA.118.037657, lire en ligne)
- ↑ Abdisamad M. Ibrahim et Momin S. Siddique, StatPearls, StatPearls Publishing, (PMID 30422578, lire en ligne)
- ↑ A. Le Bot, P. Jégo, E. Donal et E. Flécher, « Les endocardites non infectieuses », La Revue de Médecine Interne, vol. 39, no 10, , p. 782–791 (ISSN 0248-8663, DOI 10.1016/j.revmed.2018.03.020, lire en ligne)
- ↑ « Les endocardites fongiques : mise au point » (consulté le 11 septembre 2022)
