Choc septique
| Maladie | |||
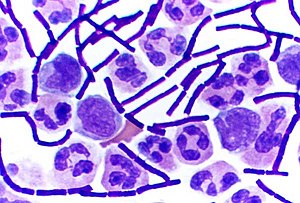 Bâtonnets Gram + dans le LCR | |||
| Caractéristiques | |||
|---|---|---|---|
| Signes | Fasciite nécrosante, Endocardite, Péritonite, Empyème, Pétéchies, Arthrite septique, Peau marbrée, Pneumonie acquise en communauté, Muqueuses sèches, Pli cutané, ... [+] | ||
| Symptômes |
Confusion, Frissons, Hypotension orthostatique, Myalgies, Oligurie, Nausées, Anurie, Dyspnée , Vertige , Céphalée , ... [+] | ||
| Diagnostic différentiel |
Insuffisance surrénalienne, Choc cardiogénique, Choc distributif, Choc obstructif, Anaphylaxie, Choc hémorragique, Syndrome de réponse inflammatoire systémique, Choc spinal, Choc hypovolémique, Intoxication (approche clinique) | ||
| Informations | |||
| Terme anglais | Septic shock | ||
| Wikidata ID | Q1765564 | ||
| SNOMED CT ID | 76571007 | ||
| Spécialités | Soins intensifs, Médecine d'urgence, Médecine interne, Infectiologie | ||
| |||
Le choc septique est une forme plus sévère de sepsis avec hypoperfusion d'organe. Le sepsis se définit par une dysfonction organique menaçant la vie causée par une réponse de l'hôte dysrégulée à une infection.[1] Lorsqu'il progresse en sévérité il peut engendrer une dysfonction multi-organique (MOF - multiorgan failure).[2][3]
Épidémiologie
Le sepsis affecte 1 à 2 % des patients hospitalisés. [4] Près de 15 % de ces patients évoluent vers le choc septique, représentant ainsi 10 % des admissions aux soins intensifs. [5]
En 2017, son incidence était de près de 50 millions de cas dans le monde, dont plus de 120 000 au Canada [6], et engendre au pays des coûts supérieurs à 325 millions annuellement. [5]
Son incidence importante pourrait être expliquée par la prévalence accrue de maladies chroniques dans les populations vieillissantes, à l'augmentation de la résistance aux agents antimicrobiens et à l'augmentation des procédures invasives, de la prescription d'agents immunosuppresseurs et de chimiothérapie. [7]
Le sepsis est la première cause de décès intra-hospitalier aux États-Unis. [6] Son taux de mortalité est de 25 % et s'élève à 50 % dans le choc septique. [8]
Étiologies
Ce sont les infections bactériennes à Gram négatif qui sont le plus fréquemment retrouvées chez les patients en état de sepsis. En effet, chez les patients ayant une culture positive, une bactérie à Gram négatif est présente dans 62% des cas, alors qu'une bactérie à Gram positif est isolée dans 47% des cas. [9] Ainsi, il arrive que des pathogènes à Gram négatif et à Gram positif soient présents chez un même patient. Une augmentation de la prévalence de ces derniers peut être attribuable à la performance de procédures plus invasives et à une incidence accrue d'infections nosocomiales. [8] Les micro-organismes prédominants isolés chez les patients sont staphylococcus aureus (20 %), pseudomonas spp (20 %) et escherichia coli (16 %). [10] Les sites d'infection prédominants comprennent les voies respiratoires (42%), la circulation sanguine (21%) et les voies génito-urinaire (10%). [8] Cependant, pour près du tiers des patients en sepsis, aucune culture positive ne pourra être obtenue. Par conséquent, ces données doivent être interprétées avec modération. [11][2]
Les syndromes septiques causés par des souches bactériennes multirésistantes comme le staphylococcus résistant à la méthicilline (SARM) et les entérocoques résistants à la vancomycine (ERV) sont en augmentation avec une incidence actuelle pouvant atteindre 25%. Les virus et les parasites sont moins fréquents et sont identifiés dans 2% à 4% des cas.[12][2]
Physiopathologie
La physiopathologie du choc septique demeure incomprise dans sa totalité. Il émerge d'abord d'un état de sepsis, soit une réponse dérégulée de l'hôte face à une infection. Cette réponse dérégulée entraîne une inflammation excessive, l'activation de la cascade de coagulation, l'apoptose des cellules et ultimement une dysfonction organique, pouvant mener au choc. [13]
Activation de la cascade inflammatoire
En présence d'une infection par un micro-organisme pathogène, les réponses pro-inflammatoires et anti-inflammatoires du système immunitaire sont activées.
Les cellules du système immunitaire inné, telles que les cellules dendritiques, les macrophages et certaines cellules épithéliales, induisent d'abord une réponse pro-inflammatoire, afin d'éradiquer le pathogène en cause. La libération de cytokines pro-inflammatoires entraînent ensuite l'activation des monocytes, des macrophages et des neutrophiles. [13] Ces cellules travaillent de concert à l'élaboration de produits cytotoxiques (les cytokines, les protéases, les kinines, les dérivés réactifs de l'oxygène et l'oxyde nitrique) de manière à supprimer le microorganisme responsable. [14] Lorsqu'il y a suractivation de la réponse inflammatoire, la libération des produits cytotoxiques est exagérée, ce qui cause des dommages aux tissus environnants.
La cascade anti-inflammatoire est également activée de manière concomitante pour limiter la réponse inflammatoire. Lorsque suractivée, elle supprime le système immunitaire et prédispose à une seconde infection. [13]
Activation de la cascade de coagulation
L'état inflammatoire produit par le système immunitaire endommage l'endothélium vasculaire, entrainant l'activation des mécanismes de coagulation endovasculaire et de la cascade du complément, ce qui crée un état prothrombotique et la perpétration de l'état inflammatoire. [15] Les dommages subséquents à l'endothélium engendrent éventuellement une fuite capillaire et la formation de petits thrombi, qui diminuent l'apport sanguin aux organes. Le développement d'une coagulopathie s'en suit, notamment par consommation de plaquettes, de facteurs de coagulation et par la fibrinolyse excessive. [13]
Apoptose cellulaire
L'apoptose est un mécanisme d'autodestruction des cellules inflammatoires permettant de diminuer la réponse pro-inflammatoire de l'hôte. Une suractivation de ce mécanisme entraine l'affaiblissement du système immunitaire, et donc augmente les risques de développer une seconde infection. [13]
Choc septique
La dysfonction organique est la conséquence des dommages tissulaires engendrés par la libération excessive de produits cytotoxiques et par l'hypoxie découlant du manque de perfusion des organes. La vasodilatation périphérique, l'augmentation de la perméabilité vasculaire et l'état pro-coagulable induits par l'état inflammatoire sont tous responsables de cette baisse de perfusion. [13][15] Alors que l'augmentation du rythme cardiaque peut initialement combler le déficit en oxygène, ce mécanisme est éventuellement surpassé et l'hypotension n'est plus compensé. [14][2] Si elle persiste malgré une réanimation liquidienne adéquate, et que l'hypoxie est trop importante, on parle d'un état de choc septique.
Présentation clinique
Facteurs de risque
Les facteurs de risque qui prédisposent au sepsis comprennent[2][16][6]:
- le sexe féminin
- les maladies chroniques concomitantes :
- les portes d'entrée pour les pathogènes :
- les brûlures
- une intervention chirurgicale majeure récente
- un traumatisme
- une sonde urinaire
- des cathéters veineux et artériels
- un faible statut socioéconomique
- une hospitalisation prolongée
- l'utilisation de corticostéroïdes systémiques
- l'immunosuppression
- les extrêmes d'âge: > 65 ans ou < 1 an.
Questionnaire
Lors d'un choc septique, les symptômes systémiques d'infection à rechercher sont :[17][18]
- la fièvre et les frissons
- de la confusion
- la fatigue
- un malaise (vague)
- des myalgies
- une dyspnée
- une oligurie ou une anurie
- des étourdissements et de l'orthostatisme
- des nausées et des vomissements.
Une revue des systèmes assez large devra être réalisée pour déterminer le siège du sepsis[17][18] :
- une céphalée et une raideur nucale (méningite)
- de la toux, des crachats, de la dyspnée et une douleur pleurétique (foyer pulmonaire)
- de la douleur abdominale, des vomissements ou des diarrhées (foyer gastrointestinale)
- une douleur aux flancs, de la dysurie et de la pollakiurie (foyer urinaire)
- des pertes vaginales anormales (foyer génital)
- une arthralgie ou des douleurs osseuses (ostéomyélite ou arthrite septique).
Examen physique
Comme le diagnostic du sepsis est majoritairement clinique, un examen clinique complet recherchant les signes systémiques et les sites d'infections possibles permet de déterminer l'importance d'agir rapidement. [17][18]
Les signes vitaux peuvent nous indiquer la gravité de l'atteinte infectieuse. Les indices d'un état de sepsis ou de choc sont :
- de la fièvre > 38,5 °C ou une hypothermie < 36 °C
- une hypotension artérielle (TAS < 90 mmHg ou TAM < 70 mmHg)
- une tachycardie (> 90 bpm)
- une tachypnée (> 20 respirations par minute)
- une altération de l'état de conscience.
D'autres signes systémiques secondaires à l'infection peuvent être retrouvés comme :
- des signes d'hypoperfusion
- un remplissage capillaire allongé (> 3 secondes)
- la peau froide et marbrée (une peau moite et chaude est également possible)
- une altération de l'état de conscience (hypoperfusion)
- des muqueuses sèches
- un pli cutané persistant
- de la diaphorèse
- du purpura ou des pétéchies.
Les patients évoluant vers un choc septique présenteront des signes et symptômes de sepsis sévère avec hypotension. Il convient de noter qu'à un stade précoce du choc compensé, la pression artérielle peut être maintenue et d'autres signes de choc distributif peuvent être présents, par exemple, des extrémités chaudes, une recharge capillaire éclair (moins d'une seconde) et des impulsions de délimitation, également connu sous le nom de choc chaud. Ce stade de choc, s'il est géré de manière agressive avec une réanimation liquidienne et un soutien vasoactif, peut être inversé. Avec la progression du choc septique dans le stade non compensé, une hypotension s'ensuit et les patients peuvent présenter des extrémités froides, une recharge capillaire retardée (plus de trois secondes) et des impulsions vibrantes, également appelées choc froid. [2]
Des signes d'atteinte infectieuse plus spécifiques sont également à rechercher[18].
| Système | Signes à rechercher à l'examen physique |
|---|---|
| examen cardiaque |
|
| examen pulmonaire | |
| examen abdominal |
|
| examen cutané |
|
| Autres |
|
Examens paracliniques
Bien que le diagnostic de choc septique soit avant tout clinique, il importe d'effectuer le bilan biochimique, microbiologique et radiologique nécessaire à la détection de l'étiologie infectieuse et à l'évaluation de l'atteinte organique [18].
| Éléments | Signification |
|---|---|
| FSC |
|
| Électrolytes (Na, K, Cl) |
|
| Glycémie |
|
| Créatininémie |
|
| Gaz |
|
| Bilan hépatique |
|
| Protéine C réactive Procalcitonine |
|
| INR |
|
| Recherche de la source de l'infection |
|
Diagnostic
Le sepsis se définit par une dysfonction organique menaçant la vie causée par une réponse de l'hôte dysrégulée à une infection.[1] En d'autres mots, le sepsis est une maladie potentiellement mortelle qui survient lorsque la réponse du corps à une infection blesse ses propres tissus et organes.[1]
Le choc septique est un sous-type de sepsis dans lequel les dysfonctions d'organes sont suffisamment sévères pour augmenter significativement la mortalité[1]. Plus précisément, le choc septique se définit par un sepsis avec [1]:
- une hypotension artérielle persistante nécessitant des vasopresseurs pour maintenir une TAM ≥ 65 mm Hg OU
- des lactates sériques > 2 mmol/L malgré une réanimation liquidienne adéquate.
La dysfonction d'organe se définit par un changement aiguë de l'échelle SOFA ≥ 2 points provoquée par une infection[note 3].[1]
| Indicateur | Score | ||||
|---|---|---|---|---|---|
| 0 | 1 | 2 | 3 | 4 | |
| PaO2/FiO2 (mmHg) | ≥ 400 | < 400 | < 300 | < 200 avec
support respiratoire |
< 100 avec
support respiratoire |
| Plaquettes (109/L) | ≥ 150 | < 150 | < 100 | < 50 | < 20 |
| Bilirubine (μmol/L) | < 20 | 20-32 | 33-101 | 102-204 | > 204 |
| Tension artérielle (mmHg) | TAM ≥ 70 | TAM < 70 | Dopamine < 5 OU
Dobutamine |
Dopamine 5.1-15 OU
Épinéphrine ≤ 0.1 OU Norépinéphrine ≤ 0.1 |
Dopamine > 15 OU
Épinéphrine > 0.1 OU Norépinéphrine > 0.1 |
| Échelle de Glasgow | 15 | 13-14 | 10-12 | 6-9 | < 6 |
| Créatinine (μmol/L) | < 110 | 110-170 | 171-299 | 300-440 | > 440 |
| Débit urinaire (mL/jour) | - | - | - | < 500 | < 200 |
Approche clinique
- Le diagnostic de choc septique doit donc être suspecté en cas d'infection avec une instabilité hémodynamique réfractaire à la réplétion volémique ou d'une dysfonction d'organe progressive malgré le traitement initial.
- Des outils de dépistages rapides ont été développés (NEWS, qSOFA, MEWS, etc.), mais aucun n'est suffisamment sensible pour être utilisé isolément. Ils doivent tous être combinés au jugement clinique (lequel est supérieur aux scores pour diagnostiquer le sepsis[19]). [3]
- qSOFA 2/3 critères suivants :
- la tension artérielle systolique < 100 mmHg
- une tachypnée > 22 respirations/min
- un GCS < 15.
- qSOFA 2/3 critères suivants :
- Il est important de se rappeler que l'état de sepsis et de choc entrainent des dommages organiques. La gravité de cette atteinte peut être surveiller à l'aide d'examens paracliniques (voir section bilans paracliniques).
Diagnostic différentiel
Le diagnostic différentiel du choc septique comprend les autres formes de chocs et des causes de dysfonction d'organes[2]:
- le choc distributif :
- le choc hypovolémique, incluant le choc hémorragique
- le choc cardiogénique
- le choc obstructif (dont l'embolie pulmonaire)
- l'insuffisance surrénalienne
- une intoxication.
Traitement
Il est à noter qu'il n'a pas été démontré dans des études plus récentes que la thérapie ciblée précoce (EGDT) confère un avantage de survie lorsque comparé à la pratique courante[20]. Néanmoins, les principes de l'EGDT sont présents dans la pratique courante, soit l'initiation précoce d'une réplétion volémique et le maintient d'une pression artérielle à l'aide de vasopresseurs si nécessaires, tout en réévaluant la réponse du patient à ces thérapies.[21]
Le patient est généralement admis aux soins intensifs.
| Étape | Recommandations |
|---|---|
| Identification de l'infection |
|
| Gestion des voies aériennes |
|
| Stabilisation hémodynamique |
|
| Antibiothérapie |
|
| Thérapies adjuvantes |
|
Suivi
Au cours de la prise en charge du patient en choc septique, il est important de suivre la réponse clinique aux différents traitements administrés. Cette réponse se traduit par l'amélioration ou la stabilité des paramètres cliniques, hémodynamiques et biochimiques.
Vous référer aux sections investigations et traitements pour les cibles des différents paramètres.
| Éléments | |
|---|---|
| Signes vitaux et paramètres cliniques |
|
| Bilans sanguins | Un suivi sérié des bilans devrait être considéré selon la clinique, dont :
|
| Contrôle de la source |
|
Complications
Les complications comprennent : [2]
- le syndrome de détresse respiratoire aiguë
- l'insuffisance respiratoire
- l'acidose métabolique
- l'insuffisance rénale aiguë
- la coagulation intravasculaire disséminée (CIVD)
- l'ischémie mésentérique
- l'insuffisance hépatique aiguë
- l'infarctus du myocarde.
Évolution
Le choc septique est une maladie grave et malgré toutes les avancées de la médecine, il est toujours porteur d'une mortalité élevée qui peut dépasser 40%. De nombreux scores cliniques ont été développés pour estimer la mortalité : SOFA, APACHE, SAPS, etc. La mortalité dépend de nombreux facteurs, notamment le type d'organisme, la sensibilité aux antibiotiques, le nombre d'organes touchés et l'âge du patient. Plus il y a de facteurs qui correspondent au SIRS, plus la mortalité est élevée. La tachypnée et l'état mental altéré sont d'excellents prédicateurs d'un pronostic défavorable. Enfin, l'utilisation prolongée d'inotropes pour maintenir la pression artérielle est également associée à un pronostic défavorable. Une portion importante des survivants se retrouvent avec des déficits fonctionnels et cognitifs significatifs.[2]
Prévention
La prévention du choc septique passe par une prise un diagnostique et une prise charge rapide du sepsis pour diminuer le risque de progression en choc septique. De manière générale, la prévention des infections va prévenir les sepsis et chocs septiques.
- la prévention des infections acquises en communauté [18] :
- la vaccination
- les soins des plaies adéquate
- une hygiène personnelle adéquate
- les soins buccaux en général (pneumonie)
- la prévention des infections iatrogéniques :
- l'hygiène des mains
- les mesures de contrôle des infections intrahospitalière
- le positionnement du patient pour éviter l'aspiration
- le retrait des cathéters et autres appareillage lorsque non nécessaires
- les soins des plaies chirurgicales.
Notes
- ↑ Parfois, les personnes âgées ou les patients dénutris peuvent avoir des créatininémie assez basse (40-50). Une augmentation de la créatininémie à 110 est alors fort significative. De la même façon, certains patients ont une créatininémie de base à 150 : une augmentation à 170 ne pourrait être interprété de la même façon dans le contexte.
- ↑ Il est très important d'identifier adéquatement l'hémoculture qui provient du cathéter pour le laboratoire.
- ↑ Un score SOFA = 0 peut être présumée chez les patients chez qui on ne connait pas d'insuffisance d'organe préalable.
- ↑ SIRS : Systemic Inflammatory Response Syndrome
- ↑ Une nutrition précoce peut aider à protéger la muqueuse intestinale et à empêcher la translocation d'organismes du tractus gastro-intestinal dans la circulation systémique.
Références
- Cette page a été modifiée ou créée le 2020/07/12 à partir de Septic Shock (Sepsis) (StatPearls / Septic Shock (Sepsis) (2020/06/25)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/28613689 (livre).
- ↑ 1,0 1,1 1,2 1,3 1,4 1,5 et 1,6 (en) Mervyn Singer, Clifford S. Deutschman, Christopher Warren Seymour et Manu Shankar-Hari, « The Third International Consensus Definitions for Sepsis and Septic Shock (Sepsis-3) », JAMA, vol. 315, no 8, , p. 801 (ISSN 0098-7484, PMID 26903338, Central PMCID PMC4968574, DOI 10.1001/jama.2016.0287, lire en ligne)
- ↑ 2,00 2,01 2,02 2,03 2,04 2,05 2,06 2,07 2,08 2,09 2,10 et 2,11 (en) Mahapatra S et Heffner Ac, « Septic Shock (Sepsis) », sur PubMed, 2020 jan (PMID 28613689, consulté le 7 août 2020)
- ↑ 3,0 3,1 et 3,2 (en) Laura Evans, Andrew Rhodes, Waleed Alhazzani et Massimo Antonelli, « Surviving Sepsis Campaign: International Guidelines for Management of Sepsis and Septic Shock 2021 », Critical Care Medicine, vol. 49, no 11, , e1063–e1143 (ISSN 0090-3493, DOI 10.1097/CCM.0000000000005337, lire en ligne)
- ↑ Min Huang, Shaoli Cai et Jingqian Su, « The Pathogenesis of Sepsis and Potential Therapeutic Targets », International Journal of Molecular Sciences, vol. 20, no 21, , E5376 (ISSN 1422-0067, PMID 31671729, Central PMCID 6862039, DOI 10.3390/ijms20215376, lire en ligne)
- ↑ 5,0 et 5,1 « Fondation Canadienne du Sepsis », sur canadiansepsisfoundation.ca, (consulté le 12 juin 2022)
- ↑ 6,0 6,1 et 6,2 (en) Kristina E Rudd, Sarah Charlotte Johnson, Kareha M Agesa et Katya Anne Shackelford, « Global, regional, and national sepsis incidence and mortality, 1990–2017: analysis for the Global Burden of Disease Study », The Lancet, vol. 395, no 10219, , p. 200–211 (PMID 31954465, Central PMCID PMC6970225, DOI 10.1016/S0140-6736(19)32989-7, lire en ligne)
- ↑ (en) Siddharth Dugar, Chirag Choudhary et Abhijit Duggal, « Sepsis and septic shock: Guideline-based management », Cleveland Clinic Journal of Medicine, vol. 87, no 1, , p. 53–64 (ISSN 0891-1150 et 1939-2869, PMID 31990655, DOI 10.3949/ccjm.87a.18143, lire en ligne)
- ↑ 8,0 8,1 et 8,2 Florian B. Mayr, Sachin Yende, Walter T. Linde-Zwirble et Octavia M. Peck-Palmer, « Infection rate and acute organ dysfunction risk as explanations for racial differences in severe sepsis », JAMA, vol. 303, no 24, , p. 2495–2503 (ISSN 1538-3598, PMID 20571016, Central PMCID 3910506, DOI 10.1001/jama.2010.851, lire en ligne)
- ↑ J. L. Vincent, « EPIC II: sepsis around the world », Minerva Anestesiologica, vol. 74, no 6, , p. 293–296 (ISSN 1827-1596, PMID 18500201, lire en ligne)
- ↑ Jean-Louis Vincent, Jordi Rello, John Marshall et Eliezer Silva, « International study of the prevalence and outcomes of infection in intensive care units », JAMA, vol. 302, no 21, , p. 2323–2329 (ISSN 1538-3598, PMID 19952319, DOI 10.1001/jama.2009.1754, lire en ligne)
- ↑ M. S. Rangel-Frausto, « The epidemiology of bacterial sepsis », Infectious Disease Clinics of North America, vol. 13, no 2, , p. 299–312, vii (ISSN 0891-5520, PMID 10340168, DOI 10.1016/s0891-5520(05)70076-3, lire en ligne)
- ↑ Djillali Annane, Philippe Aegerter, Marie Claude Jars-Guincestre et Bertrand Guidet, « Current epidemiology of septic shock: the CUB-Réa Network », American Journal of Respiratory and Critical Care Medicine, vol. 168, no 2, , p. 165–172 (ISSN 1073-449X, PMID 12851245, DOI 10.1164/rccm.2201087, lire en ligne)
- ↑ 13,0 13,1 13,2 13,3 13,4 et 13,5 (en) Luis E Huerta et Todd W Rice, « Pathologic Difference between Sepsis and Bloodstream Infections », The Journal of Applied Laboratory Medicine, vol. 3, no 4, , p. 654–663 (ISSN 2576-9456 et 2475-7241, DOI 10.1373/jalm.2018.026245, lire en ligne)
- ↑ 14,0 et 14,1 H. Bryant Nguyen, Emanuel P. Rivers, Fredrick M. Abrahamian et Gregory J. Moran, « Severe sepsis and septic shock: review of the literature and emergency department management guidelines », Annals of Emergency Medicine, vol. 48, no 1, , p. 28–54 (ISSN 1097-6760, PMID 16781920, DOI 10.1016/j.annemergmed.2006.02.015, lire en ligne)
- ↑ 15,0 et 15,1 « Sepsis et choc septique », sur merckmanuals.com, (consulté le 5 mai 2022)
- ↑ 16,0 16,1 16,2 et 16,3 (en) Adrian Purcarea et Silvia Sovaila, « Sepsis, a 2020 review for the internist », Romanian Journal of Internal Medicine, vol. 58, no 3, , p. 129–137 (ISSN 2501-062X, DOI 10.2478/rjim-2020-0012, lire en ligne)
- ↑ 17,0 17,1 et 17,2 « Service central d'authentification – Université de Sherbrooke », sur cas.usherbrooke.ca (consulté le 5 juin 2022)
- ↑ 18,0 18,1 18,2 18,3 18,4 18,5 18,6 et 18,7 « Sepsis », sur clinicalkey.com, (consulté le 26 juillet 2022)
- ↑ Sarah K. S. Knack, Nathaniel Scott, Brian E. Driver et Matthew E. Prekker, « Early Physician Gestalt Versus Usual Screening Tools for the Prediction of Sepsis in Critically Ill Emergency Patients », Annals of Emergency Medicine, , S0196–0644(24)00099–4 (ISSN 1097-6760, PMID 38530675, DOI 10.1016/j.annemergmed.2024.02.009, lire en ligne)
- ↑ D. C. Angus, A. E. Barnato, D. Bell et R. Bellomo, « A systematic review and meta-analysis of early goal-directed therapy for septic shock: the ARISE, ProCESS and ProMISe Investigators », Intensive Care Medicine, vol. 41, no 9, , p. 1549–1560 (ISSN 1432-1238, PMID 25952825, DOI 10.1007/s00134-015-3822-1, lire en ligne)
- ↑ Tiffany M. Osborn, « Severe Sepsis and Septic Shock Trials (ProCESS, ARISE, ProMISe): What is Optimal Resuscitation? », Critical Care Clinics, vol. 33, no 2, , p. 323–344 (ISSN 1557-8232, PMID 28284298, DOI 10.1016/j.ccc.2016.12.004, lire en ligne)
- ↑ Alan E. Jones et Michael A. Puskarich, « The Surviving Sepsis Campaign guidelines 2012: update for emergency physicians », Annals of Emergency Medicine, vol. 63, no 1, , p. 35–47 (ISSN 1097-6760, PMID 24067755, DOI 10.1016/j.annemergmed.2013.08.004, lire en ligne)
- ↑ Andrew Rhodes, Laura E. Evans, Waleed Alhazzani et Mitchell M. Levy, « Surviving Sepsis Campaign: International Guidelines for Management of Sepsis and Septic Shock: 2016 », Critical Care Medicine, vol. 45, no 3, , p. 486–552 (ISSN 1530-0293, PMID 28098591, DOI 10.1097/CCM.0000000000002255, lire en ligne)
- ↑ Andréa M. C. Ventura, Huei Hsin Shieh, Albert Bousso et Patrícia F. Góes, « Double-Blind Prospective Randomized Controlled Trial of Dopamine Versus Epinephrine as First-Line Vasoactive Drugs in Pediatric Septic Shock », Critical Care Medicine, vol. 43, no 11, , p. 2292–2302 (ISSN 1530-0293, PMID 26323041, DOI 10.1097/CCM.0000000000001260, lire en ligne)
- ↑ E. Rivers, B. Nguyen, S. Havstad et J. Ressler, « Early goal-directed therapy in the treatment of severe sepsis and septic shock », The New England Journal of Medicine, vol. 345, no 19, , p. 1368–1377 (ISSN 0028-4793, PMID 11794169, DOI 10.1056/NEJMoa010307, lire en ligne)
- ↑ D. Annane, « Corticosteroids for septic shock », Critical Care Medicine, vol. 29, no 7 Suppl, , S117–120 (ISSN 0090-3493, PMID 11445745, DOI 10.1097/00003246-200107001-00036, lire en ligne)
- ↑ Djillali Annane, Alain Renault et Eric Bellissant, « Glucocorticoids with or without Fludrocortisone in Septic Shock », The New England Journal of Medicine, vol. 379, no 9, 08 30, 2018, p. 895–896 (ISSN 1533-4406, PMID 30179381, DOI 10.1056/NEJMc1804993, lire en ligne)
- ↑ 28,0 28,1 et 28,2 (en) Centre universitaire de santé McGill, « Empiric Management of Sepsis », sur MUHCASP, (consulté le 29 mars 2023)
- ↑ (en-US) Laura Evans, Andrew Rhodes, Waleed Alhazzani et Massimo Antonelli, « Surviving Sepsis Campaign: International Guidelines for Management of Sepsis and Septic Shock 2021 », Critical Care Medicine, vol. 49, no 11, , e1063 (ISSN 0090-3493, DOI 10.1097/CCM.0000000000005337, lire en ligne)
- ↑ (en) « Evaluation and management of suspected sepsis and septic shock in adults », sur uptodate.com, (consulté le 31 juillet 2022)
