Carie dentaire
| Maladie | |
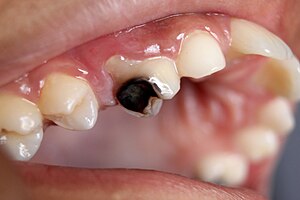 Carie dentaire | |
| Caractéristiques | |
|---|---|
| Signes | Tâche dentaire blanche, Tâche dentaire colorée, Cavitations, Défectuosités au niveau de la structure dentaire, Puit dentaire, Fissure dentaire, Variation de la texture de la dent |
| Symptômes |
Odontalgie, Rétention dentaire d'aliments, Décoloration dentaire, Cavitation visible, Gingivorrhagie , Asymptomatique |
| Diagnostic différentiel |
Hypominéralisation dentaire, Fluorose dentaire, Hypoplasie dentaire, Résorption cervicale externe |
| Informations | |
| Terme anglais | Dental caries, Dental cavities |
| Spécialité | Médecine dentaire |
|
| |
La carie dentaire est une maladie multifactorielle causée par les bactéries cariogènes présentent à la surface des dents. Cette affection est une cause majeur de problèmatique en santé publique, étant la maladie infectieuse chronique la plus répandue à travers le monde.[1][2][3]
La carie dentaire peut se développer à la surface d'une ou de plusieurs dents à la fois. De multiples caries présentent chez un même patient peuvent être défini par le terme de caries ramplantes. Elles seront alors classées selon l'étiologie probable soit les caries du biberon, les caries de radiation ou d'utilisation de drogues.[4]
Épidémiologie
La carie dentaire est un problème de santé mondial qui touche plus de 80% de la population, dont 60 à 90% des enfants d'âge scolaire, représentant plus de 2.3 milliards de personnes présentant une carie non traitée sur des dents permanentes et plus de 530 millions sur une dent primaire selon les plus récentes données.[5][6][7] Selon l'étude mondiale sur la morbidité réalisée en 2015, le Global Burden of Disease 2015, il semble y avoir une prévalence mondiale relativement stable de la carie dentaire non traitée en dentition permanente entre 1990 et 2017 avec un taux d'environ 34%.[8] Malgré tout, il semble y avoir une amélioration dans les pays industrialisés quant à la sévérité et la prévalence de la carie avec évidence de cavitation dans le groupe d'âge 5-12 ans ainsi que chez les 35-44 ans. Il semble de plus y avoir une diminution du nombre de dents manquantes au sein de la population veillante en comparaison aux décennies antérieures, possiblement attribuable en partie à la diminution des extractions pour cause de caries dentaires.[9]
La carie dentaire peut affecter tous les groupes d'âge indépendamment du sexe. Un pic de prévalence peut être observé entre 1 et 4 ans pour les caries non traités en dentition primaire alors que celui en dentition permanente se situe autour de 15 à 19 ans. La prévalence de la carie dentaire diminue par la suite avec l'âge avec un second pic d'incidence vers 70 ans. [8][9] Les nourrissons sont également sujets aux caries, décrites comme des «caries de biberon», qui affectent une ou plusieurs dents primaires dès leur apparition en bouche, entre la période de la naissance et 71 mois. [9][10][11]
Au Canada, selon le rapport de 2017 de l'Association Dentaire canadienne sur la santé buccodentaire, la carie dentaire serait responsable du tiers des chirurgies d'un jour chez les enfants canadiens âgées entre un et cinq ans. Toujours selon ce rapport, basé sur des résultats de statistiques Canada de 2010, le pourcentage d'enfant présentant au moins une carie aurait diminué de 74% à 23% en 40 ans et de 96% à 58% chez les adolescents durant cette même période de temps. Chez les Premières Nations, notamment chez les Inuits où une enquête fut réalisé en 2008-2009, le taux d'enfant d'âge scolaire présentant une carie dentaire serait de 85% et augmentait à 100% chez la population adulte, démontrant que la carie dentaire reste un problème majeur de santé publique au sein de cette population.[1] Une étude clinique sur l’état de santé buccodentaire des élèves québécois du primaire, réalisée en 2012-2013, démontrait de son côté que les élèves de deuxième et sixième année du primaire présenteraient toujours un taux important de dents touchées par la carie de toute forme. C'est en fait 9 enfants sur 10 qui seraient atteints de carie dentaire, qu'elle soit évidente ou non, tous stades confondus. Depuis la fin des années 1990, les élèves de deuxième année ne semblent pas présenter d'amélioration en matière de carie dentaire, avec un taux passant de 56% à 53% des élèves présentant une carie évidente de stade 4 à 6, une dent extraite ou obturée. Cependant, en ce qui concerne les élèves de sixième année, ce taux chute de 59% à seulement 36%, démontrant une nette amélioration pour ce dernier groupe. [12]
Le statut socioéconomique semble être directement lié à la prévalence de la carie, surtout en dentition primaire.[13]
Étiologies
La carie dentaire est une maladie multifactorielle dont la dynamique dépend de trois facteurs primaires essentiels et qui ne peut exister sans l'un de ceux-ci. Ces facteurs sont la présence d'une ou plusieurs dents, une alimentation avec des glucides fermentescibles et la présence de plaque dentaire contenant une flore bactérienne diversifiée. Le facteur temps, qui englobe ces facteurs et qui décrit la durée de l'interaction entre ceux-ci, est également un facteur non négligeable à considérer, car la carie dentaire peut prendre jusqu'à plusieurs années pour s'installer. À cela, s'ajoutent les facteurs environnementaux et ceux de l'hôte qui peuvent moduler et accentuer la sévérité de la carie. Ils sont donc, pour le clinicien, important à considérer pour la prise en charge de cette affection complexe. [14][13]
Plaque dentaire
La cavité orale est un environnement hétérogène unique contenant plus de 700 types de microorganismes différents qui varie en composition et en nombre selon le site. L'acquisition de cette flore buccale se fait par transmission et colonisation à partir de la naissance, où la bouche de l'enfant est encore stérile. L'acquisition notamment de Streptococci et de bactéries à Gram négatifs, se fait principalement par transmission verticale de la mère à l'enfant. L'éruption des dents permet la colonisation de sites où les bactéries peuvent s'attacher et colonisé pour former ce qu'on appelle la plaque dentaire ou biofilm dentaire. Une fois établie, la flore buccale semble demeurer stable, dans un état d'homéostasie, mais qui sera sujet aux débalancements. Par exemple, un changement majeur dans les habitudes, tel une consommation nouvelle de sucre qui peut alors favoriser certaines espèces au détriment de d'autres. [4]
Au niveau de la plaque dentaire, certaines bactéries semblent plus spécifiquement asssociées à la carie dentaire et comprennent diverses espèces tels les Streptococci, dont Streptococcus mutans et Streptococcus sobrinus, les lactobacilles ainsi que les Actinomyces.[15][3]
Ces bactéries sont dites cariogènes, car elles ont la capacité de coloniser la surface dentaire, de transformer en acide, principalement de l'acide lactique, les sucres fermentescibles à partir de glucides alimentaires, d'effectuer leurs activités métaboliques en condition acide et de produire des polysaccarides extra et intracellulaires favorisant l'adhésion et l'établissement du biofilm dentaire.[3][14][4][16] Le Streptococcus mutans est la bactérie retrouvée en plus grand nombre dans la plaque dentaire et une bactérie importante dans le processus carieux, car celle-ci présente toutes ces caractéristiques. [3][14][16]
De façon générale, le Streptococcus mutans serait une des premières bactéries impliquées dans la formation de la carie dentaire alors que les lactobacilles seraient quant à eux davantage des bactéries contributives à un processus carieux déjà enclenché.[13] La proportion et les espèces retrouvées dans la plaque associée à la carie dentaire tendent à changer selon le site d'atteinte, l'individu et l'âge. [4][16]
Les plus récentes études tendent à démontrer que pour développer la carie dentaire, la présence d'une communauté complexe de bactéries d'espèces différentes serait nécessaire. De plus, bien que la carie dentaire semble avoir longtemps été associé au S. mutans, les études démontrent maintenant que la plaque dentaire causant la carie de stade 3 à 6, ne serait pas majoritairement composée de S. mutans. Celles-ci démontre de plus qu'un risque carieux important peut être présent chez des individus présentant une faible proportion de S. mutans, et inversement. [4] [16]
Il est à retenir que, bien qu'essentielle à la formation de carie, la présence de plaque dentaire à la surface des dents n'induit pas toujours le déclenchement du processus carieux.[4]
Alimentation
Dans le domaine de l'alimentation, ce sont les glucides, dont le saccharose, le glucose, le fructose, qui sont essentiels pour le métabolisme des bactéries. Les bactéries, lors de ce processus, métabolisent ceux-ci et rejetteront de l'acide organique qui viendra déminéraliser la surface de la dent. [13] Une prise importante de sucre fermentescible ainsi qu'un environnement acide favorise la multiplication et la colonisation de S. mutans et des lactobacilles.[13]
Il a été prouvé que la fréquence de consommation de sucre serait tout aussi importante dans le développement du processus carieux que la quantité ingérée.[4] De plus, plus un aliment est collant, plus celui-ci devient cariogène, car le temps de clairance par la salive s'en trouve augmenté, rendant les glucides présents davantage disponible pour le métabolisme des bactéries.[13][4] Le saccarose est le glucide considéré comme ayant le pouvoir cariogène le plus important en étant facilement fermentescible pour les bactéries et en pouvant être utilisé pour la production de polysaccarides extracellulaires. Il est aussi un glucide retrouvé le plus couramment dans les aliments sucrés.[3]
Surface dentaire
Finalement, la présence de la dent est un facteur clé, car sans tissu dur dentaire, il ne peut y avoir de carie. L'émail, la dentine et le cément représentent les divers tissus durs dentaires qui peuvent être affectés par la carie. Ces tissus sont composés de matière organique et inorganique en différente proportion. L'émail est le tissu le plus minéralisé et est composé à 95% de matière inorganique. Cette matrice inorganique composée de minéraux de phosphate, de calcium et d'hydroxyde s'organise en cristaux appelés hydroxyapatite. La dentine et le cément contiennent quant à eux une proportion plus importante de matière organique. [3][14][4]
Les surfaces dentaires les plus affectées par la carie sont les puits et fissures, sous le point de contact des dents ainsi que la zone près de la gencive marginale.[4]
Physiopathologie
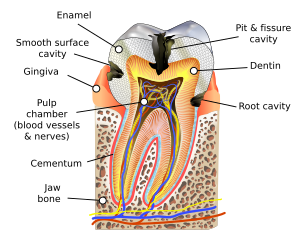
La carie est processus dynamique qui s'effectue dans le temps et dont la première étape est l'adhésion de bactéries à la surface dentaire et la formation de plaque. Pour se faire, certaines bactéries ont la capacité d'adhérer à la surface dentaire par divers mécanismes d'attachement. Par la suite, d'autres bactéries peuvent s'agglomérer et former ainsi la plaque dentaire. Ces bactéries agglomérées entre elles, forme un environnement à l'abri de la salive qui leur permet de croitre et de créer un micro-environnement acide.[14][4]
Les minéraux de la dent sont en équilibre avec l'environnement dans lequel ils se trouvent et sont sujet au processus de déminéralisation et reminéralisation. Lorsque les bactéries cariogènes présentent à la surface des dents sont en contact avec des sucres fermentescibles, celles-ci transforment ces substrats et excrète de l'acide comme déchets. Cet acide entraine une chute de pH qui entraine le processus de déminéralisation. Celui-ci se traduit par la dissolution des cristaux d'hydroxyapatite par l'acide en ions phosphate et calcium qui diffusent vers le milieu environnant. Cet équilibre est influencé par les ions présents et le pouvoir tampon de la salive ainsi que la perméabilité et la structure de la dent. Une attaque acide répétée créera une déminéralisation soutenue et caractérisera le début du processus carieux. Ce processus est également est influencé par les facteurs locaux et systémiques présents. [3][14][4]

Les travaux de Stephan (1940) ont su démontre que la zone critique sous laquelle une déminéralisation de l'émail de la dent est possible se situant entre 5.2 et 5.5 de pH, alors que la dentine débute sa déminéralisation à un pH de 6.4. Le pH chute rapidement sous le seuil critique soit quelques minutes seulement après une consommation de sucre. C'est l'effet tampon et la clairance des glucides par la salive qui permettent un retour graduel à un pH normal et une reminéralisation. [14][4][13]
L'émail est beaucoup plus résistant aux agressions acides que la dentine ou le cément qui, dû à leur composition plus organique, sont plus facilement déminéralisable. L'émail des dents primaires se trouve également plus facilement déminéralisé, ayant une structure plus poreuse et moins bien minéralisée que celle des dents permanentes. [13][11][15]
Lors du premier stade de déminéralisation, appeler carie initiale ou tache blanche, le processus de reminéralisation est encore possible, car il n'y a encore aucune perte de l'intégrité de la structure. Ce processus est donc réversible. Cependant lors que la déminéralisation progresse dans la dent en direction de la dentine, une cavitation se crée, car la dentine devient trop fragile pour supporter l'émail et se brise. Le processus devient alors irréversible.[14][13]
Présentation clinique
Facteurs de risque
Les facteurs de risque de la carie permet au clinicien de statuer le risque carieux du patient, ce qui inclue
- facteurs cliniques et biologiques [18][13][17] :
- présence de plaque dentaire
- exposition des surfaces radiculaires
- perte d'attache gingivale ou une récession gingivale
- restaurations dentaires défectueuses ou des appareils dentaires qui permettent la rétention de plaque
- manque de scellant dentaire
- flot salivaire diminué ou une composition salivaire inadéquate
- nombre important de bactéries cariogènes
- facteurs génétiques
- facteurs autres [13][17][18] :
- Utilisation de certains médicaments
- xérostomie (causé par la médication, la radiothérapie tête et cou, le Syndrome de Sjogren, etc.)
- antécédent de caries ou restaurations récentes dans les 3 dernières années
- antécédents familiaux dans la famille du premier degré (mère ou les frères et soeurs)
- déficience physique ou troubles cognitifs
- présence de comorbidité et de maladies chroniques (diabète, maladie auto-immune, stress, troubles alimentaires, etc.)
- histoire de radiothérapie tête et cou
- âge
- faible statut socioéconomique
- accès aux soins dentaires limités
- les facteurs de protection[13]:
- Bonne hygiène orale
- Bonne composition et bon flot salivaire.
- Application de scellant au niveau des puits et fissures
- Utilisation de fluor ou agents anticaries
Oncologie chirurgicale et radio-oncologie
Une tumeur maligne de la glande salivaire nécessite souvent un traitement chirurgical. La chirurgie pourrait impliquer l'ablation d'une partie ou de la totalité de la glande salivaire occasionnant ainsi une réduction du flux salivaire et augmentant par le fait même le risque de carie.[11][4]
La radiothérapie affecte les tissus des tissus buccaux de plusieurs manières. Les premiers changements après la radiothérapie comprennent la mucite, l'atrophie et l'amincissement de la muqueuse buccale, des modifications fibrotiques et des dysgueusies suite à l'atrophie des papilles gustatives. [19][11] Lorsque la région touchée par la radiothérapie inclue les glandes salivaires, cela conduit à des dommages irréversibles et un défaut rapide de la salivation. Une dose de plus de 26 Gy engendrera une perte irréversible de près de la totalité de la fonction salivaire de la glande.[4] Suite à des traitements de radiothérapie, si aucun traitement préventifs n'est introduit, les patient peuvent développer rapidement de multiples caries, connu sous le nom de caries radiologiques, une forme grave de caries rampantes. Les principales caractéristiques des caries radiologiques est l'atteinte de la cervicale de la dent ainsi que l'implication de la pointe des cuspides. Le taux de progression de la carie radiologique est beaucoup plus rapide que le processus carieux normal. [19][11]
Différentes chimiothérapies peuvent également engendrer une altération du flux salivaire à court terme mais les conséquences à long terme ne semble pas être clairement définies. [4]
Le dentiste doit être mis au courant des traitements du patient pour pouvoir par la suite planifier les traitements ainsi que le suivi de ces patients et ce, même avant le début des traitements.[4]
Questionnaire
- Revoir les facteurs de risque précédents
- Au stade initial, la carie est généralement asymptomatique.
- Lorsque la carie progresse, les patients se plaignent [11][13]:
- de douleur dentaire, provoqué par le froid, la chaleur, à la mastication ou lors d'ingestion de certains aliments
- la gravité de la douleur varie en fonction du stade d'implication, de l'étendue, de la perte de la structure dure et de la réponse réparatrice de l'hôte
- de saignement gingival
- d'aliments se logent dans la zone affectée
- d'une décoloration ou d'une cavitation visible.[4]
- de douleur dentaire, provoqué par le froid, la chaleur, à la mastication ou lors d'ingestion de certains aliments
L'évaluation du risque carieux sera complétée par l'examen clinique du patient et permettra de classifier le risque comme étant faible, modéré ou sévère.[13][17]

Examen clinique
La carie peut se présenter à divers endroits soit :
- sur les surfaces lisses
- au niveau des puits et fissures
- sous une restauration dentaire, etc. [4]
Elle peut également se développer avec une prédilection pour certains sites selon l'âge:
- Enfants en âge préscolaire : surfaces interproximales des molaires primaires
- Enfants d'âge scolaire : surfaces occlusales des molaires des dents permanentes
- Adolescents : surfaces interproximales des molaires et prémolaires
- Personnes âgées présentant des récessions gingivales : surface radiculaire, nommé carie de racine. [4]
La lésion de surface lisse d'émail initiale se représente généralement par une tache blanche sur la surface de la dent due à une augmentation de sa porosité suite à la déminéralisation. Due à cette porosité, la dent finira par colorée avec la prise d'aliments pour devenir brunâtre ou noirâtre à cet endroit. Si la lésion se trouve en zone apparente, le patient peut se plaindre d'une décoloration à la surface de la dent.[11][4]
La lésion initiale de puits et fissure peut facilement passer inaperçue, car elle peut débuter avec un très léger défaut d'émail.[13]
Le dentiste pourra, lors de l'examen physique du patient, procéder à une évaluation visuelle et tactile. Une bonne lumière ainsi que des dents préalablement nettoyer et sèches sont essentielles à un bon examen clinique. Le clinicien pourra alors visualiser la présence d'un changement de coloration, des cavitations ou défectuosités au niveau de la structure dentaire. Il pourra évaluer tactilement la lésion à l'aide de l'explorateur pour sentir la texture ou la présence de cavité, bien que son utilisation soit controversée de nos jours.[13][18] La présence de plaque, l'aspect de la gencive, la présence de restaurations défectueuses ainsi que le débit salivaire sont quelques exemples d'autres indices qui peuvent être évalués par le dentiste et augmenter la suspicion de la présence de lésion carieuse. [13][4]
Encore aujourd'hui, l'examen visuel et tactile, combiné aux radiographies, reste la procédure diagnostique utilisée par les dentistes, bien qu'elle soit imparfaite ayant une sensibilité entre 39-59%, mais une spécificité de plus de 95%. [13][18] Ceci reste cependant le choix d'examen à utiliser étant rapide et facile pour le clinicien. Le fait qu'il n'y ait aucun examen de détection de la carie parfait renforci l'importance du diagnostic précoce ainsi que l'utilisation de traitement préventif permettant de minimiser l'impact des erreurs diagnostiques. [18]
Une carie peut se présenter sous forme active ou arrêtée.
- Une carie active aura une apparence opaque plutôt blanchâtre ou jaunâtre, avec une perte du lustre de surface. Elle peut être couverte de plaque et avoir une texture collante.
- En comparaison, une carie arrêtée sera de couleur plutôt brunâtre avec une apparence lustrée et dur au touché.[17]
L'évaluation du risque carieux clinique sera statué selon la présence de lésions caries actives, débutantes ou extensives. Par exemple, un patient ayant une lésion carieuse extensive, mais avec un risque carieux faible au questionnaire, sera classé comme ayant une probabilité modérée de développer de nouvelles lésions carieuses ou que celle présente progresse alors qu'un patient ayant seulement des lésions carieuses débutantes avec un risque carieux élevé au questionnaire sera classé comme à haut risque de développer de nouvelles caries ou de voir celles présentent se développer. Pour sa part, un patient n'ayant aucune lésion carieuse active pourra être défini comme à un risque faible ou modéré de développer de nouvelles caries selon l'évaluation du risque carieux au questionnaire. [17]
Examens paracliniques
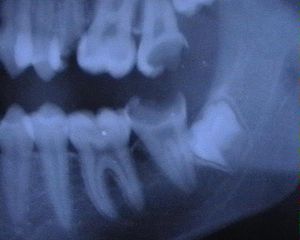
Radiographie
Dans le diagnostic de la lésion carieuse, les radiographies sont utilisées pour visualiser la présence de caries non visibles à l'oeil ou déterminer la profondeur de la lésion, bien qu'elles soient utilisées pour détecter de nombreuses autres affectations buccodentaires.[4]
La carie dentaire se présente radiologiquement par une zone foncée, radiotranslucide. Une certaine quantité de structure dentaire doit être perdue pour pouvoir apercevoir une lésion carieuse radiologiquement. [4]
La carie interproximale, difficile à évaluer à l'examen clinique, se détectera majoritairement à l'aide de radiographie. [13] Des radiographies intraorales périapicales ou interproximales peuvent être prises selon le cas. [4] L'examen radiographie permet également au clinicien de détecter la présence de restaurations défectueuses, de contacts dentaires défectueux, de déterminé l'intégrité de la structure des dents, de voir la présence de traitements endodontiques, de voir des lésions périapicales, de déterminer la proximité pulpaire, etc. [4][13]
La décision de prendre des radiographies ainsi que sa fréquence doivent toujours être effectué selon le jugement clinique du clinicien, en pesant les risques et bénéfices de cet examen qui expose le patient à une dose de radiation.[4] . Lors de l'interprétation de radiographie, la corrélation clinique est de mise pour s'assurer du bon diagnostic. La radiographie est surtout utile pour la détection de caries avancées qui atteignent la dentine, étant peu sensible pour la détection de caries d'émail débutante. Il a été prouvé que la radiographie sous-estime la profondeur des lésions carieuses.[13][18]
Transillumination
L'utilisation de transillumination (FOTI) peut facilement être utilisée par le clinicien en étant un outil rapide et peu dispendieux. Il permet de mieux visualiser les ombrages sous-jacents et peut aider pour la détection de caries occlusales ou interproximales en antérieur. Cet outil bien qu'ayant une sensibilité de moins de 85%, est un outil documenté aidant le clinicien dans la détection de carie dentinaire.[13]
Vitalomètre
Lorsque nécessaire, des tests de vitalité pulpaire peuvent être effectuée pour les dents ayant une carie ou une restauration extensive et dont la vitalité semble douteuse. L'utilisation de froid et du vitalomètre peuvent alors être de bon adjuvant et guider le clinicien vers le bon plan de traitement.[13]
Technologies émergentes
Plusieurs autres technologies, qui tentant d'offrir une aide pour le clinicien dans la détection de la carie, ont vu le jour dans les dernières années. Ces nouvelles technologies, utilisant par exemple la transmission de lumière, la conduction électrique ou les propriétés de transmissions des ultrasons, tentent de détecter et surveiller l'activité carieuse. [13]
Des appareils laser utilisant la transmission de la lumière fluorescente, ont été grandement étudier au cours des dernières années. Cet appareil qui, selon une revue systématique, démontre une meilleure sensibilité que la méthode traditionnelle, démontre également un taux de faux positif élevé, détectant positivement le tartre ou du matériel dentaire fluorescent, et ne devrait donc pas être une méthode primaire de diagnostic de carie. Il peut cependant être utilisé en clinique comme adjuvant et offrir une seconde opinion pour les caries de surfaces occlusales. L'avantage de ces appareils serait cependant de pouvoir diminuer la fréquence de la prise de radiographies pour surveiller la progression de lésions carieuses. [4]
Diagnostic
Le diagnostic de la carie est complexe et requiert une compréhension approfondie de la situation du patient. Pour poser un diagnostic de carie, le dentiste doit corréler les informations retenues au questionnaire, à l'examen clinique ainsi qu'à l'examen radiographie.
Divers systèmes ont été introduits pour déterminer le stade de la carie dentaire et aider le clinicien dans la gestion du traitement des lésions carieuses. Le plus courant est le Système international de détection et d'évaluation des caries (ICDAS), qui est associé au Système international de classification et de gestion des caries (ICCMS). La classification des lésions carieuses et leur activité, corrélé au risque carieux du patient, permettront par la suite de proposer des soins et un plan de traitement adapter au stade de la lésion ainsi qu'au risque carieux du patient.[13][17]
La classification ICDAS, propose une division des lésions carieuses en 6 stades; allant de la dent saine sans évidence de carie au stade 0, à la carie extensive avec cavitation et dentine visible au stade 5-6.[17] Un score radiographique est aussi présent permettant de stratifier les lésions carieuses occlusales visibles sur la radiographie du stade 0 à 6 et déterminer approximativement la profondeur de la lésion carieuse. Par exemple, un code radiographique ICDAS RA 3, signifie une carie initale avec une atteinte du 1/3 externe de la dentine. [17]
-
dent saine
-
Carie d'émail
-
carie atteignant la dentine
-
carie avec atteinte pulpaire
-
Nécrose dentaire et infection périapicale
Diagnostic différentiel
Le diagnostic différentiel des caries dentaires comprend :
- la fluorose dentaire, qui se présente comme une lésion blanchâtre
- les défauts de développement, tels que l'hypominéralisation et l'hypoplasie de la dent. [4][11]
Les caries de racines doivent également être différenciées de résorption cervicale externe. [4]
Traitement
La prise en charge des lésions carieuses dépend de l'étendue, de la gravité et du stade des caries dentaires et les traitements peuvent être de type préventif ou curatif. [11] La gestion de la carie est de plus en plus orientée vers une approche conservatrice.[18]
Au stade initial, une reminéralisation est possible et un traitement préventif doit être envisagé. Celui-ci comprenant le retrait de la plaque dentaire lors du nettoyage dentaire, l'application de gel ou de vernis fluoré, l'application de scellant au niveau des puits et fissures, le renforcement de l'hygiène orale à la maison, le changement des habitudes de vies, alimentaires et orales, etc. Ces traitements non invasifs implique directement le patient et renvoie à l'importance de bien les éduquer et les conscientiser au rôle primaire qu'il joue dans le traitement et la prévention du processus carieux.[18][4]
Lorsqu'il y a perte de l'intégrité de la dent, douleur dentaire, lorsque la carie progresse malgré les traitements préventifs, si la pulpe dentaire est en danger ou que la fonction est entravée, un traitement curatif doit être envisager. L'excavation est alors effectuée et il y aura mise en place de matériaux de restauration, permettant de nettoyer la dent de tout tissu affecté, retrouver l'anatomie de la dent et ainsi améliorer le contrôle de la plaque et ramener le processus carieux à zéro.[11][4][18] Divers matériaux de restauration et techniques existent aujourd'hui et ceux-ci devront être choisi selon le jugement clinique du dentiste. Les matériaux tel le composite permet d'effectuer des traitements restauratifs en préservant au maximum la structure dentaire lorsque le cas le permet. Certains matériels, tel le verre ionomère libère du fluor en continu permettant de reminéraliser la dent. [18]
Les restaurations dentaires ont une durée de vie limités et celles-ci dans la grande majorité des cas à changer au cours de la vie du patient.[4]
Suivi
Le suivi des patients est important puisque la carie est un processus qui se développe dans le temps et qui expérimente des phases de déminéralisation et de reminéralisation. Suite à des traitements dentaires, préventifs ou curatifs, le dentiste, en collaboration avec le patient, pourra déterminer un intervalle de temps pour évaluer l'efficacité des traitements et la réponse à celui-ci. Certains auteurs recommandent un suivi aussi rapide que deux à trois semaines suivant le traitement initiale.
Le suivi à long terme pourra être individualisé selon les besoins du patient. Selon leur situation, le suivi devrait être fait à tous les trois à 24 mois selon la situation du patient. [13][4] Celui-ci est important pour prévenir et détecter l'apparition ou le développement de lésions carieuses, pour faire le suivi des conseils et traitements mis en place, pour motiver les patients et pour trouver de nouvelles avenues ou renforcer les habitudes mis en place. [13]
Une des stratégies de suivi à long terme consiste à établir celui-ci selon l'évaluation du risque carieux du patient. En ce sens, l'ICCMS propose une gestion de la carie selon le niveau de risque faible, modéré ou sévère et propose diverses mesures à mettre en place pour le patient tant à la maison que des traitements au cabinet dentaire. [17] Ces mesures peuvent inclure une amélioration des techniques de brossage et d'hygiène orale, l'usage de dentifrice à haute teneur en fluor, la prescription d'un rince-bouche fluoré, etc. Au cabinet dentaire ceci peut se traduire par des entrevues motivationnelles, des rencontres nutritionnelles, l'application de scellant, l'application de vernis fluoré, des rendez-vous de suivi 3 mois, etc. [17]
Chaque patient doit en en fait avoir un suivi personnalisé qui répond à ses besoins et sa situation ainsi qu'à sa motivation et son parcours. Le dentiste doit identifier les facteurs de risques principales dans la situation du patient pour assurer d'une gestion efficace de la carie. Des changements doivent être encouragés, mais pas plus que quelques-uns à la fois. [4]
Complications
Lorsque non traité la carie dentaire peut progresser et atteindre la pulpe. Lorsque la pulpe est atteinte, la vitalité de la dent est compromise et une infection se déclenche. Elle peut alors entrainer des complications tels pulpite, parodontite périapicale, abcès périapical ou un granulome périapical, un kyste périapical, une cellulite, un abcès, une périostite et peuvent évoluer vers une ostéomyélite.[11]
La carie dentaire peut également engendrer la fracture des dents, de la douleur, une halitose, la perte de dents, une limitation dans la fonction et même un handicap. [4]
Prévention
Le déclin de la carie dentaire a été attribué à plusieurs facteurs. Parmi tous les facteurs, l'éducation des patients joue un rôle clé. Les facteurs liés au patient comprennent le maintien de l'hygiène buccodentaire, la réduction de la consommation de sucre, l'utilisation efficace des fluorures et le suivi dentaire de routine en cabinet.[11]
Brossage des dents et soie dentaire
Les patients doivent être éduqués à effectuer un brossage régulier des dents avec un dentifrice fluoré et une soie dentaire. [11] Les enfants devraient avoir une aide pour le brossage ainsi que les personnes âgées avec des difficultés physiques ou cognitives. La technique de brossage est importante ainsi que la motivation du patient à l'effectuer de façon régulière et appropriée. Les brosses à dents électriques sont selon des études plus efficaces pour le retrait de la plaque dentaire que le brossage manuel. Un brossage des dents de façon régulière permet de prévenir la carie en retirant la plaque dentaire, si celui-ci est correctement effectué et si effectué avec un dentifrice fluoré.[4] L'utilisation de la soie dentaire est importante et peut être personnalisée selon la motivation et les besoins du patient en sélectionnant certains sites plus problématiques par exemple.[4] L'utilisation de la soie dentaire aide également à diminuer l'accumulation de plaque dentaire dans la région interdentaire et sa technique d'utilisation devrait être enseignée au patient.[4]
Application de fluor
L'utilisation de fluor est aujourd'hui reconnue comme étant le facteur primairesayant occasionné le déclin de la prévalence de la carie dentaire.[16] Des études ont en effet prouvé que la fluoration serait plus bénéfique pour la prévention de la carie dentaire comparativement à une diminution de la prise de sucres.[13] Le fluor est disponible sous forme topique ou systémique. Le fluor pour utilisation systémique peut se retrouver sous forme d'eau fluorée, de sel, de lait ou de suppléments contenant du fluor. La fluoration de l'eau est une solution recommandée dans plusieurs pays au travers le monde, mais son utilisation est encore controversé dans au sein de la communauté scientifique tant qu'à ses risques et bénéfices.[16] En application topique, on peut retrouver du fluor dans les pâtes à dent, en rince-bouche, en gel, en mousse, en vernis, etc. Son utilisation doit être adaptée au patient et les applications topiques sont plus efficaces que les méthodes de fluoration systémique.[16] Une revue systématique à conclue en 2004 que l'utilisation du dentifrice fluor réduirait de 24% des caries en dentition permanente chez les adolescents et les enfants et que l'utilisation du vernis fluoré réduirait la carie de 33% en dentition primaire et 46% en dentition permanente.[4] Le fluorure aurait en fait le potentiel d'inhiber la déminéralisation et améliorer la reminéralisation de la structure dentaire par la formation d'un cristal de fluorapatite résistant aux acides, tant au niveau de l'émail que de la dentine. Il augmenterait ainsi la résistance à l'acide, diminuant la solubilité de la dent et augmentant sa qualité. Il faut cependant être prudent lors de l'administration de fluor systémique lors de la formation des dents, car un excès pourrait causer la fluorose dentaire, si administré en quantité importante.[16][13]
Utilisation de rince-bouche à la chlorexidine
La chlorexidine est reconnue pour avoir un effet bactériostatique à faible concentration et des propriétés antimicrobienne et antiplaquetaire tout en ayant des effets systémiques rares. Des effets secondaires tels une décoloration des dents ou de la langue ainsi qu'un changement au niveau du gout peuvent être notés. [4]
Application de scellants pour puits et fissures
Les puits et les fissures présentent une morphologie non nettoyable et sont donc le site le plus sensible pour le développement initial des caries. L'application des scellants agit comme une barrière mécanique privant les bactéries sous jacentes des nutriments et arrête ainsi la progression des caries dentaires. L'utilisation des scellants sur les surfaces occlusales est largement recommandée par plusieurs études, mais la prévalence de carie de la population et des individus doit être prise en compte. Son application doit être bien réalisé pour que ceux-ci soient efficaces. [18]
Changement des habitudes alimentaires
La consommation de sucre étant l'un des principaux facteurs étiologiques de la carie dentaire, le contrôle de la diète devrait également faire parti du plan de traitement préventif. Les patients devraient toujours être informés des risques d'une diète cariogène riche en sucre, mais certains patients pourraient bénéficier d'un suivi plus serré avec une analyse complète de leur alimentation. Ceci devient un travail d'équipe entre le patient et le dentiste pour trouver des solutions acceptables pour réduire le risque carieux et la fréquence de prise d'aliments cariogènes. [4] La quantité de salive, la composition de la plaque, l'utilisation de fluor ainsi que le statut socioéconomique du patient devraient être pris en compte lorsque l’on traite de changement au niveau de la diète. Bien que l'ingestion de sucre est le facteur qui a une influence majeure sur la carie dentaire, celui-ci devrait être pris en considération selon son mode de consommation. En effet, la consommation de sucre entre les repas est beaucoup plus à risque de créer un environnement favorable à la carie comparativement à la prise de ces aliments lors des repas qui stimule davantage la production de salive et diminue le risque carieux.[3][4] Des aliments tels les céréales sucrés, divers breuvages sucrés, la marmemade, le ketchup, les chips, et bien plus encore, renferment également beaucoup de sucre. Les médicaments, surtout ceux pour enfants, peuvent également contenir du sucre, certains sont composés jusqu'à 70% de sucre. [13][4] Certains aliments tels le fromage ou les noix ont pouvoir de protection contre la carie dentaire aidant entre autres à diminuer la production acide et aidant à nettoyer la surface des dents lorsque consommé. [4]
Utilisation d'agents sucrants anticarie
Le xylitol est un agent sucrant pouvant remplacer le saccarose ayant non seulement un potentiel non cariogène, mais également des propriétés anticaries. Le mécanisme anticarie de ce produit proviendrait de sa capacité à prévenir de la liaison du saccarose à S. mutans, interrompant ainsi la production d'acide, en plus de prévenir l'adhésion de ces bactéries avec les autres en diminuant sa production de polysaccarides.[11][4][16] D'autres agents sucrants alternatifs tels le sorbitol, le mannitol, le lyrasin et le maltitol sont également des agents non cariogènes. [4]
Flot salivaire
Une autre avenue de prévention importante comprend une composition et un flot salivaire adéquat. En effet la salive permet de nettoyer la surface des dents, de neutraliser l'acidité créer, d'aider la reminéralisation, de prévenir la déminéralisation en plus d'avoir des propriétés antimicrobiennes importantes.[13][4] Le manque de salive a des conséquences importantes sur la progression rapide de la carie dentaire. [18] Des adjuvants tels des bonbons sans sucre stimulant la salivation ainsi des produits de salive artificiels peuvent être utilisés pour les patients ayant de la xérostomie et diminuer les symptômes associés. La prévention de la carie dentaire sera faite par une utilisation de gouttières de fluor, une hygiène orale adéquate ainsi que la réduction au maximum de la consommation d'aliments cariogènes.[4]
Références
- Cette page a été modifiée ou créée le 2020/07/11 à partir de Dental Caries (StatPearls / Dental Caries (2020/06/03)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/31869163 (livre).
- ↑ 1,0 et 1,1 « L'état de la santé buccodentaire au Canada », sur www.cda-adc.ca (consulté le 18 août 2020)
- ↑ « Santé bucco dentaire », sur www.who.int (consulté le 19 août 2020)
- ↑ 3,0 3,1 3,2 3,3 3,4 3,5 3,6 et 3,7 Piette, Étienne. et Goldberg, Michel., La dent normale et pathologique, De Boeck Université, (ISBN 2-8041-3489-X et 978-2-8041-3489-1, OCLC 50336149, lire en ligne)
- ↑ 4,00 4,01 4,02 4,03 4,04 4,05 4,06 4,07 4,08 4,09 4,10 4,11 4,12 4,13 4,14 4,15 4,16 4,17 4,18 4,19 4,20 4,21 4,22 4,23 4,24 4,25 4,26 4,27 4,28 4,29 4,30 4,31 4,32 4,33 4,34 4,35 4,36 4,37 4,38 4,39 4,40 4,41 4,42 4,43 4,44 4,45 4,46 4,47 et 4,48 Fejerskov, Ole. et Kidd, Edwina A. M., Dental caries : the disease and its clinical management, Blackwell Munksgaard, (ISBN 978-1-4051-3889-5 et 1-4051-3889-0, OCLC 136316302, lire en ligne)
- ↑ Paula Moynihan, « Sugars and Dental Caries: Evidence for Setting a Recommended Threshold for Intake », Advances in Nutrition (Bethesda, Md.), vol. 7, no 1, , p. 149–156 (ISSN 2156-5376, PMID 26773022, Central PMCID 4717883, DOI 10.3945/an.115.009365, lire en ligne)
- ↑ Spencer L James, Degu Abate, Kalkidan Hassen Abate et Solomon M Abay, « Global, regional, and national incidence, prevalence, and years lived with disability for 354 diseases and injuries for 195 countries and territories, 1990–2017: a systematic analysis for the Global Burden of Disease Study 2017 », The Lancet, vol. 392, no 10159, , p. 1789–1858 (ISSN 0140-6736, PMID 30496104, Central PMCID PMC6227754, DOI 10.1016/s0140-6736(18)32279-7, lire en ligne)
- ↑ Poul Erik Petersen, Denis Bourgeois, Hiroshi Ogawa et Saskia Estupinan-Day, « The global burden of oral diseases and risks to oral health », Bulletin of the World Health Organization, vol. 83, no 9, , p. 661–669 (ISSN 0042-9686, PMID 16211157, Central PMCID 2626328, DOI /S0042-96862005000900011, lire en ligne)
- ↑ 8,0 et 8,1 (en-US) N.J. Kassebaum, A.G.C. Smith, E. Bernabé et T.D. Fleming, « Global, Regional, and National Prevalence, Incidence, and Disability-Adjusted Life Years for Oral Conditions for 195 Countries, 1990–2015: A Systematic Analysis for the Global Burden of Diseases, Injuries, and Risk Factors », Journal of Dental Research, vol. 96, no 4, , p. 380–387 (ISSN 0022-0345 et 1544-0591, PMID 28792274, Central PMCID PMC5912207, DOI 10.1177/0022034517693566, lire en ligne)
- ↑ 9,0 9,1 et 9,2 Jo E. Frencken, Praveen Sharma, Laura Stenhouse et David Green, « Global epidemiology of dental caries and severe periodontitis - a comprehensive review », Journal of Clinical Periodontology, vol. 44 Suppl 18, , S94–S105 (ISSN 1600-051X, PMID 28266116, DOI 10.1111/jcpe.12677, lire en ligne)
- ↑ (en) Tungare S et Paranjpe Ag, « Baby Bottle Syndrome », sur PubMed, 2020 jan (PMID 30570970, consulté le 28 juillet 2020)
- ↑ 11,00 11,01 11,02 11,03 11,04 11,05 11,06 11,07 11,08 11,09 11,10 11,11 11,12 et 11,13 (en) Rathee M et Sapra A, « Dental Caries », sur PubMed, 2020 jan (PMID 31869163, consulté le 28 juillet 2020)
- ↑ Galarneau C, Arpin S, Boiteau V, Dubé MA, Hamel D, Wassef N. Étude clinique sur l’état de santé buccodentaire des élèves québécois du primaire 2012-2013 (ÉCSBQ) – Rapport national. 2e éd. Montréal : Institut national de santé publique du Québec; 2018.
- ↑ 13,00 13,01 13,02 13,03 13,04 13,05 13,06 13,07 13,08 13,09 13,10 13,11 13,12 13,13 13,14 13,15 13,16 13,17 13,18 13,19 13,20 13,21 13,22 13,23 13,24 13,25 13,26 13,27 13,28 13,29 13,30 et 13,31 Hilton, Thomas J.,, Ferracane, Jack L., et Broome, James C.,, Summitt's fundamentals of operative dentistry : a contemporary approach (ISBN 978-0-86715-657-7 et 0-86715-657-0, OCLC 880878412, lire en ligne)
- ↑ 14,0 14,1 14,2 14,3 14,4 14,5 14,6 et 14,7 HIREMATH, S. S., Textbook of preventive and community dentistry., ELSEVIER INDIA, (ISBN 81-312-2530-5 et 978-81-312-2530-1, OCLC 993695037, lire en ligne)
- ↑ 15,0 et 15,1 Carounanidy Usha et Sathyanarayanan R, « Dental caries - A complete changeover (Part I) », Journal of conservative dentistry: JCD, vol. 12, no 2, , p. 46–54 (ISSN 0974-5203, PMID 20617066, Central PMCID 2898091, DOI 10.4103/0972-0707.55617, lire en ligne)
- ↑ 16,0 16,1 16,2 16,3 16,4 16,5 16,6 16,7 et 16,8 Zhou, Xuedong, 1957-, Dental caries : principles and management (ISBN 978-3-662-47450-1 et 3-662-47450-6, OCLC 926047075, lire en ligne)
- ↑ 17,00 17,01 17,02 17,03 17,04 17,05 17,06 17,07 17,08 17,09 et 17,10 Pitts, N. B., Ismail, A. I., Martignon, S., Ekstrand, K., Douglas, G. V. A., Longbottom, C., ... Zero, D. (2014). ICCMS™ Guide for Practitioners and Educators. ICDAS Foundation.
- ↑ 18,00 18,01 18,02 18,03 18,04 18,05 18,06 18,07 18,08 18,09 18,10 et 18,11 Robert H. Selwitz, Amid I. Ismail et Nigel B. Pitts, « Dental caries », Lancet (London, England), vol. 369, no 9555, , p. 51–59 (ISSN 1474-547X, PMID 17208642, DOI 10.1016/S0140-6736(07)60031-2, lire en ligne)
- ↑ 19,0 et 19,1 Samuel J. Rubin, Kevin Y. Wu, Diana N. Kirke et Waleed H. Ezzat, « Head and Neck Cancer Complications in the Geriatric Population Based on Hospital Case Volume », Ear, Nose, & Throat Journal, , p. 145561319856006 (ISSN 1942-7522, PMID 31170822, DOI 10.1177/0145561319856006, lire en ligne)





