Rougeole
| Maladie | |
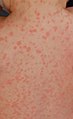
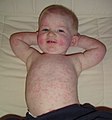
 Un enfant avec un rash au jour 4 | |
| Caractéristiques | |
|---|---|
| Signes | Diminution de l'état général, Conjonctivite bulbaire , Macules érythémateuses, Papules, Taches de Koplik, Exanthème, Énanthème , Muqueuse nasale congestive , Température corporelle élevée |
| Symptômes |
Irritabilité, Congestion nasale, Rhinorrhée, Mal de gorge, Toux , Prurit cutané , Malaises |
| Diagnostic différentiel |
Septicémie, Maladie de Kawasaki, Érythème infectieux, Scarlatine, Exanthème médicamenteux, Infection à parvovirus B19, Infections entérovirales pédiatriques, Syndrome du choc toxique, Rubéole, Méningite |
| Informations | |
| Terme anglais | Measles |
| Wikidata ID | Q79793 |
| Spécialité | Infectiologie |
|
| |
La rougeole est une maladie virale fébrile aiguë évitable, hautement contagieuse. Elle reste une cause importante de mortalité et de morbidité mondiale, notamment dans les régions d'Afrique et d'Asie du Sud-Est.[1][2] La rougeole est une MADO au Québec[3].
Les responsables de la santé publique ont déclaré l'élimination de la rougeole aux États-Unis en 2000, marquant l'absence de transmission continue de la maladie pendant un an et depuis la région des Amériques en 2016. Cependant, des épidémies continuent de se produire par le biais de maladies importées et de transmission parmi des groupes d'enfants non vaccinés. dans la communauté. La rougeole est une maladie à déclaration obligatoire dans la plupart des pays, y compris les États-Unis.[4][5]
Épidémiologie

L'épidémiologie de la rougeole est variable à travers le monde et est liée aux niveaux de vaccination atteints dans une région particulière. Avant la mise en œuvre de programmes de vaccination à grande échelle, la rougeole était à l'origine d'environ 2,6 millions de décès. Malgré la vaccination à l'époque actuelle, l'OMS a signalé qu'environ 134 200 décès (15 décès/heure) sont survenus en 2015 en raison de la rougeole. Selon le CDC, il y avait 372 cas en 2018 et 764 cas jusqu'en mai 2019. La rougeole est une maladie à déclaration obligatoire dans la plupart des pays.[5]
Le virus de la rougeole n'a pas de réservoir animal et n'est présent que chez l'homme. Le virus est très contagieux, chaque cas pouvant provoquer 14 à 18 cas secondaires parmi les populations sensibles. La rougeole se transmet de personne à personne par des gouttelettes respiratoires, des aérosols de petites particules et un contact étroit. La période d'incubation est de 10 à 14 jours bien que des périodes plus longues aient été signalées. Les jeunes enfants non vaccinés et les femmes enceintes courent un risque élevé de contracter la rougeole, et la rougeole affecte le plus souvent les jeunes enfants. Plus récemment, il y a eu un glissement vers les enfants plus âgés et les adolescents en raison de l'augmentation des niveaux de couverture vaccinale et des modifications des niveaux d'immunité de la population à différents âges. Les jeunes nourrissons nés de mères dotées d'une immunité acquise sont protégés contre la rougeole en raison du transfert passif d'anticorps, mais à mesure que ces anticorps diminuent, ils deviennent sensibles. L'infectiosité d'un cas est maximale dans les quatre jours avant et quatre jours après l'apparition de l'éruption cutanée, ce qui coïncide avec les pics de virémie et les caractéristiques de la toux, de la conjonctivite et du coryza.[6][7][8][9]
Étiologies
L'organisme responsable est le virus de la rougeole , membre de la famille des Paramyxoviridae et du genre Morbillivirus. Il s'agit d'un virus à ARN de sens négatif enveloppé, simple brin, non segmenté. Le génome code six protéines structurelles et deux protéines non structurelles, V et C. Les protéines structurelles sont la nucléoprotéine, la phosphoprotéine, la matrice, la fusion, l'hémagglutinine (HA) et la grande protéine. La protéine HA est responsable de l'attachement du virus à la cellule hôte.[10]
Physiopathologie
Le virus inhalé à partir des gouttelettes exposées infecte initialement les lymphocytes des voies respiratoires, les cellules dendritiques et les macrophages alvéolaires. Il se propage ensuite au tissu lymphoïde adjacent et se diffuse dans la circulation sanguine, entraînant une virémie et se propageant à des organes distants. Le virus résidant dans les cellules dendritiques et les lymphocytes se transfère aux cellules épithéliales des voies respiratoires qui sont excrétées et expulsées sous forme de gouttelettes respiratoires lors de la toux et des éternuements, infectant les autres et perpétuant le cycle. L'inflammation initiale entraîne des symptômes de coryza, de conjonctivite et de toux. L'apparition de la fièvre coïncide avec le développement de la virémie. L'éruption cutanée survient après dissémination et est due à des infiltrats périvasculaires et lymphocytaires.[5]
Pendant la phase prodromique, le virus de la rougeole déprime l'immunité de l'hôte en supprimant la production d'interféron par ses protéines non structurelles, V et C. La réplication virale croissante déclenche alors des réponses immunologiques humorales et cellulaires. La réponse humorale initiale consiste en une production d'anticorps IgM, qui est détectable 3 à 4 jours après l'apparition de l'éruption cutanée et peut persister pendant 6 à 8 semaines. Par la suite, des anticorps IgG sont produits, principalement contre la nucléoprotéine virale. Les réponses immunitaires cellulaires sont essentielles pour la récupération, comme le montrent les niveaux élevés d'interféron gamma plasmatique dépendant de Th1 pendant la phase aiguë, et l'élévation subséquente des niveaux d'interleukine 4, d'interleukine 10 et d'interleukine 13 dépendant de Th2.[11][5]
Le virus de la rougeole est connu pour induire une immunosuppression qui peut durer des semaines, des mois, voire des années. Cela provoque une susceptibilité accrue aux infections bactériennes et autres secondaires. Bien que les mécanismes à l'origine de ce phénomène ne soient pas clairs, l'hypothèse est que l'infection rougeoleuse induit la prolifération de lymphocytes spécifiques de la rougeole qui remplacent les cellules mémoire précédemment établies provoquant une « amnésie immunitaire ». Cela se traduit par une sensibilité accrue de l'hôte aux infections secondaires, entraînant la plupart de la morbidité et de la mortalité associées à la rougeole. Les anticorps IgG neutralisants contre l'hémagglutinine sont responsables d'une immunité à vie car ils empêchent les récepteurs de la cellule hôte de se lier au virus.[5]
Présentation clinique
Toute contribution serait appréciée.
| Description: | Cette section contient la sous-section optionnelle Facteurs de risque et les sous-sections obligatoires Questionnaire et Examen clinique. |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: |
|
| Exemple: |
(Aucun texte)
(Texte)
(Texte)
(Texte) |
La définition de cas clinique de la rougeole par l'OMS est « toute personne présentant de la fièvre, une éruption maculopapuleuse généralisée, de la toux, un coryza ou une conjonctivite ». La rougeole est un exanthème fébrile aigu caractérisé par les trois « C » : toux, coryza et conjonctivite. Les taches de Koplik, de petites papules blanches sur la muqueuse buccale, sont pathognomoniques de la rougeole et apparaissent un jour ou deux avant l'éruption, bien qu'elles ne soient pas toujours visibles. L'éruption précède l'apparition de la fièvre, apparaissant d'abord sur le visage et s'étendant caudale pour se généraliser. La rougeole non compliquée disparaît généralement en une semaine après l'apparition de l'éruption cutanée.[12][5]
Facteurs de risque
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section contient les facteurs de risque de la maladie. Ces facteurs de risque peuvent être des maladies, des anomalies génétiques, des caractéristiques individuelles (l'âge, le sexe, l'origine ethnique, un certain type d'alimentation), etc. |
| Formats: | Liste à puces, Tableau |
| Balises sémantiques: | Facteur de risque |
| Commentaires: |
|
| Exemple: | Les facteurs de risque de l'infarctus du myocarde sont :
|
Questionnaire
Toute contribution serait appréciée.
| Description: | Cette section traite des symptômes à rechercher à l'anamnèse (questionnaire). Les symptômes sont ressentis et exprimés par les patients. |
| Formats: | Liste à puces |
| Balises sémantiques: | Symptôme, Élément d'histoire |
| Commentaires: |
|
| Exemple: | Les symptômes de l'infarctus du myocarde sont :
D'autres éléments à rechercher au questionnaire de l'infarctus sont :
Il est parfois pertinent de mentionner des symptômes qui sont absents, comme dans la pharyngite à streptocoque. Les symptômes de la pharyngite à streptocoque sont :
|
Examen clinique
Toute contribution serait appréciée.
| Description: | Cette section traite des signes à rechercher lors de l'examen clinique. |
| Formats: | Liste à puces |
| Balises sémantiques: | Examen clinique, Signe clinique |
| Commentaires: |
|
| Exemple: | L'examen physique de l'appendicite démontrera les éléments suivants :
|
Examens paracliniques
Toute contribution serait appréciée.
| Description: | Cette section concerne les tests à demander lorsque la maladie est suspectée et les résultats attendus en présence de la maladie. |
| Formats: | Liste à puces, Tableau |
| Balises sémantiques: | Examen paraclinique, Signe paraclinique |
| Commentaires: |
|
| Exemple: | Les examens suivants sont utiles dans la démarche d'investigation du VIPome :
|
- Examen paraclinique 1 : signe paraclinique 1, signe paraclinique 2, ...
- Examen paraclinique 2 : signe paraclinique 3, signe paraclinique 4, ...
- ...
Le diagnostic de rougeole repose sur une forte suspicion clinique, en particulier lors de l'évaluation d'enfants atteints d'une maladie fébrile et d'une éruption maculopapuleuse. Une formule sanguine complète peut montrer une leucopénie, en particulier une lymphopénie, et une thrombocytopénie. Des anomalies électrolytiques peuvent être détectées chez les enfants ayant un apport insuffisant ou une diarrhée. L'identification d'anticorps IgM spécifiques du virus de la rougeole dans le sérum ou le plasma confirme le diagnostic, bien qu'elle puisse être un faux négatif dans jusqu'à 25 % des cas lorsqu'elle est effectuée tôt (moins de 3 jours après l'apparition de l'éruption cutanée). Ces anticorps atteignent généralement leur pic en 1 à 3 semaines après le début d'une éruption cutanée et deviennent indétectables en 4 à 8 semaines. Le test de référence est le test de neutralisation par réduction de plaque qui a la sensibilité la plus élevée. Le virus de la rougeole peut être cultivé à partir de sécrétions nasopharyngées, mais cela demande beaucoup de travail et n'est pas pratique.[13][5]
Dans la pratique clinique actuelle, la détection par réaction en chaîne de la polymérase de l'acide ribonucléique viral à partir d'échantillons de gorge, de nez, de nasopharynx et d'urine est le plus souvent effectuée, avec une sensibilité approchant les 100 %. [5]
Approche clinique
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Alors que les sections Questionnaire, Examen clinique et Examens paracliniques servent à énumérer, cette section sert à intégrer tous ces éléments pour discuter du raisonnement du clinicien. C'est en quelque sorte la manière dont les cliniciens réfléchissent lorsque confrontés à cette maladie : c'est la section par excellence pour l'enseignement. |
| Formats: | Texte, Liste à puces, Tableau |
| Balises sémantiques: | |
| Commentaires: |
|
| Exemple: | |
Diagnostic
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section traite de la manière dont on peut diagnostiquer une maladie en tenant compte de l'histoire, de l'examen clinique et des investigations. C'est dans cette section que se retrouveront les critères permettant d'infirmer ou de confirmer la présence de la maladie (lorsqu'ils existent). |
| Formats: | Texte, Liste à puces, Tableau |
| Balises sémantiques: | |
| Commentaires: |
|
| Exemple: | L'asystolie est un diagnostic électrocardiographique. L'absence d'activité électrique chez un patient inconscient sans pouls permet de confirmer le diagnostic, tout en s'assurant qu'il n'y a pas de cable débranché et que la calibration du moniteur est adéquate.
Selon le Fourth Universal Definition of Myocardial Infarction, l'infarctus aigu du myocarde est diagnostiqué lorsqu'il y a :
|
Diagnostic différentiel
Le diagnostic différentiel[5]:
- Exanthème médicamenteux
- Erythème infectieux
- Maladie de Kawasaki
- Méningite
- Infection à parvovirus B19
- Infections entérovirales pédiatriques
- Rubéole pédiatrique
- Septicémie pédiatrique
- Syndrome du choc toxique pédiatrique
- Scarlatine
-
Rash à l'amoxicilline
-
Rash de la rubéole
-
Rask de la maladie de Kawasaki
-
Rash de la cinquième maladie (Parvovirux B19)
-
Rash de la scarlatine, notez les joues rouges
Traitement
Toute contribution serait appréciée.
| Description: | Cette section décrit le traitement de la maladie. |
| Formats: | Liste à puces, Tableau, Texte |
| Balises sémantiques: | Traitement, Traitement pharmacologique |
| Commentaires: |
|
| Exemple: | |
Il n'y a pas de traitement antiviral spécifique pour la rougeole ; le traitement est principalement de soutien. Le contrôle de la fièvre, la prévention et la correction de la déshydratation et les mesures de contrôle des infections, y compris l'isolement approprié, constituent la base du traitement.[14][5]
L'OMS recommande l'administration de doses quotidiennes de vitamine A pendant 2 jours et plus pour les enfants malnutris. Les complications de la rougeole doivent être identifiées tôt et un traitement approprié initié.[15][5]
Suivi
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section traite du suivi de la maladie. |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: |
|
| Exemple: | |
Complications
Toute contribution serait appréciée.
| Description: | Cette section traite des complications possibles de la maladie. |
| Formats: | Liste à puces, Texte |
| Balises sémantiques: | Complication |
| Commentaires: |
|
| Exemple: | Les complications de l'infarctus du myocarde sont :
|
Les complications de la rougeole surviennent le plus souvent chez les jeunes nourrissons, les femmes enceintes et les enfants malnutris ou immunodéprimés. La complication la plus courante est la pneumonie qui peut être due au virus de la rougeole lui-même (pneumonie à cellules géantes de Hecht) ou à une infection bactérienne secondaire. D'autres complications incluent le croup, l'otite moyenne et la diarrhée due aux infections secondaires. Les femmes enceintes atteintes de rougeole courent un risque accru de décès maternel, d'avortement spontané, de mort fœtale intra-utérine et de nourrissons de faible poids à la naissance. La kératoconjonctivite rougeoleuse survient principalement chez les enfants présentant une carence en vitamine A et peut conduire à la cécité. Les complications du système nerveux central comprennent l'encéphalomyélite aiguë disséminée (ADEM), l'encéphalite à inclusions de rougeole (MIBE) et la panencéphalite sclérosante subaiguë (SSPE).[16] L'ADEM est une maladie démyélinisante auto-immune qui survient en quelques jours à quelques semaines. infection cérébrale chez les patients présentant une immunité cellulaire altérée survenant dans les mois suivant l'infection initiale. La PESS est une maladie neurologique progressive qui se présente 5 à 10 ans après la maladie aiguë et qui serait causée par une réponse anormale de l'hôte à la production de virions mutés.[17] Elle survient principalement chez les enfants qui ont développé la rougeole avant convulsions et perte progressive des fonctions cognitives et motrices.[5]
Évolution
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section contient le pronostic et évolution naturelle de la maladie. Le pronostic est lié à la survie du patient atteint de la maladie. L'évolution naturelle est la manière dont évoluera la maladie du patient dans le temps. |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: | |
| Exemple: | La dissection aortique est associée une mortalité très élevée. Au moins 30% des patients décèdent après leur arrivée à l'urgence, et ce, même après une intervention chirurgicale. Pour ceux qui survivent à la chirurgie, la morbidité est également très élevée et la qualité de vie est mauvaise. La mortalité la plus élevée d'une dissection aortique aiguë est dans les 10 premiers jours. Les patients qui ont une dissection chronique ont tendance à avoir un meilleur pronostic, mais leur espérance de vie est raccourcie par rapport à la population générale.[1] Sans traitement, la mortalité est de 1 à 3% par heure au cours des 24 premières heures, 30% à une semaine, 80% à deux semaines et 90% à un an. |
Bien que beaucoup se remettent de la rougeole sans complications, il existe un risque de mauvais pronostic. Les complications les plus courantes dues à l'infection par la rougeole comprennent l'otite moyenne et la diarrhée. L'otite peut entraîner une perte auditive. Les plus susceptibles d'avoir des complications graves sont les nourrissons et les enfants de moins de cinq ans, les adultes de plus de vingt ans, les femmes enceintes et les personnes immunodéprimées. Une encéphalite peut survenir chez 1 enfant infecté sur 1000 et 1 à 2 de tous les enfants infectés mourront de complications neurologiques ou respiratoires de la rougeole.[5]
Prévention
La rougeole est une maladie évitable en raison de la disponibilité d'un vaccin sûr, peu coûteux et efficace. Le vaccin est une souche de rougeole vivante atténuée qui est utilisée soit en tant que composant unique, soit en tant que vaccin combiné (ROR, ROR-V).
Pour éliminer la rougeole, les taux de vaccination de la population doivent être compris entre 93 et 95 %.[5]
Références
- Cette page a été modifiée ou créée le 2021/06/16 à partir de Measles (StatPearls / Measles (2021/02/26)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/28846330 (livre).
- ↑ William J. Moss, « Measles », Lancet (London, England), vol. 390, no 10111, , p. 2490–2502 (ISSN 1474-547X, PMID 28673424, DOI 10.1016/S0140-6736(17)31463-0, lire en ligne)
- ↑ Johan Christiaan Bester, « Measles and Measles Vaccination: A Review », JAMA pediatrics, vol. 170, no 12, , p. 1209–1215 (ISSN 2168-6211, PMID 27695849, DOI 10.1001/jamapediatrics.2016.1787, lire en ligne)
- ↑ « Démarche pour les médecins - Maladies à déclaration obligatoire (MADO) et signalements en santé publique - Professionnels de la santé - MSSS », sur www.msss.gouv.qc.ca (consulté le 16 juin 2021)
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/26610423
- ↑ 5,00 5,01 5,02 5,03 5,04 5,05 5,06 5,07 5,08 5,09 5,10 5,11 5,12 et 5,13 Noah P. Kondamudi et James R. Waymack, StatPearls, StatPearls Publishing, (PMID 28846330, lire en ligne)
- ↑ Melissa M. Coughlin, Andrew S. Beck, Bettina Bankamp et Paul A. Rota, « Perspective on Global Measles Epidemiology and Control and the Role of Novel Vaccination Strategies », Viruses, vol. 9, no 1, (ISSN 1999-4915, PMID 28106841, Central PMCID 5294980, DOI 10.3390/v9010011, lire en ligne)
- ↑ S. Santibanez, J. M. Hübschen, M. C. Ben Mamou et M. Muscat, « Molecular surveillance of measles and rubella in the WHO European Region: new challenges in the elimination phase », Clinical Microbiology and Infection: The Official Publication of the European Society of Clinical Microbiology and Infectious Diseases, vol. 23, no 8, , p. 516–523 (ISSN 1469-0691, PMID 28712666, DOI 10.1016/j.cmi.2017.06.030, lire en ligne)
- ↑ Yuki Furuse et Hitoshi Oshitani, « Global Transmission Dynamics of Measles in the Measles Elimination Era », Viruses, vol. 9, no 4, (ISSN 1999-4915, PMID 28420160, Central PMCID 5408688, DOI 10.3390/v9040082, lire en ligne)
- ↑ Francesca Colavita, Mirella Biava, Concetta Castilletti et Serena Quartu, « Measles Cases during Ebola Outbreak, West Africa, 2013-2106 », Emerging Infectious Diseases, vol. 23, no 6, , p. 1035–1037 (ISSN 1080-6059, PMID 28518027, Central PMCID 5443435, DOI 10.3201/eid2306.161682, lire en ligne)
- ↑ Brigitta M. Laksono, Rory D. de Vries, Stephen McQuaid et W. Paul Duprex, « Measles Virus Host Invasion and Pathogenesis », Viruses, vol. 8, no 8, (ISSN 1999-4915, PMID 27483301, Central PMCID 4997572, DOI 10.3390/v8080210, lire en ligne)
- ↑ Jackie Bentley, Jo Rouse et Jenny Pinfield, « Measles: pathology, management and public health issues », Nursing Standard (Royal College of Nursing (Great Britain): 1987), vol. 28, no 38, , p. 51–58 (ISSN 2047-9018, PMID 24844521, DOI 10.7748/ns.28.38.51.e8765, lire en ligne)
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/28209781
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/28412379
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/30208191
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/27580345
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/24865261
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/27315036