Dissection aortique
La dissection aortique aiguë (DAA) est due à la séparation des couches de la paroi aortique. Une déchirure dans la couche intimale entraîne la progression de la dissection (proximale ou rétrograde) principalement en raison de l'entrée de sang entre l'intima et la média. C'est une maladie rare, mais catastrophique[1].
Épidémiologie
L'incidence de la dissection aortique serait de 5 à 30 cas pour 1 million de personnes par an[1]. En ce qui concerne les présentations aux urgences, trois DAA sont diagnostiquées sur 1000 patients présentant des douleurs aiguës au dos, à la poitrine ou à l'abdomen. L'âge est un facteur de risque pour environ 75% des dissections aortiques survenant chez des patients âgés de 40 à 70 ans, la majorité se produisant entre 50 et 65 ans. La DAA est trois fois plus fréquente chez les hommes que chez les femmes, bien que les femmes aient tendance à se présenter plus tard et à connaître de pires résultats.[1]
Étiologies

La DAA est souvent observée chez des patients présentant une altération préexistante de la média aortique. Les causes les plus courantes de la dissection aortique aiguë sont [2]:
- la dissection idiopathique
- le traumatisme thoracique
- l'iatrogénécité.
Physiopathologie

La paroi aortique se compose de trois couches : l'intima, la média et l'adventice. Une exposition constante à une pression artérielle élevée et à une contrainte de cisaillement entraîne un affaiblissement de la paroi aortique chez les patients sensibles, pouvant provoquer une déchirure intimale. Suite à cette déchirure, le sang coule dans l'espace entre l'intima et la média, créant une fausse lumière. La plupart de ces déchirures ont lieu dans l'aorte ascendante, généralement dans la paroi latérale droite où se produit la plus grande force de cisaillement sur l'aorte. Une DAA peut se propager de façon antérograde et/ou rétrograde et, selon la direction de la dissection, provoquer l'obstruction d'une de ses branches qui produira alors une ischémie du territoire affecté (coronaire, cérébral, rachidien ou viscéral). Les dissections proximales de type A peuvent provoquer une tamponnade aiguë, une insuffisance aortique ou une rupture aortique. [3][1]
Dans une dissection aortique aiguë, la vraie lumière est bordée par l'intima tandis que la fausse lumière est entre l'intima et la média. Dans la plupart des cas, la vraie lumière est plus petite que la fausse. Souvent, le sang circulant à travers la fausse lumière conduit au développement d'un anévrisme avec un potentiel de rupture.
Les trois sites communs pour une DAA sont les suivants[1] :
- 2 à 2,5 cm au-dessus de la racine aortique (le site le plus courant)
- juste en distal de l'origine de l'artère sous-clavière gauche
- dans l'arc aortique.
Présentation clinique
Facteurs de risque
Les facteurs de risques associés à la DAA sont principalement reliés à l'âge et les comorbidités associées[4]
- l'âge (> 65 ans) : patients plus susceptibles de présenter :
- de l'hypertension artérielle (comorbide dans 70% des cas de DAA distale de Standford de type B)
- une maladie athérosclérotique
- un anévrisme aortique
- une valve aortique bicuspide
- une coarctation de l'aorte
- une altération préexistante de la média aortique (dissection iatrogène, hématome intramural).
- plus jeunes ( < 65 ans): maladies associées selon[1][2]:
- des antécédents familiaux de dissection aortique
- les malformations congénitales telles que:
- les troubles du tissu conjonctif :
- le syndrome de Marfan (présent chez 50% des moins de 40 ans, contre seulement 2% des patients plus âgés)
- le syndrome d'Ehlers-Danlos
- les affectations génétiques:
- les maladies inflammatoires ou infectieuses (qui sont à l'origine de vascularites des gros vaisseaux (syphilis, consommation de cocaïne)) [1]
- les troubles du tissu conjonctif :
- les traumatismes thoraciques
- toute instrumentation ou chirurgie aortique (pontage aortocoronarien, remplacement de la valve aortique ou mitrale, pose d'un tuteur coronarien, toute cathétérisation coronarienne)
- une crise hypertensive (par exemple, une musculation intense ou l'utilisation d'agents sympathomimétiques tels que la cocaïne, l'ecstasy ou les boissons énergisantes)
- la grossesse et l'accouchement (aggravé si la femme est atteinte de troubles du tissu conjonctif).
Questionnaire

À son arrivée à l'hôpital, le patient doit être questionné sur trois aspects fondamentaux de sa douleur, c'est-à-dire la qualité, l'irradiation et l'intensité de sa douleur initiale. Classiquement, la dissection aortique aiguë se présente de façon suivante[5] :
- un douleur thoracique à début soudain[LR+: 2.6][LR-: 0.3][5]
- une douleur thoracique sévère
- des douleurs décrites comme déchirantes[LR+: 10.8][LR-: 0.4][5]
- une douleur thoracique antérieure[LR+: 7.6][LR-: 0.6][5], si la dissection est plus ascendante,
- une douleur thoracique transfixiante[LR+: 7.6][LR-: 0.6][note 1] si la dissection est descendante.
On suspecte fréquemment la dissection aortique en questionnant les complications en lien avec celle-ci. Selon les artères extra-aortiques disséquées, les symptômes varient[6]:
- des symptômes neurologiques en lien avec une dissection de la carotide interne ou d'une dissection de l'artère sous-clavière (atteinte de l'état de conscience, douleur à un membre, parésie, paresthésie, syndrome de Horner, enrouement de la voix)[6][1]
- des symptômes cardio-pulmonaires en lien avec une dissection coronarienne ou une tamponnade (dyspnée, douleur thoracique, syncope, sueur) [6]
- des symptômes gastro-intestinaux en lien avec une dissection du tronc coeliaque ou des artères mésentériques (douleur abdominale intense).
Diverses études ont identifié l'intensité d'apparition de la douleur comme le facteur historique le plus fiable.[1] Il peut y avoir un caractère migrateur, car la dissection peut se propager caudalement.[1] La présentation de la DAA représente l'ampleur de la dissection, avec des plaintes correspondant aux structures cardiovasculaires touchées. Chez environ 10% des patients, la DAA est indolore, ce qui est plus fréquemment rencontré chez les patients présentant un syndrome de Marfan.
Examen clinique
Certains signes physiques associés sont classiquement cités, mais présents dans moins de 50% des cas confirmés de DAA. Ce qui doit alerter le clinicien sur la possibilité d'une DAA est énuméré ici [1]:
- aux signes vitaux :
- l'hypertension artérielle[LR+: 1.5][LR-: 0.4][5]
- une tension artérielle différentielle augmentée de >20 mmHg entre les bras
- une hypotension artérielle[Sp: 0.95 %] [7](signe grave indiquant très probablement une rupture, un hémopéricarde ou un choc cardiogénique)
- une syncope (peut être due à une hypovolémie, une arythmie, un infarctus du myocarde ou une augmentation du tonus vagal)
- à l'examen cardiaque :
- une insuffisance aortique nouvelle ou exacerbée
- des bruits cardiaques diminués (suggérant une tamponnade cardiaque)
- une perte de pouls[Sp: 0.91 %][LR+: 2.7][LR-: 0.63] [5][7](asymétrie et si antérograde et implication des vaisseaux des membres, avec paresthésies et une douleur ischémique[1])
- une masse pulsatile palpable à l'abdomen
- à l'examen neurologique :
- des signes neurologiques focaux[Sp: 0.95 %][LR+: 33.0][LR-: 0.87][5](présents chez 20% des patients)
- une douleur thoracique accompagnée d'une faiblesse musculaire ou d'une paresthésie[1]
- une altération de l'état de conscience
- un syndrome de Horner[1]
- un enrouement de la voix.
- des signes neurologiques focaux[Sp: 0.95 %][LR+: 33.0][LR-: 0.87][5](présents chez 20% des patients)
Examens paracliniques
Laboratoire
Les examens de routine sont probablement d'une utilité limitée pour établir le diagnostic de la DAA. Cependant, ces examens peuvent mettre en évidence un dysfonctionnement aigu d'un organe (par exemple, une insuffisance rénale, une hépatite secondaire à une ischémie ou une acidose lactique associée à une hypoperfusion), ce qui peut être utile pour établir la gravité de la dissection du patient. Par ailleurs, ils peuvent être utiles au diagnostic différentiel, mais aussi à la planification chirurgicale. Les prises de sang suivantes peuvent être réalisées :
- la FSC
- les ions
- la créatininémie
- les troponines élevées [Pr: 18 %] (une dissection coronarienne peut compliquer une dissection aortique)
- un gaz veineux
- des lactates
- le typage avec groupé-croisé (en vue d'une chirurgie probable).
L'usage des D-Dimères dans la DA n'est pas encore établi, mais il s'agit d'une voie en cours de validation (algorithme ADD-RS). [8] Ceci pourrait permettre de réduire le nombre d'angio-TDM demandé pour cette condition. [note 2]
ECG
Un ECG est obligatoire pour exclure un infarctus du myocarde.[1] À noter qu'une dissection aortique peut se compliquer d'une dissection coronarienne, ce qui se présente par un infarctus du myocarde.
Imagerie
La confirmation de la DAA nécessite une imagerie cardiovasculaire pour identifier la présence d'une déchirure intimale, établir la classification de Stanford et détecter une atteinte valvulaire ou de branche. La plupart des lignes directrices recommandent soit l'aortographie par tomodensitométrie, soit l'échocardiographie transoesophagienne (ETO) pour le diagnostic de la DAA. Le choix de la modalité d'imagerie à utiliser comme examen de première ligne doit être basé sur la disponibilité locale. Pour la plupart des urgences, l'angio-TDM sera probablement la première technique d'imagerie avancée en raison de sa large disponibilité.[9][1]
| Modalité / imagerie | Commentaires |
|---|---|
| Angio-TDM aortique | Si le patient est stable, un Angio-TDM est recommandé. Il peut détecter rapidement l'emplacement de la déchirure intimale et aider le chirurgien à planifier la procédure. Les résultats suggérés par la DAA incluent: [1]
|
| Radiographie thoracique | La radiographie thoracique peut montrer un médiastin élargi (> 8 cm) ou une collection de liquide dans un hémithorax en raison d'une rupture. Les caractéristiques de radiographie suggérant la DAA comprennent: [1] |
| Échocardiographie | L'échocardiographie est également une modalité utile pour détecter la DAA. L'EDU est la technique préférée qui peut être pratiquée au chevet du patient et utilisée pour la visualisation peropératoire. [1]
|
Classification
Il existe deux principales classifications anatomiques utilisées pour classifier la dissection aortique: [1]
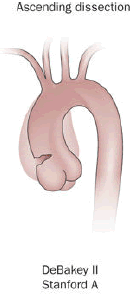
Le système de Stanford est plus fréquemment utilisé. Il classe les dissections aortiques en deux types selon que la partie ascendante ou descendante de l'aorte est impliquée. [1]
- Le type A concerne l'aorte ascendante, quel que soit le site de la déchirure intimale primaire. La dissection de type A est définie comme une dissection proximale à l'artère brachiocéphalique.
- Le type B concerne une dissection partant de l'artère sous-clavière gauche et n'impliquant que l'aorte descendante.[1]
La classification DeBakey est basée sur le site d'origine de la dissection.[1]
- Le type 1 provient de l'aorte ascendante et au moins de l'arc aortique.
- Le type 2 provient et est limité à l'aorte ascendante.
- Le type 3 commence dans l'aorte descendante et s'étend distalement au-dessus du diaphragme (type 3a) ou en dessous du diaphragme (type 3b) .[1]
Les dissections aortiques ascendantes sont presque deux fois plus fréquentes que les dissections descendantes.[10][1] 67% des DAA sont de type A selon la classification de Stanford contre 33% de type B.
| Classification selon le Système Stanford | Classification DeBakey | |||
|---|---|---|---|---|
| Type A | Type B | Type 1 | Type 2 | Type 3 |
 |
 |
 |
 | |
Approche clinique
Il existe un algorithme afin d'aider au diagnostic clinique de la DAA. Cet algorithme n'a toutefois pas été étudié sur le point de vue de la validité externe, mais il demeure très prometteur. Cet algorithme se nomme l'ADD-RS (Aortic Dissection Detection Risk Score) et est illustré ci-dessous. Il consiste à attribuer un point si le facteur est présent.
| Critères représentant un risque élevé | Caractéristiques | Pointage |
|---|---|---|
| Antécédents |
|
1 |
| Questionnaire | Douleurs à la poitrine, au dos ou abdominales :
|
1 |
| Examen physique |
|
1 |
Un score ≥ 2 : envisager de passer directement à l'angio-TDM aortique ou toute autre imagerie concluante[11].
Un score ≤ 1: Procéder au test de D-Dimères. Si les D-Dimères sont < 500 ng/ml, envisager d'arrêter le bilan de dissection. S'ils sont ≥ 500 ng/ml envisager l'angio-TDM aortique.
Diagnostic
La dissection aortique est un diagnostic suspecté cliniquement et confirmé par les imageries (angio-TDM et ETO).
Diagnostic différentiel
Le diagnostic différentiel de la dissection aortique comprennent les conditions suivantes [1]:
- un syndrome coronarien aigu
- la pneumonie
- le spasme oesophagien
- la pancréatite aiguë
- l'anévrisme de l'aorte
- la tamponnade cardiaque (d'une autre cause)
- la rupture de l'œsophage (syndrome de Boerhaave)
- le pneumothorax
- l'embolie pulmonaire
- l'accident vasculaire cérébral ou un accident ischémique transitoire.
Traitement
Traitement médical[12][13]
Une fois le diagnostic de DAA confirmé ou hautement suspecté, une consultation urgente en chirurgie thoracique ou vasculaire doit être obtenue.
Le traitement médical consiste avant tout à stabiliser l'hémodynamie du patient[14]. Les mesures générales suivantes sont généralement recommandées [1]:
- la pose d'une canule artérielle pour avoir un monitoring optimal de la TA
- au moins 2 cathéters intraveineux de gros calibre
- la pose de cathéters veineux centraux (idéalement)
- le patient est mis NPO
- un bilan increta/excreta
- la pose d'une sonde urinaire pour le monitoring du débit urinaire
- une analgésie adéquate (morphine ou fentanyl) pour diminuer l'activation du SN sympathique qui conduirait à la tachycardie et à l'hypertension.
Chez les patients hypertendus, le contrôle de la TA est une priorité. La stratégie à deux agents pharmacologiques consiste à combiner un bêtabloquant (doivent être utilisés avec prudence dans les situations de régurgitation aortique aiguë, car ils bloquent la tachycardie compensatrice[1]), suivi d'un BCC ou d'un vasodilatateur :
- un bêtabloquant IV pour contrôler la FC et la TA (courte durée et viser 60 bpm)
- l'esmolol IV 500-1000 μg/kg en bolus sur 1 minute, suivi de 50 μg/kg/min en perfusion, titrage de 25-50 μg/kg/min q 5-15 min, max 300 μg/kg/min[12]
- le labétalol IV 10-20 mg q 10-20 min (max 300 mg) puis perfusion de de 0.5-10 mg/min[12][note 3]
- le métroprolol 2,5-5 mg IV q 5 min x 3, puis infuser à 2-5mg/hr
- des bloqueurs des canaux calciques :
- le diltiazem IV 0,25 mg/kg sur 2 à 5 min puis 5 mg/h[12]
- la nicarpidine IV 5 mg/h puis augmentation de 2,5 mg/h q 5-10 min PRN (maximum 15 mg/h)[12]
- le véramipril
- des vasodilatateurs (viser < 140/90 mmHg ou 130/80 mmHg pour les diabétiques[15])
- de la nitroglycérine IV 5 µg/min IV à augmenter 5 µg de q 3-5 min (maximum de 200 µg/min).[12]
Chez les patients hypotendus, l'administration intraveineuse de cristalloïdes en premier lieu est raisonnable. Des vasopresseurs peuvent être ajoutés, si nécessaire, pour maintenir une perfusion minimale adéquate, mais peuvent provoquer une propagation de fausse lumière supplémentaire. [1]
Les agents inotropes doivent être évités, car ils sont susceptibles d'augmenter la force de cisaillement et le taux de contraction ventriculaire et par conséquent d'aggraver la tension sur la paroi aortique.[1]
Traitement chirurgical
Différentes procédures chirurgicales peuvent être envisagées [16][17][18][1]:
- une reconstruction aortique avec greffe synthétique
- une endoprothèse aortique
- un remplacement de valve aortique
- un tuteur endovasculaire.
Suivi
- Une fois que le patient est traité chirurgicalement ou médicalement, la pression artérielle doit être contrôlée
- Le patient doit être étroitement surveillé pour la progression de la dissection aortique
- Une tomodensitométrie thoracique régulière ou une IRM est recommandée tous les 3 à 6 mois pour vérifier la progression de la maladie [1]
Complications
Les délais de diagnostique ou encore l'omission de considérer une DAA contribuent à un taux de mortalité très élevé. Les dissections peuvent se compliquer de différentes conditions [1]:
- une tamponnade cardiaque
- une insuffisance aortique aiguë
- un choc cardiogénique
- une rupture aortique
- une ischémie des organes terminaux
- une dissection coronarienne, ce qui entraine un infarctus du myocarde
- une ischémie mésentérique aiguë
- une dissection de l'artère rénale, ce qui entraine un infarctus rénal
- une dissection carotidienne
- une dissection de l'artère subclavière
- une dissection de l'artère brachio-céphalique.
Évolution
La dissection aortique est associée une mortalité très élevée. Au moins 30% des patients décèdent après leur arrivée à l'urgence, et ce, même après une intervention chirurgicale. Pour ceux qui survivent à la chirurgie, la morbidité est également très élevée et la qualité de vie est mauvaise. La mortalité la plus élevée d'une dissection aortique aiguë est dans les 10 premiers jours. Les patients qui ont une dissection chronique ont tendance à avoir un meilleur pronostic, mais leur espérance de vie est raccourcie par rapport à la population générale.[1] Sans traitement, la mortalité est de 1 à 3% par heure au cours des 24 premières heures, et approche 50% dans les 48 premières heures suivant son apparition.[1]
La mortalité hospitalière chez le patient traité est d'environ 30% pour les dissections proximales et 10% pour les dissections distales. La survie des patients qui survivent à l'épisode aigu est d'environ 60 % à 5 ans et 40% à 10 ans. Environ 1/3 des décès tardifs sont dus à des complications de la dissection; le reste est dû à d'autres troubles.
Environ 20% des patients qui présentent une DAA décéderont avant leur arrivée à l'hôpital. Sans traitement médical, 30% décéderont à une semaine, 80 % à 2 semaines et 90% à 1 an.[1]
Prévention
Dans la population en général, tout comme chez les patients à haute risque (ayant des maladies du collagène, par exemple) la prévention consiste à:
- contrôler l'hypertension
- contrôler la dyslipidémie
- l'abandon tabagique
- éviter l'utilisation d'agents sympathomimétique (cocaïne, méthamphétamine).
Pour les patients à risque élevés seulement, s'ajouteraient les mesures suivantes:
- éviter l'entrainement musculaire
- avoir un suivi régulier avec un cardiologue.
Notes
- ↑ Qui traverse de part en part, qui irradie dans le dos. Douleur thoracique que irradie dans le dos.
- ↑ Dans le contexte où il est impossible d'obtenir une angio-TDM rapidement (notamment pour les patients qui habitent en région isolé), des D-dimères normaux en l'absence de caractéristiques à l'examen physique ou d'antécédent à haut risque pourrait être considéré comme acceptable, en autant que la décision soit partagée avec le patient.
- ↑ Le labetalol a à la fois des effets alpha et bêta.
Références
- Cette page a été modifiée ou créée le 2021/01/30 à partir de Aortic Dissection (StatPearls / Aortic Dissection (2020/12/17)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/28722992 (livre).
- ↑ 1,00 1,01 1,02 1,03 1,04 1,05 1,06 1,07 1,08 1,09 1,10 1,11 1,12 1,13 1,14 1,15 1,16 1,17 1,18 1,19 1,20 1,21 1,22 1,23 1,24 1,25 1,26 1,27 1,28 1,29 1,30 1,31 1,32 1,33 1,34 1,35 1,36 1,37 et 1,38 David Levy, Amandeep Goyal, Yulia Grigorova et Fabiola Farci, StatPearls, StatPearls Publishing, (PMID 28722992, lire en ligne)
- ↑ 2,0 et 2,1 « Dissection aortique - Troubles cardiovasculaires », sur Édition professionnelle du Manuel MSD (consulté le 5 février 2021)
- ↑ Tao Zeng, Lei Shi, Qingwei Ji et Ying Shi, « Cytokines in aortic dissection », Clinica Chimica Acta; International Journal of Clinical Chemistry, vol. 486, , p. 177–182 (ISSN 1873-3492, PMID 30086263, DOI 10.1016/j.cca.2018.08.005, lire en ligne)
- ↑ (en) Joanna Gawinecka, Felix Schönrath et Arnold von Eckardstein, « Acute aortic dissection: pathogenesis, risk factors and diagnosis », Swiss Medical Weekly, vol. 147, no 3334, (DOI 10.4414/smw.2017.14489, lire en ligne)
- ↑ 5,0 5,1 5,2 5,3 5,4 5,5 et 5,6 Michael Klompas, « Does this patient have an acute thoracic aortic dissection? », JAMA, vol. 287, no 17, , p. 2262–2272 (ISSN 0098-7484, PMID 11980527, DOI 10.1001/jama.287.17.2262, lire en ligne)
- ↑ 6,0 6,1 et 6,2 Loren F. Hiratzka, George L. Bakris, Joshua A. Beckman et Robert M. Bersin, « 2010 ACCF/AHA/AATS/ACR/ASA/SCA/SCAI/SIR/STS/SVM guidelines for the diagnosis and management of patients with Thoracic Aortic Disease: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines, American Association for Thoracic Surgery, American College of Radiology, American Stroke Association, Society of Cardiovascular Anesthesiologists, Society for Cardiovascular Angiography and Interventions, Society of Interventional Radiology, Society of Thoracic Surgeons, and Society for Vascular Medicine », Circulation, vol. 121, no 13, , e266–369 (ISSN 1524-4539, PMID 20233780, DOI 10.1161/CIR.0b013e3181d4739e, lire en ligne)
- ↑ 7,0 et 7,1 Robert Ohle, Hashim Khaliq Kareemi, George Wells et Jeffrey J. Perry, « Clinical Examination for Acute Aortic Dissection: A Systematic Review and Meta-analysis », Academic Emergency Medicine: Official Journal of the Society for Academic Emergency Medicine, vol. 25, no 4, , p. 397–412 (ISSN 1553-2712, PMID 29265487, DOI 10.1111/acem.13360, lire en ligne)
- ↑ 8,0 et 8,1 Peiman Nazerian, Christian Mueller, Alexandre de Matos Soeiro et Bernd A. Leidel, « Diagnostic Accuracy of the Aortic Dissection Detection Risk Score Plus D-Dimer for Acute Aortic Syndromes: The ADvISED Prospective Multicenter Study », Circulation, vol. 137, no 3, , p. 250–258 (ISSN 1524-4539, PMID 29030346, DOI 10.1161/CIRCULATIONAHA.117.029457, lire en ligne)
- ↑ R. Erbel, « [Aortic diseases : Modern diagnostic and therapeutic strategies] », Herz, vol. 43, no 3, , p. 275–290 (ISSN 1615-6692, PMID 29569149, DOI 10.1007/s00059-018-4694-2, lire en ligne)
- ↑ Paolo Berretta, Mariano Cefarelli, Andrea Montalto et Carlo Savini, « [Surgical indications for thoracic aortic disease: beyond the "magic numbers" of aortic diameter] », Giornale Italiano Di Cardiologia (2006), vol. 19, no 7, , p. 429–436 (ISSN 1827-6806, PMID 29989600, DOI 10.1714/2938.29539, lire en ligne)
- ↑ 11,0 et 11,1 « MD+calc »
- ↑ 12,0 12,1 12,2 12,3 12,4 et 12,5 Prateek K. Gupta, Himani Gupta et Ali Khoynezhad, « Hypertensive Emergency in Aortic Dissection and Thoracic Aortic Aneurysm-A Review of Management », Pharmaceuticals (Basel, Switzerland), vol. 2, no 3, , p. 66–76 (ISSN 1424-8247, PMID 27713224, Central PMCID 3978532, DOI 10.3390/ph2030066, lire en ligne)
- ↑ Thomas T. Tsai, Christoph A. Nienaber et Kim A. Eagle, « Acute aortic syndromes », Circulation, vol. 112, no 24, , p. 3802–3813 (ISSN 1524-4539, PMID 16344407, DOI 10.1161/CIRCULATIONAHA.105.534198, lire en ligne)
- ↑ (en) « EM:RAP CorePendium: Aortic dissection », sur EM:RAP CorePendium (consulté le 29 mars 2021)
- ↑ Munir Boodhwani, Gregor Andelfinger, Jonathon Leipsic et Thomas Lindsay, « Canadian Cardiovascular Society position statement on the management of thoracic aortic disease », The Canadian Journal of Cardiology, vol. 30, no 6, , p. 577–589 (ISSN 1916-7075, PMID 24882528, DOI 10.1016/j.cjca.2014.02.018, lire en ligne)
- ↑ Christopher Lau, Jeremy R. Leonard, Erin Iannacone et Mario Gaudino, « Surgery for Acute Presentation of Thoracoabdominal Aortic Disease », Seminars in Thoracic and Cardiovascular Surgery, vol. 31, no 1, , p. 11–16 (ISSN 1532-9488, PMID 30071280, DOI 10.1053/j.semtcvs.2018.07.018, lire en ligne)
- ↑ Sabreen Mkalaluh, Marcin Szczechowicz, Bashar Dib et Alexander Weymann, « Open surgical thoracoabdominal aortic aneurysm repair: The Heidelberg experience », The Journal of Thoracic and Cardiovascular Surgery, vol. 156, no 6, , p. 2067–2073 (ISSN 1097-685X, PMID 30041925, DOI 10.1016/j.jtcvs.2018.05.081, lire en ligne)
- ↑ Karl Sörelius et Anders Wanhainen, « Challenging Current Conservative Management of Uncomplicated Acute Type B Aortic Dissections », EJVES short reports, vol. 39, , p. 37–39 (ISSN 2405-6553, PMID 29988823, Central PMCID 6031758, DOI 10.1016/j.ejvssr.2018.05.010, lire en ligne)

