Coagulation
| Concept | |
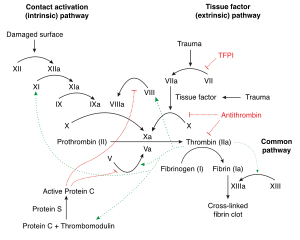 Cascade de la coagulation | |
| Informations | |
|---|---|
| Autres noms | Cascade de la coagulation, voies de la coagulation |
| Wikidata ID | Q179217 |
| Spécialité | Hématologie |
|
| |
La coagulation est une cascade d'événements qui conduit à l'hémostase. Elle permet une guérison rapide et la prévention des saignements spontanés.
Deux voies, intrinsèque et extrinsèque, débutent séparément mais convergent en un point spécifique, conduisant à l'activation de la fibrine. Le but est de stabiliser à terme le bouchon plaquettaire avec un maillage de fibrine. [1][2][3][4]
Fonction
La fonction de la voie de la coagulation est de maintenir l'hémostase, qui est le blocage d'un saignement ou d'une hémorragie:[4]
- L'hémostase primaire est une agrégation de plaquettes formant un bouchon sur le site endommagé des cellules endothéliales exposées.
- L'hémostase secondaire comprend les deux voies de coagulation principales, intrinsèque et extrinsèque, qui se rejoignent en un point pour former la voie commune. La voie commune active finalement le fibrinogène en fibrine.
- Ces sous-unités de fibrine ont une affinité les unes pour les autres et se combinent en brins de fibrine qui lient les plaquettes entre elles, stabilisant le bouchon plaquettaire.
Mécanisme
Le mécanisme par lequel la coagulation permet l'hémostase est un processus complexe qui se fait par une série de facteurs de coagulation. La voie intrinsèque comprend les facteurs I, II, IX, X, XI et XII. Respectivement, chacun est nommé, fibrinogène, prothrombine, facteur de Noël, facteur Stuart-Prower, la thromboplastine plasmatique et le facteur Hageman. La voie extrinsèque comprend les facteurs I, II, VII et X. Le facteur VII est appelé facteur stable. La voie commune comprend les facteurs I, II, V, VIII, X. Les facteurs circulent dans la circulation sanguine sous forme de zymogènes et sont activés en sérine protéases. Ces sérine protéases agissent comme un catalyseur pour cliver le prochain zymogène en plus de sérine protéases et finalement activer le fibrinogène. Les sérine protéases sont les suivantes: facteurs II, VII, IX, X, XI et XII. Ce ne sont pas des sérine protéases: les facteurs V, VIII, XIII. La voie intrinsèque est activée par le collagène endothélial exposé, et la voie extrinsèque est activée par le facteur tissulaire libéré par les cellules endothéliales après des dommages externes.[4]
Voie intrinsèque[4]
Cette voie est la voie la plus longue de l'hémostase secondaire. Il commence par l'activation du facteur XII (un zymogène, sérine protéase inactivée) qui devient le facteur XIIA (sérine protéase activée) après exposition au collagène endothélial. Le collagène endothélial n'est exposé qu'en cas de lésion endothéliale. Le facteur XIIA agit comme un catalyseur pour activer le facteur XI en facteur XIA. Le facteur XIA active ensuite le facteur IX en facteur IXA. Le facteur IXA sert ensuite de catalyseur pour transformer le facteur X en facteur Xa. C'est ce qu'on appelle une cascade. Lorsque chaque facteur est activé, il active de nombreux autres facteurs dans les étapes suivantes. Au fur et à mesure que vous descendez la cascade, la concentration de ce facteur augmente dans le sang. Par exemple, la concentration du facteur IX est supérieure à celle du facteur XI. Lorsque le facteur II est activé par la voie intrinsèque ou extrinsèque, il peut renforcer la voie intrinsèque en donnant une rétroaction positive aux facteurs V, VII, VIII, XI, XIII. Cela rend le facteur XII moins critique; les patients peuvent effectivement bien coaguler sans facteur XII. La voie intrinsèque est mesurée cliniquement comme le temps de céphaline partielle (PTT) .[4]
Extrinsic Pathway[4]
La voie extrinsèque est la voie la plus courte de l'hémostase secondaire. Une fois que le dommage au vaisseau est fait, les cellules endothéliales libèrent un facteur tissulaire qui active ensuite le facteur VII en facteur VIIa. Le facteur VIIa active ensuite le facteur X en facteur Xa. C'est à ce moment que les voies extrinsèques et intrinsèques ne font plus qu'un. La voie extrinsèque est mesurée cliniquement comme le temps de prothrombine (PT) .[4]
Common Pathway[4]
Cette voie commence au facteur X qui est activé en facteur Xa. Le processus d'activation du facteur Xa est une réaction compliquée. La ténase est le complexe qui clive le facteur X en facteur Xa. La ténase a deux formes: extrinsèque, constituée du facteur VII, du facteur III (facteur tissulaire) et du Ca2 +, ou intrinsèque, constituée du cofacteur facteur VIII, du facteur IXA, d'un phospholipide et du Ca2 +. Une fois activé en facteur Xa, il active ensuite le facteur II (prothrombine) en facteur IIa (thrombine). En outre, le facteur Xa nécessite le facteur V comme cofacteur pour cliver la prothrombine en thrombine. Le facteur IIa (thrombine) active ensuite le fibrinogène en fibrine. La thrombine active également d'autres facteurs de la voie intrinsèque (facteur XI) ainsi que les cofacteurs V et VIII et le facteur XIII. Les sous-unités de fibrine se réunissent pour former des brins de fibrine et le facteur XIII agit sur les brins de fibrine pour former un maillage de fibrine. Ce treillis aide à stabiliser le bouchon plaquettaire.[4]
Commentaires négatifs [4]
Pour éviter la sur-coagulation, qui provoque une thrombose généralisée, il existe certains processus pour contrôler la cascade de la coagulation. Comme la thrombine agit comme un procoagulant, elle agit également comme une rétroaction négative en activant le plasminogène en plasmine et en stimulant la production d'antithrombine (AT). La plasmine agit directement sur le maillage de fibrine et le décompose. L'AT diminue la production de thrombine à partir de la prothrombine et diminue la quantité de facteur X activé.[4]
Les protéines C et S agissent également pour empêcher la coagulation, principalement en inactivant les facteurs V et VIII.[4]
Organes impliqués[4]
L'un des organes intimement impliqués dans le processus de coagulation est le foie. Le foie est responsable de la formation des facteurs I, II, V, VII, VIII, IX, X, XI, XIII et de la protéine C et S. Le facteur VII est créé par l'endothélium vasculaire.[4]
La pathologie du foie peut entraîner un manque de facteurs de coagulation et entraîner une hémorragie. Une diminution des facteurs de coagulation signifie généralement de graves lésions hépatiques. Le facteur VII a la demi-vie la plus courte, conduisant à une PT élevée d'abord dans les maladies du foie. L'INR peut être supérieur à 6,5 (la normale est proche de 1,0). La coagulopathie dans les maladies du foie est traitée avec du plasma frais congelé.[4]
Physiopathologie
L'hémophilie A et B sont héritées selon un schéma récessif lié à l'X. Dans l'hémophilie A, il existe une carence en facteur VIII. Dans l'hémophilie B, il y a une déficience en facteur IX.[2][5][6][7][8][4]
L'hémophilie C est une mutation autosomique récessive, où il y a une carence en facteur XI.[4]
Le facteur V Leiden est une mutation génétique plus répandue chez les personnes d'origine européenne. Ce défaut provoque un état d'hypercoagulabilité. La mutation génétique provoque un défaut du facteur V tel que la protéine C ne peut pas l'inactiver, permettant au facteur V d'activer en continu les facteurs en aval.
Des carences en protéines C et S peuvent également conduire à des états hypercoagulables en raison d'une incapacité à inhiber de manière appropriée les facteurs V et VIII respectivement.
Signification clinique
PT et PTT évaluent le temps nécessaire pour que les voies extrinsèques et intrinsèques prennent effet, respectivement.[4]
Des études de mélange sont effectuées pour déterminer si un PT ou un PTT est élevé en raison d'un déficit en facteur ou d'un inhibiteur de facteur (anticorps dirigés contre des facteurs spécifiques). Cela se fait en mélangeant le plasma du patient avec un plasma témoin. Si le plasma mixte PT et PTT se normalisent, l'allongement du PT et du PTT est dû à un déficit en facteur. S'ils ne se normalisent pas, l'allongement est dû à un facteur inhibiteur. Un exemple d'inhibiteur est l'anticoagulant du lupus.[4]
Une carence en vitamine K peut entraîner une augmentation du PT et du PTT. Il peut se présenter sous forme d'hémarthrose, de saignement intramusculaire ou de saignement gastro-intestinal. Une carence en vitamine K est fréquemment observée chez les nouveau-nés en raison du manque de colonisation intestinale par des bactéries. Elle peut également être observée dans la malabsorption (fibrose kystique, maladie cœliaque, maladie de Crohn) .[4]
L'héparine est un anticoagulant utilisé en milieu hospitalier pour la prophylaxie de la thrombose veineuse profonde. L'héparine se lie et active l'AT. AT continue à inactiver la thrombine et le facteur Xa.[4]
La warfarine est utilisée pour un traitement à long terme chez les patients atteints de fibrillation auriculaire pour empêcher la formation d'un thrombus dans l'oreillette gauche. Il agit en inhibant l'époxyde réductase. L'époxyde réductase est un composant essentiel de la production de facteurs de coagulation car elle aide à recycler la vitamine K. Sans vitamine K, plus de facteurs de coagulation ne peuvent pas être produits par le foie.[4]
Références
- ↑ Shruti Chaturvedi, Robert A. Brodsky et Keith R. McCrae, « Complement in the Pathophysiology of the Antiphospholipid Syndrome », Frontiers in Immunology, vol. 10, , p. 449 (ISSN 1664-3224, PMID 30923524, Central PMCID 6426753, DOI 10.3389/fimmu.2019.00449, lire en ligne)
- ↑ 2,0 et 2,1 Thomas Franchi, Simon Eaton, Paolo De Coppi et Stefano Giuliani, « The emerging role of immunothrombosis in paediatric conditions », Pediatric Research, vol. 86, no 1, , p. 19–27 (ISSN 1530-0447, PMID 30808021, DOI 10.1038/s41390-019-0343-6, lire en ligne)
- ↑ Aida Habib, Giovanna Petrucci et Bianca Rocca, « Pathophysiology of Thrombosis in Peripheral Artery Disease », Current Vascular Pharmacology, vol. 18, no 3, , p. 204–214 (ISSN 1875-6212, PMID 30727897, DOI 10.2174/1570161117666190206234046, lire en ligne)
- ↑ 4,00 4,01 4,02 4,03 4,04 4,05 4,06 4,07 4,08 4,09 4,10 4,11 4,12 4,13 4,14 4,15 4,16 4,17 4,18 4,19 4,20 et 4,21 (en) Chaudhry R et Usama Sm, « Physiology, Coagulation Pathways », sur PubMed, 2020 jan (PMID 29489185, consulté le 1er août 2020)
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/30523120
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/30451721
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/29999440
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/29126301
- Cette page a été modifiée ou créée le 2020/07/31 à partir de Physiology, Coagulation Pathways (StatPearls / Physiology, Coagulation Pathways (2020/04/08)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/29489185 (livre).
