« Épanchement pleural » : différence entre les versions
Aucun résumé des modifications |
(Remodelage de la structure + physiopatho) |
||
| Ligne 12 : | Ligne 12 : | ||
|démo=0|révision_par_les_pairs=|révision_par_le_comité_éditorial=|littérature_à_jour_date=|révision_par_les_pairs_date=|révision_par_le_comité_éditorial_date=}}{{Page d'objectif du CMC|nom=Épanchement pleural|identificateur=76}} | |démo=0|révision_par_les_pairs=|révision_par_le_comité_éditorial=|littérature_à_jour_date=|révision_par_les_pairs_date=|révision_par_le_comité_éditorial_date=}}{{Page d'objectif du CMC|nom=Épanchement pleural|identificateur=76}} | ||
L''''épanchement pleural''' est l'accumulation de liquide dans la cavité pleurale. Il peut survenir seul ou être le résultat d'une maladie | L''''épanchement pleural''' est l'accumulation de liquide dans la cavité pleurale, c'est-à-dire entre les plèvres viscérales et pariétales. Il peut survenir seul ou être le résultat d'une maladie localisée ou systémique comme une infection, une malignité ou des conditions inflammatoires<ref name=":0">{{Citation d'un ouvrage|prénom1=Rachana|nom1=Krishna|prénom2=Mohan|nom2=Rudrappa|titre=StatPearls|éditeur=StatPearls Publishing|date=2020|pmid=28846252|lire en ligne=http://www.ncbi.nlm.nih.gov/books/NBK448189/|consulté le=2021-01-04}}</ref>. | ||
== Épidémiologie == | == Épidémiologie == | ||
{{Section ontologique | classe = Classe de maladie | nom = Épidémiologie}} | {{Section ontologique | classe = Classe de maladie | nom = Épidémiologie}} | ||
L'épanchement pleural est la maladie la plus courante parmi toutes les | L'épanchement pleural est la maladie la plus courante parmi toutes les pathologies pleurales, elle affecte 1,5 million de patients par an aux États-Unis. Une grande variété d'affections peuvent se présenter avec des épanchements pleuraux comme des maladies impliquant principalement le poumon ou la plèvre, des désordres systémiques et même des maladies qui affectent principalement d'autres organes. <ref name=":6">https://www.ncbi.nlm.nih.gov/pubmed/29377972</ref><ref name=":0" /> | ||
== | == Physiopathologie == | ||
{{Section ontologique | classe = Classe de maladie | nom = Étiologies}} | {{Section ontologique | classe = Classe de maladie | nom = Étiologies}}Tous les humains en bonne santé ont une petite quantité de liquide pleural qui lubrifie l'espace et facilite les mouvements pulmonaires normaux pendant la respiration. La quantité de liquide pleural normale est d'environ 0,1 ml / kg à 0,3 ml/kg et est constamment échangée. Cet équilibre délicat de fluide est maintenu par la pression oncotique, la pression hydrostatique et le drainage lymphatique.<ref name=":0" /> | ||
Le liquide pleural provient des vaisseaux des membranes pleurales et est absorbé par les lymphatiques dans les surfaces diaphragmatiques et médiastinales dépendantes de la plèvre pariétale. On pense que la pression hydrostatique des vaisseaux systémiques qui alimentent la plèvre pariétale entraîne le liquide interstitiel dans l'espace pleural, il y possède donc une teneur en protéines inférieure à celle du sérum. L'accumulation d'un excès de liquide peut se produire s'il y a une production excessive, une diminution de l'absorption ou si les deux phénomènes submergent le mécanisme homéostatique normal. <ref name=":7" /><ref name=":8" /><ref name=":0" /> | |||
Le liquide pleural est | |||
== Étiologies == | |||
Les causes courantes d'exsudats comprennent les infections pulmonaires comme la pneumonie ou la tuberculose, les tumeurs malignes, les troubles inflammatoires comme la pancréatite, le lupus, la polyarthrite rhumatoïde, le syndrome de traumatisme post-cardiaque, le chylothorax (dû à une obstruction lymphatique), l'hémothorax (sang dans la cavité pleurale) et l'épanchement pleural d'amiante bénin .<ref name=":0" /> | {{Section ontologique | classe = Classe de maladie | nom = Maladies}} | ||
* {{Membre | nom = Maladie 1}} | |||
Certaines des causes moins fréquentes d'épanchement pleural sont une embolie pulmonaire qui peut être un exsudat ou un transsudat, d'origine médicamenteuse (p. Ex., Méthotrexate, amiodarone, phénytoïne, dasatinib, généralement exsudat), post-radiothérapie (exsudat), rupture œsophagienne (exsudat) et le syndrome d'hyperstimulation ovarienne (exsudat) .<ref name=":0" /> | * {{Membre | nom = Maladie 2}} | ||
* ... | |||
Les épanchements pleuraux sont qualifiés de [[Transsudat|transsudatifs]] ou [[Exsudat|exsudatifs]]. En temps normal, l'espace pleural contient peut contenir jusqu'à 25ml de [[liquide pleural]]. Les [[critères de Light]] permettent de déterminer la nature d'un épanchement. | ** {{Étiologie | nom = Étiologie 1}} | ||
** {{Étiologie | nom = Étiologie 2}} | |||
** {{Étiologie | nom = Étiologie 3}} | |||
** ... Le liquide pleural est classé comme transsudat ou exsudat sur la base des critères de Light modifiés (voir ci-dessous). Le liquide pleural est considéré comme un épanchement exsudatif si au moins un des critères est rempli. <ref name=":4">https://www.ncbi.nlm.nih.gov/pubmed/30190139</ref><ref name=":5">https://www.ncbi.nlm.nih.gov/pubmed/30005142</ref><ref name=":0" /> | |||
** Rapport protéines du liquide pleural / protéines sériques supérieur à 0,5 | |||
** Ratio lactate déshydrogénase (LDH) du liquide pleural / LDH sérique supérieur à 0,6 | |||
** La LDH du liquide pleural représente plus des deux tiers des limites supérieures de la valeur de laboratoire normale pour la LDH sérique. <ref name=":0" /> Les causes courantes de transsudats comprennent des conditions qui modifient les pressions hydrostatiques ou oncotiques dans l'espace pleural comme l'insuffisance cardiaque congestive gauche, le syndrome néphrotique, la cirrhose du foie, l'hypoalbuminémie conduisant à la malnutrition et avec l'initiation de la dialyse péritonéale.<ref name=":0" /> Les causes courantes d'exsudats comprennent les infections pulmonaires comme la pneumonie ou la tuberculose, les tumeurs malignes, les troubles inflammatoires comme la pancréatite, le lupus, la polyarthrite rhumatoïde, le syndrome de traumatisme post-cardiaque, le chylothorax (dû à une obstruction lymphatique), l'hémothorax (sang dans la cavité pleurale) et l'épanchement pleural d'amiante bénin .<ref name=":0" /> Certaines des causes moins fréquentes d'épanchement pleural sont une embolie pulmonaire qui peut être un exsudat ou un transsudat, d'origine médicamenteuse (p. Ex., Méthotrexate, amiodarone, phénytoïne, dasatinib, généralement exsudat), post-radiothérapie (exsudat), rupture œsophagienne (exsudat) et le syndrome d'hyperstimulation ovarienne (exsudat) .<ref name=":0" /> Les épanchements pleuraux sont qualifiés de [[Transsudat|transsudatifs]] ou [[Exsudat|exsudatifs]]. En temps normal, l'espace pleural contient peut contenir jusqu'à 25ml de [[liquide pleural]]. Les [[critères de Light]] permettent de déterminer la nature d'un épanchement. | |||
===Étiologies transsudatives=== | ===Étiologies transsudatives=== | ||
| Ligne 96 : | Ligne 95 : | ||
*{{Étiologie|nom=Hypothyroïdisme}} | *{{Étiologie|nom=Hypothyroïdisme}} | ||
|} | |} | ||
* | |||
* | |||
== Physiopathologie == | == Physiopathologie == | ||
Version du 16 janvier 2021 à 17:00
| Classe de maladie | |
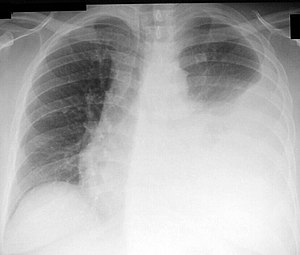 Épanchement pleural au poumon gauche | |
| Caractéristiques | |
|---|---|
| Signes | |
| Symptômes |
|
| Étiologies |
Embolie pulmonaire, Insuffisance cardiaque, Hypothyroïdie, Syndrome néphrotique, Dialyse péritonéale, Cirrhose hépatique |
| Informations | |
| Terme anglais | Pleural effusion |
| Spécialité | Pneumologie |
|
| |
Épanchement pleural (76)
L'épanchement pleural est l'accumulation de liquide dans la cavité pleurale, c'est-à-dire entre les plèvres viscérales et pariétales. Il peut survenir seul ou être le résultat d'une maladie localisée ou systémique comme une infection, une malignité ou des conditions inflammatoires[1].
Épidémiologie
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section contient les données épidémiologiques sur la maladie (ex. incidence, prévalence, coûts en hospitalisation, proportion d'hommes-femmes, régions où la prévalence est plus élevée, etc.). Chaque donnée épidémiologique doit être appuyée par une référence. Idéalement, des statistiques canadiennes et québécoises sont mentionnées lorsque disponibles. |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: | Les facteurs de risque ne sont pas présentés ici, mais bien dans la sous-section Facteurs de risque (Présentation clinique). Le pronostic et l'évolution naturelle de la maladie sont décrits dans la section Évolution. |
| Exemple: | La FRP est une maladie relativement rare qui affecte le plus souvent les patients âgés de 40 à 60 ans. Une prédominance masculine est observée avec un ratio H : F estimé à environ 2:1 ou 3:1. L'incidence de la FRP est inconnue, mais est estimée à 1 pour 200 000 à 500 000 par an. |
L'épanchement pleural est la maladie la plus courante parmi toutes les pathologies pleurales, elle affecte 1,5 million de patients par an aux États-Unis. Une grande variété d'affections peuvent se présenter avec des épanchements pleuraux comme des maladies impliquant principalement le poumon ou la plèvre, des désordres systémiques et même des maladies qui affectent principalement d'autres organes. [2][1]
Physiopathologie
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section décrit les étiologies de la maladie, c'est-à-dire ce qui cause la maladie (ex. le diabète de type 2 cause la néphropathie diabétique). Les étiologies doivent être identifiées avec le modèle Étiologie. |
| Formats: | Texte, Liste à puces, Tableau |
| Balises sémantiques: | Étiologie |
| Commentaires: |
|
| Exemple: | Parmi les étiologies les plus courantes d'occlusion de l'intestin grêle, on retrouve :
|
Tous les humains en bonne santé ont une petite quantité de liquide pleural qui lubrifie l'espace et facilite les mouvements pulmonaires normaux pendant la respiration. La quantité de liquide pleural normale est d'environ 0,1 ml / kg à 0,3 ml/kg et est constamment échangée. Cet équilibre délicat de fluide est maintenu par la pression oncotique, la pression hydrostatique et le drainage lymphatique.[1]
Le liquide pleural provient des vaisseaux des membranes pleurales et est absorbé par les lymphatiques dans les surfaces diaphragmatiques et médiastinales dépendantes de la plèvre pariétale. On pense que la pression hydrostatique des vaisseaux systémiques qui alimentent la plèvre pariétale entraîne le liquide interstitiel dans l'espace pleural, il y possède donc une teneur en protéines inférieure à celle du sérum. L'accumulation d'un excès de liquide peut se produire s'il y a une production excessive, une diminution de l'absorption ou si les deux phénomènes submergent le mécanisme homéostatique normal. [3][4][1]
Étiologies
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: | |
| Exemple: | |
- Maladie 1
- Maladie 2
- ...
- Étiologie 1
- Étiologie 2
- Étiologie 3
- ... Le liquide pleural est classé comme transsudat ou exsudat sur la base des critères de Light modifiés (voir ci-dessous). Le liquide pleural est considéré comme un épanchement exsudatif si au moins un des critères est rempli. [5][6][1]
- Rapport protéines du liquide pleural / protéines sériques supérieur à 0,5
- Ratio lactate déshydrogénase (LDH) du liquide pleural / LDH sérique supérieur à 0,6
- La LDH du liquide pleural représente plus des deux tiers des limites supérieures de la valeur de laboratoire normale pour la LDH sérique. [1] Les causes courantes de transsudats comprennent des conditions qui modifient les pressions hydrostatiques ou oncotiques dans l'espace pleural comme l'insuffisance cardiaque congestive gauche, le syndrome néphrotique, la cirrhose du foie, l'hypoalbuminémie conduisant à la malnutrition et avec l'initiation de la dialyse péritonéale.[1] Les causes courantes d'exsudats comprennent les infections pulmonaires comme la pneumonie ou la tuberculose, les tumeurs malignes, les troubles inflammatoires comme la pancréatite, le lupus, la polyarthrite rhumatoïde, le syndrome de traumatisme post-cardiaque, le chylothorax (dû à une obstruction lymphatique), l'hémothorax (sang dans la cavité pleurale) et l'épanchement pleural d'amiante bénin .[1] Certaines des causes moins fréquentes d'épanchement pleural sont une embolie pulmonaire qui peut être un exsudat ou un transsudat, d'origine médicamenteuse (p. Ex., Méthotrexate, amiodarone, phénytoïne, dasatinib, généralement exsudat), post-radiothérapie (exsudat), rupture œsophagienne (exsudat) et le syndrome d'hyperstimulation ovarienne (exsudat) .[1] Les épanchements pleuraux sont qualifiés de transsudatifs ou exsudatifs. En temps normal, l'espace pleural contient peut contenir jusqu'à 25ml de liquide pleural. Les critères de Light permettent de déterminer la nature d'un épanchement.
Étiologies transsudatives
L'épanchement pleural transsudatif est causé par une altération des facteurs systémiques affectant al formation et la résorption du liquide pleural, comme l'augmentation de la pression hydrostatique dans les capillaires pulmonaires ou la diminution de la pression oncotique.[7]
- insuffisance cardiaque
- cirrhose
- syndrome néphrotique (par perte de protéines)
- embolie pulmonaire (peut aussi causer un épanchement exsudatif)
- dialyse péritonéale, hypothyroïdisme
Étiologies exsudatives
L'épanchement pleural exsudatif est causé par un déséquilibre entre la formation et la résorption du liquide pleural.[7] Ses étiologies possibles sont nombreuses.
| Étiologie | Exemples |
|---|---|
| Infectieuse |
|
| Maligne |
|
| Inflammatoire | |
| Intra-abdominale | |
| Intra-thoracique | |
| Traumatique | |
| Autre |
Physiopathologie
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | La physiopathologie traite des mécanismes biologiques qui conduisent à l'apparition d'une maladie. |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: | L'histopathologie doit figurer dans la section Examen paraclinique, et non dans la section Physiopathologie. |
| Exemple: | Le VIP est une neurohormone composée de 28 acides aminés et appartenant à la famille des sécrétines-glucagon. Il est produit dans le système nerveux central ainsi que dans les neurones des voies gastro-intestinales, respiratoires et urogénitales. Il agit, via l'expression d'adénylate cyclase cellulaire (AMPc), à titre de vasodilatateur et de régulateur de l'activité des muscles lisses, de stimulateur de la sécrétion d'eau et d'électrolytes par le tractus intestinal, d'inhibiteur de la sécrétion d'acide gastrique et de promoteur du flux sanguin principalement dans le tractus gastro-intestinal. L'ensemble de ces éléments peuvent entraîner une hypokaliémie, une hyperglycémie, une hypomagnésémie et une hypercalcémie qui sont habituellement responsables de la présentation clinique. |
Tous les humains en bonne santé ont une petite quantité de liquide pleural qui lubrifie l'espace et facilite les mouvements pulmonaires normaux pendant la respiration. Cet équilibre délicat de fluide est maintenu par la pression oncotique et hydrostatique et le drainage lymphatique; des perturbations dans l'un de ces systèmes peuvent conduire à une accumulation de liquide pleural.[1]
Chez l'adulte sain normal, la cavité pleurale a un liquide minimal qui agit comme un lubrifiant pour les deux surfaces pleurales. La quantité de liquide pleural est d'environ 0,1 ml / kg à 0,3 ml / kg et est constamment échangée. Le liquide pleural provient du système vasculaire des surfaces de la plèvre pariétale et est absorbé par les lymphatiques dans les surfaces diaphragmatiques et médiastinales dépendantes de la plèvre pariétale. On pense que la pression hydrostatique des vaisseaux systémiques qui alimentent la plèvre pariétale entraîne le liquide interstitiel dans l'espace pleural et a donc une teneur en protéines inférieure à celle du sérum. L'accumulation d'un excès de liquide peut se produire s'il y a une production excessive ou une diminution de l'absorption ou si les deux submergent le mécanisme homéostatique normal. Si l'épanchement pleural est principalement dû à des mécanismes qui conduisent à un épanchement pleural principalement dû à une augmentation de la pression hydrostatique sont généralement transsudatifs, et conduisant à un épanchement pleural ont modifié l'équilibre entre les pressions hydrostatique et oncotique (généralement transsudats), augmentation de la perméabilité mésothéliale et capillaire (généralement exsudats ) ou un drainage lymphatique altéré. [3][4][1]
Présentation clinique
Toute contribution serait appréciée.
| Description: | Cette section contient la sous-section optionnelle Facteurs de risque et les sous-sections obligatoires Questionnaire et Examen clinique. |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: |
|
| Exemple: |
|
Un patient avec un épanchement pleural peut être asymptomatique ou peut présenter un essoufflement à l'effort en fonction de la déficience de l'excursion thoracique. Le patient présentant une inflammation pleurale active appelée pleurésie se plaint d'une douleur aiguë, sévère et localisée crescendo / decrescendo accompagnée d'une respiration ou d'une toux. Lorsque l'épanchement se développe, la douleur peut s'atténuer, ce qui implique à tort une amélioration de l'état. La douleur constante est également une caractéristique des maladies malignes comme le mésothéliome. En fonction de la cause de l'épanchement, le patient peut également se plaindre d'une toux, de la fièvre et des symptômes systémiques.[1]
L'examen physique peut être subtil. En grand épanchement, il y aura la plénitude des espaces intercostaux, et la matité à la percussion de ce côté. L'auscultation révèle une diminution des bruits respiratoires et une diminution du frémitus tactile et vocal. L'égophonie est la plus prononcée à l'aspect supérieur de l'épanchement.[1]
Un frottement pleural, souvent confondu avec des crépitements grossiers, peut être entendu lors d'une pleurésie active sans aucun épanchement.[1]
L'épanchement pleural étant le résultat d'une maladie variée, les antécédents et l'examen physique doivent également être axés sur la cause pulmonaire ou systémique sous-jacente de l'épanchement. Par exemple, dans l'insuffisance cardiaque congestive (ICC), rechercher une distension veineuse jugulaire, S3 et un œdème de la pédale, dans une cirrhose conduisant à un hydrothorax hépatique, rechercher des ascites et d'autres stigmates de la maladie du foie. [1]
Facteurs de risque
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section contient les facteurs de risque de la maladie. Ces facteurs de risque peuvent être des maladies, des anomalies génétiques, des caractéristiques individuelles (l'âge, le sexe, l'origine ethnique, un certain type d'alimentation), etc. |
| Formats: | Liste à puces, Tableau |
| Balises sémantiques: | Facteur de risque |
| Commentaires: |
|
| Exemple: | Les facteurs de risque de l'infarctus du myocarde sont :
|
Questionnaire
Toute contribution serait appréciée.
| Description: | Cette section traite des symptômes à rechercher à l'anamnèse (questionnaire). Les symptômes sont ressentis et exprimés par les patients. |
| Formats: | Liste à puces |
| Balises sémantiques: | Symptôme, Élément d'histoire |
| Commentaires: |
|
| Exemple: | Les symptômes de l'infarctus du myocarde sont :
D'autres éléments à rechercher au questionnaire de l'infarctus sont :
Il est parfois pertinent de mentionner des symptômes qui sont absents, comme dans la pharyngite à streptocoque. Les symptômes de la pharyngite à streptocoque sont :
|
L'épanchement pleural est souvent asymptomatique, mais il peut entraîner:
Examen clinique
Toute contribution serait appréciée.
| Description: | Cette section traite des signes à rechercher lors de l'examen clinique. |
| Formats: | Liste à puces |
| Balises sémantiques: | Examen clinique, Signe clinique |
| Commentaires: |
|
| Exemple: | L'examen physique de l'appendicite démontrera les éléments suivants :
|
À l'examen pulmonaire, les signes suivants pourront être mis en évidence:
- diminution du murmure vésiculaire du côté de l'épanchement;
- matité à la percussion;
- asymétrie de l'amplitude respiratoire (diminution du côté de l'épanchement);
- crépitants;
- déviation de la trachée (du côté contralatéral).;
- frottement pleural;
Si les signes sont bilatéraux, c'est que l'étiologie est probablement transsudative.
Selon l'étiologie, d'autres trouvailles permettront d'orienter le diagnostic:
- stigmates de cirrhose;
- cachexie (cause néoplasique).
Examens paracliniques
Toute contribution serait appréciée.
| Description: | Cette section concerne les tests à demander lorsque la maladie est suspectée et les résultats attendus en présence de la maladie. |
| Formats: | Liste à puces, Tableau |
| Balises sémantiques: | Examen paraclinique, Signe paraclinique |
| Commentaires: |
|
| Exemple: | Les examens suivants sont utiles dans la démarche d'investigation du VIPome :
|
- Investigation 1: signe paraclinique 1, signe paraclinique 2, ...
- Investigation 2: signe paraclinique 3, signe paraclinique 4, ...
- ...
Les radiographies thoraciques sont utiles pour confirmer la présence d'un épanchement. Les résultats de l'épanchement varient avec la quantité d'épanchement. Sur une vue postéro-antérieure (AP) verticale, un minimum de 200 ml de liquide est nécessaire pour effacer l'angle costophrénique, appelé signe ménisque d'un épanchement pleural. Cependant, en vue latérale, 50 ml de liquide peuvent être diagnostiqués avec ce signe. L'échographie thoracique est plus sensible et utile pour le diagnostic de l'épanchement pleural et aide également à planifier la thoracentèse. Tout épanchement unilatéral chez l'adulte nécessite une thoracentèse pour déterminer la cause du liquide pleural. Ceci est également connu pour améliorer les symptômes du patient et faciliter le rétablissement. [8][9][10][1]
Déterminer si le fluide est un exsudat ou un transsudat réduit le différentiel. Cependant, les critères de Light doivent être interprétés dans le contexte clinique car ils diagnostiquent à tort 20% des transsudats comme exsudatifs. Un exemple serait qu'un patient qui a subi une diurèse chronique pour une insuffisance cardiaque peut augmenter le niveau de protéines du liquide pleural et peut être classé comme un exsudat.[1]
Les tests couramment effectués sur le liquide pleural pour déterminer l'étiologie sont une mesure du pH du fluide, des protéines fluides, de l'albumine et de la LDH, du glucose fluide, des triglycérides fluides, du différentiel de numération des cellules fluides, de la coloration et de la culture de Gram et de la cytologie des fluides. Les exsudats sont caractérisés par une protéine élevée, une LDH élevée et une diminution du glucose. Une LDH du liquide pleural supérieure à 1000 U / L peut être observée dans la tuberculose, le lymphome et l'empyème. Un pH bas (pH inférieur à 7,2) indique un épanchement pleural complexe dans le contexte d'une pneumonie et nécessite presque toujours l'insertion d'un tube thoracique pour le drainage. Les autres causes de pH bas peuvent être une rupture de l'œsophage et la polyarthrite rhumatoïde.[1]
Les comptages de cellules fluides dans les transsudats montrent principalement des cellules mésothéliales. Dans les épanchements parapneumoniques, la pleurite lupique et la pancréatite aiguë, il existe une prédominance neutrophile dans le nombre de cellules. Certaines causes d'épanchement à prédominance lymphocytaire comprennent la malignité, le lymphome, la tuberculose, la sarcoïde, l'épanchement pleural rhumatoïde chronique et la malignité. L'éosinophilie dans l'épanchement pleural est rare et généralement en présence d'air (pneumothorax), de sang (hémothorax), d'une maladie parasitaire ou d'un épanchement d'origine médicamenteuse.[1]
La présence d'organismes par coloration de Gram ou culture conduit à un diagnostic d'empyème et nécessite un drain thoracique pour le drainage du pus. La cytologie est nécessaire pour déterminer la présence de cellules malignes dans le liquide pleural. La sensibilité de la cytologie du liquide pleural en présence d'un épanchement malin dans la première thoracentèse est d'environ 60%, et le rendement augmente avec d'autres tentatives, approchant 95% de trois échantillons à des jours différents. Cependant, si un épanchement malin est fortement suspecté et que la cytologie est négative, alors une thoracoscopie médicale avec biopsie pleurale peut être réalisée après deux à trois thoracentèses pour obtenir un diagnostic.[1]
D'autres tests qui peuvent être effectués sur le liquide pleural pour déterminer l'étiologie comprennent l'adénosine désaminase (ADA) qui, lorsqu'elle est élevée, est suspecte de tuberculose dans les zones à forte prévalence de la tuberculose. En cas de rupture œsophagienne, la présence d'amylase dans le liquide pleural est diagnostique. En cas d'insuffisance cardiaque, un taux élevé de NT-proBNP peut être observé dans le liquide pleural. La présence de plus de 110 mg / dL de triglycérides dans le liquide pleural indique un chylothorax. Le liquide pleural est généralement de couleur paille et s'il est blanc laiteux, un chylothorax doit être suspecté. Le diagnostic d'hémothorax peut être posé si l'hématocrite du liquide pleural est plus de 0,5 fois supérieur à celui de l'hématocrite sérique.[1]
La radiographie thoracique peut révéler un déplacement médiastinal vers la cavité thoracique controlatérale. Il peut également y avoir un déplacement de la trachée vers le côté ipsilatéral si la bronche est obstruée. Le scan CT est utile pour déterminer la cause comme une tumeur maligne.[1]
L'investigation de base de l'épanchement pleural est composée de:
- radiographie pulmonaire: [11]
- l'épanchement pleural sera visible s'il est supérieur à 200ml en antéro-postérieur ou 50 ml en latéral;
- les transsudats sont généralement bilatéraux;
- TDM thoracique: permet d'évaluer le parenchyme pulmonaire et la plèvre pour déterminer la source de l'épanchement, mettre en évidence des loculations;[11]
- échographie thoracique: pour guider une thoracocentèse ou mettre en évidence un épanchement de petite taille;
- thoracocentèse[note 1] afin d'analyser le liquide pleural:
- attention au risque d'oedème de réexpansion si plus de 1.5L est retiré;
- LDH, protéines, glucose, pH, culture, coloration Gram, cytologie, amylase
- Biopsie pleurale: si l'on suspecte la tuberculose, un mésothéliome ou une néoplasie (et que la cytologie est négative)
Approche clinique
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Alors que les sections Questionnaire, Examen clinique et Examens paracliniques servent à énumérer, cette section sert à intégrer tous ces éléments pour discuter du raisonnement du clinicien. C'est en quelque sorte la manière dont les cliniciens réfléchissent lorsque confrontés à cette maladie : c'est la section par excellence pour l'enseignement. |
| Formats: | Texte, Liste à puces, Tableau |
| Balises sémantiques: | |
| Commentaires: |
|
| Exemple: | |
Lignes directrices actuelles sur la prise en charge des épanchements pleuraux [1]
- L'utilisation de l'échographie au chevet améliore les taux de réussite et réduit le risque de pneumothorax pendant l'aspiration
- L'échographie peut détecter les séquestrations de liquide pleural
- Envoyez toujours du liquide pour la biochimie, la culture et la cytologie
- Utilisez les critères de la lumière pour distinguer l'exsudat du transsudat
- Les épanchements à prédominance lymphocytaire sont généralement dus à une insuffisance cardiaque, une tumeur maligne et une tuberculose
- Vérifiez le pH lors de l'aspiration d'épanchements pleuraux
- N'injectez pas d'air ou d'anesthésique local dans l'échantillon car cela pourrait modifier le pH du liquide
- Si le pH est inférieur à 7,2, un drainage du fluide est recommandé
- Des épanchements malins peuvent être détectés en cytologie (40-60%)
- La tomodensitométrie est recommandée lorsque l'élimination complète du liquide pleural n'est pas possible
- La thoracoscopie peut être utilisée pour poser un diagnostic de malignité
- La bronchoscopie flexible de routine n'est pas recommandée pour les épanchements pleuraux [1]
Diagnostic
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section traite de la manière dont on peut diagnostiquer une maladie en tenant compte de l'histoire, de l'examen clinique et des investigations. C'est dans cette section que se retrouveront les critères permettant d'infirmer ou de confirmer la présence de la maladie (lorsqu'ils existent). |
| Formats: | Texte, Liste à puces, Tableau |
| Balises sémantiques: | |
| Commentaires: |
|
| Exemple: | L'asystolie est un diagnostic électrocardiographique. L'absence d'activité électrique chez un patient inconscient sans pouls permet de confirmer le diagnostic, tout en s'assurant qu'il n'y a pas de cable débranché et que la calibration du moniteur est adéquate.
Selon le Fourth Universal Definition of Myocardial Infarction, l'infarctus aigu du myocarde est diagnostiqué lorsqu'il y a :
|
Diagnostic différentiel
Toute contribution serait appréciée.
| Description: | Cette section traite du diagnostic différentiel de la maladie, c'est-à-dire aux autres diagnostics à évoquer lorsque confronté à ce diagnostic. |
| Formats: | Liste à puces |
| Balises sémantiques: | Diagnostic différentiel |
| Commentaires: |
|
| Exemple: | Le diagnostic différentiel de l'appendicite comprend :
|
- Diagnostic différentiel 1
- Diagnostic différentiel 2
- Diagnostic différentiel 3
- ...
- Insuffisance cardiaque congestive
- Blessure au diaphragme
- Paralysie diaphragmatique
- Mésothéliome malin
- Pneumonie
- Atélectasie[1]
Traitement
Toute contribution serait appréciée.
| Description: | Cette section décrit le traitement de la maladie. |
| Formats: | Liste à puces, Tableau, Texte |
| Balises sémantiques: | Traitement, Traitement pharmacologique |
| Commentaires: |
|
| Exemple: | |
Une fois l'étiologie de l'épanchement pleural déterminée, la prise en charge consiste à s'attaquer à la cause sous-jacente. En cas d'épanchement parapneumonique complexe ou d'empyème (pH du liquide pleural inférieur à 7,2 ou présence d'organismes), un drainage par sonde thoracique est généralement indiqué avec des antibiotiques. Les drains de petit diamètre (10 G à 14 G) sont aussi efficaces que les drains de grand diamètre à cette fin. Si les patients ne répondent pas aux antibiotiques appropriés et à un drainage adéquat, une décortication ou un débridement thoracoscopique peut être nécessaire. L'instillation de fibrinolytiques intrapleuraux et de DNAse peut être utilisée pour améliorer le drainage et chez ceux qui ne répondent pas à une antibiothérapie suffisante et ceux qui ne sont pas candidats à une intervention chirurgicale. [1]
Si un patient présentant un épanchement pleural malin n'est pas symptomatique, le drainage n'est pas toujours indiqué sauf si une infection sous-jacente est suspectée. Pour les épanchements pleuraux malins nécessitant un drainage fréquent, les options de prise en charge sont la pleurodèse (où l'espace pleural est oblitéré mécaniquement ou chimiquement en induisant des irritants dans l'espace pleural) et la mise en place d'un cathéter pleural tunnelé.
Les épanchements chyleux sont initialement gérés de manière conservatrice, mais la plupart nécessitent une intervention chirurgicale.[1]
Il ne faut pas retirer plus de 1500 ml de liquide au cours d'une seule tentative car cela peut entraîner un œdème pulmonaire de ré-expansion. Une radiographie thoracique est obligatoire après avoir effectué une thoracentèse pour déterminer le liquide résiduel et la présence d'un pneumothorax.[1]
Si l'épanchement devient trop important, une thoracentèse peut être effectuée. S'il est récidivant, un drain thoracique peut-être installé ou une pleurodèse effectuée.[12]
Suivi
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section traite du suivi de la maladie. |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: |
|
| Exemple: | |
Complications
Toute contribution serait appréciée.
| Description: | Cette section traite des complications possibles de la maladie. |
| Formats: | Liste à puces, Texte |
| Balises sémantiques: | Complication |
| Commentaires: |
|
| Exemple: | Les complications de l'infarctus du myocarde sont :
|
Évolution
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section contient le pronostic et évolution naturelle de la maladie. Le pronostic est lié à la survie du patient atteint de la maladie. L'évolution naturelle est la manière dont évoluera la maladie du patient dans le temps. |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: | |
| Exemple: | La dissection aortique est associée une mortalité très élevée. Au moins 30% des patients décèdent après leur arrivée à l'urgence, et ce, même après une intervention chirurgicale. Pour ceux qui survivent à la chirurgie, la morbidité est également très élevée et la qualité de vie est mauvaise. La mortalité la plus élevée d'une dissection aortique aiguë est dans les 10 premiers jours. Les patients qui ont une dissection chronique ont tendance à avoir un meilleur pronostic, mais leur espérance de vie est raccourcie par rapport à la population générale.[1] Sans traitement, la mortalité est de 1 à 3% par heure au cours des 24 premières heures, 30% à une semaine, 80% à deux semaines et 90% à un an. |
Le pronostic dépend de la cause de l'épanchement pleural. Les épanchements bénins peuvent être guéris mais si la cause est une tumeur maligne, le pronostic est très mauvais. Une autre caractéristique des épanchements pleuraux est la récidive qui peut également survenir avec des troubles bénins tels que le lupus, l'urémie et la polyarthrite rhumatoïde. Si l'épanchement pleural n'est pas drainé, il peut conduire à une dyspnée et même à un empyème.[1]
Prévention
Si la section est n'est pas jugée nécessaire, elle peut être supprimée.
| Description: | Cette section traite des mesures préventives et du dépistage précoce de la maladie (lorsque pertinent). |
| Formats: | Texte |
| Balises sémantiques: | |
| Commentaires: | |
| Exemple: | La prévention primaire consiste à la prise en charge des facteurs de risque :
|
Concepts clés
Si un épanchement pleural important est drainé rapidement et que des volumes supérieurs à 1,5 L sont retirés, la ré-expansion rapide du poumon effondré peut occasionnellement conduire à un œdème pulmonaire de ré-expansion. La manométrie pleurale et la surveillance de la pression pleurale pendant le drainage de grands volumes et la fin du drainage supplémentaire une fois que la pression pleurale est tombée en dessous de -20 cm d'eau ou se terminant avec l'apparition d'une douleur thoracique peuvent empêcher la ré-expansion de l'œdème pulmonaire.
Consultations
- Pneumologue
- Chirurgien thoracique [1]
Notes
- ↑ S'assurer d'envoyer un échantillon de sang pour comparer les valeurs du liquide pleural avec celles du sérum.
Références
- Cette page a été modifiée ou créée le 2021/01/04 à partir de Pleural Effusion (StatPearls / Pleural Effusion (2020/10/28)), écrite par les contributeurs de StatPearls et partagée sous la licence CC-BY 4.0 international (jusqu'au 2022-12-08). Le contenu original est disponible à https://www.ncbi.nlm.nih.gov/pubmed/28846252 (livre).
- ↑ 1,00 1,01 1,02 1,03 1,04 1,05 1,06 1,07 1,08 1,09 1,10 1,11 1,12 1,13 1,14 1,15 1,16 1,17 1,18 1,19 1,20 1,21 1,22 1,23 1,24 1,25 1,26 1,27 1,28 et 1,29 Rachana Krishna et Mohan Rudrappa, StatPearls, StatPearls Publishing, (PMID 28846252, lire en ligne)
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/29377972
- ↑ 3,0 et 3,1 https://www.ncbi.nlm.nih.gov/pubmed/30252207
- ↑ 4,0 et 4,1 https://www.ncbi.nlm.nih.gov/pubmed/30262573
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/30190139
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/30005142
- ↑ 7,0 et 7,1 (en) Tina Binesh Marvasti et Sydney McQueen, Toronto Notes 2018, 34e éd., R22
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/30272503
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/30272486
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/29916720
- ↑ 11,0 et 11,1 (en) Tina Binesh Marvasti et Sydney McQueen, Toronto Notes 2018, 34e éd., R22
- ↑ (en) Tina Binesh Marvasti et Sydney McQueen, Toronto Notes 2018, 34e éd., R22
